Professional Documents
Culture Documents
Monografia Glucolisis Biokmik
Uploaded by
PAúl Casa OrtizOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Monografia Glucolisis Biokmik
Uploaded by
PAúl Casa OrtizCopyright:
Available Formats
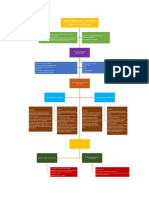
INTRODUCCION La gluclisis es una va que permite obtener ATP a las clulas.
La gluclisis (o gliclisis) es una va catablica a travs de la cual tanto las clulas de los animales como vegetales, hongos y bacterias oxidan diferentes molculas de glcidos y obtienen energa. El hecho de que esta va ocurra en organismos muy diversos, indica que es una va metablica conservada, es decir presente en organismos filogenticamente distantes. Para su estudio, describiremos 9 reacciones enzimticas que ocurren en el citoplasma y permiten la transformacin de una molcula de glucosa a dos molculas de piruvato. La degradacin hasta priuvato es parte del proceso catablico o degradativo de los glcidos, porque estas molculas pueden seguir oxidndose y continuar entregando energa a la clula. El balance neto para la reaccin global de la gluclisis es: Hexosa + 2 NAD+ + 2 ADP + 2 Pi 2 NADH + 2 piruvato + 2 ATP En la gluclisis se pueden establecer dos fases Primera fase Activacin de la hexosa (glucosa por ej.), con gasto de energa como ATP. Segunda fase Obtencin de energa que se conserva como ATP. La primera fase es endergnica, porque se consumen 2 ATP, y consta en la transformacin de una hexosa (por ejemplo, glucosa) en dos triosas (dihidroxicetona 3 P y gliceraldehdo 3P). La segunda fase es exergnica, dado que se forman 4 ATP utilizando la energa liberada de la conversin de 2 gliceraldehdos 3P en 2 piruvatos. La gluclisis ocurre a travs de reacciones enzimticas, donde cada enzima cataliza una reaccin o paso especfico. De esta forma, cuando se hace referencia a una isomerasa, lo es a una especfica para determinada molcula, y no a una isomerasa universal que catalice cualquier reaccin de isomerizacin. Lo mismo sucede con las quinasas, deshidrogenasas, etc.
Pgina 1
OBJETIVOS OBJETIVO GENERAL Comprender la importancia de la funcin que desempean la glucolisis en las clulas
OBJETIVO ESPECIFICO Definir que es la glucolisis Identificar las diferentes etapas Conocer su rendimiento energtico Aprender las funciones de la glucolisis Comprender las diferentes regulaciones
Pgina 2
GLUCLISIS La gluclisis o glicolisis proviene del griego glycos, azcar y lysis, ruptura. Es la va metablica encargada de oxidar la glucosa con la finalidad de obtener energa para la clula. Consiste en 10 reacciones enzimticas consecutivas que convierten a la glucosa en dos molculas de piruvato, el cual es capaz de seguir otras vas metablicas y as continuar entregando energa al organismo.
VISIN GENERAL Durante la gluclisis se obtiene un rendimiento neto de dos molculas de ATP y dos molculas de NADH; el ATP puede ser usado como fuente de energa para realizar trabajo metablico, mientras que el NADH puede tener diferentes destinos. Puede usarse como fuente de poder reductor en reacciones anablicas; si hay oxgeno, puede oxidarse en la cadena respiratoria, obtenindose tres ATPs; si no hay oxgeno, se usa para reducir el piruvato a lactato (fermentacin lctica), o a CO2 y etanol (fermentacin alcohlica), sin obtencin adicional de energa. La gluclisis es la forma ms rpida de conseguir energa para una clula y, en el metabolismo de carbohidratos, generalmente es la primera va a la cual se recurre. Se encuentra estructurada en 10 reacciones enzimticas que permiten la transformacin de una molcula de glucosa a dos molculas de piruvato mediante un proceso catablico.
Pgina 3
La gluclisis es una de las vas ms estudiadas, y generalmente se encuentra dividida en dos fases: la primera, de gasto de energa y la segunda fase, de obtencin de energa. La primera fase consiste en transformar una molcula de glucosa en dos molculas de gliceraldehdo (una molcula de baja energa) mediante el uso de 2 ATP. Esto permite duplicar los resultados de la segunda fase de obtencin energtica. En la segunda fase, el gliceraldehdo se transforma en un compuesto de alta energa, cuya hidrlisis genera una molcula de ATP, y como se generaron 2 molculas de gliceraldehdo, se obtienen en realidad dos molculas de ATP. Esta obtencin de energa se logra mediante el acoplamiento de una reaccin fuertemente exergnica despus de una levemente endergnica. Este acoplamiento ocurre una vez ms en esta fase, generando dos molculas de piruvato. De esta manera, en la segunda fase se obtienen 4 molculas de ATP.
Reacciones posteriores Luego de que una molcula de glucosa se transforme en 2 molculas de piruvato, las condiciones del medio en que se encuentre determinarn la va metablica a seguir. En organismos aerbicos, el piruvato seguir oxidndose por la enzima piruvato deshidrogenasa y el ciclo de Krebs, creando intermediarios como NADH y FADH2. Estos intermediarios no pueden cruzar la membrana mitocondrial, y por lo tanto, utilizan sistemas de intercambio con otros compuestos llamados lanzaderas (en ingls, shuttles). Los ms conocidos son la lanzadera malato-aspartato y la lanzadera glicerol-3fosfato. Los intermediarios logran entregar sus equivalentes al interior de la membrana mitocondrial, y que luego pasarn por la cadena de transporte de electrones, que los usar para sintetizar ATP.
Pgina 4
De esta manera, se puede obtener hasta 30 moles de ATP a partir de 1 mol de glucosa como ganancia neta. Sin embargo, cuando las clulas no posean mitocondrias (ej: eritrocito) o cuando requieran de grandes cantidades de ATP (ej.: el msculo al ejercitarse), el piruvato sufre fermentacin que permite obtener 2 moles de ATP por cada mol de glucosa, por lo que esta va es poco eficiente respecto a la fase aerbica de la gluclisis. El tipo de fermentacin vara respecto al tipo de organismos: en levaduras, se produce fermentacin alcohlica, produciendo etanol y CO2 como productos finales, mientras que en msculo, eritrocitos y algunos microorganismos se produce fermentacin lctica, que da como resultado cido lctico o lactato. ETAPAS DE LA GLUCLISIS La gluclisis se divide en dos partes principales y diez reacciones enzimticas, que se describen a continuacin. Fase de gasto de energa (ATP) Esta primera fase de la gluclisis consiste en transformar una molcula de glucosa en dos molculas de gliceraldehdo. 1er paso: Hexoquinasa La primera reaccin de la gluclisis es la fosforilacin de la glucosa, para activarla (aumentar su energa) y as poder utilizarla en otros procesos cuando sea necesario. Esta activacin ocurre por la transferencia de un grupo fosfato del ATP, una reaccin catalizada por la enzima hexoquinasa,5 la cual puede fosforilar (aadir un grupo fosfato) a molculas similares a la glucosa, como la fructosa y manosa. Las ventajas de fosforilar la glucosa son 2: La primera es hacer de la glucosa un metabolito ms reactivo, mencionado anteriormente, y la segunda ventaja es que la glucosa-6-fosfato no puede cruzar la membrana celular a diferencia de la glucosa ya que en la clula no existe un transportador de G6P. De esta forma se evita la prdida de sustrato energtico para la clula. Tcnicamente hablando, la hexoquinasa slo fosforila las Dhexosas, y utiliza de sustrato MgATP2+, ya que este catin permite que el ltimo fosfato del ATP (fosfato gamma, -P o P) sea un blanco ms fcil para el ataque nucleoflico que realiza el grupo hidroxilo (OH) del sexto carbono de la glucosa, lo que es posible debido al Mg2+ que apantalla las cargas de los otros dos fosfatos. Esta reaccin posee un G negativo, y por tanto se trata de una reaccin en la que se pierde energa en forma de calor. En numerosas bacterias
Pgina 5
esta reaccin esta acoplada a la ltima reaccin de la gluclisis (de fosfoenolpiruvato a piruvato) para poder aprovechar la energa sobrante de la reaccin: el fosfato del fosfoenolpiruvato se transfiere de una a otra protena de un sistema de transporte fosfotransferasa, y en ltima instancia, el fosfato pasar a una molcula de glucosa que es tomada del exterior de la clula y liberada en forma de G6P en el interior celular. Se trata por tanto de acoplar la primera y la ltima reaccin de esta va y usar el excedente de energa para realizar un tipo de transporte a travs de membrana denominado translocacin de grupo. 2 paso: Glucosa-6-P isomerasa ste es un paso importante, puesto que aqu se define la geometra molecular que afectar los dos pasos crticos en la gluclisis: El prximo paso, que agregar un grupo fosfato al producto de esta reaccin, y el paso 4, cuando se creen dos molculas de gliceraldehido que finalmente sern las precursoras del piruvato.1 En esta reaccin, la glucosa-6-fosfato se isomeriza a fructosa-6-fosfato, mediante la enzima glucosa-6-fosfato isomerasa. La isomerizacin ocurre en una reaccin de 4 pasos, que implica la apertura del anillo y un traspaso de protones a travs de un intermediario cis-enediol. Puesto que la energa libre de esta reaccin es igual a +1,7 kJ/mol la reaccin es no espontnea y se debe acoplar. 3er paso: Fosfofructoquinasa Fosforilacin de la fructosa 6-fosfato en el carbono 1, con gasto de un ATP, a travs de la enzima fosfofructoquinasa-1 (PFK1). Tambin este fosfato tendr una baja energa de hidrlisis. Por el mismo motivo que en la primera reaccin, el proceso es irreversible. El nuevo producto se denominar fructosa-1,6-bifosfato. La irreversibilidad es importante, ya que la hace ser el punto de control de la gluclisis. Como hay otros sustratos aparte de la glucosa que entran en la gluclisis, el punto de control no est colocado en la primera reaccin, sino en sta. La fosfofructoquinasa tiene centros alostricos, sensibles a las concentraciones de intermediarios como citrato y cidos grasos. Liberando una enzima llamada fosfructocinasa-2 que fosforila en el carbono 2 y regula la reaccin. 4 paso: Aldolasa La enzima aldolasa (fructosa-1,6-bifosfato aldolasa), mediante una condensacin aldlica reversible, rompe la fructosa-1,6-bifosfato en dos molculas de tres carbonos (triosas): dihidroxiacetona fosfato y gliceraldehdo-3-fosfato. Existen dos tipos de aldolasa, que difieren tanto en el tipo de organismos donde se expresan, como en los intermediarios de reaccin.
Pgina 6
Esta reaccin tiene una energa libre (G) entre 20 a 25 kJ/mol, por lo tanto en condiciones estndar no ocurre de manera espontnea. Sin embargo, en condiciones intracelulares la energa libre es pequea debido a la baja concentracin de los sustratos, lo que permite que esta reaccin sea reversible. 5 paso: Triosa fosfato isomerasa Puesto que slo el gliceraldehdo-3-fosfato puede seguir los pasos restantes de la gluclisis, la otra molcula generada por la reaccin anterior (dihidroxiacetona-fosfato) es isomerizada (convertida) en gliceraldehdo-3-fosfato. Esta reaccin posee una energa libre en condiciones estndar positiva, lo cual implicara un proceso no favorecido, sin embargo al igual que para la reaccin 4, considerando las concentraciones intracelulares reales del reactivo y el producto, se encuentra que la energa libre total es negativa, por lo que la direccin favorecida es hacia la formacin de G3P. ste es el ltimo paso de la "fase de gasto de energa". Slo se ha consumido ATP en el primer paso (hexoquinasa) y el tercer paso (fosfofructoquinasa-1). Cabe recordar que el 4to paso (aldolasa) genera una molcula de gliceraldehdo-3-fosfato, mientras que el 5to paso genera una segunda molcula de ste. De aqu en adelante, las reacciones a seguir ocurrirn dos veces, debido a las 2 molculas de gliceraldehdo generadas de esta fase. Hasta esta reaccin hay intervencin de energa (ATP). Fase de beneficio energtico (ATP, NADH) Hasta el momento solo se ha consumido energa (ATP), sin embargo, en la segunda etapa, el gliceraldehdo es convertido a una molcula de mucha energa, donde finalmente se obtendr el beneficio final de 4 molculas de ATP. 6 paso: Gliceraldehdo-3-fosfato deshidrogenasa Esta reaccin consiste en oxidar el gliceraldehdo-3-fosfato utilizando NAD+ para aadir un ion fosfato a la molcula, la cual es realizada por la enzima gliceraldehdo-3-fosfato deshidrogenasa o bien, GAP deshidrogenasa en 5 pasos, y de sta manera aumentar la energa del compuesto. Tcnicamente, el grupo aldehdo se oxida a un grupo acil-fosfato, que es un derivado de un carboxilo fosfatado. Este compuesto posee una energa de hidrlisis sumamente alta (cercana a los 50 kJ/mol) por lo que se da inicio al proceso de reacciones que permitirn recuperar el ATP ms adelante.
Pgina 7
Mientras el grupo aldehdo se oxida, el NAD+ se reduce, lo que hace de esta reaccin una reaccin redox. El NAD+ se reduce por la incorporacin de algn [H+] dando como resultado una molcula de NADH de carga neutra. 7 paso: Fosfoglicerato quinasa En este paso, la enzima fosfoglicerato quinasa transfiere el grupo fosfato de 1,3-bisfosfoglicerato a una molcula de ADP, generando as la primera molcula de ATP de la va. Como la glucosa se transform en 2 molculas de gliceraldehdo, en total se recuperan 2 ATP en esta etapa. Ntese que la enzima fue nombrada por la reaccin inversa a la mostrada, y que sta opera en ambas direcciones. Los pasos 6 y 7 de la gluclisis nos muestran un caso de acoplamiento de reacciones, donde una reaccin energticamente desfavorable (paso 6) es seguida por una reaccin muy favorable energticamente (paso 7) que induce la primera reaccin. En otras palabras, como la clula se mantiene en equilibrio, el descenso en las reservas de 1,3 bifosfoglicerato empuja a la enzima GAP deshidrogenasa a aumentar sus reservas. La cuantificacion de la energa libre para el acople de ambas reacciones es de alrededor de -12 kJ/mol. sta manera de obtener ATP sin la necesidad de O2 se denomina fosforilacin a nivel de sustrato. 8 paso: Fosfoglicerato mutasa Se isomeriza el 3-fosfoglicerato procedente de la reaccin anterior dando 2-fosfoglicerato, la enzima que cataliza esta reaccin es la fosfoglicerato mutasa. Lo nico que ocurre aqu es el cambio de posicin del fosfato del C3 al C2. Son energas similares y por tanto reversibles, con una variacin de energa libre cercana a cero. Cataliza la transferencia interna de un grupo fosfato desde el carbono C-3 al carbono C-2 que resulta en la conversin de 3-fosfoglicerato a 2fosfoglicerato a traves del compuesto intermedio 2,3-bisfosfoglicerato. La reaccin implica a dos grupos fosfato diferentes, es decir el grupo fosfato final del 2-fosfoglicerato no es el mismo que el grupo fosfato inicial del 3fosfoglicerato. 9 paso: Enolasa o fosfopiruvato hidratasa Consideramos aqu a dos reacciones sucesivas, la isomerizacin del 3fosfoglicerato a 2-fosfoglicerato y la otra corresponde a la transformacin del 2-fosfoglicerato en fosfoenolpiruvato (PEP), por accin de la enolasa. La enzima enolasa propicia la formacin de un doble enlace en el 2fosfoglicerato, eliminando una molcula de agua formada por el hidrgeno del C2 y el OH del C3. El resultado es el fosfoenolpiruvato.
Pgina 8
10 paso: Piruvato quinasa Desfosforilacin del fosfoenolpiruvato, obtenindose piruvato y ATP. Reaccin irreversible mediada por la piruvato quinasa. La transferencia del grupo fosfato del PEP al ADP la cataliza una quinasa (piruvato quinasa). Es la segunda fosforilacin a nivel de sustrato: se fosforila el ADP a ATP independientemente de la cadena respiratoria. El enzima piruvato quinasa es dependiente de magnesio y potasio. La energa libre es de -31,4 kJ/mol, por lo tanto la reaccin es favorable e irreversible. El rendimiento total de la gluclisis de una sola glucosa (6C) es de 2 ATP y no 4 (dos por cada gliceraldehdo-3-fosfato (3C)), ya que se consumen 2 ATP en la primera fase, y 2 NADH (que dejarn los electrones Nc en la cadena de transporte de electrones para formar 3 ATP por cada electrn). Con la molcula de piruvato, mediante un paso de oxidacin intermedio llamado descarboxilacin oxidativa, mediante el cual el piruvato pasa al interior de la mitocondria, perdiendo CO2 y un electrn que oxida el NAD+, que pasa a ser NADH ms H+ y ganando un CoA-SH (coenzima A), formndose en acetil-CoA gracias a la enzima piruvato deshidrogenasa, se puede entrar al ciclo de Krebs (que, junto con la cadena de transporte de electrones, se denomina respiracin). EL NADH.H GENERADO EN LA GLUCLISIS DEBE REOXIDARSE Y GENERAR NAD Para que la gluclisis contine se debe reoxidar el NADH.H generado en la reaccin GA3P a 1,3 P glicerato, de manera de mantener disponible NAD, necesario para que ocurra esa reaccin (sexta). De no ser as la gluclisis se interrumpira porque la enzima no tiene el cofactor oxidado para aceptar los hidrgenos. Segn las clulas sean fermentativas o sean aerobias, hay dos formas de reoxidar el NADH.H glicoltico: 1. Las fermentaciones. Este proceso consiste en reoxidar el NADH.H, reduciendo por ejemplo el piruvato que rinde lactato. Hay diferentes fermentaciones adems de la lctica que se acaba de describir, como la alcohlica, la actica, la propinica etc. 2. Las lanzaderas. Estas corresponden a la estrategia aerobia de reoxidacin del NADH.H. Una de las lanzaderas es la del glicerol 3-P. El mecanismo de la lanzadera es el siguiente: el D3P se reduce a glicerol 3-P a partir del NADH.H, de manera que ste se oxida a NAD y se mantiene una concentracin de NAD que permite la actividad de la enzima. El glicerol 3-P tiene transportador en la membrana mitocondrial y pasa a la
Pgina 9
matriz, donde es oxidado y regenera el D3P por una deshidrogenasa que tiene como cofactor al FAD de la cadena respiratoria. De esta forma, mientras el D3P vuelve al citoplasma, el FADH2 se oxida a FAD y ese poder reductor es usado para reducir al oxgeno y formar H2O a travs de la cadena respiratoria, donde se forman 2 ATP. Otra lanzadera es la del malato-oxalacetato, con la misma funcin que la del glicerol 3-P, pero a diferencia de sta es el malato el transportador, y quien se oxida a oxalacetato a travs de una deshidrogenasa que usa NAD como cofactor: se generan 3 ATP. BALANCE NETO El balance neto de la glucolisis es: glucosa + 2 ADP + 2 Pi + 2 NAD+---> 2 piruvatos + 2 ATP + 2 (NADH + H+) La energa total que se puede obtener de la glucosa por oxidacin aerbica es = 688 kcal/mol. La energa total acumulada en 2 ATP = 2 x 7.3 = 14.6 kcal/mol Esto es un - 2% de rendimiento, si se tiene en cuenta la posibilidad de oxidar completamente la glucosa, es decir que el 98% de la energa potencialmente disponible no es usada por la clula. Los dos NADH + H+ pasan a la cadena de transporte de electrones en ambiente aerobios y pueden dar mas ATP, recuperndose el NAD en su forma oxidada. EL PIRUVATO TIENE DIFERENTES DESTINOS En organismos aerbicos, el piruvato seguir oxidndose en el ciclo de Krebs, donde se generan intermediarios de cadena respiratoria reducidos, como NADH.H y FADH2. El poder reductor generar H2O y parte de la energa liberada ATP. En organismos fermentativos, como algunas levaduras, a partir del piruvato tiene lugar la fermentacin, y se generan diferentes molculas como el lactato, etanol, etc. En las clulas musculares que son aerobias el piruvato deriva al ciclo de Krebs. Sin embargo, cuando el oxgeno no es suficiente en ese tejido por determinadas razones fisiolgicas, puede haber en el msculo fermentacin lctica.
Pgina 10
ANLISIS ESTEQUIOMTRICO DE LA GLUCLISIS Glucosa + 2Pi + 2 ADP + 2 NAD+ H2O 2 Pyr + 2 ATP + 2 NADH + 2 H+ + 2
La gluclisis es una va que transforma la glucosa en Piruvato y, a su vez, reduce 2 NAD+ del citosol a NADH y usa 2 ADP para formar 2 ATP. La clula en cuanto puede, transforma otros monosacridos a molculas que estn en la va de la gluclisis. Fructosa Se encuentra en el azcar, se metaboliza segn: En el hgado: la fructosa se transforma en fructosa-1-P. Se gasta 1 ATP que pasa a ADP. Lo realiza la fructoquinasa. La fructosa-1-P es degradada por una aldolasa, que da lugar a dihidroxiacetona-P y a gliceraldehido. El gliceraldehido es fosforilado con gasto de ATP a G3P. Se produce el mismo rendimiento que en la glucosa. En el tejido adiposo: la fructosa es fosforilada a fructosa-6-P a partir de la transformacin de ATP a ADP por la hexoquinasa. La hexoquinasa tiene mucha menos afinidad por la fructosa que por la glucosa. Por eso, en el hgado, la hexoquinasa fosforila glucosa. En el tejido adiposo la hexoquinasa (HK) acta sobre la fructosa porque no hay tanta glucosa. Galactosa La galactosa se fosforila en Gal-1-P y se gasta ATP que pasa a ADP. Lo hace la galactoquinasa. La Gal-1-P es transferida al Uridindifosfoglucosa (UDPglucosa), que es la forma activada de la glucosa, por la Gal-1-P-uridiltransferasa y se genera UDPgalactosa y se libera Glucosa-1-P Despus se transforma la Glucosa-1-P en Glucosa-6-P mediante la fosfoglucomutasa. Para que el circuito funcione correctamente, hay que regenerar UDPglucosa. Hay una epimerasa que retransforma UDP-galactosa en UDPglucosa. La galactosa rinde igual que la glucosa. RENDIMIENTO ENERGTICO DE LA GLUCLISIS El rendimiento de la gluclisis es diferente segn: Condiciones anaerobias: Fermentacin Condiciones aerobias: Ciclo de krebs, Cadena transportadora de electrones y Fosforilacion oxidativa
Pgina 11
FERMENTACIN Se llama fermentacin a un conjunto de rutas metablicas, que se realizan en el hialoplasma, por las cuales ciertos organismos obtienen energa por la oxidacin incompleta de compuestos orgnicos. Los electrones liberados en esta oxidacin no son llevados al oxgeno molecular (tal como ocurre en la respiracin celular), sino que son aceptados por un compuesto orgnico sencillo que es el producto final de la fermentacin. As, la oxidacin de la materia orgnica no es completa (no se transforma totalmente en materia inorgnica) y el rendimiento energtico es bajo. El combustible que con ms frecuencia se utiliza es algn tipo de azcar, pero pueden ser utilizados otros compuestos orgnicos en estos procesos. La fermentacin la llevan a cabo diferentes tipos de bacterias capaces de vivir sin oxgeno, pero tambin se da en clulas aerobias como las musculares, que la utilizan como mecanismo complementario de la respiracin celular al faltar el oxgeno. La mayora de las fermentaciones son anaerobias, y su finalidad es que no se bloquee completamente el catabolismo en ausencia de oxgeno, permitiendo al organismo obtener energa, aunque sea poca, en esas condiciones.
Tipos de fermentacin: Fermentacin anaerobia, son las ms tpicas; no requieren oxgeno. Fermentacin lctica. En la que el producto final que se obtiene es cido lctico (fermentacin homolctica) unido, en ocasiones, a otros compuestos (heterolctica). La realizan
Pgina 12
ciertas bacterias como las del gnero Lactobacillus (utilizadas para la obtencin de yogur y queso) y las clulas musculares cuando el aporte de oxgeno es insuficiente. Fermentacin alcohlica. En la que se obtiene alcohol etlico. La realizan ciertas levaduras (gnero Saccharomyces) utilizadas para fabricar gran variedad de bebidas alcohlicas (vino, cerveza, etc.) a partir de diversos azcares (de uva, de cereales, etc). Fermentacin oxidativa. Requieren oxgeno (son aerobias) pero ste no acta como ltimo aceptor de electrones sino como oxidante del sustrato. La ms conocida es la fermentacin actica (se produce vinagre a partir del vino) y en la cual, el alcohol etlico es oxidado a cido actico mediante el oxgeno. CICLO DE KREBS Llamado ciclo del cido ctrico o ciclo de los cidos tricarboxlicos es una ruta metablica, es decir, una sucesin de reacciones qumicas, que forma parte de la respiracin celular en todas las clulas aerbicas. En clulas eucariotas se realiza en la mitocondria. En las procariotas, el ciclo de Krebs se realiza en el citoplasma, especficamente en el citosol. En organismos aerbicos, el ciclo de Krebs es parte de la va catablica que realiza la oxidacin de glcidos, cidos grasos y aminocidos hasta producir CO2, liberando energa en forma utilizable (poder reductor y GTP).
Pgina 13
Se encarga de transformar los carbonos de la acetil-CoA en CO2 y H2O Reacin sumaria: AcetIl-CoA + 3 NAD+ + FAD + GDP + Pi ------------> 3 NADH + FADH2 + CoA-SH + GTP + 3 CO2 Es un mecanismo que incorpora el Acetil del Acetil Co-Enzima-A sobre un oxaloacetato y resulta en la eliminacin de 2 C ms oxidados (CO2), a expensas del paso de algunas molculas de NAD a NADH y de FAD a FADH. Es un proceso central en el metabolismo de carbohidratos y de lpidos y de muchos aminocido. Las reacciones que implica el ciclo de Krebs son: Una molcula de Acetil Co-A se incorpora en una molcula de oxaloacetato, dando el cido ctrico. La condensacin se da por el enzima citratosintasa. Esta reaccin tiende hacia la incorporacin de Acetil Co-A incluso en concentraciones muy pequeas. El citrato tiene un OH central, que se transfiere a un C adyacente mediante la aconitasa. Se forma un intermedio, que es el cisaconitato. Es una reaccin de deshidratacin, seguida de rehidratacin. El agua que entra, entra en el otro C involucrado en el proceso. El isocitrato se deshidrata formando NADH por la isocitrato deshidrogenasa. Da lugar al oxalosuccinato (es qumicamente -cetocido (descarboxilan muy -cetoglutarato. El -cetoglutarato, mediante la -cetoglutarato deshidrogenasa, es descarboxilado, reduciendo un NAD, y se genera succinil co-A. Se trata de la misma reaccin que realiza la piruvato deshidrogenasa. -cetoglutarato es un complejo proteico con 4 aminocidos y 5 coenzimas. La hidrlisis del tioster (succinil Co-A), se acopla a la sntesis de una molcula de GTP a partir de GDP. Lo hace la Succinil Co-A sintetasa). El GTP est informando a la piruvato deshidrogenasa de como va el metabolismo. El GTP pasa a ATP gracias a la nuclesidodifosfoquinasa: Lo que queda del ciclo, sirve para regenerarel oxaloacetato. El succinato con grupo ceto, da lugar a un oxaloacetato. Se va a oxidar este C a cetona. Se hace introduciendo 1 doble enlace entre los C centrales del succinato mediante la succinato deshidrogenasa.
Pgina 14
Se reduce FAD a FADH2. Es el nico enzima que est en la membrana interna mitocondrial. Se relaciona con la cadena de transporte de electrones. Se forma el cido fumaral. El fumaral es hidratado por la fumarasa, que es estereoespecfica. Forma la L-Malato, que es oxidada a cetona para dar oxaloacetato mediante la malatodeshidrogenasa, que reduce NAD a NADH. CADENA TRANSPORTADORA DE ELECTRONES Es un sistema multienzimtico ligado a membrana que transfiere electrones desde molculas orgnicas al oxgeno. La CTE comprende dos procesos: 1. Los electrones son transportados a lo largo de la membrana, de un complejo de protenas transportador ("carrier") a otro. 2. Los protones son translocados a travs de la membrana, estos significa que son pasados desde el interior o matriz hacia el espacio intermembrana. Esto construye un gradiente de protones. El oxgeno es el aceptor terminal del electrn, combinndose con electrones e iones H+para producir agua.
Los tres componentes de la cadena respiratoria son: 3 grandes complejos proteicos con molculas trasnportadoressa y sus enzimas correspondientes, un componente no proteico: UBIQUINONA (Q) que estn embebidos en la membrana y una pequea protena llamada citocromo c que es perifrica y se ubica en el espacio intermembrana, pero afdosado laxamente a la membrana interna. El NADH transfiere iones H+ y electrones dentro de la cadena transportadora de electrones.
Pgina 15
La secuencia de eventos: 1. Pasa los electrones a travs de el 1 complejo (NADH-Q reductasa) hasta la ubiquinona, los iones H+ traspasan la membrana hacia el espacio intermembrana. 2. el 2 complejo (citocromo c reductasa) trasnsfiere electrones desde la Q a el citocromo c, generando un nuevo bombeo de protones al exterior. 3. el 3 complejo es una citocromo c oxidasa, pasa los e- del citocromo c al oxgeno, el oxgeno reducido (1/2 O2-) toma dos iones H+ y forma H2O. Balance neto Los electrones entran a la CTE desde portadores tales como el NADH o el FADH, llegan a la "oxidasa terminal" (una oxgeno-reductasa) y se "pegan" al oxgeno. FOSFORILACION OXIDATIVA La fosforilacin oxidativa es un proceso metablico que utiliza energa liberada por la oxidacin de nutrientes para producir adenosn trifosfato (ATP). Se le llama as para distinguirla de otras rutas que producen ATP con menor rendimiento, llamadas "a nivel de sustrato". Se calcula que hasta el 90% de la energa celular en forma de ATP es producida de esta forma. Consta de dos etapas: en la primera, la energa libre generada mediante reacciones qumicas redox en varios complejos multiproteicos conocidos en su conjunto como cadena de transporte de electrones- se emplea para producir, por diversos procedimientos como bombeo, ciclos quinona/quinol o bucles redox, un gradiente electroqumico de protones a travs de una membrana asociada en un proceso llamado quimiosmosis. La cadena respiratoria est formada por tres complejos de protenas principales (complejo I,III, IV), y varios complejos "auxiliares", utilizando una variedad de donantes y aceptores de electrones. Los tres complejos se asocian en super complejos para canalizar las molculas transportadoras de electrones, la coenzima Q y el citocromo c, haciendo ms eficiente el proceso. La energa potencial de ese gradiente, llamada fuerza protn-motriz, se libera cuando se translocan los protones a travs de un canal pasivo, la enzima ATP sintasa, y se utiliza en la adicin de un grupo fosfato a una molcula de ADP para almacenar parte de esa energa potencial en los enlaces anhidro "de alta energa" de la molcula de ATP mediante un mecanismo en el que interviene la rotacin de una parte de la enzima
Pgina 16
a medida que fluyen los protones a travs de ella. En vertebrados, y posiblemente en todo el reino animal, se genera un ATP por cada 2,7 protones translocados. Algunos organismos tienen ATPasas con un rendimiento menor. Existen tambin protenas desacopladoras que permiten controlar el flujo de protones y generar calor desacoplando ambas fases de la fosforilacin oxidativa. Aunque las diversas formas de vida utilizan una gran variedad de nutrientes, casi todas realizan la fosforilacin oxidativa para producir ATP, la molcula que provee de energa al metabolismo. Esta ruta es tan ubicua debido a que es una forma altamente eficaz de liberacin de energa, en comparacin con los procesos alternativos de fermentacin, como la gluclisis anaerbica. Pese a que la fosforilacin oxidativa es una parte vital del metabolismo, produce una pequea proporcin de especies reactivas del oxgeno tales como superxido y perxido de hidrgeno, lo que lleva a la propagacin de radicales libres, provocando dao celular, contribuyendo a enfermedades y, posiblemente, al envejecimiento. Sin embargo, los radicales tienen un importante papel en la sealizacin celular, y posiblemente en la formacin de enlaces disulfuro de las propias protenas de la membrana interna mitocondrial. Las enzimas que llevan a cabo esta ruta metablica son blancas de muchas drogas y productos txicos que inhiben su actividad.
Pgina 17
SINTESIS DEL RENDIMIENTO ENERGETICO En clulas anaerobias A partir de una hexosa se generan 2ATP por cada triosa, dado que ocurren 2 fosforilaciones a nivel de sustrato. Como a partir de una hexosa se forman 2 triosas se producen 4 ATP. A su vez, se consumen 2 ATP desde la hexosa no foslorilada hasta fructosa 1,6P, de manera que el balance neto es de 2 ATP/hexosa. En clulas aerobias A partir de una hexosa se generan, igual que en clulas fermentativas 4 ATP por fosforilaciones a nivel de sustrato. En clulas aerbias el NADH.H que se genera en la gluclisis se reoxida y genera glicerol 3-P o malato. En el caso de la lanzadera del glicerol 3-P el poder reductor va a cadena respiratoria y genera 2 ATP por triosa. Como se producen 2 triosas por cada hexosa, se generan 4 ATP/hexosa por lanzadera de glicerol 3-P. En resumen se generan 4 ATP (fosforilacin a nivel de sustrato) + 4 ATP (lanzadera) = 8 ATP/hexosa. Como se consumen 2 ATP para producir la fructosa 1,6P el balance neto son 6 ATP/hexosa. Si la lanzadera fuera la del malato-oxalacetato se generan 3 ATP/ triosa, es decir, 6 ATP/hexosa. En este caso el balance neto es 8 ATP/hexosa. Mientras el grupo aldehdo se oxida, el NAD+ se reduce, lo que hace de esta reaccin una reaccin redox. El NAD+ se reduce por la incorporacin de algn [H+] dando como resultado una molcula de NADH de carga neutra
Pgina 18
REGULACIN REGULACIN ENZIMTICA
La gluclisis se regula enzimticamente en los tres puntos irreversibles de esta ruta, esto es, en la primera reaccin (G -- >G-6P), por medio de la hexoquinasa; en la tercera reaccin (F-6P --> F-1,6-BP) por medio de la PFK1(fosfofructoquinasa) y en el ltimo paso (PEP --> Piruvato) por la piruvato quinasa. La hexoquinasa es un punto de regulacin poco importante, ya que se inhibe cuando hay mucho G-6P en msculo. Es un punto poco importante ya que el G-6P se utiliza para otras vas. HQ: Inhibe G-6P
La PFK1 es la enzima principal de la regulacin de la gluclisis, acta como una llave de agua, si est activa cataliza muchas reacciones y se obtiene ms Fructosa 1,6 bisfosfato, lo que permitir a las enzimas siguientes transformar mucho piruvato. Si est inhibida, se obtienen bajas concentraciones de producto y por lo tanto se obtiene poco piruvato.
Esta enzima es controlada por regulacin alostrica mediante: Por un lado se activa gracias a niveles energticos elevados de ADP y AMP, inhibiendose en abundancia de ATP y citrato, y por otro se activa en presencia de un regulador generado por la PFK2 que es la Fructosa-2,6Bisfosfato (F-2,6-BP), que no es un metabolito ni de la glucolisis ni de la gluconeognesis, sino un regulador de ambas vas que refleja el nivel de glucagn en sangre.
Pgina 19
La lgica de la inhibicin y activacin son las siguientes: ATP: inhibe esta enzima pues si hay una alta concentracin de ATP entonces la clula no necesita generar ms.
Citrato: Si la concentracin de citrato es alta el Ciclo de Krebs va ms despacio de lo que el sustrato (acetil-CoA) llega para degradarse, y la concentracin de glucosa ser ms alta. En el Ciclo de Krebs se produce mucho NADH y FADH2, para que funcionen se han de reoxidar en la cadena de transporte electrnico creando gradiente de protones, si el gradiente no se gasta los coenzimas no se reoxidan y el Ciclo de Krebs se para. AMP, ADP: la alta concentracin de estas molculas implica que hay una carencia de ATP, por lo que es necesario realizar gluclisis, para generar piruvato y energa.
PFK1: Inhibe: ATP - Activa: ADP, AMP y F-2,6-BP. La piruvatoquinasa se regula distintamente segn el tejido en el que trabaje, pero en hgado se inhibe en presencia de ATP y Acetil Coenzima-A (Acetil-CoA), y se activa gracias de nuevo ante la F2,6-BP y la concentracin de fosfoenolpiruvato. PQ: Inhibe: ATP, A-CoA - Activa: PEP y F-2,6-BP REGULACIN POR INSULINA Al aumentar la glucosa en la sangre, despus de una comida, las clulas beta del pncreas estimulan la produccin de insulina, y sta a su vez aumenta la actividad de la glucocinasa en los hepatocitos. Las concentraciones altas de glucagon y las bajas de insulina disminuyen la concentracin intracelular de fructosa 2,6 bisfosfato. Esto trae por consecuencia la disminucin de la gliclisis y el aumento de la gluconeogensis. La insulina, secretada por las clulas- del pncreas, entra directamente al hgado por va de la vena porta, en donde ejerce efectos metablicos profundos. Estos efectos son la respuesta de la activacin del receptor de la insulina que pertenece a la clase de receptores de la superficie celular que tienen una actividad de tirosina cinasa intrnseca. El receptor de la insulina es un heterotetrmero de 2 sub-unidades extracelulares unidas por puentes bisulfuro a 2 sub-unidades transmembrana . Con relacin a la homeostasis de glucosa heptica, los efectos de la activacin del receptor son eventos especficos de fosforilacin que llevan a un incremento en el almacenamiento de glucosa con una disminucin concomitante en la secrecin de glucosa por el hgado a la circulacin
Pgina 20
como se esquematiza luego (solamente se representan aquellas respuestas en el nivel de fosforilacin de la sintasa de glicgeno y de la glicgeno fosforilasa). SNTESIS DE GLUCOSA POR GLUCOGNESIS OCURRE CUANDO LA RELACIN ATP/ADP ES ALTA La glucognesis corresponde a la va anablica que permite la sntesis de glucosa a partir de molculas no glucdicas como el lactato, piruvato, glicerol, as como algunos aminocidos e intermediarios del ciclo de Krebs. Esta va ocurre en algunos rganos como el hgado y el rin. En la glucognesis se evitan o saltean las reacciones irreversibles de la gluclisis: piruvato a PEP, fructosa 1,6 P a fructosa y glucosa 6P a glucosa. Estas reacciones constituyen las nicas diferentes a la guclisis. Para que estas reacciones tengan lugar la relacin ATP/ADP debe ser alta, de manera que la FFQ estar modulada negativamente y la piruvato carboxilasa positivamente. FUNCIONES Las funciones de la gluclisis son: La generacin de molculas de alta energa (ATP y NADH) como fuente de energa celular en procesos de respiracin aerbica (presencia de oxgeno) y fermentacin (ausencia de oxgeno). La generacin de piruvato que pasar al ciclo de Krebs, como parte de la respiracin aerbica. La produccin de intermediarios de 6 y 3 carbonos que pueden ser utilizados en otros procesos celulares. CATABOLISMO DE LA GLUCOSA A PIRUVIRATO La vida es un estado dinmico de equilibrio inestable, que, por lo mismo, requiere un consumo continuo de energa. Esta energa es extrada de los alimentos provistos por el medio: carbohidratos, lpidos y protenas, pero no puede ser utilizada si no es almacenada previamente en una molcula de ATP. El ATP est compuesto por la Adenosina, un nucletido (formado por adenina y ribosa) que tiene la propiedad de establecer tres enlaces consecutivos con grupos fosfato. El ltimo enlace, al hidrolizarse, desprende gran cantidad de energa libre, que es utilizada por la clula para sus procesos metablicos. Como resultado, se producen una
Pgina 21
molcula de ADP y una de fosfato, las que luego sern utilizadas para regenerar ATP, mediante una serie de procesos. Las clulas obtienen energa a travs de la oxidacin de los nutrientes, como la glucosa. Esa energa llamada ATP que el organismo necesita para su funcionamiento se produce en gran parte a partir de la glucosa, ya sea de forma circulante o extrayndola del glucgeno (su forma de almacenamiento). De este modo, la glucosa constituye la principal fuente de energa, y por algunos tejidos, como nica fuente de energa (como el corazn y el cerebro). El catabolismo es la fase de degradacin del metabolismo mediante la cual las molculas complejas se convierten en otras ms simples. Durante este proceso se produce oxidacin, liberacin de energa libre y reacciones de convergencia.
FINALIDAD DEL CATABOLISMO Obtencin de energa (ATP) que se utilizar para las funciones vitales: biosntesis, transporte activo y movimiento. Otras: por un lado encontramos la obtencin de coenzimas reducidos (NADH, FADH) que aportarn los electrones necesarios para la reduccin de sustratos en el anabolismo; y por otro la obtencin de algunos precursores metablicos necesarios para la sntesis de algunas molculas orgnicas en el anabolismo.
Pgina 22
BIBLIOGRAFIA
Textos 1. LYNCH,M. (1991). Mtodos de Laboratorio. Tercera edicin. Editorial: Interamericana, Mxico,D.F. 2. DEVLIN, M. (1993). Textbook of Biochemistry with clinical correlations. Editorial: Willey-Liss. New York. 3. LEHNINGER, Albert L. (1991). Bioqumica. Las Bases Moleculares de la Estructura y Funcin Celular. 2da. Edicin. Editorial: Ediciones Omega S, A. Barcelona. 4. GONZLEZ, J. & SNCHEZ, A. (2000). Bioqumica Clnica.1. Edicin. Editorial: Mc Graw Hill- Interamericana. 5. Mathews, C & Van Holde, K. (1998). Bioqumica. 1a. edicin. Editorial: Mc Graw Hill Interamericana. Madrid-Espaa. 6. MURRAY, R. (1992).Bioqumica de Harper. 14a. edicin. Editorial: El Manual Moderno. 7. MCKEE, J. (2003). Bioqumica: la base molecular de la vida. Editorial Interamericana. Madrid- Espaa. 8. MCPHEE, S. (1998). Fisiopatologa Mdica.1a. edicin. Editorial: El Manual Moderno. 9. HARPER, A. (2004). Bioqumica ilustrada. Editorial: El manual moderno. Barcelona. Internet http://iescarin.educa.aragon.es https://docs.google.com/viewer?a=v&q=cache:LNjJV2BkMwUJ:ww w.fagro.edu.uy/~bioquimica/docencia/material%2520nivelacion/GL UCOLISIS.pdf+glucolisis&hl=es&gl=ec&pid=bl&srcid=ADGEESitpcoqGVqF1wiH_mtBqijj01HhGYolHR5IYWQTRdXNe3RVfHjX1tgHmbu ESOHwr6WZIt9H2u49ZIEgUcyIiu7AtSBqlbTu7ZM2hVwdfmMFMnzSt SQGA7FgUAiJ4GHxWLp3qXx&sig=AHIEtbTXd4ZZezv8ZkBDL0JUbCo RUgewNg http://www.iesbanaderos.org/html/departamentos/biogeo/Apuntes/Bio/T%2012%20Cat_Ana/2%20Catabolismo%20Gluci dos.htm http://es.wikipedia.org/wiki/Gluc%C3%B3lisis
Pgina 23
You might also like
- GlucogenogénesisDocument2 pagesGlucogenogénesisJose FranciscoNo ratings yet
- Carta de RecomendaciónDocument1 pageCarta de RecomendaciónPAúl Casa Ortiz0% (1)
- 05.e Via Del Acido GlucuronicoDocument13 pages05.e Via Del Acido GlucuronicoRony Rosete100% (1)
- Informe 4 BioquimicaDocument14 pagesInforme 4 BioquimicaVelasquez NeiserNo ratings yet
- HeteroglucanosDocument3 pagesHeteroglucanosMarisol RodriguezNo ratings yet
- Transporte y Almacenamiento de LípidosDocument25 pagesTransporte y Almacenamiento de LípidosGreissy Campos Cabrera50% (2)
- Transaminacion y Desaminacion - Itzayana SandovalDocument3 pagesTransaminacion y Desaminacion - Itzayana SandovalItza SPNo ratings yet
- PRACTICA 19. Digestión de Enzimas Pancréticas Sobre CaseinaDocument3 pagesPRACTICA 19. Digestión de Enzimas Pancréticas Sobre CaseinaGaby Lisbeth LlhNo ratings yet
- Inhibidores y Desacopladores de La Cadena RespiratoriaDocument17 pagesInhibidores y Desacopladores de La Cadena RespiratoriaAndy ST80% (5)
- Informe Laboratorio Glicólisis y FermentacionDocument6 pagesInforme Laboratorio Glicólisis y FermentacionFernanda M. EspañaNo ratings yet
- Efecto Del PH Sobre La Glucosa OxidasaDocument6 pagesEfecto Del PH Sobre La Glucosa OxidasaJose Narciso Panta FiestasNo ratings yet
- Reporte 7 CatalasaDocument3 pagesReporte 7 CatalasaAntonio BarrerasNo ratings yet
- Informe de Glucogenolisis Uu12Document24 pagesInforme de Glucogenolisis Uu12dieg0280% (1)
- Exposición GlucolisisDocument17 pagesExposición GlucolisisDiana GomezNo ratings yet
- Informe de Glucolisis Uu12Document13 pagesInforme de Glucolisis Uu12dieg028100% (1)
- Regulación de La GlucólisisDocument3 pagesRegulación de La Glucólisisfrancisco lozano gomezNo ratings yet
- Practica 04 Inhibidores de Cadena RespiratoriaDocument3 pagesPractica 04 Inhibidores de Cadena Respiratoriafelix50% (2)
- Caso 4 Deficiencia de FumarasaDocument20 pagesCaso 4 Deficiencia de FumarasaEric José Rodríguez Camarena50% (2)
- Digestión y Absorción de Hidratos de CarbonoDocument7 pagesDigestión y Absorción de Hidratos de CarbonoSTUDY ACCOUNTNo ratings yet
- BIOQUIMICADocument6 pagesBIOQUIMICAMarcos ChávezNo ratings yet
- Degradacion de La SacarosaDocument42 pagesDegradacion de La Sacarosamusicon17No ratings yet
- Discusión y Resultados CarbohidratosDocument4 pagesDiscusión y Resultados CarbohidratosAnonymous iJoRozpP33% (3)
- Biologia Discusiones Amilasa SalivalDocument1 pageBiologia Discusiones Amilasa SalivalMadara SantosNo ratings yet
- Marco Teórico de Intolerancia A La LactosaDocument3 pagesMarco Teórico de Intolerancia A La LactosaAlexandra ReyesNo ratings yet
- Informe Bioquimica PapaDocument10 pagesInforme Bioquimica PapaGerardo Mogollon RamosNo ratings yet
- Metabolismo Del GlucogenoDocument17 pagesMetabolismo Del GlucogenoTeresaRossanaMoscolZarateNo ratings yet
- Metabolitos IntermediariosDocument3 pagesMetabolitos IntermediariosFelipe ChimborazoNo ratings yet
- Reacciones Anapleróticas - Wikipedia, La Enciclopedia Libre PDFDocument5 pagesReacciones Anapleróticas - Wikipedia, La Enciclopedia Libre PDFRamon Edickson Placencia EncarnacionNo ratings yet
- 11 GluconeogénesissDocument13 pages11 GluconeogénesissEdmy Shasary Gutierrez Narvaez100% (2)
- ENZIMAS II TranscripcionDocument9 pagesENZIMAS II Transcripcionapi-369665675% (4)
- Factores Físicos y Químicos Que Alteran La Función y Estructura de Las ProteínasDocument3 pagesFactores Físicos y Químicos Que Alteran La Función y Estructura de Las ProteínasCristian Contreras100% (2)
- Informe de Enzima CatalasaDocument4 pagesInforme de Enzima CatalasaJulio RiveraNo ratings yet
- Intercambio de Líquidos y Electrolitos Entre Los Medios ExteDocument16 pagesIntercambio de Líquidos y Electrolitos Entre Los Medios ExteLesly Huarcaya CondoriNo ratings yet
- Tabla ComparativaDocument6 pagesTabla ComparativaAna Maria Ambriz Castillo57% (7)
- Marco TeoricoDocument8 pagesMarco TeoricoSebastian AlmeidaNo ratings yet
- Acción de La Soya Sobre La Digestión de La ProteínaDocument1 pageAcción de La Soya Sobre La Digestión de La ProteínaJhoel Zuñiga Luna100% (2)
- Inhibidores Del Ciclo de KrebsDocument4 pagesInhibidores Del Ciclo de Krebsingjuferdima2240No ratings yet
- Investigacion Formativa de ProteinasDocument51 pagesInvestigacion Formativa de ProteinasFátima Sanchez Castillo100% (1)
- Bioqui 2Document4 pagesBioqui 2Arturo Basantez100% (1)
- Demostración de La Degradación Del Almidón y Sacarosa Por Alfa Amilasa y SacarasaDocument16 pagesDemostración de La Degradación Del Almidón y Sacarosa Por Alfa Amilasa y SacarasaNayelly Moreno GarridoNo ratings yet
- Bioquimica Practica N 5Document10 pagesBioquimica Practica N 5Bryan Medrano0% (1)
- Determinación de Oxido Reductasas en Material BiológicoDocument16 pagesDeterminación de Oxido Reductasas en Material Biológicoluciaelena777No ratings yet
- Metabolismo Del GlucogenoDocument30 pagesMetabolismo Del GlucogenoMAURICIO AUGUSTO ORELLANA CARDOZO100% (1)
- Marco TeóricoDocument2 pagesMarco TeóricoLEO100% (2)
- Importancia de Las Sales Biliares en La Digestión de Los LipidosDocument2 pagesImportancia de Las Sales Biliares en La Digestión de Los LipidosMilhy QP83% (18)
- Conclusiones CatalasaDocument1 pageConclusiones CatalasaAnonymous Xpw5D0dKbyNo ratings yet
- Agua y Sales MineralesDocument3 pagesAgua y Sales MineralesleperoteroNo ratings yet
- PolisacaridosDocument13 pagesPolisacaridosCindy Ramos Qs100% (1)
- Informe de Laboratorio de La CatalasaDocument5 pagesInforme de Laboratorio de La CatalasaJorge Barrios DiazNo ratings yet
- DBCA (Autoguardado)Document24 pagesDBCA (Autoguardado)Michael Zevallos RamosNo ratings yet
- Glucogeno Objetivos, Marco TeoricoDocument3 pagesGlucogeno Objetivos, Marco TeoricoBeronica LeonNo ratings yet
- Que Es La DecantaciónDocument4 pagesQue Es La Decantaciónpooy088% (8)
- Discusión y Resultados Practica 7Document4 pagesDiscusión y Resultados Practica 7CharlieTitoValleLeon50% (2)
- Accion de Las Ensimas Pancreaticas Sobre El SuccionatoDocument10 pagesAccion de Las Ensimas Pancreaticas Sobre El SuccionatoAnonymous QLhG8GdNo ratings yet
- Regulación de La GlucólisisDocument6 pagesRegulación de La GlucólisisLorik90No ratings yet
- Gomezniño Adriana Ejerciciosu1 B4aDocument6 pagesGomezniño Adriana Ejerciciosu1 B4aAdriana GomezNo ratings yet
- CONCLUSIÓN de PeroxisomasDocument1 pageCONCLUSIÓN de PeroxisomaschristianNo ratings yet
- Informe #4Document9 pagesInforme #4Wilder OblitasNo ratings yet
- CUESTIONARIOintolerancia A La LactosaDocument4 pagesCUESTIONARIOintolerancia A La LactosaFernanda Colque100% (2)
- Discuciones, Conclusiones y Recomendaciones de Las Practicas de Carbohidratos y Proteinas de Quimica Organica de SAN MARCOSDocument5 pagesDiscuciones, Conclusiones y Recomendaciones de Las Practicas de Carbohidratos y Proteinas de Quimica Organica de SAN MARCOSPaulo PPajueloNo ratings yet
- GlucólisisDocument16 pagesGlucólisisEliseo CMNo ratings yet
- GlucólisisDocument14 pagesGlucólisisCesar RenteriaNo ratings yet
- Final Thesis SubmissionDocument225 pagesFinal Thesis SubmissionPAúl Casa OrtizNo ratings yet
- Hallmer2016 EsDocument36 pagesHallmer2016 EsPAúl Casa OrtizNo ratings yet
- Endo Anatomia Dientes AnterioresDocument53 pagesEndo Anatomia Dientes AnterioresrichardksNo ratings yet
- Protocolo Manejo de PinchazosDocument14 pagesProtocolo Manejo de PinchazosPAúl Casa Ortiz0% (1)
- Porphyromonas Treponema and Mogibacterium Promote IL8 IFN TNF Based Pro Inflammation in Patients With Medication Related Osteonecrosis of The JawDocument8 pagesPorphyromonas Treponema and Mogibacterium Promote IL8 IFN TNF Based Pro Inflammation in Patients With Medication Related Osteonecrosis of The JawPAúl Casa OrtizNo ratings yet
- 436-Artículo CompletoDocument8 pages436-Artículo CompletoGabriela SantiagoNo ratings yet
- Modificaciones PPRDocument9 pagesModificaciones PPRVanesa Sigueñas CajoNo ratings yet
- Protocolos OdontologicosDocument256 pagesProtocolos OdontologicosPatty Calapi50% (2)
- Insu-Renal Caso ClinicoDocument51 pagesInsu-Renal Caso ClinicoPAúl Casa OrtizNo ratings yet
- Bioetica TrabajoDocument6 pagesBioetica TrabajoPAúl Casa OrtizNo ratings yet
- Hiposalivacion Xerostomia Definicion IbañezDocument8 pagesHiposalivacion Xerostomia Definicion IbañezPAúl Casa OrtizNo ratings yet
- Buen Trato 1 EneroDocument3 pagesBuen Trato 1 EneroPAúl Casa OrtizNo ratings yet
- Sistema Nervioso AutonomoDocument4 pagesSistema Nervioso AutonomoPAúl Casa OrtizNo ratings yet
- Levantamiento de ColgajoDocument10 pagesLevantamiento de ColgajoPAúl Casa OrtizNo ratings yet
- Insu-Renal Caso ClinicoDocument51 pagesInsu-Renal Caso ClinicoPAúl Casa OrtizNo ratings yet
- Tesina LeasingDocument54 pagesTesina LeasingAlberto GuevaraNo ratings yet
- MONOGRAFIA Radio Extraorales TerminadaDocument43 pagesMONOGRAFIA Radio Extraorales TerminadaPAúl Casa Ortiz100% (1)
- Instrumntocion en Cirugia BUCALDocument30 pagesInstrumntocion en Cirugia BUCALPAúl Casa OrtizNo ratings yet
- Caratula CIRUDocument2 pagesCaratula CIRUPAúl Casa OrtizNo ratings yet
- RESUMEN Tumores OdontogenicosDocument8 pagesRESUMEN Tumores OdontogenicosPAúl Casa OrtizNo ratings yet
- Administracion de Recursos HumanosDocument33 pagesAdministracion de Recursos HumanosPAúl Casa OrtizNo ratings yet
- Intervencion QuirurgicaDocument27 pagesIntervencion QuirurgicaPAúl Casa OrtizNo ratings yet
- Incision en Cirugia Oral PCODocument16 pagesIncision en Cirugia Oral PCOPAúl Casa Ortiz100% (1)
- Marcas de Sellantes Cario Paul CoDocument10 pagesMarcas de Sellantes Cario Paul CoPAúl Casa OrtizNo ratings yet
- Brazil EnglishDocument1 pageBrazil EnglishPAúl Casa OrtizNo ratings yet
- Protocolos Farmacológicos en Diferentes Especialidades OdontologicasDocument87 pagesProtocolos Farmacológicos en Diferentes Especialidades OdontologicasPAúl Casa OrtizNo ratings yet
- Antivirales Paul CasaDocument89 pagesAntivirales Paul CasaPAúl Casa OrtizNo ratings yet
- Nuevos Procedimeintos en Anestesia LocalDocument9 pagesNuevos Procedimeintos en Anestesia LocalPAúl Casa OrtizNo ratings yet
- Marcas de Sellantes Cario Paul CasaDocument10 pagesMarcas de Sellantes Cario Paul CasaPAúl Casa OrtizNo ratings yet
- Sistemas Energeticos en Las Carreras de VelocidadDocument6 pagesSistemas Energeticos en Las Carreras de VelocidadEDGAR FLORES SORIANo ratings yet
- Bioquímica Maqueta 2Document5 pagesBioquímica Maqueta 2J Mora GañanNo ratings yet
- Clase Glucólisis y FermentaciónDocument30 pagesClase Glucólisis y FermentaciónvalentinaNo ratings yet
- Metabolismo de CH BDocument84 pagesMetabolismo de CH BJaviera Mendoza CañeteNo ratings yet
- El Sistema CirculatorioDocument4 pagesEl Sistema CirculatorioLazaro VazquezNo ratings yet
- Práctica 7: Ruidos CardíacosDocument12 pagesPráctica 7: Ruidos CardíacosDiana Gomez100% (1)
- Actividades de CirculacionDocument17 pagesActividades de CirculacionJusta Carmen Concha RevillaNo ratings yet
- 2 Metabolismo 1Document33 pages2 Metabolismo 1juan carlosNo ratings yet
- Foro Sistema CardiovascularDocument1 pageForo Sistema CardiovascularKimberly OrtizNo ratings yet
- Seminario Cadena RespiratoriaDocument3 pagesSeminario Cadena RespiratoriaIvette Jossain Aguilar RamírezNo ratings yet
- Cardiaco 1Document41 pagesCardiaco 1Valeria ValentinaNo ratings yet
- Ciclo de CoriDocument7 pagesCiclo de CoriJeanette PaulinaNo ratings yet
- (2, 4) DinitrofenolDocument1 page(2, 4) DinitrofenolIsmari FloNo ratings yet
- Fisio Circulatorio VirtualDocument55 pagesFisio Circulatorio VirtualGreyss GamboaNo ratings yet
- Presentacion de Glucolisis Umg 2023Document46 pagesPresentacion de Glucolisis Umg 2023xenia poma reyesNo ratings yet
- Degradación de Carbohidratos Lipidos y ProteinasDocument22 pagesDegradación de Carbohidratos Lipidos y ProteinasSunflower HanNo ratings yet
- EiouDocument27 pagesEiouthais pizarro contrerasNo ratings yet
- Sistema Circulatorio-CUARTODocument3 pagesSistema Circulatorio-CUARTOParis MatcNo ratings yet
- SEMINARIO 4. Volumen Minuto CardiacoDocument22 pagesSEMINARIO 4. Volumen Minuto CardiacoLuz Angélica Aredo AlvaNo ratings yet
- Fisiologia Del Ciclo Cardiaco y BombeoDocument23 pagesFisiologia Del Ciclo Cardiaco y BombeoTamara Ruiz MaureiraNo ratings yet
- Frecuencia Cardíaca - Wikipedia, La Enciclopedia LibreDocument7 pagesFrecuencia Cardíaca - Wikipedia, La Enciclopedia Libreanthny7421No ratings yet
- Órganos Principales Del Sistema Circulatorio para Tercero de PrimariaDocument4 pagesÓrganos Principales Del Sistema Circulatorio para Tercero de PrimariaMaria Lna Medina100% (1)
- (4-Farm) Guia de Lectura CardiovascularDocument6 pages(4-Farm) Guia de Lectura CardiovascularEugenia EspinozaNo ratings yet
- Respiracion CelularDocument17 pagesRespiracion CelularEfren Dario Aramendiz50% (2)
- HEMODINAMIADocument35 pagesHEMODINAMIAAstrid EligioNo ratings yet
- Reacciones de La GlucólisisDocument3 pagesReacciones de La GlucólisisKenia HernándezNo ratings yet
- Guía de Ejercicios Unidad 2Document4 pagesGuía de Ejercicios Unidad 2jeremiasandreeNo ratings yet
- Beta OxidacionDocument6 pagesBeta Oxidacionsdfdvdf100% (1)
- Cómo Fabrican Atp Las CélulasDocument55 pagesCómo Fabrican Atp Las CélulasValmore Jose BermudezNo ratings yet