Professional Documents
Culture Documents
Jurnal Defisiensi Vitamin D Dan Rakhitis
Uploaded by
Wildan SaputraOriginal Description:
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Jurnal Defisiensi Vitamin D Dan Rakhitis
Uploaded by
Wildan SaputraCopyright:
Available Formats
Kebangkitan Defisiensi Vitamin D dan Rakhitis
Momok epidemi rakhitis pada abad ke-19 disebabkan oleh kekurangan vitamin D akibat paparan sinar matahari yang tidak memadai dan menyebabkan retardasi pertumbuhan, kelemahan otot, rangka deformitas, hipokalsemia, tetani, dan kejang. Dukungan dari paparan sinar matahari yang masuk akal dan fortifikasi susu dengan vitamin D mengakibatkan hampir tuntasnya pemberantasan penyakit ini. Vitamin D (dimana D mewakili D2 atau D3) secara biologis disimpan dan dimetabolisme di hati untuk 25-hydroxyvitamin D [25 (OH) D], bentuk sirkulasi utama vitamin D yang digunakan untuk menentukan status vitamin D. 25 (OH) D adalah diaktifkan dalam ginjal untuk 1,25-dihydroxyvitamin D [1,25 (OH) 2D], yang mengatur kalsium, fosfor, dan metabolisme tulang. Kekurangan vitamin D telah kembali menjadi epidemi pada anak-anak, dan rakitis telah menjadi isu kesehatan global. Selain kekurangan vitamin D, kalsium kekurangan dan gangguan yang diperoleh dan diwariskan vitamin D, kalsium, dan fosfor menyebabkan rakhitis metabolisme. Tinjauan ini meringkas peran vitamin D dalam pencegahan rakhitis dan pentingnya dalam kesehatan secara keseluruhan dan kesejahteraan bayi dan anak.
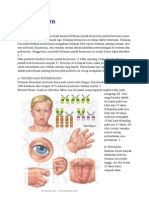
Perspektif sejarah Pada pertengahan 1600-an, kebanyakan anak yang tinggal di kotakota industri yang penuh sesak dan tercemar dari utara Eropa mengalami deformasi tulang yang parah. penyakit ini ditandai dengan retardasi pertumbuhan, pembesaran epiphyses tulang panjang, deformitas kaki,
tulang belakang melengkung, tulang rusuk menonjol, dan otot lemah serta datar (1, 2) (Gambar (Gambar1) .1). Di bagian akhir abad ke-19, otopsi penelitian yang dilakukan di Boston dan Leiden, Belanda, menunjukkan bahwa 80-90% anak-anak menderita rakhitis. Pada 1822, Sniadecki (3) mengakui pentingnya paparan sinar matahari untuk pencegahan dan penyembuhan rakhitis. Palm (4) pengamatan ini diperpanjang pada tahun 1890 dan mempromosikan penggunaan sistemik mandi matahari untuk mencegah rakhitis. Pada tahun 1919, Huldschinski (5, 6) menemukan bahwa mengekspos anakanak untuk radiasi dari matahari kuarsa lampu (merkuri lampu busur) atau lampu busur karbon selama satu jam 3 kali seminggu efektif dalam mengobati rakhitis, seperti yang ditunjukkan oleh peningkatan yang ditandai dalam mineralisasi kerangka, terutama ujung-ujung tulang panjang, yang terlihat dari hasil x-ray (Gambar (Figure2) .2). Sebuah kelompok studi terhadap anak-anak yang tidak terkena radiasi UV menunjukkan hanya sedikit perbaikan (6). Dia menyimpulkan bahwa paparan radiasi UV adalah "sempurna obat" terhadap semua bentuk rakhitis pada anak-anak. Dua tahun kemudian, Hess dan Unger (7) meneliti 7 anak rachitic di New York City untuk periode yang bervariasi dari sinar matahari dan melaporkan peningkatan yang ditandai dalam rakhitis setiap anak yang dibuktikan dengan kalsifikasi dari epiphyses.
Pada tahun 1918, Mellanby dkk. (8) mencegah rakhitis pada anak anjing dengan minyak ikan cod. McCollum et al. (9) menyebutkan faktor ini sebagai nutrisi yang baru bernama vitamin D. Hess dan Weinstock (10) dan Steenbock dan Black (11) mengamati bahwa iradiasi UV berbagai makanan dan minyak dikenal sebaga aktivitas antirachitic. Hal ini menyebabkan peningkatan aktivitas antirachitic susu dengan mengekspos susu untuk radiasi UV atau memberi makan sapi dengan iradiasi UV ragi. Setelah vitamin D struktural diidentifikasi dan disintesis secara kimiawi
dari ragi, langsung ditambahkan ke susu pada standar 400 IU (1 IU = 25 ng) per liter (12, 13). Ia berpikir bahwa vitamin D yang diperoleh dari ragi iradiasi adalah vitamin D yang sama yang diproduksi di kulit. Namun, ketika diamati bahwa vitamin D dari ragi iradiasi memiliki aktivitas antirachitic sedikit pada ayam, sedangkan minyak hati ikan cod efektif, disimpulkan bahwa vitamin D diproduksi di kulit harus berbeda (14). Vitamin D diisolasi dan diidentifikasi dari kulit babi dan terbukti berasal dari 7-dehydrocholesterol (1, 2, 14). Untuk membedakan dua vitamin D, vitamin D dari ragi yang disebut vitamin D2 dan satu dari babi dan manusia kulit vitamin D3 (1, 2). Photobiology dari vitamin D3 Sinar matahari direkomendasikan sebagai metode terapi untuk mencegah rakhitis pada bayi, dan penjelasan rinci diterbitkan dalam Folder Biro Amerika Serikat Anak pada tahun 1931 (13, 14). Hal itu diakui bahwa di zona beriklim sedang, sinar matahari adalah lemah dalam sifat antirachitic di musim dingin, dan dengan demikian, direkomendasikan bahwa anak-anak akan terkena radiasi UV dari busur merkuri atau lampu busur karbon di musim dingin (5, 6, 13 , 14) (Gambar (Figure2) .2). Selama paparan sinar matahari, ultraviolet B (UVB) radiasi (290-315 nm) diserap oleh 7-dehydrocholesterol di kulit untuk membentuk previtamin D3 (1, 15). Previtamin D3 (1, 15) secara inheren tidak stabil dan cepat mengkonversi dengan proses suhu tergantung dengan vitamin D3 (Gambar (Figure3) .3). Setelah terbentuk, itu dikeluarkan dari sel kulit ke dalam ruang ekstraselular, di mana ia ditarik ke tempat tidur kapiler kulit oleh protein pengikat vitamin D-(DBP) (1). Efisiensi sintesis vitamin D3 di kulit tergantung pada jumlah foton yang menembus ke UVB epidermis. Peningkatan pigmentasi kulit melanin (16) dan aplikasi topikal dari tabir surya (17), yang keduanya efisien menyerap foton UVB, nyata dapat mengurangi lebih dari 90% produksi
vitamin D3. Paparan berlebihan sinar matahari tidak dapat menyebabkan keracunan vitamin D karena sinar matahari akan menghancurkan kelebihan vitamin D3 yang diproduksi di kulit (18, 19). Kebanyakan UVB foton dari matahari diserap oleh ozon stratosfer. Peningkatan hasil sudut matahari puncak dalam panjang jalur meningkat untuk foton UVB untuk bepergian, dan ini menjelaskan mengapa di lintang yang lebih tinggi (di atas ~ 35 lintang ), sangat sedikit, jika ada, vitamin D3 diproduksi di kulit dari November sampai Maret (19, 20). Metabolisme vitamin D dan perannya dalam metabolisme kalsium dan fosfor Vitamin D2 dan vitamin D3 (D mewakili baik D2 atau D3) yang berasal dari suplemen, makanan yang diperkaya, dan ikan dicerna dari makanan (Tabel (Table1) 1) dimasukkan ke dalam kilomikron dan diserap ke dalam sistem limfatik. Dari sini mereka memasuki sirkulasi, di mana mereka terikat pada DBP dan lipoprotein (1, 20-22). Vitamin D dilepaskan dari DBP ke hati dan mengalami hidroksilasi pada C-25 oleh vitamin D-25hydroxylases (25-OHase, juga dikenal sebagai CYP27A1,, CYP3A4 CYP2R1, CYP2J3) untuk 25-hidroksivitamin D [25 (OH ) D] (20-22) (Gambar (Figure3) .3). 25 (OH) D adalah bentuk beredar utama vitamin D yang diukur untuk menentukan seseorang status vitamin D karena memiliki waktu paruh dalam sirkulasi dari 2 minggu dan itu berkorelasi dengan hiperparatiroidisme sekunder, rakhitis, dan osteomalacia (20, 2224). 25 (OH) D adalah terikat untuk DBP, dan kompleks ini mengikat megalin pada membran plasma sel tubulus ginjal dan diangkut ke dalam sel (20, 22). Begitu masuk, 25 (OH) D adalah dilepaskan dan dikonversi dalam mitokondria oleh 25-hidroksivitamin D-1-hidroksilase [1-OHase, juga dikenal sebagai CYP27B1] untuk membentuk 1,25-dihydroxyvitamin D [1,25 (OH ) 2D]. 1,25 (OH) 2D adalah bentuk biologis aktif vitamin D yang bertanggung jawab untuk menjaga homeostasis kalsium dan fosfor. Ia menyelesaikan ini dengan berinteraksi dengan reseptor nuklirnya,
reseptor vitamin D (VDR) dalam sel-sel usus kecil (22, 25). The 1,25 (OH) 2D struktur kompleks-VDR dengan asam retinoat X reseptor (RXR) dalam nukleus. The 1,25 (OH) 2D-VDR-RXR kompleks mengikat unsur vitamin D-responsif (VDRE) untuk saluran kalsium epitel (22, 25). Ekspresi yang meningkat dari saluran kalsium memungkinkan lebih banyak kalsium masuk ke dalam sel, di mana vitamin D-kalsium bergantung-binding protein calbindin 9k membantu translokasi kalsium ke dalam aliran darah. 1,25 (OH) 2D juga meningkatkan penyerapan fosfor dalam usus kecil (1, 22, 25). Ketika diet kalsium tidak memadai, vitamin D membantu
mempertahankan homeostasis kalsium dengan berinteraksi dengan VDR pada osteoblas untuk menginduksi ekspresi protein membran plasma aktivator reseptor NF-kB ligan (RANKL). Para RANK pada membran plasma mengikat preosteoclasts RANKL, yang menginduksi preosteoclast untuk menjadi osteoklas matang (20, 22, 26). Para osteoklas matang melepaskan asam klorida dan kolagenase untuk melarutkan tulang dan melepaskan kalsium berharga dan toko fosfor ke dalam sirkulasi. Dengan demikian, fungsi fisiologis utama vitamin D adalah untuk mempertahankan kalsium serum dan kadar fosfor dalam kisaran fisiologis normal untuk mendukung fungsi yang paling metabolisme, transmisi neuromuskular, dan mineralisasi tulang (1, 20, 22, 24) (Gambar (Figure3). 3). Vitamin D dan kekurangan kalsium sebagai penyebab rakhitis Kekurangan vitamin D adalah penyebab paling umum dari rakhitis. Kekurangan vitamin D mencegah penyerapan kalsium efisien dan fosfor. Dalam keadaan kekurangan vitamin D-, hanya 10-15% dari kalsium diet dan 50-60% fosfor makanan diserap. Penyerapan kalsium yang buruk menyebabkan penurunan serum kalsium terionisasi tingkat. Hal ini segera diakui oleh sensor kalsium dalam kelenjar paratiroid, mengakibatkan peningkatan dalam ekspresi, sintesis, dan sekresi hormon paratiroid
(PTH) (1, 20, 22, 27). PTH menghemat kalsium dengan meningkatkan reabsorpsi tubular kalsium baik di tubulus proksimal dan distal rumit. PTH, seperti 1,25 (OH) 2D, meningkatkan ekspresi RANKL pada osteoblas untuk meningkatkan produksi osteoklas matang untuk memobilisasi kalsium dari toko kerangka. PTH juga menurunkan reabsorpsi fosfor dalam ginjal, menyebabkan hilangnya fosfor ke dalam urin (Gambar (Figure4) .4). Tingkat kalsium serum biasanya normal pada bayi Dkekurangan vitamin atau anak. Namun, tingkat serum fosfor rendah, sehingga ada tidak memadai kalsium-fosfor produk, yang diperlukan untuk termineralisasi dengan osteoid ditetapkan oleh osteoblas (1, 20, 22, 24, 28) (Gambar (Figure4) .4) . Jadi, biasanya, bayi dengan defisiensi vitamin D-rakitis memiliki tingkat kalsium yang normal dalam serum, rendah yang normal atau rendah puasa kadar serum fosfor, peningkatan kadar fosfatase alkali, dan rendah 25 (OH) D tingkat (<15 ng / ml) (23, 28-31) (Tabel (Tabel 2) .2). Hiperparatiroidisme sekunder yang merangsang ginjal untuk menghasilkan 1,25 (OH) 2D, dan dengan demikian, 1,25 (OH) 2D tingkat normal atau sering meningkat, yang mengapa pengukuran 1,25 (OH) 2D tidak ada nilainya dalam menentukan keadaan kekurangan vitamin D (24). Hanya ketika toko kalsium dalam kerangka benar-benar habis akan bayi atau anak menjadi hypocalcemic. Kekurangan vitamin D menyebabkan mineralisasi yang buruk global kerangka. Klinis dan manifestasi tulang radiologi mendominasi di daerah pertumbuhan tulang yang cepat, termasuk epiphyses tulang panjang dan persimpangan costochondral (5, 6, 12-14, 30-32). Inilah sebabnya mengapa kebanyakan rakhitis diamati sebelum usia 18 bulan, dengan frekuensi maksimum antara usia 4 dan 12 bulan. Kelainan rangka biasanya merupakan hasil dari lama rakhitis. Hipertrofi dari sambungan costochondral mengarah ke manik-manik dan klasik rachitic rosario yang berlangsung dengan involusi dari tulang rusuk dan tonjolan sternum (dada merpati) dan resesi dari sambungan costochondral dan depresi
menyebabkan melintasi alur Harrison. Setelah anak mulai berdiri, gravitasi mendorong pada hasil baik anggota tubuh bagian bawah ke dalam (genu valgum) atau luar (genu varum) tibialis dan femoralis membungkuk. Tarik otot juga bisa menyebabkan kelainan bentuk tulang pada tungkai atas dan bawah baik bahkan sebelum bayi mulai berjalan. Otot traksi pada tulang rusuk melunak bertanggung jawab untuk deformasi dada, menyebabkan pectus carinatum, asimetri toraks, dan pelebaran dasar dada. Pelunakan dari daerah oksipital (craniotabes rachitic), jahitan membesar dan fontanelles, menutup keterlambatan fontanelles, dan oksipital atau parietal merata dapat diamati (5, 6, 12, 13, 30-32) (Gambar (Gambar1) .1) . Perkembangan gigi terganggu, dengan letusan tertunda, enamel hipoplasia, dan karies gigi dini (12-14). Struktur tulang panggul yang diratakan pada anak-anak rachitic. Karena tingginya insiden morbiditas bayi dan ibu dan kematian pada wanita rachitic, anak-anak sering disampaikan oleh bagian raja (1, 2). Extraskeletal manifestasi yang terkait dengan timbal hipokalsemia tetani untuk, kejang, laryngospasm, dan myocardiopathy hypocalcemic dan kematian (6, 12-14, 32). Sering ada tertunda perkembangan motorik dengan hipotonia tanpa adanya hipokalsemia. Kelemahan otot-otot dada bersama dengan pelunakan tulang rusuk hasil dalam cacat ventilasi dengan obstruksi pernapasan dan infeksi. Pada anak yang lebih tua dan remaja, gejala serupa dengan yang diamati pada orang dewasa osteomalacia, termasuk nyeri tulang, gaya berjalan terhuyung-huyung, dan kelelahan, mungkin ada (12-14, 24, 30-32). Gangguan hematologi yang sering diamati dalam rakhitis umum, termasuk anemia hipokromik dan Von langka Jacksch-Luzet sindrom. Sindrom ini dikaitkan dengan anemia berat dan profil leukemia myeloid kronis dengan eritroblastosis, leukositosis, myelocytosis, dan myeloblastosis mungkin. Limpa dan hati dapat diperbesar sebagai akibat dari hematopoiesis extramedullary.
Sumsum tulang adalah hipoplasia. Sindrom ini sering disembuhkan dengan terapi sederhana vitamin D (31).
Kekurangan kalsium yang parah dapat menyebabkan rakhitis pada banyak cara yang sama seperti kekurangan vitamin D (32-35). Asupan kalsium diet sangat rendah menyebabkan penurunan kalsium terionisasi dan hiperparatiroidisme sekunder. Hal ini menyebabkan cacat mineralisasi dalam kerangka yang menghasilkan penghambatan pertumbuhan dan banyak dari manifestasi tulang terlihat pada kekurangan vitamin D, tetapi ini keparahan yang lebih besar karena hypocalcemia (31-35) (Gambar (Figure4). Asupan kalsium tidak memadai selama trimester ke-3 kehamilan dapat menyebabkan defisit kalsium yang serius dalam kerangka janin yang cepat sedang mineralisasi selama 7 minggu terakhir di dalam rahim. Biasanya pada 28 minggu, 100 mg / d kalsium yang disimpan dalam rangka, sedangkan pada 35 minggu 350 mg / d yang disimpan (30, 31, 36). Oleh karena itu, susu ibu mengandung 240-340 mg / l kalsium tidak dapat memenuhi tuntutan tingkat pertambahan pascakelahiran pada bayi prematur(30,31). Anak-anak dan remaja, terutama non-putih individu, pada diet vegetarian yang ketat atau diet yang tinggi fitat, yang mengikat kalsium, juga bisa kekurangan kalsium, yang menyebabkan rakhitis (33-35). Ini, dalam kombinasi dengan kekurangan vitamin D, seringkali menjadi penyebab pemicu dari rakhitis pada anak-anak yang hidup keturunan Timur Tengah di Inggris dan anak-anak Afrika-Amerika di Amerika Serikat (32-35). Kekurangan kalsium dan hiperparatiroidisme sekunder yang terkait peningkatan kebutuhan untuk vitamin D, karena vitamin D dengan cepat dimetabolisme menjadi 1,25 (OH) 2D. Kombinasi kekurangan kalsium dan
vitamin D kekurangan mempercepat dan membuat lebih parah kelainan skeletal dan hipokalsemia. Prevalensi subklinis defisiensi vitamin D Parah kronis kekurangan vitamin D [25 (OH) D tingkat kurang dari 15 ng / ml] mengarah ke kelainan tulang terbuka pada anak-anak yang biasanya didefinisikan sebagai rakhitis (23, 30-32). Namun, ada sejumlah besar bayi, anak, dan remaja yang vitamin D tidak cukup tetapi tidak memiliki kelainan metabolisme tulang jelas atau kalsium (Tabel (Tabel 2) . 2). Kami mengamati bahwa dari 40 "sehat" pasangan ibu-bayi yang umumnya non-putih, 73% ibu dan 80 bayi% memiliki 25 (OH) tingkat D kurang dari 20 ng / ml meskipun fakta bahwa 80% dari ibu mengambil multivitamin prenatal harian yang berisi 400 IU vitamin D (37). Sullivan et al. (38) melaporkan bahwa 48% anak perempuan kulit putih berusia 9-11 tahun di Maine telah 25 (OH) D tingkat kurang dari 20 ng / ml pada akhir musim dingin dan 17% tetap kekurangan vitamin D pada akhir musim panas karena baik untuk menghindari paparan sinar matahari atau selalu memakai perlindungan matahari. Empat puluh dua persen dari remaja anak-anak Amerika dan Hispanik Afrika memiliki 25 (OH) tingkat D kurang dari 20 ng / ml di Boston (39), yang konsisten dengan pengamatan oleh Centers for Disease Control bahwa 48% dari wanita Afrika Amerika berusia 15-49 tahun di seluruh seluruh Amerika Serikat telah 25 (OH) tingkat D kurang dari 15 ng / ml pada akhir musim dingin (40). Pengamatan serupa telah dibuat di Kanada dan Eropa, di mana beberapa makanan yang diperkaya dengan vitamin D dan garis lintang batas tinggi produksi vitamin D di kulit (41-45). Hebatnya, di daerah tercerah di dunia, rakhitis merupakan masalah kesehatan utama. Karena praktik purdah atau mengenakan burqa (45, 46), menghindari paparan dari setiap kulit terhadap sinar matahari, dan fakta bahwa beberapa makanan yang diperkaya dengan vitamin D, naik dari 35-80% anak di Arab Saudi (46 , 47), India (48), Turki (29), Selandia Baru (49), Israel (50), Mesir (51), Hong
Kong (52), Cina (53), Libia (54), Lebanon (55) , Spanyol (56), Australia (57), San Diego, California (58), dan tenggara Amerika Serikat (59) adalah vitamin D kekurangan. Ketika defisiensi terjadi selama hidup janin, ada data yang menunjukkan bahwa hal ini dapat menyebabkan peningkatan risiko patah tulang pinggul dan pengeroposan tulang di kemudian hari (56, 60, 61). Subklinis kekurangan vitamin D pada neonatus berhubungan dengan tingkat serum kalsium yang normal, rendah 25 (OH) D konsentrasi (biasanya antara 10 dan 20 ng / ml), dan peningkatan serum PTH, 1,25 (OH) tingkat fosfatase 2D dan basa ( 30-32). Diwariskan penyebab dari rakhitis Setelah diakui bahwa vitamin D harus dimetabolisme di hati dan ginjal sebelum dapat melaksanakan efek biologis pada kalsium, fosfor, dan metabolisme tulang, itu adalah hipotesis bahwa cacat di hati 25hidroksilasi atau ginjal 1-hidroksilasi langkah akan mengakibatkan ketidakmampuan untuk mengaktifkan vitamin D, sehingga menyebabkan kekurangan vitamin D-seperti negara yang tahan terhadap dosis fisiologis vitamin D (Gambar (Figure4) .4). Hanya ada satu kasus didokumentasikan dari 25-OHase-kekurangan rakhitis (62). Alasan yang paling mungkin mengapa lebih banyak kasus yang tidak dilaporkan adalah bahwa setidaknya ada 4 enzim berbeda yang memiliki kemampuan untuk mengubah vitamin D untuk 25 (OH) D (63). Karena vitamin D mengalami aktivasi akhir pada ginjal, beberapa penelitian individu dengan "D-tahan vitamin" penyakit menyebabkan rakhitis pada mana pasien dievaluasi untuk cacat dalam metabolisme 25 (OH) D untuk 1,25 (OH) 2D telah dilaporkan. Pseudovitamin Dkekurangan rakhitis (juga dikenal sebagai turun-temurun, vitamin D tergantung rakhitis tipe 1), gangguan herediter langka, yang ditemukan terkait dengan tingkat yang sangat rendah atau tidak terdeteksi 1,25 (OH) 2D dalam sirkulasi (64) . Anak-anak menanggapi oral 1,25 (OH) 2D3 (64). Kloning dari enzim 1-OHase ginjal menyebabkan identifikasi dari banyak
mutasi titik gen CYP27B1, yang mengakibatkan baik buruk fungsional 1OHase atau tidak adanya lengkap 1-OHase aktivitas (65).
Beberapa peneliti melaporkan anak-anak dengan rakhitis berat yang sering alopecia dan tingkat yang sangat tinggi dari 1,25 (OH) 2D (65, 66). Beberapa anak dengan penyakit ini, vitamin D-tahan rakhitis (turuntemurun, vitamin D tergantung rakhitis tipe 2), menanggapi dosis farmakologis dari vitamin D atau 1,25 (OH) 2D3, sementara yang lain tidak (66, 67). Mutasi titik pada gen VDR bertanggung jawab untuk perlawanan vitamin D. Chen et al. (68) melaporkan suatu bentuk baru perlawanan vitamin D, vitamin D herediter rakitis yang bergantung tipe 3, yang disebabkan oleh ekspresi abnormal respon hormon elemen-binding protein (HRBP) yang mengikat dan karena itu VDRE mencegah 1,25 (OH) 2D-VDR-RXR kompleks dari mengikat ke elemen responsif nya. Pasien ini memiliki ekspresi VDR biasa dan benar-benar tahan terhadap 1,25 (OH) 2D3 tindakan. Anak-anak dengan vitamin D-resistensi sindrom sering menderita cacat tulang yang parah dan hipokalsemia lebih menonjol dibanding anak-anak dengan defisiensi vitamin D-rakhitis. Pengobatan tergantung pada penyebab dan beratnya perlawanan vitamin D. Anakanak memiliki dosis farmakologis menanggapi vitamin D, dosis fisiologis dan farmakologis dari 1,25 (OH) 2D3 dan analog 1-hydroxyvitamin D3, serta infus intravena kalsium dan fosfor (30, 64, 66-69). Diwarisi dan diperoleh hypophosphatemic rickets Gangguan ini ditandai dengan hypophosphatemia, penurunan reabsorpsi fosfor oleh tubulus ginjal, penurunan penyerapan kalsium dan fosfor dari saluran pencernaan, dan berbagai derajat rakhitis atau osteomalacia (70, 71). Pasien sering memiliki kadar serum normal atau berkurang dari 1,25 (OH) 2D, yang dianggap normal, karena hypophosphatemia menyebabkan peningkatan serum 1,25 (OH) 2D
tingkat karena meningkatkan produksi ginjal 1,25 ( OH) 2D (70, 72). Awalnya ia berpikir bahwa gangguan hypophosphatemic disebabkan oleh cacat pada protein transportasi fosfat ginjal. Namun, bukti terbaru menunjukkan bahwa faktor lain asal tulang berpartisipasi dalam mempertahankan homeostasis fosfor, termasuk faktor pertumbuhan fibroblast 23 (FGF23), phosphoglycoprotein matriks ekstraseluler, dan frizzled-related protein 4. Faktor-faktor ini secara kolektif dikenal sebagai phosphatonins (73). Ketika FGF23 yang ditinggikan, hal itu menyebabkan internalisasi dari cotransporter natrium fosfat di kedua ginjal dan usus, sehingga menyebabkan phosphaturia dan penurunan penyerapan usus fosfat (74). Hal ini juga menghambat aktivitas CYP27B1. Pasien dengan autosomal dominan hypophosphatemic rickets (ADHR) memiliki mutasi pada gen FGF23 yang mencegah atau mengurangi kerusakan FGF23 metabolik, yang mengarah ke peningkatan tingkat FGF23 (70, 75). Diinduksi tumor osteomalasia disebabkan oleh tumor kecil yang sering jinak dan mengeluarkan FGF23 (70, 71, 73, 74). Penyebab pasti terkait-X hypophosphatemic rickets kurang dipahami dengan baik. Ini telah dikaitkan dengan mutasi dari homolog fosfat endopeptidase mengatur, terkait-X (PHEX) gen. Kehilangan ekspresi yang menyebabkan berlebih dari FGF23 dan phosphatonins mungkin lainnya dalam tulang, yang menyebabkan peningkatan tingkat sirkulasi FGF23 (74). Jadi, rakhitis hypophosphatemic disebabkan oleh ketidakmampuan untuk memetabolisme FGF23 atau produksi berlebihan FGF23 (70, 71, 73, 74) (Gambar (Figure4) .4). Fosfat pengiriman intravena telah efektif dalam mengobati rakhitis dan osteomalacia (70, 71, 76), dan penghapusan tumor kuratif (77, 78). Perawatan meliputi pemberian fosfat sering oral, biasanya 250-500 mg sampai 5 kali sehari, serta pemberian oral dua kali sehari dari 0,5-1,0 ug 1,25 (OH) 2D3 (70, 71, 76). Administrasi kurang sering dosis tinggi fosfat adalah berkecil hati, karena peningkatan sementara dalam serum fosfat menyebabkan penurunan kalsium terionisasi dan
peningkatan tingkat PTH dan menyebabkan kelenjar paratiroid menjadi hiperplastik dan otonom, yang mengarah pada hiperparatiroidisme tersier. Pencegahan dan pengobatan vitamin D dan kalsiumdefisiensi rakhitis Pada tahun 1940, asupan vitamin D direkomendasikan untuk bayi adalah 100 IU / d untuk mencegah rakhitis (14). Namun, rekomendasi diterima saat ini untuk mencegah rakhitis adalah 400 IU sehari dosis vitamin D dan asupan kalsium yang cukup (32-35, 79). Uji klinis pada bayi prematur (16 hari usia) secara acak untuk harian vitamin D 200 IU asupan (90 IU / kg), 400 IU (180 IU / kg), atau 800 IU (360 IU / kg) sampai satu bulan. Tidak ada perbedaan radiologi yang diamati antara kelompokkelompok (80). The 25 (OH) D tingkat dalam kelompok penerima 200 IU vitamin D untuk 24-29 hari tidak berubah, sedangkan kelompok yang menerima 400 IU dan 800 IU untuk periode waktu yang sama menunjukkan peningkatan 25 (OH) tingkat D sekitar 30%. Penelitian serupa juga menyatakan bahwa bayi prematur 'plasma 25 (OH) D tingkat dipertahankan dari kehidupan neonatal dini untuk 3 bulan dengan pemberian suplemen vitamin D 400 IU / d. Tidak ada manfaat dalam status vitamin D atau densitas mineral tulang lengan diamati pada dosis yang lebih tinggi dari 900 IU / d (30, 81). Di Eropa, Komite Nutrisi untuk Masyarakat Eropa Pediatric Gastroenterology, Hepatology dan Gizi merekomendasikan asupan vitamin D dari 800-1,600 IU / d (36). Mawer et al. (36) memberikan 1.000 atau 3.000 baik IU vitamin D2 harian untuk rendah berat lahir bayi dengan berat rata-rata 1,36 kg dan menemukan bahwa 25 (OH) D meningkat dari baseline 6-10 ng / ml ke rata-rata 33 ng / ml dalam kedua kelompok dosis setelah 7 minggu. Mereka juga mengamati bahwa 25 (OH) D tingkat cepat naik selama minggu pertama dan mulai ke dataran tinggi di 7 minggu di sekitar 33 ng / ml. Markestad et al. (23) dirawat anak-anak dengan 1,700-4,000 IU vitamin D2/day hingga 10 minggu dan menunjukkan rata-rata 25 (OH) D sekitar 30 ng / ml dan
koreksi kelainan biokimia dan rangka mereka. Neonatus prematur diobati dengan 1.200 IU vitamin D3/day selama 7 hari mengangkat 25 mereka (OH) tingkat D dari 8 ng / ml sampai 18 ng / ml (81). Meskipun tidak diketahui apa tingkat normal minimal 25 (OH) D harus untuk bayi dan neonatus berdasarkan pengamatan ini, tidak masuk akal untuk tingkat darah minimal 20 ng / ml. Namun, karena mereka studi menunjukkan bahwa 25 (OH) D tingkat mencapai dataran tinggi di sekitar 33 ng / ml, hal ini kemungkinan tingkat sehat yang ideal untuk bayi dan anak-anak dan mirip untuk orang dewasa (23, 24, 30, 36, 81 - 84). Untuk mencapai 25 sehat (OH) tingkat D lebih besar dari 30 ng / ml, bayi memerlukan setidaknya 400-1,000 IU vitamin D / hari tergantung pada 25 mereka (OH) tingkat D pada saat lahir. Bayi yang kekurangan vitamin D seharusnya tidak hanya menerima apa yang dianjurkan asupan yang memadai AS (200 IU / d) (85) atau bahkan 400 IU / d melainkan harus agresif diobati dengan dosis farmakologis vitamin D dalam rangka untuk membangun tubuh menyimpan dari vitamin D dan cepat memperbaiki kekurangan vitamin D. Metode terbaik untuk secara efektif mengobati dan menyembuhkan riketsia adalah untuk memberikan total 5-15 mg (200,000-600,000 IU) vitamin D2 atau vitamin D3 secara oral dengan kalsium diet yang cukup (86). Dosis ini dapat diberikan secara aman baik sebagai terapi tunggalhari atau sebagai dosis harian 2000-4000 IU / d (50-100 mg / d) untuk 3-6 bulan (30, 86, 87). Biasanya ada koreksi cepat dari kedua kalsium serum dan kadar fosfor dalam 6-10 hari dan normalisasi tingkat PTH dalam waktu 1-2 bulan. Fosfatase alkali dan penyembuhan penurunan tandatanda radiologis dari rakhitis yang diamati dalam waktu 3-6 bulan tergantung pada tingkat keparahan kekurangan (30, 86). Bagi mereka yang mungkin tidak sesuai dengan rezim ini, dianjurkan bahwa 5 mg (200.000 IU) vitamin D diberikan sebagai dosis tunggal oral, dengan dosis tindak lanjut dari 5 mg 3 bulan kemudian. Sangat penting untuk memulai
terapi dengan dosis besar vitamin D, karena memberikan dosis harian kecil dari 200-400 IU / d tidak akan mengembalikan toko yang memadai dari vitamin D sebagai cepat sebagai salah satu dosis besar tunggal atau dosis harian yang 10 - untuk 20 kali lipat lebih tinggi dari asupan yang direkomendasikan (AI) (30, 85, 86, 87). Untuk bayi dan anak-anak yang telah malabsorpsi lemak, termasuk pasien cystic fibrosis (88), direkomendasikan bahwa subkutan atau intramuskular administrasi digunakan. Atau, paparan sinar matahari atau dikendalikan untuk radiasi UV dari lampu komersial adalah dianjurkan (5, 6, 12-14, 30, 33, 88). Sinar matahari, iradiasi UV, dan bayi dan ibu suplementasi vitamin D Teratur dan bijaksana paparan sinar matahari selama bulan tahun ketika produksi vitamin D dipromosikan masih merupakan cara yang paling fisiologis untuk mencegah kekurangan vitamin D pada bayi dan anak-anak (1, 24, 80, 89). Variasi musiman dalam serum 25 (OH) D pada anak-anak dan orang dewasa adalah didokumentasikan dengan baik, dengan tingkat mencapai puncaknya pada tengah musim panas dan nadir pada akhir musim dingin di kedua belahan utara dan selatan, (1, 19, 24, 57, 89). Karena ASI memiliki sedikit, jika ada, vitamin D (biasanya tidak lebih dari 25 IU / l), biasanya tidak memadai dalam memuaskan kebutuhan bayi (85, 87, 90). Jadi, jika bayi hanya menerima nutrisi dari menyusui dan jika ibu kekurangan vitamin D, bayi akan menjadi kekurangan vitamin D dan kemungkinan akan mengembangkan rakhitis (30,37,90). Neonatus dan anak-anak muda yang tidak menerima vitamin D dari diet mereka merespon dengan baik untuk dosis oral 1.000-1.500 IU / d sepanjang tahun sampai usia 2 dan selama musim dingin hingga usia 5 tahun tanpa ada tanda-tanda keracunan vitamin D (30). Skema pencegahan telah sangat efektif di Eropa untuk di-risiko bayi yang ASI eksklusif atau yang terlalu tua untuk mengambil rumus (30). Pencegahan dengan dosis harian yang lebih rendah dari 400-500 IU / d dianjurkan
untuk lainnya menyusui bayi dan berisiko untuk neonatus dan bayi muda menerima susu formula. Efek memberikan ibu atau bayi selama menyusui dengan suplemen 400 IU vitamin D menunjukkan bahwa itu adalah yang paling efektif untuk memberikan bayi suplementasi vitamin D harian. Namun, Hollis et al. (90) melaporkan bahwa pemberian wanita menyusui 4.000 IU vitamin D3 setiap hari menyediakan vitamin D yang cukup dalam ASI untuk memenuhi kebutuhan bayi. Noncalcemic dan nonskeletal konsekuensi dari defisiensi vitamin D pada anak-anak Anak-anak dengan defisiensi vitamin D sering menderita
kelemahan otot yang parah dengan kaki datar dan lembek (1, 2, 12-14, 30-32). Sekarang diakui bahwa otot rangka memiliki VDR dan bahwa 1,25 (OH) 2D meningkatkan fungsi otot (91). Serum 25 (OH) D tingkat di atas 30 ng / ml memaksimalkan fungsi otot kaki proksimal pada orang dewasa (92). Hal ini diamati pada orang dewasa sehat bahwa jika serum 25 (OH) D lebih besar dari 20 ng / ml, ada peningkatan yang signifikan dalam fungsi paru-paru, dengan peningkatan rata-rata volume ekspirasi paksa dari 176 ml (93). Camargo et al. (94) melaporkan studi prospektif asupan vitamin D ibu selama kehamilan dan diamati bahwa kekurangan vitamin D sangat prediksi peningkatan risiko untuk asma. VDR ini hadir tidak hanya pada jaringan yang mengatur kalsium serum, termasuk usus kecil, sel-sel tulang, dan ginjal, tetapi juga di dasarnya semua jaringan dan sel dalam tubuh, termasuk otak, payudara kolon, prostat, pankreas, jantung, kulit , otot rangka, monosit, dan diaktifkan T dan limfosit B (1, 20-22, 24). Wawasan pertama ke peran noncalcemic dari 1,25 (OH) 2D3 diamati ketika 1,25 (OH) 2D3 diinkubasi dengan mouse dan sel leukemia manusia. 1,25 (OH) 2D3 menghambat proliferasi sel leukemia dan diinduksi sel untuk dewasa (20-22, 95, 96). Banyak sel kanker dan budaya garis kanker primer sel yang dimiliki VDR menunjukkan, ditandai penghambatan pertumbuhan dan induksi
pematangan bila terkena 1,25 (OH) 2D3 atau analog aktif (1, 20-22, 24, 96) (Gambar (Figure5) .5). 1,25 (OH) D melakukan hal ini dengan menginduksi pematangan sel, mengatur ekspresi p21 dan p27 dan apoptosis, dan bertindak sebagai faktor antiangiogenic (20-22, 24, 95, 96). Tinggal di lintang yang lebih tinggi dan menjadi rentan terhadap defisiensi vitamin D meningkatkan risiko kanker usus besar, prostat, payudara, ovarium, kerongkongan, dan beberapa jaringan lain (1, 24, 9799). Ia telah mengemukakan bahwa pemeliharaan tingkat 25 (OH) D yang lebih besar dari 20 ng / ml mengurangi risiko usus besar, prostat, payudara, dan kanker ovarium sebanyak 30-50% (24, 97-99). Meskipun tidak diketahui apakah kekurangan vitamin D dalam rahim dan selama masa bayi dan kanak-kanak akan membekas pada anak selama sisa hidupnya peningkatan risiko kanker ini mematikan, pengamatan baru-baru ini bahwa anak-anak terkena sinar matahari yang paling memiliki 40% penurunan risiko pengembangan limfoma non-Hodgkin (100) dan kelangsungan hidup meningkat dari melanoma maligna (101) menunjukkan bahwa pemeliharaan yang memadai 25 (OH) tingkat D sepanjang hidup dapat membantu mengurangi risiko kanker mematikan banyak(24,97-99,102) . Hidup di atas lintang 35 untuk 10 tahun pertama jejak kehidupan di anak selama sisa hidupnya 100% peningkatan risiko mengembangkan multiple sclerosis di mana pun mereka tinggal sesudahnya (24, 103, 104). Tinggal di lintang yang lebih tinggi dan menjadi rentan terhadap defisiensi vitamin D meningkatkan risiko penyakit autoimun beberapa lainnya termasuk diabetes tipe 1 dan penyakit Crohn (105, 106). Anak-anak di Finlandia pada tahun 1960 yang menerima 2.000 IU vitamin D direkomendasikan / hari setidaknya selama tahun pertama kehidupan dan diikuti untuk 31 tahun ke depan menunjukkan penurunan risiko pengembangan diabetes tipe 1 dengan 80% (105). Selanjutnya, anakanak dari kohort yang sama yang kekurangan vitamin D pada usia satu
tahun memiliki risiko meningkat 2,4 kali lipat terkena diabetes tipe 1. Kekurangan vitamin D dalam rahim dan selama tahun pertama kehidupan juga telah dikaitkan dengan peningkatan risiko diabetes tipe 1 (107). 1,25 (OH) 2D mempengaruhi sistem kekebalan tubuh (106, 108), dan, sebagai sel islet pankreas telah VDR, itu juga merangsang sekresi insulin (20-22, 24) (Gambar (Figure5) .5). Jadi, hypovitaminosis D pada anak-anak dapat meningkatkan risiko mereka tidak hanya dari diabetes tipe 2, tetapi juga resistensi insulin dan disfungsi sel islet (109). Tinggal di lintang yang lebih tinggi dan kekurangan vitamin D juga terkait dengan hipertensi dan penyakit jantung kardiovaskular (24, 110, 111). Li et al. (112) melaporkan bahwa 1,25 (OH) 2D3 adalah suatu regulator efektif dari produksi renin, yang mengontrol tekanan darah. Sebuah penelitian pada orang dewasa hipertensi yang terkena sinar matahari simulasi 3 kali seminggu selama 3 bulan menghasilkan peningkatan di 25 mereka (OH) tingkat D oleh lebih dari 150% dan pengurangan (6 mmHg) yang signifikan di kedua sistolik dan tekanan darah diastolik (113 ). Autokrin produksi serta fungsi dari 1,25 (OH) 2 D Beredar tingkat 1,25 (OH) 2D yang sangat rendah atau tidak terdeteksi pada pasien dengan penyakit ginjal kronis (114). Telah diasumsikan bahwa ginjal merupakan sumber tunggal 1,25 (OH) 2D. Namun, seperti sebagian besar jaringan dan sel-sel dalam tubuh telah VDR, demikian juga melakukan hal-jaringan dan sel-sel memiliki kemampuan untuk mengekspresikan CYP27B1. Jadi, kulit, prostat, payudara, usus besar, paru-paru, otak, dan plasenta tidak hanya mengungkapkan VDR tetapi juga memiliki kapasitas untuk memproduksi 1,25 (OH) 2D (22, 24, 115, 116). Sekarang diakui bahwa 1,25 (OH) 2D membantu mengontrol ekspresi lebih dari 200 gen (20-22, 24, 117). Diperkirakan bahwa 1,25 (OH) 2D mempertahankan kesehatan seluler dengan bertindak sebagai sentinel untuk mencegah keganasan (24, 95, 96)(Gambar(Figure5).5).
Diaktifkan makrofag juga mengungkapkan CYP27B1 dan dengan demikian menghasilkan 1,25 (OH) 2D. Ini adalah mekanisme yang pasien dengan penyakit granulomatosa kronis seperti sarkoidosis dan TBC mengembangkan gangguan dalam metabolisme kalsium yang menyebabkan hypercalcuria dan hiperkalsemia (1, 22, 24). Mengapa makrofag menghasilkan 1,25 (OH) 2D tidak diketahui sampai Liu et al. (118) melaporkan bahwa aktivasi TLRs dengan LPS mengakibatkan upregulation ekspresi tidak hanya VDR tetapi juga gen CYP27B1. Produksi lokal 1,25 (OH) 2D diinduksi ekspresi dari cathelicidin peptida antimikroba (LL-37), yang diduga menjadi faktor kunci dalam respon imun bawaan saat TLR diaktifkan oleh agen infektif misalnya Mycobacterium tuberculosis (Gambar (Figure5) .5). Ini pengamatan yang luar biasa menjelaskan mengapa pasien dengan TB sering berbuat lebih baik ketika ditempatkan di solarium dan terkena sinar matahari atau dibawa ke ketinggian yang lebih tinggi di mana produksi vitamin D3 dalam kulit lebih efisien (14). Ini juga adalah alasan yang mungkin mengapa orang Amerika Afrika, yang sering kekurangan vitamin D, dan anak-anak dengan kekurangan vitamin D memiliki peningkatan kerentanan terhadap infeksi TB (118). Ini mungkin juga menjelaskan mengapa hal itu banyak dilaporkan bahwa anak-anak dengan rakhitis sering lebih rentan terhadap penyakit menular, termasuk virus flu biasa (12-14, 119).
Kesimpulan Kekurangan vitamin D-rakitis adalah penyakit kekurangan sinar matahari. Ketidakmampuan untuk menghargai efek menguntungkan dari sinar matahari untuk kesehatan telah menghancurkan konsekuensi bagi anak-anak dan orang dewasa untuk lebih dari 300 tahun. Ketika akhirnya menyadari bahwa paparan sinar matahari dapat mencegah dan mengobati rakhitis, hal ini menyebabkan rekomendasi bahwa semua anak terkena sinar matahari masuk akal untuk memaksimalkan kesehatan
tulang. Susu fortifikasi dengan vitamin D diberantas rakhitis sebagai masalah kesehatan utama, dan, karenanya, ia berpikir telah ditaklukkan. Rakitis, bagaimanapun, membuat comeback menguntungkan (120). Penyebab utama dari rakhitis pada Amerika Serikat adalah kurangnya apresiasi bahwa susu manusia mengandung sangat sedikit jika ada vitamin D untuk memenuhi kebutuhan bayi. Wanita Amerika Afrika sering kekurangan vitamin D, dan perempuan yang selalu memakai pelindung matahari dan hanya mengambil multivitamin prenatal juga pada risiko tinggi kekurangan vitamin D. Jika mereka memberikan ASI kepada bayi mereka sebagai satu-satunya sumber gizi, bayi akan menjadi kekurangan vitamin D. Jika bayi tidak terkena sinar matahari atau tidak menerima suplemen vitamin D, bayi pasti akan mengembangkan rakhitis. Namun, manifestasi kerangka rakhitis hanya mewakili ujung gunung es defisiensi vitamin D. Kekurangan vitamin D dalam rahim dan selama tahun pertama kehidupan kehidupan memiliki mungkin konsekuensi tentang yang menghancurkan kronis anak dan yang jejak akan penyakit
mempersingkat / rentang hidupnya (24, 57). Dalam rahim, hasil kekurangan vitamin D dalam pertumbuhan tulang berkurang intrauterin panjang dan kehamilan sedikit lebih pendek (121). Ini telah dikaitkan dengan peningkatan risiko osteoporosis dan patah tulang di kemudian hari (24, 60, 61, 82, 122). Anak yang lahir dan dibesarkan di lintang bawah 35 selama 10 tahun pertama memiliki risiko 50% terkena multiple sclerosis di kemudian hari (103, 104). Neonatus yang adalah vitamin D kekurangan selama tahun pertama kehidupan adalah 2,4 kali lipat lebih mungkin untuk mengembangkan diabetes tipe 1 dibandingkan dengan anak yang menerima 2.000 IU vitamin D3/day (105). Ia telah mengemukakan bahwa peningkatan risiko skizofrenia berkembang dapat dimulai di dalam rahim dan selama masa kanak-kanak karena kekurangan vitamin D (102). Fungsi otot, imunitas bawaan, pertumbuhan sel dan pematangan, immunomodulation, sekresi insulin, serta regulasi kalsium, fosfor, dan metabolisme tulang semua dipengaruhi atau dikendalikan oleh vitamin D.
Jadi, memastikan bahwa perempuan selama kehamilan adalah vitamin D yang cukup dan bahwa bayi yang baru lahir baik segera dievaluasi untuk status vitamin D dengan mengukur 25 (OH) tingkat D dalam darah tali pusat atau diberikan profilaksis vitamin D harus menjadi prioritas tinggi. Kekurangan vitamin D harus segera diobati dengan setidaknya 1.000 IU vitamin D2 atau D3/day vitamin untuk minggu pertama kehidupan. Atau, dosis tunggal 200.000 IU vitamin D harus cukup untuk beberapa bulan pertama kehidupan. Telah ada ketakutan besar tentang menyebabkan keracunan vitamin D pada neonatus. Hal ini mengakibatkan dari wabah buruk dijelaskan dari hiperkalsemia neonatal pada tahun 1950 di Inggris (123), yang menyebabkan berlakunya undang-undang di Eropa melarang produk susu fortifikasi serta semua produk lainnya dengan vitamin D. Pada tahun 1997 Institut Kedokteran merekomendasikan bahwa AI untuk bayi dan anakanak dari segala usia dapat 200 IU / d. Rekomendasi yang sama dibuat untuk wanita hamil dan menyusui. Batas atas aman untuk bayi usia 0-12 bulan adalah 1.000 IU / d dan untuk anak-anak lebih tua dari usia 1 tahun, 2.000 IU / d. Namun, sekarang jelas berdasarkan literatur sejarah (14-16) serta literatur terbaru (23, 24, 30, 36, 81, 86, 87) bahwa rekomendasi ini tidak memadai tanpa paparan sinar matahari masuk akal. Hal ini juga mencatat bahwa neonatus dan anak-anak dapat mentolerir dosis tunggal 200.000 IU vitamin D2 atau vitamin D3 atau dosis vitamin D sampai 3.000 IU / d tanpa efek samping tak diinginkan. Memang 400-1,000 IU / d untuk mempertahankan serum 25 (OH) tingkat D antara 30-50 ng / ml harus menjadi tujuan, seperti itu pada orang dewasa. Bayi dan anak-anak secara rutin menerima 400-2,000 IU vitamin D2 atau D3/day vitamin untuk tahun-tahun pertama kehidupan tanpa ada laporan toksisitas (23, 80, 105, 107). Biasanya, dosis lebih dari 50.000 IU / d vitamin D2 ditemukan menyebabkan toksisitas (12-14). Di Kanada, dianjurkan agar semua bayi menerima 400 IU / d dari
lahir. Rekomendasi ini telah berhasil diimplementasikan dan tidak menghasilkan dalam setiap kasus yang dilaporkan keracunan vitamin D atau hiperkalsemia. Saya percaya bahwa 200 IU vitamin D yang direkomendasikan akan mengenai oleh American Academy of Pediatrics vitamin meningkatkan adalah D. risiko suboptimal (124). Dosis ini dapat mencegah rakhitis terbuka tetapi tidak mencegah paparan sinar kekurangan matahari langsung Semoga, sejarah tidak akan mengulangi dirinya sendiri. Kekhawatiran luas skuamosa relatif jinak dan tidak mematikan dan kanker sel basal perlu dimasukkan ke dalam perspektif. Ini adalah paparan kronis yang berlebihan sinar matahari dan tersengat sinar matahari pengalaman masa kanak-kanak yang meningkatkan risiko kanker kulit nonmelanoma (125). Melanoma, salah satu kanker yang paling ditakuti karena kemampuannya untuk cepat bermetastasis sebelum jelas baik pasien atau dokter, telah dicap sebagai kanker kulit yang disebabkan sinar matahari. Namun, melanoma paling banyak terjadi pada setidaknya terkena sinar matahari, daerah, dan telah dilaporkan bahwa pajanan terhadap sinar matahari menurunkan risiko melanoma (125). Kampanye 30 tahun untuk merekomendasikan berpantang dari paparan sinar matahari tidak berasal peningkatan kejadian kanker kulit (125). Hal ini aneh bahwa pada 1930-an dan 1940-an, ketika anak-anak didorong untuk terkena sinar matahari dan radiasi UV buatan untuk mengobati rakhitis, insiden kanker kulit tidak meningkat. Jadi, perlu ada evaluasi ulang dari efek menguntungkan dari paparan sinar matahari yang masuk akal seperti dicatat oleh Australian College of Dermatologists dan Cancer Council Australia, yang merekomendasikan keseimbangan antara menghindari risiko kanker kulit meningkat dan mencapai cukup radiasi UV untuk mempertahankan kadar vitamin D yang memadai.
You might also like
- Muskuloskeletal P ('t':3) Var B Location Settimeout (Function (If (Typeof Window - Iframe 'Undefined') (B.href B.href ) ), 15000)Document178 pagesMuskuloskeletal P ('t':3) Var B Location Settimeout (Function (If (Typeof Window - Iframe 'Undefined') (B.href B.href ) ), 15000)George YohanesNo ratings yet
- Sindrom DownDocument19 pagesSindrom DownFirstiafina TiffanyNo ratings yet
- Ilmu Penyakit Dalam 1Document53 pagesIlmu Penyakit Dalam 1Altius Rangngan ParatteNo ratings yet
- OnkogenesisDocument11 pagesOnkogenesisDyan Lihawa100% (3)
- Fraktur - RD2002 by Dr. Ali Residen BedanDocument39 pagesFraktur - RD2002 by Dr. Ali Residen BedanRatnaPNNo ratings yet
- 5 - Oksidasi BiologiDocument34 pages5 - Oksidasi BiologihestyrosalinaNo ratings yet
- Pengantar ToksikologiDocument29 pagesPengantar Toksikologidesti aliahNo ratings yet
- Makalah OsteoporosisDocument23 pagesMakalah OsteoporosisDiaz RahmadiNo ratings yet
- Konseling Genetika (Tugas Kelompok 5)Document11 pagesKonseling Genetika (Tugas Kelompok 5)rakatsuNo ratings yet
- Referat DiGeorge SyndromeDocument69 pagesReferat DiGeorge Syndromenunung100% (1)
- Laprak PK RanaDocument7 pagesLaprak PK RanaRana Salsabila PutrilajaNo ratings yet
- Soal Ujian Blok 1Document9 pagesSoal Ujian Blok 1Mirza AmryaNo ratings yet
- Refrat RabiesDocument16 pagesRefrat Rabiestasti_imoeyNo ratings yet
- Sin Dak TiliDocument11 pagesSin Dak TiliSarah AndrianiNo ratings yet
- Defisiensi MineralDocument34 pagesDefisiensi MineralLeo AzuzphreNo ratings yet
- Reumatism Non ArtikularDocument30 pagesReumatism Non ArtikularRizky Dahliyani PutriNo ratings yet
- Profil Singkat Bidang ISMKI Wilayah 1 Periode 2013-2014Document3 pagesProfil Singkat Bidang ISMKI Wilayah 1 Periode 2013-2014bimaindra97No ratings yet
- Mutasi ChaidarWarianto 17.daniDocument5 pagesMutasi ChaidarWarianto 17.daniMuhammad_maadaniNo ratings yet
- Biologi MolekulerDocument25 pagesBiologi Molekuleryeslina pattyNo ratings yet
- Dopamin YaniDocument37 pagesDopamin YaniTiya SyahraniNo ratings yet
- Salinan Terjemahan Book InTech Human Embryo CC byDocument79 pagesSalinan Terjemahan Book InTech Human Embryo CC byrahmi andritaNo ratings yet
- RADIOLOGIDocument35 pagesRADIOLOGIMerrytiana FadilaNo ratings yet
- Dms146 Slide Pengetahuan Dasar Imunologi KulitDocument11 pagesDms146 Slide Pengetahuan Dasar Imunologi KulitRonalda BudyantaraNo ratings yet
- Abnormalitas KromosomDocument9 pagesAbnormalitas KromosomlimNo ratings yet
- MCQ It Blok 8 2012 Tipe BDocument24 pagesMCQ It Blok 8 2012 Tipe BninaNo ratings yet
- No. Gambar Keterangan Clinical Application: ShakavelsDocument6 pagesNo. Gambar Keterangan Clinical Application: ShakavelsFajar RamadhanNo ratings yet
- Deoksihemoglobin Dan OksihemoglobinDocument2 pagesDeoksihemoglobin Dan OksihemoglobinGiavanny Eka Rani PuteriNo ratings yet
- Teknologi Dna RekombinanDocument13 pagesTeknologi Dna RekombinanMuhammad FauzanNo ratings yet
- Tabel Etiologi Diferensial Diagnosis Nyeri Punggung BawahDocument5 pagesTabel Etiologi Diferensial Diagnosis Nyeri Punggung BawahahlibedahNo ratings yet
- Ekspresi Gen, PCR & KloningDocument18 pagesEkspresi Gen, PCR & KloningM Wahyu NovianiNo ratings yet
- Pleno Pemicu 1 KJPDocument53 pagesPleno Pemicu 1 KJPdeyshieNo ratings yet
- USG CranialDocument12 pagesUSG CranialTiasNo ratings yet
- Fibrosis ParuDocument9 pagesFibrosis ParuAhmad Nurhadi Al-GhazaliNo ratings yet
- Diagnosis OsteoporosisDocument3 pagesDiagnosis OsteoporosisLatiff IqramieNo ratings yet
- Biokimia Jaringan Ikat, CA Dan TulangDocument40 pagesBiokimia Jaringan Ikat, CA Dan TulangWara Permeswari WardhaniNo ratings yet
- ClubfootDocument19 pagesClubfootArdy TjandraNo ratings yet
- Jembatan KedelaiDocument7 pagesJembatan KedelaiRizky EliandiNo ratings yet
- Bone Mineral DensitometriDocument4 pagesBone Mineral Densitometriponti.rouliNo ratings yet
- Gangguan Perilaku Dan Emosional Dengan Onset Biasanya PadaDocument30 pagesGangguan Perilaku Dan Emosional Dengan Onset Biasanya PadaNauli PanjaitanNo ratings yet
- Askep Trauma GinjalDocument15 pagesAskep Trauma GinjalGina IskandarNo ratings yet
- Imunologi DasarDocument22 pagesImunologi DasarLa Ode RinaldiNo ratings yet
- Jurnal TA OsteoarthritisDocument17 pagesJurnal TA OsteoarthritisAkuf Suradal WibisonoNo ratings yet
- Biosintesis Asam Lemak-EicosanoidDocument31 pagesBiosintesis Asam Lemak-EicosanoidMheerna JewelfishyNo ratings yet
- Latihan Soal Forensik 2 (Autopsi) - FK UNSDocument4 pagesLatihan Soal Forensik 2 (Autopsi) - FK UNSAnggita DewiNo ratings yet
- Monoklonal and Poliklonal AntibodiDocument10 pagesMonoklonal and Poliklonal AntibodiShelpi NovitaNo ratings yet
- Fisiologi TulangDocument19 pagesFisiologi Tulangkarinaastheria100% (11)
- AntibiotikDocument8 pagesAntibiotikumar asadullahNo ratings yet
- OsteogenesisDocument6 pagesOsteogenesisnayaNo ratings yet
- Guideline CraniosinostosisDocument47 pagesGuideline CraniosinostosislilaningNo ratings yet
- DNA RepairDocument23 pagesDNA RepairKatou Jeffrey ShigehitoNo ratings yet
- Pemendekan Telomer Dan ApoptosisDocument10 pagesPemendekan Telomer Dan ApoptosisAhmad Zaki AzzamNo ratings yet
- Patofisiologi OsteoporosisDocument7 pagesPatofisiologi OsteoporosisAdy Sanjaya PutraNo ratings yet
- Pengantar Teori SelDocument13 pagesPengantar Teori SelSiti HartatiNo ratings yet
- 06-Fraktur Pada DewasaDocument20 pages06-Fraktur Pada DewasaDumora FatmaNo ratings yet
- Pelayanan Kesehatan Pada Komunitas DifabelDocument11 pagesPelayanan Kesehatan Pada Komunitas Difabeltiara haprlNo ratings yet
- Bakteri Gram NegatifDocument9 pagesBakteri Gram NegatifNordin At-damsNo ratings yet
- LO Histologi GasterDocument3 pagesLO Histologi GasterPravangesta Anggit ANo ratings yet
- Ricketsia Pada Anak Asuhan Keperawatan LDocument27 pagesRicketsia Pada Anak Asuhan Keperawatan LNadila BellaNo ratings yet
- Vitamin D and SkinDocument15 pagesVitamin D and SkinerikajuniarthaNo ratings yet
- Referat Vitamin DDocument14 pagesReferat Vitamin DHans NatanaelNo ratings yet
- KetaminDocument5 pagesKetaminWildan SaputraNo ratings yet
- Daftar Pembimbing JurnalDocument1 pageDaftar Pembimbing JurnalWildan SaputraNo ratings yet
- Status KulkelDocument2 pagesStatus KulkelWildan SaputraNo ratings yet
- Abses Leher DalamDocument19 pagesAbses Leher DalamWildan SaputraNo ratings yet