Professional Documents
Culture Documents
ESTANDARIZACIÓN DE UNA DISOLUCIÓN DE NaOH
Uploaded by
Nubia MorenoCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
ESTANDARIZACIÓN DE UNA DISOLUCIÓN DE NaOH
Uploaded by
Nubia MorenoCopyright:
Available Formats
ESTANDARIZACIN DE UNA DISOLUCIN DE NaOH Para preparar una disolucin de una determinada concentracin (por ejemplo 0.
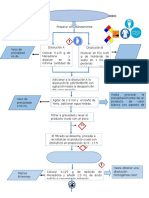
1 N) se parte de hidrxido sdico slido comercial, se disuelve un peso conocido en agua destilada y se diluye a un volumen conocido. Al no ser el hidrxido sdico un patrn primario, esta disolucin solo ser aproximadamente 0.1 N, por lo que es necesario estandarizarla para conocer exactamente su concentracin. La estandarizacin puede realizarse con ftalato cido de potasio, que s es una sustancia patrn primario. Como indicador de la titulacin se emplea fenolftalena. El viraje de la fenolftaleina se produce cuando todo el NaOH ha reaccionado, formndose ftalato de sodio y potasio. + NaOH + H2O COOK COOH COOK COONa 3.2.1 Reactivos - Disolucin de NaOH. Pesar 4 g de NaOH, disolver en un vaso de precipitado, y diluir con agua destilada a 1000 ml en un matraz aforado. - Ftalato cido de potasio, tipo patrn primario. - Disolucin de fenolftalena al 0.1% en etanol. 3.2.2 Procedimiento - Pesar exactamente (en la balanza analtica) entre 0.40 y 0.50 g de ftalato cido de potasio sobre un vaso de precipitado de 25 ml. Previamente, es conveniente secar el ftalato de potasio durante 30 minutos a 110C y dejar enfriar en un desecador. - Pasar la cantidad pesada a un erlenmeyer de 250 ml y disolver con unos 25 ml de agua destilada. - Lavar con agua destilada el vaso de precipitado y aadir al erlenmeyer. - Aadir 2 3 gotas de solucin de fenolftalena. - Valorar con la disolucin de NaOH 0.1N, lentamente y con agitacin, hasta que la disolucin adquiera una tonalidad rosa persistente. - Anotar el volumen V (ml) gastado y calcular el factor F de la disolucin - Repetir la valoracin y calcular de nuevo el factor, y su incertidumbre. 3.3 ESTANDARIZACIN DE UNA DISOLUCIN DE HCl Para preparar una disolucin de una determinada concentracin (por ejemplo 0.1 N) se parte de la disolucin de ClH concentrado, comercial, y se diluye con agua destilada en un matraz aforado hasta el volumen adecuado. Al no ser el cido clorhdrico un patrn primario, esta disolucin solo ser aproximadamente 0.1 N, por lo que es necesario estandarizarla para conocer exactamente su concentracin. La estandarizacin suele realizarse con CO3Na2, que si es una sustancia patrn primario. Como indicadores de la titulacin se emplean fenolftalena y naranja de metilo. El viraje de la fenolftalena se produce cuando el CO3 se ha transformado en CO3H-. CO3Na2 + ClH CO3HNa + ClNa En este punto se aade naranja de metilo, que vira cuando el CO3H- ha
pasado a CO3H2: CO3HNa + ClH CO3H2 + ClNa CO2 + H2O 3.3.1 Reactivos - Disolucin de HCl 0.1 N. Pipetear 9.8 ml de HCl al 32% (p/v) y diluir a 1000 ml en un matraz aforado. - CO3Na2, tipo patrn primario. - Disolucin de fenolftalena al 0.1% en etanol. - Disolucin de naranja de metilo al 0.1% en agua. 3.3.2 Procedimiento - Pesar exactamente (en la balanza analtica) entre 0.20 y 0.25 g de CO3Na2 sobre un vaso de precipitado de 25 ml. - Pasar la cantidad pesada a un erlenmeyer de 250 ml, y disolver con unos 25 ml de agua destilada. - Lavar con agua destilada el vaso de precipitado y aadir al erlenmeyer. - Aadir 2 3 gotas de solucin de fenolftalena. - Valorar con la disolucin de ClH 0.1 N, lentamente y con agitacin, hasta decoloracin de la disolucin. - Aadir 2 3 gotas de disolucin de naranja de metilo. - Continuar la valoracin hasta viraje del indicador de amarillo a rojonaranja. - Anotar el volumen V (ml) gastado y calcular el factor F de la disolucin
You might also like
- Accesibilidad símboloDocument7 pagesAccesibilidad símboloDavid Buritica Marin100% (1)
- Análisis Agua DurezaDocument15 pagesAnálisis Agua DurezaOty Ruiz LaulateNo ratings yet
- TDR Apuntalamiento GlorietaDocument4 pagesTDR Apuntalamiento GlorietaLeandro Valdivieso AntonNo ratings yet
- X. Preparación y Estandarización de SolucionesDocument22 pagesX. Preparación y Estandarización de SolucionesEd CotNo ratings yet
- Estandarización de Disoluciones ValorantesDocument7 pagesEstandarización de Disoluciones ValorantesGabriel Rojas del CuadroNo ratings yet
- ESTANDARIZACIÓN DE UNA DISOLUCIÓN DE HCLDocument1 pageESTANDARIZACIÓN DE UNA DISOLUCIÓN DE HCLLina Guerrero Ochoa100% (2)
- Preparacion de SolucionesDocument5 pagesPreparacion de SolucionesMaruja Del Pópolo GrzonaNo ratings yet
- Modelo PreinformeDocument14 pagesModelo PreinformeKevin Rosero ChilamaNo ratings yet
- Preparación y estandarización de soluciones ácido-base para análisis volumétricoDocument2 pagesPreparación y estandarización de soluciones ácido-base para análisis volumétricoAle JaimeNo ratings yet
- Practica de VolumetriaDocument5 pagesPractica de VolumetriaAlexander Guarenas-ManzanoNo ratings yet
- TP 1 - Volumetria Acido BaseDocument6 pagesTP 1 - Volumetria Acido BaseShoot DieselNo ratings yet
- Informe de SolucionesDocument11 pagesInforme de SolucionesJhonatan Jesus Peña BeldyNo ratings yet
- Anexo 2 Preparación de Soluciones 1-6Document6 pagesAnexo 2 Preparación de Soluciones 1-6Juan Pa Velazquez TamayoNo ratings yet
- Quimica IndustrialDocument19 pagesQuimica IndustrialOscar HuertaNo ratings yet
- Redo XXXDocument9 pagesRedo XXXantonesproNo ratings yet
- TEMA 6 Preparacion de AcidosDocument46 pagesTEMA 6 Preparacion de AcidosYENNE MIRYAN MUÑOZ HUARANCCANo ratings yet
- Esque MaDocument23 pagesEsque MaJoannie S'cNo ratings yet
- Guia Practica 4 - Analisis de AguaDocument6 pagesGuia Practica 4 - Analisis de AguaArturo BasantezNo ratings yet
- Determinacion Del Dioxido de Azufre Por El Metodo ColorimetricoDocument7 pagesDeterminacion Del Dioxido de Azufre Por El Metodo ColorimetricoML XairoNo ratings yet
- Preparación de SolucionesDocument4 pagesPreparación de SolucionesAugusto M. RouxNo ratings yet
- Informe. Práctica 2Document16 pagesInforme. Práctica 2Melina HernándezNo ratings yet
- Práctica Acido AceticoDocument5 pagesPráctica Acido AceticoluceroNo ratings yet
- Estandarización de disoluciones valorantesDocument2 pagesEstandarización de disoluciones valorantesCarolinaQuimbayaNo ratings yet
- Acido AceticoDocument3 pagesAcido AceticoPamelaNo ratings yet
- ACIDEZ Sanitaria LaboratorioDocument9 pagesACIDEZ Sanitaria LaboratorioAndrea Carolina Peñaranda BlancoNo ratings yet
- Acido AceticoDocument3 pagesAcido AceticoFátima PonceNo ratings yet
- Antes de La Practica 10 PQADocument4 pagesAntes de La Practica 10 PQACesia CastilloNo ratings yet
- Volumetria de NeutralizacionDocument12 pagesVolumetria de Neutralizacionjuan carlosNo ratings yet
- Análisi Quelatométrico de Plomo en Concentrados 2Document7 pagesAnálisi Quelatométrico de Plomo en Concentrados 2KevinSalazarNo ratings yet
- Preparación de Soluciones para Indice de YodoDocument2 pagesPreparación de Soluciones para Indice de YodoCAROLINA RODRÍGUEZ CARDONANo ratings yet
- Preparacion de SolucionesDocument4 pagesPreparacion de SolucionesDaniel Apaza SolanoNo ratings yet
- Acidimetria y AlcalimetriaDocument2 pagesAcidimetria y AlcalimetriaSandoval Angeliica67% (3)
- Anexo 1 Cyta IVDocument6 pagesAnexo 1 Cyta IVRené SalgadoNo ratings yet
- Practica 4 Agua OxigenadaDocument5 pagesPractica 4 Agua OxigenadaMaria JaraNo ratings yet
- Diagrama EpoxidoDocument2 pagesDiagrama EpoxidoSandraNo ratings yet
- Trabajo Practico Sobre Preparacion de SolucionesDocument7 pagesTrabajo Practico Sobre Preparacion de SolucionesSebastián Tovar MolinaNo ratings yet
- Guia Practica 5 Analisis de AguaDocument6 pagesGuia Practica 5 Analisis de AguaIsabel PachuchoNo ratings yet
- Preparación y valoración de soluciones de HCl y NaOHDocument3 pagesPreparación y valoración de soluciones de HCl y NaOHBRIGITH STHEFANIA BENITES GARCIANo ratings yet
- Practica 2Document7 pagesPractica 2Daniel SantillánNo ratings yet
- Química Inorgánica Practico #1Document5 pagesQuímica Inorgánica Practico #1Maruja Del Pópolo GrzonaNo ratings yet
- Universidad Autónoma "Benito Juárez" de Oaxaca: Facultad de Ciencias QuimicasDocument7 pagesUniversidad Autónoma "Benito Juárez" de Oaxaca: Facultad de Ciencias QuimicasDiego O PerezNo ratings yet
- Valoracion 1Document8 pagesValoracion 1Angie CampoverdeNo ratings yet
- Informes TodoDocument98 pagesInformes TodoHappy MomentsNo ratings yet
- PRÁCTICA 3. PREPARACIÓN DE NaOH 0.1 MDocument3 pagesPRÁCTICA 3. PREPARACIÓN DE NaOH 0.1 MAlejandro Montalvo100% (1)
- LABORATORIO DurezaDocument3 pagesLABORATORIO DurezaeddyNo ratings yet
- Mga SDocument30 pagesMga SGwenderland LpzNo ratings yet
- AcidezDocument47 pagesAcidezSheler Perez NzNo ratings yet
- Bebidas alcohólicas y análisisDocument5 pagesBebidas alcohólicas y análisisSeoba LeeNo ratings yet
- Oxigeno DisueltoDocument5 pagesOxigeno DisueltoYiya CamargoNo ratings yet
- Preparación y Valoración de Una Disolucion de NCL 0.1 NDocument2 pagesPreparación y Valoración de Una Disolucion de NCL 0.1 NluisNo ratings yet
- Soluciones QuimicasDocument12 pagesSoluciones QuimicasANo ratings yet
- Reporte de Practica LAQIDocument9 pagesReporte de Practica LAQIErick CastellanosNo ratings yet
- Preparación y Normalización de Una Solución de EdtaDocument5 pagesPreparación y Normalización de Una Solución de EdtaRodrigoMoranCoralNo ratings yet
- Acidos Bases EstandarDocument2 pagesAcidos Bases EstandarRomina CentofanteNo ratings yet
- Guia de TPsDocument25 pagesGuia de TPsGastón AristizabalNo ratings yet
- Práctica Acidez IntercambiableDocument3 pagesPráctica Acidez IntercambiableJorge Jaramillo50% (2)
- Preparacion y Valoracion de HCL 0Document62 pagesPreparacion y Valoracion de HCL 0Merly Lizeth Aparicio Cayetano50% (4)
- EDTA-CS-FEUM 10ed Tomo I v1Document3 pagesEDTA-CS-FEUM 10ed Tomo I v1Yamilet MenfozaNo ratings yet
- Preparación de soluciones estándaresDocument7 pagesPreparación de soluciones estándaresIvan TotoNo ratings yet
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadFrom EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadNo ratings yet
- 2 FCuantica ACTDocument9 pages2 FCuantica ACTrocio sanchezNo ratings yet
- Tipos de MarketingDocument1 pageTipos de MarketingMathius Nuñez CasillaNo ratings yet
- Derechos Humanos FundamentosDocument6 pagesDerechos Humanos FundamentosyonivelNo ratings yet
- Cómo Se Identifican Las Averías Por Sobretensión en TransformadoresDocument5 pagesCómo Se Identifican Las Averías Por Sobretensión en TransformadoresLedred1No ratings yet
- Técnicas e Instrumentos para Recolección de DatosDocument4 pagesTécnicas e Instrumentos para Recolección de DatosAnayelii MoOralezNo ratings yet
- Símbolos MatemáticosDocument5 pagesSímbolos MatemáticosBaldomero Vasquez GonzalezNo ratings yet
- La Tradición Draconiana y El Left Hand PathDocument5 pagesLa Tradición Draconiana y El Left Hand PathDevanandaNo ratings yet
- Los efectos psicológicos de la ausencia paternaDocument2 pagesLos efectos psicológicos de la ausencia paternasariangel39100% (1)
- Nueva PlanificaciónDocument4 pagesNueva PlanificaciónEric GuillenNo ratings yet
- 04 Educacion para La SaludDocument21 pages04 Educacion para La SaludCarmenTatianaCadimaMarañon100% (1)
- Formato ReservacionDocument2 pagesFormato ReservacionLUIS100% (1)
- Organizador Gráfico de Las 3 Generaciones de La TCC - Katia CondoriDocument3 pagesOrganizador Gráfico de Las 3 Generaciones de La TCC - Katia Condorikatia Condori100% (2)
- Prueba de DiagnósticoDocument19 pagesPrueba de DiagnósticoPriscila Catalan SotoNo ratings yet
- Practica 4 Ingenieria de ControlDocument6 pagesPractica 4 Ingenieria de ControlKOLEMANNo ratings yet
- Anexo 1. Caso de Estudio Unidad 2 Fase 3 INTELIGENCIA DE NEGOCIOSDocument18 pagesAnexo 1. Caso de Estudio Unidad 2 Fase 3 INTELIGENCIA DE NEGOCIOSluisa fernanda pinillos peñaNo ratings yet
- Estándares de Informes de Artículos de Metaanálisis CualitativoDocument3 pagesEstándares de Informes de Artículos de Metaanálisis CualitativoUNIVERSIDAD DEL SURESTE UDS LOS REYES LA PAZNo ratings yet
- Lobo EsteparioDocument2 pagesLobo EsteparioAlejandro ValenciaNo ratings yet
- 738-748 TSP1 - 2023-2Document3 pages738-748 TSP1 - 2023-2NayibyNo ratings yet
- Objetivos PPP IIIDocument2 pagesObjetivos PPP IIIAlexNo ratings yet
- Lista de Empresas para ContactarDocument11 pagesLista de Empresas para Contactarisabel_93_2011No ratings yet
- Tarea 3 ADocument5 pagesTarea 3 AMk LucyNo ratings yet
- Construcción embarcaciones pesquerasDocument28 pagesConstrucción embarcaciones pesquerasJean GomezNo ratings yet
- Obtencion de NitratosDocument7 pagesObtencion de NitratosAdrian VelascoNo ratings yet
- Procesos Del Yogurt de GuanábanaDocument4 pagesProcesos Del Yogurt de GuanábanaRoy Medina VilcapomaNo ratings yet
- 200 Tareas Terapia BreveDocument5 pages200 Tareas Terapia BrevePremarthi PrabhuNo ratings yet
- TOPCART2016 L5 Observacion v20170222Document252 pagesTOPCART2016 L5 Observacion v20170222juanhk69100% (1)
- Indicadores de Logro Tesis GuatemalaDocument96 pagesIndicadores de Logro Tesis GuatemalaKaren Olivares0% (1)