Professional Documents
Culture Documents
Tema - 1 - Formulacion - Inorganica PDF
Uploaded by
JavierOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Tema - 1 - Formulacion - Inorganica PDF
Uploaded by
JavierCopyright:
Available Formats
1 BACHILLERATO
Qumica I
FORMULACIN / FORMULACIN INORGNICA
TEMA Te 1.
FORMULACIN INORGNICA
1. Introduccin a la qumica inorgnica.
Qumica inorgnica. Compuesto orgnico. Valencia. Frmula qumica. Formular y nombrar. Nomenclaturas. Tabla de valencias. Clasificacin de los compuestos inorgnicos.
2. Combinaciones binarias con el oxgeno.
2.1 xidos metlicos.. 2.2 xidos no metlicos.
3. Perxidos. 4. Combinaciones binarias con el hidrgeno.
4.1 Hidruros metlicos. 4.2 Hidruros no metlicos. 4.2.1. Hidruros no metlicos de los grupos 13, 14 y 15. 4.2.2. Hidruros no metlicos de los grupos 16 y 17. cidos hidrcidos.
5. Sales binarias y sales de amonio.
5.1 Sales binarias. 5.2 Sales de amonio.
6. Combinaciones binarias entre no metales. 7. Hidrxidos. 8. cidos oxcidos.
8.1 cidos oxcidos de Cl, Br y I. 8.2 cidos oxcidos de C. 8.3 cidos oxcidos de N. 8.4 cidos oxcidos de S ,Se y Te. 8.5 cidos oxcidos de B, P, As, Sb y Si. 8.6 cidos oxcidos de Cr y Mn.
9. Sales de cidos oxcidos.
9.1 Sales neutras de cidos oxcidos. 9.2 Sales cidas de cidos oxcidos.
10. Iones.
10.1 Iones monoatmicos. 10.2 Iones poliatmicos. 10.3 Disolucin de cidos, hidrxidos y sales. Disociacin.
Alejandro Jimnez Cano
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Perxidos.
1.
INTRODUCCIN A LA QUMICA INORGNICA
La qumica inorgnica es la parte de la qumica que estudia la formacin, formulacin y reacciones
entre compuestos inorgnicos.
Un compuesto inorgnico es en general cualquier compuesto que no posea enlaces covalentes entre
tomos de carbono o entre el carbono y otros elementos como el hidrgeno. # Se dice en general porque algunos compuestos que contienen carbono, como los carbonatos, son inorgnicos.
La valencia o nmero de valencia representa la capacidad de un tomo para combinarse con otros
mediante enlaces qumicos. # Ms adelante se comprobar que la valencia es el nmero de electrones que el tomo tiende a ceder, ganar o compartir, para ser estable. Observa la tabla de valencias en la pgina siguiente. Los compuestos se representan mediante frmulas qumicas.
Una frmula qumica es la representacin simblica de la molcula o unidad estructural de una
sustancia qumica. Contiene los smbolos de los elementos que forman el compuesto y junto a ellos, unos subndices que indican el nmero de tomos de dichos elementos. # CO2 es la frmula qumica del dixido de carbono. # KOH es la frmula qumica del hidrxido de potasio. # H2Se es la frmula qumica del seleniuro de hidrgeno. # HNO2 es la frmula qumica del cido nitroso.
Formular un compuesto es representar su frmula qumica. Nombrar un compuesto es simplemente decir o escribir el nombre del compuesto representado por
su frmula qumica El nombre que recibe un compuesto no es arbitrario sino que sigue las reglas de una nomenclatura. Se aceptan tres nomenclaturas para nombrar los compuestos inorgnicos: la nomenclatura sistemtica o de la IUPAC (tambin llamada estequiomtrica), la nomenclatura Stock y la nomenclatura tradicional. 1) Nomenclatura sistemtica o de la IUPAC. (International Union of Pure and Applied Chemistry) Es aquella en la que se utilizan prefijos numerales griegos: mono, di, tri, tetra, penta, hexa, hepta, octa, enea, deca, endeca, dodeca... # Pb(OH)4: tetrahidrxido de plomo. # Cl2O5 pentaxido de dicloro. Si el elemento tiene valencia nica y es 1, no es necesario poner el prefijo mono.
Alejandro Jimnez Cano
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Perxidos.
TABLA DE VALENCIAS DE LOS ELEMENTOS MS IMPORTANTES DEL SISTEMA PERIDICO
Metales 1 Litio Sodio Potasio Rubidio Cesio Francio Plata 1, 2 Cobre Mercurio 2, 4 Estao Plomo Platino * Valencia como no metal. Otras valencias que conviene conocer son las siguientes: Titanio (Ti): 3, 4 Bismuto (Bi): 3, 5 Uranio (U): 3, 4, 6 Vanadio (V): 2, 3, 4, 5 Wolframio (W): 2, 3, 4, 5, 6 Li Na K Rb Cs Fr Ag 2 Berilio Magnesio Calcio Estroncio Bario Radio Zinc Cadmio 1, 3 Oro Talio 2, 3, 6* Cromo Be Mg Ca Sr Ba Ra Zn Cd Au Tl 3 Aluminio Al
Cu Hg
Sn Pb Pt
Cr
2, 3 Hierro Cobalto Nquel 2, 3, 4, 6*, 7* Manganeso
Fe Co Ni Mn
No metales 1 2 Hidrgeno H Oxgeno Otros no metales Boro Carbono*, silicio Nitrgeno*, fsforo, arsnico, antimonio Azufre, selenio, teluro Cloro, bromo, yodo O B C, Si N, P, As, Sb S, Se, Te Cl, Br, I 1 Flor Con H (y metales) 3 4 3 2 1 F Con O 3 4 3, 5 4, 6 1, 3, 5, 7
* Al formar xidos (pero no oxocidos) el carbono tambin presenta valencia 2; y el nitrgeno 1, 2, 4.
Alejandro Jimnez Cano
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Perxidos.
2) Nomenclatura de Stock. En esta nomenclatura, cuando el elemento que forma el compuesto tiene ms de una valencia, sta se indica al final, en nmeros romano y entre parntesis: # Fe(OH)2: Hidrxido de hierro (II) # Fe(OH)3: Hidrxido de hierro (III). 3) Nomenclatura tradicional. (Se halla en desuso, se dar pero apenas la trabajaremos) En esta nomenclatura se distingue la valencia con que actan los elementos por medio de una serie de prefijos y sufijos que dependen del nmero de valencias que tenga dicho elemento, cuando el elemento: 1 valencia: -ico 2 valencias (en orden creciente): -oso, -ico 3 valencias (en orden creciente): Hipo-oso, -oso, -ico 4 valencias (en orden creciente): Hipo-oso, -oso, -ico, per-ico
CLASIFICACIN DE LOS COMPUESTOS INORGNICOS
Metlicos xidos Perxidos
Metal + grupo perxido Metal + O
No metlicos
No metal + O
Compuestos binarios (2 tomos distintos)
Metlicos
Metal + H
Ej.: Fe2O3 xido de hierro (III) Ej.: SO3 Trixido de azufre Ej.: Li2O2 Perxido de litio Ej.: CaH2 Hidruro de calcio Ej.: H2S Sulfuro de hidrgeno Ej.: NaCl Cloruro de sodio Ej.: CCl4 Tetracloruro de carbono Ej.: HNO3 cido ntrico Ej.: Al (OH)3 Hidrxido de aluminio Ej.: KNO3 Nitrato de potasio Ej.: Ba (SH)2 Hidrogeno sulfuro de bario Ej.: NaH2PO4 Dihidrgeno fosfato de sodio Ej.: Fe+2 In hierro (III) Ej.: (SO4)-2 In sulfato S-2 In sulfuro
Hidruros
No metlicos (si el no metal es
del grupo 16 o 17 se denominan cidos hidrcidos) No metal + H
Sales binarias
(sales neutras de cidos hidrcidos) Metal + No metal
Combinaciones binarias entre no metales
No metal + No metal
cidos oxcidos
H + No metal + O
Compuestos ternarios (3 tomos distintos)
Hidrxidos
Metal + OH
Sales neutras de cidos oxcidos
Metal + No metal + O
Sales cidas de cidos hidrcidos
Metal + H + No metal
Compuestos cuaternarios (4 tomos distintos) Iones
Sales cidas de cidos oxcidos
Metal + H + No metal + O
Iones monoatmicos Iones poliatmicos
Alejandro Jimnez Cano
10
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Combinaciones binarias con el oxgeno.
2.
COMBINACIONES BINARIAS CON EL OXGENO
Los xidos son combinaciones del oxgeno con cualquier elemento.
# Segn se combinen con metales o no metales, distinguimos dos tipos de xidos: metlicos y no metlicos.
2.1 XIDOS METLICOS (xidos bsicos)
xidos no metlicos: son combinaciones del oxgeno con un metal.
Formulacin: se escribe primero el smbolo del metal y despus el del oxgeno. Se intercambian las valencias y se simplifica si es posible.
# Ejercicio resuelto: Formula todos los xidos posibles de hierro. El hierro posee dos valencias: 2 y 3, por lo que se podrn formular dos xidos: Pasos: 1) Metal-Oxgeno 2) Se intercambian las valencias. 1) FeO 2) Fe2O2 3) FeO 1) FeO 2) Fe2O3 3) Se simplifica si es posible.
Para nombrar los xidos metlicos: Nomenclatura stock: se escribe oxido de + nombre del metal seguido de la valencia del metal entre parntesis (si es nica debe omitirse). Nomenclatura sistemtica: se escribe oxido de + nombre del metal y se aaden a la palabra oxido y al nombre del metal los prefijos convenientes (mono, di, tri, tetra, etc.) Nomenclatura tradicional: se escribe oxido de + nombre del metal aadiendo al nombre del metal los prefijos/sufijos correspondientes (-oso, -ico, etc). # Ejercicio resuelto: Nombra los dos xidos del hierro: Fe2O3 y FeO de todas las formas posibles. Fe2O3 : xido de hierro (III) trixido de dihierro xido frrico FeO : xido de hierro (II) monxido de hierro u xido de hierro xido ferroso
Alejandro Jimnez Cano
11
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Combinaciones binarias con el oxgeno.
2.2 XIDOS NO METLICOS (xidos cidos)
xidos no metlicos: son combinaciones del oxgeno con un no metal.
Formulacin: de la misma forma que los xidos metlicos. Para nombrar los xidos no metlicos: La nomenclatura tradicional que en vez de xido utilizaba la palabra anhdrido ha sido prcticamente desechada (no la estudiamos). Nomenclatura stock: de la misma forma que los xidos metlicos. Nomenclatura sistemtica: de la misma forma que los xidos metlicos. Es la que ms se utiliza actualmente. xidos del nitrgeno (es la nica excepcin en la que se utiliza la nomenclatura tradicional): Frmula N2O NO N2O3 NO2 N2O5 Stock xido de nitrgeno xido de nitrgeno xido de nitrgeno xido de nitrgeno xido de nitrgeno Sistemtica xido de dinitrgeno xido de nitrgeno Trixido de dinitrgeno Dixido de nitrgeno Pentaxido de nitrgeno Tradicional xido nitroso xido ntrico -
Tambin existe el compuesto N2O4 (sin simplificar) llamado tetraxido de dinitrgeno. No se puede nombrar con la nomenclatura de Stock pues usara la misma denotacin que el xido de nitrgeno (IV).
Alejandro Jimnez Cano
12
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Combinaciones binarias con el oxgeno.
# Ejercicios de xidos metlicos y xidos no metlicos: 1. Formula los siguientes xidos metlicos: a) xido de dipotasio. b) xido de calcio. c) Monxido de dilitio. d) xido cprico. e) xido de plomo (II). f) xido de cobalto (III) g) Monxido de estao. h) xido de plomo (IV).
Solucin: a) K2O b) CaO c) Li2O d) CuO e) PbO f) Co2O3 g) SnO h) PbO2
2.
Nombra (de todas las formas que sepas) los siguientes xidos metlicos: a) PbO2 f) Cu2O b) Na2O g) Hg2O c) FeO h) NiO d) Ag2O i) BaO e) CoO j) PtO2
Solucin: a) Dixido de plomo. xido de plomo (IV). xido plmbico b) xido de disodio. xido de
sodio. xido sdico c) Monxido de hierro. xido de hierro (II). xido ferroso. d) Monxido de diplata. xido de plata. xido argntico. e) Monxido de cobalto. xido de cobalto (II). xido cobaltoso. f) Monxido de dicobre. xido de cobre (I). xido cuproso. g) Monxido de dimercurio. xido de mercurio (I). xido mercuroso. h) Monxido de nquel. xido de nquel (II). xido niqueloso. i) Monxido de bario. xido de bario. xido brico. j) Dixido de platino. xido de platino (IV). xido platnico. 3. Formula todos los xidos posibles de azufre, del silicio y del fsforo.
Solucin: SO2, SO3, SiO2, P2O3, P2O5
4.
Formula los siguientes xidos no metlicos: a) Dixido de silicio. b) xido de yodo (V). c) Dixido de carbono. d) xido de fsforo (III). e) xido de arsnico (V). f) xido sulfrico. g) Monxido de carbono. h) Dixido de teluro.
Solucin: a) SiO2 b) I2O5 c) CO2 d) P2O3 e) As2O5 f) SO3 g) CO h) TeO2
5.
Nombra (de todas las formas que sepas) los siguientes xidos no metlicos: a) NO g) N2O b) N2O4 h) SO2 c) P2O5 i) TeO3 d) Cl2O7 j) I2O5 e) Cl2O3 k) N2O5 f) Br2O3 l) Cl2O
Solucin: a) Monxido de nitrgeno. xido de nitrgeno (II). xido ntrico. b)
Tetraxido de dinitrgeno. c) Pentaxido de difsforo. xido de fsforo (V). d) Heptaxido de dicloro. xido de cloro (VII). e) Trixido de dicloro. xido de cloro (III) f) Trixido de dibromo. xido de bromo (III). g) Monxido de dinitrgeno. xido de nitrgeno (I). xido nitroso. h) Dixido de azufre. xido de azufre (IV). i) Trixido de teluro. xido de teluro (VI). j) Pentaxido de diyodo. xido de yodo (V). k) Pentaxido de dinitrgeno. xido de nitrgeno (V). l) Monxido de dicloro. xido de cloro (I)
Alejandro Jimnez Cano
13
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Perxidos.
3.
PERXIDOS
Los perxidos son combinaciones de un metal con el grupo perxido.
# Grupo perxido: O2 2 OO
El grupo perxido tiene valencia 2. Formulacin: se escribe primero el metal y despus el grupo perxido. Se intercambian las valencias y se simplifica siempre que el grupo perxido quede al menos con subndice 2.
# Ejercicio resuelto: Formula el perxido de magnesio y el perxido de litio. La valencia del magnesio es: 2. La valencia del litio es: 1. Pasos: 1) Metal-Grupo perxido 2) Se intercambian las valencias. 3) Se simplifica siempre que el subndice del grupo perxido sea mnimo 2. 1) MgO2 2) Mg2(O2)2 Mg2O4 3) MgO2 1) LiO2 2) Li2(O2)1 Li2O2 (No se puede simplificar)
Para nombrar los perxidos: se utiliza la palabra perxido seguida del nombre del metal. # El agua oxigenada comn es una disolucin de perxido de hidrgeno H2O2 en agua. # Ejercicios de perxidos: 6. Formula los siguientes perxidos: a) Perxido de radio. b) Perxido de calcio. c) Perxido de cesio. d) Perxido de sodio.
Solucin: a) RaO2 b) CaO2 c) Cs2O2 d) Na2O2
7.
Nombra los siguientes perxidos: a) H2O2 b) SrO2 c) BeO2 d) K2O2
Solucin: a) Perxido de hidrgeno. b) Perxido de estroncio. c) Perxido de berilio. d) Perxido de potasio.
Alejandro Jimnez Cano
14
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Combinaciones binarias con el hidrgeno.
4.
COMBINACIONES BINARIAS CON EL HIDRGENO
Los hidruros son combinaciones del hidrgeno con cualquier elemento.
# Segn se combinen con metales o no metales, distinguimos dos tipos de hidruros: metlicos y no metlicos. Los hidruros no metlicos se subdividen en dos grupos, como se ver posteriormente. 4.1 HIDRUROS METLICOS
Hidruros metlicos: son combinaciones del hidrgeno con un metal.
Formulacin: se escribe primero el smbolo del metal y despus el del hidrgeno. Se intercambian las valencias.
# Ejercicio resuelto: Formula todos los hidruros de hierro. El hierro posee dos valencias: 2 y 3, por lo que se podrn formular dos hidruros: Pasos: 1) Metal-Hidrgeno 2) Se intercambian las valencias. 1) FeH 2) FeH2 1) FeH 2) FeH3
Para nombrar los hidruros metlicos: Nomenclatura stock: se escribe hidruro de + nombre del metal seguido de la valencia del metal entre parntesis (si es nica debe omitirse). Nomenclatura sistemtica: se escribe hidruro de + nombre del metal y se aaden a la palabra hidruro y al nombre del metal los prefijos convenientes (mono, di, tri, tetra, etc.) Nomenclatura tradicional: se desaconseja su uso, por lo que no trabajaremos con esta nomenclatura. Sigue las mismas pautas que en los xidos.
# Ejercicio resuelto: Nombra los dos hidrxidos del hierro: Fe2O3 y FeO de todas las formas posibles (exceptuando la tradicional). FeH3 : hidruro de hierro (III) trihidruro de hierro FeH2 : hidruro de hierro (II) dihidruro de hierro
Alejandro Jimnez Cano
15
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Combinaciones binarias con el hidrgeno.
4.2 HIDRUROS NO METLICOS
Hidruros no metlicos: son combinaciones del hidrgeno con un no metal.
Los hidruros no metlicos se subdividen en dos grupos: los hidruros que resultan de la combinacin de no metales de los grupos 13, 14 y 15 con el hidrgeno; y los que resultan de la combinacin de no metales de los grupos 16 y 17 con el hidrgeno (cidos hidrcidos). 4.2.1 HIDRUROS NO METLICOS de los grupos 13(B), 14(C, Si) y 15 (N, P, As, Sb). Formulacin: se escribe primero el smbolo del no metal y despus el del hidrgeno. Se intercambian las valencias. Para nombrar este tipo de hidruros no metlicos se utiliza la nomenclatura sistemtica, aunque muchos de estos compuestos poseen nombres vulgares. Sistemtica Trihidruro de boro Tetrahidruro de silicio Trihidruro de nitrgeno Trihidruro de fsforo Trihidruro de arsnico Trihidruro de antimonio Nombre Borano Metano Silano Amonaco Fosfina Arsina Estibina
BH3 CH4 SiH4 NH3 PH3 AsH3 SbH3
4.2.2 HIDRUROS NO METLICOS de los grupos 16(S, Se, Te) y 17(F, Cl, Br, I). CIDOS HIDRCIDOS. Formulacin: se escribe primero el smbolo del hidrgeno y despus el del no metal. Se intercambian las valencias. Para nombrar este tipo de hidruros no metlicos se utiliza una nomenclatura muy concreta, que vara segn estn: En estado puro: nombre del no metal acabado en uro y se aade de hidrgeno. Disueltos en una disolucin acuosa: se escribe cido + nombre del no metal acabado en hdrico Nomenclatura cuando se halla en estado puro Sulfuro de hidrgeno Seleniuro de hidrgeno Telururo de hidrgeno Fluoruro de hidrgeno Cloruro de hidrgeno Bromuro de hidrgeno Yoduro de hidrgeno Nomenclatura cuando se halla en una solucin acuosa. cido sulfhdrico cido selenhdrico cido telurhdrico cido fluorhdrico cido clorhdrico cido bromhdrico cido yodhdrico
H2S H2Se H2Te HF HCl HBr HI
Ya que hablamos de los hidruros de no metales del grupo 16, no podemos dejarnos uno fundamental: H2O, que recibe un nombre muy especial agua. El agua no es un cido hidrcido.
Alejandro Jimnez Cano
16
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Combinaciones binarias con el hidrgeno.
# Ejercicios de hidruros metlicos e hidruros no metlicos: 8. Formula los siguientes hidruros metlicos: a) Dihidruro de mercurio. b) Hidruro de plomo (IV) c) Hidruro de cesio. d) Hidruro de potasio. e) Hidruro de oro (I). f) Trihidruro de cobalto. g) Dihidruro de nquel. h) Hidruro de radio.
Solucin: a) HgH2 b) PbH4 c) CsH d) KH e) AuH f) CoH3 g) NiH2 h) RaH2
9.
Nombra (sistemtica y Stock) los siguientes hidruros metlicos: a) NaH f) NiH3 b) AuH3 g) ZnH2 c) AgH h) CaH2 d) AlH3 i) HgH e) CoH2 j) PbH2
Solucin: a) Hidruro de sodio. b) Trihidruro de oro. Hidruro de oro (III). c) Hidruro de plata. d) Trihidruro
de aluminio. Hidruro de aluminio. e) Dihidruro de cobalto. Hidruro de cobalto (II). f) Trihidruro de nquel. Hidruro de nquel (III). g) Dihidruro de zinc. Hidruro de zinc. h) Dihidruro de calcio. Hidruro de calcio. i) Hidruro de mercurio. Hidruro de mercurio (I). j) Dihidruro de plomo. Hidruro de plomo (II). 10. Formula los siguientes hidruros no metlicos: a) cido fluorhdrico. b) Cloruro de hidrgeno. c) Metano. d) Yoduro de hidrgeno. e) cido sulfhdrico. f) Estibina. g) Amonaco. h) cido bromhdrico.
Solucin: a) HF b) HCl c) CH4 d) HI e) H2S f) SbH3 g) NH3 h) HBr
11.
Nombra los siguientes hidruros no metlicos: a) H2S f) HF b) AsH3 g) H2Te c) SiH4 h) H2Se d) BH3 i) HI e) PH3 j) HCl
Solucin: a) cido sulfhdrico. Sulfuro de hidrgeno. b) Arsina. c) Silano. d) Borano.
e) Fosfina. f) cido fluorhdrico. Fluoruro de hidrgeno. g) cido terurhdrico. Telururo de hidrgeno. h) cido selenhdrico. Seleniuro de hidrgeno. i) cido yodhdrico. Yoduro de hidrgeno. j) cido clorhdrico. Cloruro de hidrgeno.
Alejandro Jimnez Cano
17
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Sales binarias y sales de amonio.
5.
.SALES BINARIAS Y SALES DE AMONIO
5.1 SALES BINARIAS
Las sales binarias son combinaciones de un metal con un no metal.
Las sales binarias resultan de sustituir el hidrgeno de los cidos hidrcidos por un metal. Como se sustituye todo el hidrgeno tambin de denominan: sales neutras de cidos hidrcidos. Si solo se sustituyese parte del hidrgeno pasaran a ser sales cidas de cidos hidrcidos que se nombran igual pero aadiendo al principio: (se omite, di-, tri-,...)-hidrgeno,... segn el nmero de H que no se sustituyeron. # Por ellos los no metales actuarn con la misma valencia con la que actuaban con el hidrgeno (ver tabla de valencias). Observa: HCl NaCl H2Se Al2Se3 Formulacin: se escribe primero el smbolo del metal y despus el del no metal. Se intercambian las valencias. Se simplifica si es posible. Para nombrar las sales binarias: Nomenclatura stock: se cita el nombre del no metal con la terminacin uro seguido del nombre del metal y entre parntesis la valencia del metal (si es nica debe omitirse). Nomenclatura sistemtica: se escribe el nombre del no metal acabado en uro seguido nombre del metal; a ambos se les aaden los prefijos convenientes (mono, di, tri, tetra, etc.) Nomenclatura tradicional: se cita el no metal terminado en uro seguido del metal con los prefijos/sufijos correspondientes (-oso, -ico...).
# Ejercicio resuelto: Formula las sales binarias que resultan de combinar el nquel con el cloro de todas las formas posibles. El cloro con los metales acta con valencia 1. El nquel posee dos valencias: 2 y 3, por lo que se podrn formular dos sales: Pasos: 1) Metal-No metal 2) Se intercambian las valencias. 3) Se simplifica 1) NiCl 2) NiCl2 1) NiCl 2) NiCl3
Alejandro Jimnez Cano
18
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Sales binarias y sales de amonio.
# Ejercicios de sales binarias: 12. Formula y nombra (nomenclatura sistemtica y Stock) todas las sales binarias que resultan de combinar el magnesio, el cinc, el oro y el plomo con el bromo y el azufre. Con el azufre: MgS: Sulfuro de magnesio. ZnS: Sulfuro de cinc. Au2S: Sulfuro de dioro. Sulfuro de oro (I). Au2S3: Disulfuro de dioro. Sulfuro de oro (III). PbS: Sulfuro de plomo. Sulfuro de plomo (II). PbS2: Disulfuro de plomo. Sulfuro de plomo (IV).
Solucin:
Con el bromo: MgBr2: Dibromuro de magnesio. Bromuro de magnesio. ZnBr2: Dibromuro de cinco. Bromuro de cinc. AuBr: Bromuro de oro. Bromuro de oro (I). AuBr3: Tribromuro de oro. Bromuro de oro (III). PbBr2: Dibromuro de plomo. Bromuro de plomo (II). PbBr4: Tetrabromuro de plomo. Bromuro de plomo (IV). 13. Formula las siguientes sales binarias: a) Sulfuro de plomo (IV). d) Ioduro de mercurio (II). g) Bromuro de cobre (II). j) Sulfuro de clcio. l) Ag2S 14.
b) Seleniuro de aluminio. e) Tricloruro de nquel. h) Sulfuro de plomo (II). k) Trisulfuro de dihierro.
c) Bromuro de potasio. f) Sulfuro de hierro. i) Seleniuro de estao (IV). l) Sulfuro de diplata.
Solucin: a) PbS2 b) Al2Se3 c) KBr d) HgI2 e) NiCl3 f) FeS g) CuBr2 h) PbS i) SnSe2 j) CaS k) Fe2S3
Nombra (nomenclatura sistemtica y Stock) las sales binarias siguientes: a) FeI2 f) KCl k) Al2S3 b) CaS g) Co2S3 l) CaBr2 c) HgBr2 h) MgI2 m) CrCl3 d) Ag2Se i) Au2Se n) PtSe2 e) AuCl3 j) FeBr2 o) Ag2S
Solucin: a) Diyoduro de hierro. Yoduro de hierro (III). b) Sulfuro de calcio. c) Dibromuro de mercurio.
Bromuro de mercurio (II). d) Seleniuro de diplata. Seleniuro de plata. e) Tricloruro de oro. Cloruro de oro (III). f) Cloruro de potasio. g) Trisulfuro de dicobalto. Sulfuro de cobalto (III). h) Diyoduro de magnesio. Yoduro de magnesio. i) Seleniuro de dioro. Seleniuro de oro (I). j) Dibromuro de hierro. Bromuro de hierro (II). k) Trisulfuro de dialuminio. Sulfuro de aluminio. l) Dibromuro de calcio. Bromuro de calcio. m) Tricloruro de cromo. Cloruro de cromo (III). n) Diseleniuro de platino. Seleniuro de platino (IV). o) Sulfuro de diplata. Sulfuro de plata.
Alejandro Jimnez Cano
19
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Sales binarias y sales de amonio.
5.2 SALES DE AMONIO
Las sales de amonio son combinaciones del in amonio (NH4+) con un no metal.
Las sales de amonio resultan de sustituir el hidrgeno de los cidos hidrcidos por el in amonio. # El in amonio tiene valencia 1. Formulacin: de la misma manera que las sales binarias. Se nombran de la misma manera que las sales binarias aadiendo al final de amonio.
# Ejercicios de sales de amonio:
15.
Formula las siguientes sales de amonio: a) Bromuro de amonio. b) Cloruro de amonio. c) Telururo de amonio.
Solucin: a) NH4Br b) NH4Cl c) (NH4)2Te
16.
Nombra las siguientes sales de amonio: a) NH4Cl b) (NH4)2S c) (NH4)2Se d) NH4F
Solucin: a) Cloruro de amonio. b) Sulfuro de amonio. c) Seleniuro de amonio. d) Fluoruro de amonio.
Alejandro Jimnez Cano
20
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Combinaciones binarias entre nometales.
6.
COMBINACIONES BINARIAS ENTRE NO METALES
Ante las combinaciones binarias entre no metales surge la duda: cul se coloca a la izquierda en la frmula y cul a la derecha? El criterio que se utiliza para ello es la electronegatividad, concepto que se abordar con mayor profundidad posteriormente. # La electronegatividad es la capacidad de un tomo para captar y atraer los electrones hacia l. (Ms adelante se entender por qu es as) Los elementos de la tabla peridica de arriba y a la derecha son los ms electronegativos y los de abajo y a la izquierda los menos. A la hora de escribir un compuesto de este tipo se coloca a la izquierda el menos electronegativo y a la derecha el ms electronegativo. Nos deberamos mover en la tabla peridica de izquierda a derecha barriendo los grupos (columnas) de abajo hacia arriba: *** El oxgeno no se incluye pues en ese caso el compuesto sera un xido. B Boro C Carbono Si Silicio N Nitrgeno P Fsforo As Arsnico Sb Antimonio O*** Oxgeno S Azufre Se Selenio Te Teluro F Flor Cl Cloro Br Bromo I Yodo
Nos quedara la secuencia: B, Si, C, Sb, As, P, N, Te, Se, S, I, Br, Cl, F
# Sin embargo, esto no servir a la hora de nombrar y formular, pues las reglas de formulacin y nomenclatura nos permiten deducir cul va a cada lado. Formulacin: se coloca el ms electronegativo a la derecha (el que lleva el -uro) y se intercambian las valencias teniendo en cuenta que el ms electronegativo (el que se escribe a la derecha) acta con la misma valencia con que actuara si el otro elemento fuese un metal. El otro actuar con las valencias con que actuara en un xido. Se nombran de la misma manera que las sales binarias y con la nomenclatura sistemtica. Se aade el sufijo uro al ms electronegativo (al de la derecha). # Por ejemplo: Cl y P, el cloro es ms electronegativo, luego: PCl (cloro, valencia 1; fsforo, valencias: 3 y 5). PCl3 y PCl5, tricloruro de fsforo y pentacloruro de fsforo respectivamente. # Ejercicio de combinaciones no metal-no metal: 17. Formula o nombra los siguientes compuestos: a) IF3 b) As2Se3 f) Pentasulfuro de dinitrgeno. c) CS2 d) Si3N4 g) Dicloruro de diazufre. e) Hexafluoruro de azufre. h) Tetrayoduro de diarsnico.
Solucin: a) Trifluoruro de yodo. b) Triseleniuro de diarsnico. c) Disulfuro de carbono. d) Tetranitruro
de trisilicio. e) SF6 f) N2S5 g) S2Cl2 h) As2I4
Alejandro Jimnez Cano
21
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Hidrxidos.
7.
HIDRXIDOS
Los hidrxidos son combinaciones de un metal con el grupo hidroxilo.
# Grupo hidroxilo: OH # El grupo hidroxilo tiene valencia 1. Formulacin: se escribe primero el smbolo del metal y despus el OH. Se intercambian las valencias. Para nombrar los hidrxidos: Nomenclatura stock: se cita la palabra hidrxido seguida del metal y la valencia con que acta el metal entre parntesis (si es nica debe omitirse). Nomenclatura sistemtica: se escribe la palabra hidrxido anteponiendo un prefijo que indique el nmero de grupos OH, seguida del nombre del metal. Nomenclatura tradicional: se cita la palabra hidrxido seguida del nombre del metal con los prefijos/sufijos correspondientes (-oso, -ico,...) Al NaOH (hidrxido de sodio) tambin se le conoce como sosa castica.
# Ejercicio resuelto: Formula el hidrxido de hierro, actuando este ltimo con valencia 3. Nmbralo de todas las formas que sepas. Pasos: 1) Metal-OH 2) Se intercambian las valencias. 1) Fe(OH) 2) Fe(OH)3 Fe(OH)3 : Trihidrxido de hierro. Hidrxido de hierro (III). Hidrxido frrico.
# Ejercicios de hidrxidos: 18. Formula los siguientes hidrxidos: a) Hidrxido de cobre (II). b) Dihidrxido de nquel. c) Tetrahidrxido de plomo. d) Hidrxido de sodio. e) Hidrxido de cromo (III). f) Hidrxido de platino (II). g) Hidrxido de nquel (III). h) Hidrxido de estao (II). i) Hidrxido de clcio.
Solucin: a) Cu(OH)2 b) Ni(OH)2 c) Pb(OH)4 d) NaOH e) Cr(OH)3 f) Pt(OH)2 g) Ni(OH)3 h) Sn(OH)2
i) Ca(OH)2 19. Nombra (sistemtica y Stock) los siguientes hidrxidos: a) Au(OH)3 f) Mn(OH)2 b) LiOH g) Cu(OH)2 c) Mg(OH)2 h) Co(OH)3 d) AgOH i) Be(OH)2 e) Hg(OH)2 j) KOH
Solucin: a) Trihidrxido de oro. Hidrxido de oro (III) b) Hidrxido de litio. c) Dihidrxido de magnesio. Hidrxido de
magnesio. d) Hidrxido de plata. e) Dihidrxido de mercurio. Hidrxido de mercurio (II). f) Dihidrxido de manganeso. Hidrxido de manganeso (II). g) Dihidrxido de cobre. Hidrxido de cobre (II). h) Trihidrxido de cobalto. Hidrxido de cobalto (III). i) Dihidrxido de berilio. Hidrxido de berilio. j) Hidrxido de potasio.
Alejandro Jimnez Cano
22
1 BACHILLERATO
Qumica I
Formulacin inorgnica / cidos oxcidos.
8.
CIDOS OXCIDOS
Los cidos oxcidos u oxocidos son compuestos constituidos por oxgeno, hidrgeno y un no metal.
# Aparte de con no metales tambin hay cidos oxcidos con metales de transicin como el cromo (Cr) y el manganeso (Mn). Formulacin: podemos considerar los oxocidos como derivados de un xido no metlico al que se adiciona una o ms molculas de agua. El orden de los smbolos es: H + No metal + O Para nombrar los cidos oxcidos se utiliza principalmente la nomenclatura tradicional que consiste en la palabra cido seguida del no metal utilizando los prefijos / sufijos que correspondan segn la valencia: hipo-oso, -oso, -ico, per-ico.
8.1 CIDOS OXCIDOS DE Cl, Br y I (valencias 1, 3, 5, 7) Cl2O Cl2O3 Cl2O5 Cl2O7 + H2O + H2O + H2O + H2O H2Cl2O2 H2Cl2O4 H2Cl2O6 H2Cl2O8 HClO HClO2 HClO3 HClO4 cido hipocloroso cido cloroso cido clrico cido perclrico
Anlogamente se formulan los cidos oxcidos del bromo (Br) y del yodo (I).
8.2 CIDO OXCIDO DE C (valencia 4) CO2 + H2O H2CO3 cido carbnico
8.3 CIDOS OXCIDOS DE N (valencias 3, 5) N2O3 N2O5 + H2O + H2O H2N2O4 H2N2O6 HNO2 HNO3 cido nitroso cido ntrico
8.4 CIDOS OXCIDOS DE S, Se y Te (valencias 4, 6) SO2 SO3 + H2O + H2O H2SO3 H2SO4 cido sulfuroso cido sulfrico
Alejandro Jimnez Cano
23
1 BACHILLERATO
Qumica I
Formulacin inorgnica / cidos oxcidos.
8.5 CIDOS OXCIDOS DE B, P, As, Sb y Si Estos elementos pueden formar ms de un oxocido con la misma valencia. # Recuerda las valencias: B (3) / P, As, S (3, 5) / Si (4) Hay dos mtodos para hallar los diversos compuestos que se forman. Obsrvalos (presta atencin a la nomenclatura): Primer mtodo: xido no metlico + H2O Oxocido META Oxocido META + H2O Oxocido ORTO 2 Oxocido ORTO H2O Oxocido PIRO o DI Segundo mtodo (el que utilizaremos): xido no metlico + H2O Oxocido META xido no metlico + 2 H2O Oxocido PIRO o DI xido no metlico + 3 H2O Oxocido ORTO
# Del primer mtodo podemos deducir: Oxocido META + Oxocido ORTO Oxocido PIRO o DI # Usemos ambos mtodo para hallar los diversos cidos del fsforo. De entrada partimos de los dos xidos del fsforo (ya que posee valencia 3 y 5): P2O3 y P2O5: cido meta-...oso/ico P2O3 P2O5 P2O3 P2O5 + H2O + H2O + H2O + H2O H2P2O4 H2P2O6 H2P2O4 H2P2O6 HPO2 HPO3 HPO2 HPO3 cido metafosforoso cido metafosfrico cido metafosforoso cido metafosfrico
cido orto-...oso/ico (el orto se puede omitir) HPO2 HPO3 P2O3 P2O5 + H2O + H2O +3H2O H6P2O6 +3H2O H6P2O8 H3PO3 H3PO4 H3PO3 H3PO4 cido (orto)fosforoso cido (orto)fosfrico cido (orto)fosforoso cido (orto)fosfrico
cido piro/di-...oso/ico 2 H3PO3 2 H3PO4 P2O3 P2O5 H2O H2O +2H2O +2H2O H4P2O5 H4P2O7 H4P2O5 H4P2O7 cido pirofosforoso o difosforoso cido pirofosfrico o difosfrico cido pirofosforoso o difosforoso cido pirofosfrico o difosfrico
Alejandro Jimnez Cano
24
1 BACHILLERATO
Qumica I
Formulacin inorgnica / cidos oxcidos.
8.6 CIDOS OXCIDOS DE Cr y Mn Son importantes el cido crmico, el cido dicrmico, cido mangnico y cido permangnico. (Conviene memorizarlos) # Recuerda las valencias de estos elementos cuando se comportan como no metales: Cr (6) / Mn (6, 7) CrO3 2H2CrO4 MnO3 Mn2O7 +H2O H2O +H2O +H2O H2Mn2O8 H2CrO4 H2Cr2O7 H2MnO4 HMnO4 cido crmico cido dicrmico cido mangnico cido permangnico
# Ejercicios de cidos oxcidos: 20. Formula los siguientes cidos oxcidos: a) cido carbnico. d) cido permangnico. g) cido clrico. j) cido piroantimnico. m) cido mangnico. b) cido nitroso. e) cido dicrmico. h) cido teluroso. k) cido metaarsenioso. n) cido pirobrico. c) cido fosfrico. f) cido sulfuroso. i) cido perbrmico. l) cido ortosilcico. o) cido piroarsenioso.
Solucin: a) H2CO3 b) HNO2 c) H3PO4 d) HMnO4 e) H2Cr2O7 f) H2SO3 g) HClO3 h) H2TeO3
i) HBrO4 j) H4Sb2O7 k) HAsO2 l) H4SiO4 m) H2MnO4 n) H4B2O5 o) H4As2O5
21.
Nombra los siguientes cidos oxcidos: a) H2SO4 f) H4SiO4 k) HNO2 b) HNO3 g) H3PO3 l) H2SeO3 c) HMnO4 h) H2CrO4 m) HClO d) H3PO4 i) H2CO3 n) H3BO3 e) H4P2O7 j) HIO4 o) H6Si2O7
Solucin: a) cido sulfrico. b) cido ntrico. c) cido permangnico. d) cido (orto)fosfrico. e) cido
pirofosfrico. f) cido ortosilcico. g) cido (orto)fosforoso. h) cido crmico. i) cido carbnico. j) cido perydico. k) cido nitroso. l) cido selenioso. m) cido hipocloroso. n) cido (orto)brico. o) cido pirosilcico.
Alejandro Jimnez Cano
25
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Sales de cidos oxcidos.
9.
SALES DE CIDOS OXCIDOS
9.1 SALES NEUTRAS DE CIDOS OXCIDOS
Las sales neutras de cidos oxcidos u oxosales neutras son compuestos que derivan de los cidos
oxcidos en los que se han sustituido todos los hidrgenos por un metal o el in amonio (NH4+). Formulacin: observa el siguiente ejemplo.
# Ejercicio resuelto: Formula la oxosal neutra que resulta del cido fosfrico y el magnesio. El cido fosfrico: H3PO4 Una oxosal neutra resulta de sustituir todos los hidrgenos del cido por el metal en cuestin (Mg) H3PO4 Mg3PO4 (el metal hereda el subndice del H) A continuacin el magnesio pasa su valencia al resto de la molcula: (PO4): Mg3PO4 Mg 3(PO4) 2 Para terminar, se simplifica. En este caso no es posible.
Para nombrar sales neutras de cidos oxcidos: Nomenclatura tradicional: se cita en primer lugar el nombre del cido oxcido del que proviene cambiando el sufijo y/o prefijo (tal y como muestra la tabla siguiente) y despus el nombre del metal con los prefijos y sufijos correspondientes (-oso, -ico,...). Nomenclatura stock: se cita en primer lugar el nombre del cido oxcido del que proviene cambiando el sufijo y/o prefijo (tal y como muestra la tabla siguiente) y despus el nombre del metal con la valencia entre parntesis (Si es nica debe omitirse). * A la hora de nombrar se recomienda usar la de Stock puesto que la tradicional est cayendo en desuso. (En los ejercicios resueltos se nombrar con la dos nomenclaturas).
Prefijos y sufijos del cido oxcido Prefijos y sufijos de la sal neutra HIPO- -OSO (cido hipocloroso) HIPO- -ITO (hipoclorito de...) -OSO (cido cloroso) -ITO (clorito de...) -ICO (cido clrico) -ATO (clorato de...) PER- -ICO (cido perclrico) PER- -ATO (perclorato de...) Para recordar esto se suele utilizar la famosa frase: Cuando el OSO toca el pITO, FederICO toca el silbATO.
Alejandro Jimnez Cano
26
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Sales de cidos oxcidos.
# Ejercicios resueltos: 1. Nombra: a) MgSO3 El azufre indica que proviene de uno de los cidos oxcidos de azufre: H2SO3 / H2SO4 y el tres del oxgeno nos hace decantarnos por el primero de ellos. Hagamos ahora la comprobacin: H2SO3 Mg2(SO3)2 (simplificando) MgSO3 Como proviene del cido sulfuroso, recurramos a la tabla de prefijos y sufijos: -oso -ito ,, sulfuroso sulfito Como se trata de magnesio: sulfito de magnesio Finalmente escogemos nomenclatura: Tradicional: (como el Mg solo tiene una valencia, 2) sulfito magnsico Stock: (como el Mg solo tiene una valencia, 2) sulfito de magnesio b) Ca3(PO3)2 El fsforo indica que proviene de uno de los cidos oxcidos de fsforo: HPO2 / HPO3 / H3PO3 / H3PO4 / H4P2O5 / H4P2O5 Y el subndice del oxgeno (3) reduce nuestras posibilidades a dos: HPO3 / H3PO3 a continuacin observamos que el H que ha sido sustituido por el Ca posea subndice 3 por lo que nos decantamos por el segundo de ellos. Hagamos ahora la comprobacin: H3PO3 Ca3(PO3)2 Como proviene del cido (orto)fosforoso, recurramos a la tabla de prefijos y sufijos: -oso -ito ,, fosforoso fosfito Como se trata de calcio: fosfito de calcio Finalmente escogemos nomenclatura: Tradicional: (como el Ca solo tiene una valencia, 2) fosfito clcico Stock: (como el Ca solo tiene una valencia, 2) fosfito de calcio c) NaClO El cloro indica que proviene de uno de los cidos oxcidos del cloro: HClO / HClO2 / HClO3 / HClO4 Y el subndice del oxgeno (1) apunta a uno de ellos: HClO Hagamos ahora la comprobacin: HClO NaClO Como proviene del cido hipocloroso, recurramos a la tabla de prefijos y sufijos: Hipo- -oso Hipo- -ito ,, hipocloroso hipoclorito Como se trata de sodio: hipoclorito de sodio Finalmente escogemos nomenclatura: Tradicional: (como el Na solo tiene una valencia, 1) hipoclorito sdico Stock: (como el Na solo tiene una valencia, 1) hipoclorito de sodio
Alejandro Jimnez Cano
27
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Sales de cidos oxcidos.
2. Formula: a) Carbonato de litio. De la palabra carbonato deducimos: proviene de un cido del carbono y, ms concretamente por la terminacin ato, del cido carbnico: H2CO3 Como el litio solo tiene una valencia, sustituimos el H por Li y pasamos la valencia del litio (1) al resto: Li 2 CO 3 b) Clorito de calcio. De la palabra clorito deducimos: proviene de un cido del cloro y, ms concretamente por la terminacin ito, del cido cloroso: HClO2 Como el calcio solo tiene una valencia, sustituimos el H por Ca y pasamos la valencia del calcio (2) al resto: Ca (ClO 2) 2 c) Fosfato de hierro (II). De la palabra fosfato deducimos: proviene de un cido del fsforo y, ms concretamente por la terminacin ato, del cido fosfrico: H3PO4 El hierro posee dos valencias (2, 3) y la nomenclatura de Stock concretiza en una de ellas (II): Sustituimos el H por Fe y pasamos la valencia del hierro (2) al resto: Fe 3 (PO 4) 2 d) Dicromato de potasio. De la palabra dicromato deducimos: proviene de un cido del cromo y, ms concretamente por el comienzo y la terminacin Di...ato, del cido dicrmico: H2Cr2O7 Como el potasio solo tiene una valencia, sustituimos el H por K y pasamos la valencia del potasio (1) al resto: K 2 Cr 2 O 7 e) Sulfato de amonio. De la palabra sulfato deducimos: proviene de un cido del azufre y, ms concretamente por la terminacin ato, del cido sulfurico: H2SO4 Sustituimos el H por NH4 y pasamos la valencia del amonio (1) al resto: (NH 4) 2 SO 4
Alejandro Jimnez Cano
28
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Sales de cidos oxcidos.
9.2 SALES CIDAS DE CIDOS OXCIDOS
Las sales cidas de cidos oxcidos u oxosales cidas son compuestos que derivan de la sustitucin
parcial de los hidrgenos de los cidos oxcidos por un metal o el in amonio (NH4+). Formulacin: el metal toma el subndice del nmero de hidrgenos sustituidos. El resto de cido oxcido recibe la valencia del metal. Si es posible se simplifica. Para nombrar sales cidas de cidos oxcidos: usaremos la nomenclatura de Stock. Nomenclatura stock: se cita el nmero de hidrgenos presentes utilizando los prefijos mono-, di-, tri- (mono- puede omitirse). A continuacin se cita el nombre del cido oxcido del que proviene cambiando el sufijo y/o prefijo (oso ito / ico ato) y despus el nombre del metal con la valencia entre parntesis (Si es nica debe omitirse). Visualicemos todo esto con dos ejemplos: # H3PO4 (cido fosfrico) y Ca. Sustituimos un hidrgeno por el Ca. Ca(H2PO4) 2 Dihidrogenofosfato de calcio. Sustituimos dos hidrgenos por el Ca. Ca2 (HPO4) 2 CaHPO4 Dihidrogenofosfato de calcio. Sustituimos tres hidrgenos por el Ca. (Obtendramos la sal neutra) Ca3(PO4) 2 Fosfato de calcio. # H3PO4 (cido fosfrico) y Fe. (El hierro al poseer valencias 2 y 3 tendr dos posibilidades: ) Sustituimos un hidrgeno por el Fe. Fe(H2PO4) 2 Dihidrogenofosfato de hierro (II). Fe(H2PO4) 3 Dihidrogenofosfato de hierro (III). Sustituimos dos hidrgenos por el Fe. Fe2 (HPO4) 2 FeHPO4 Hidrogenofosfato de hierro (II). Fe2 (HPO4) 3 Hidrogenofosfato de hierro (III). Sustituimos tres hidrgenos por el Fe. (Obtendramos las sales neutras) Fe3 (PO4) 2 Fosfato de hierro (II). Fe3 (PO4) 3 Fosfato de hierro (III).
Alejandro Jimnez Cano
29
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Sales de cidos oxcidos.
# Ejercicios de oxosales neutras: 22. Formula las siguientes oxosales neutras: a) Nitrato de potasio. d) Selenito de cobre (II). g) Ortoantimoniato de nquel (III). j) Pirofosfato de cobalto (II). b) Perbromato de oro (III). e) Telurito de cobre (I). h) Silicato de plata. k) Cromato de bario. c) Sulfato de magnesio. f) Metarseniato de hierro (III). i) Carbonato de sodio. l) Metaborato de estroncio.
Solucin: a) KNO3 b) Au(BrO4)3 c) MgSO4 d) CuSeO3 e) Cu2TeO3 f) Fe(AsO3)3 g) NiSbO4
h) Ag4SiO4 i) Na2CO3 j) Co2P2O7 k) BaCrO4 l) Sr(BO2)2 23. Nombra las siguientes oxosales neutras con la nomenclatura Stock: a) AgMnO4 g) CoMnO4 b) Li4 As2O7 h) HgClO4 c) CsIO2 d) RaCr2O7 i) Au2(SO4)3 j) Sn(BrO)4 e) Rb3BO3 k) CuCO3 f) Pt(NO2)4 l) Al2(TeO3)3
Solucin: a) Permanganato de plata. b) Piroarseniato de litio. c) Yodito de cesio. d) Dicromato de radio.
e) Borato de rubidio. f) Nitrito de platino (IV). g) Manganato de cobalto (II). h) Perclorato de mercurio (I). i) Sulfato de oro (III) j) Hipobromito de estao (IV). k) Carbonato de cobre (II) l) Telurito de aluminio. # Ejercicios de oxosales cidas:
24.
Formula las siguientes oxosales cidas: a) Hidrogenosulfato de hierro(II). c) Hidrogenoantimoniato de mercurio(I). e) Hidrogenoseleniato de aluminio. g) Dihidrogenopirofosfato de estroncio. i) Trihidrogenopiroborato de oro (III) . k) Hidrogenocarbonato de cobalto (III). b) Dihidrogenoarseniato de plomo(II). d) Hidrogenoarseniato de cobre(II). f) Hidrogenotelurito de calcio. h) Hidrogenocarbonato de sodio. j) Dihidrogenofosfato de bario. l) Hidrogenomanganato de estao (IV).
Solucin: a) Fe(HSO4)2 b) Pb(H2 AsO4)2 c) Hg2HSbO4
g) SrH2P2O7 h) NaHCO3 i) Au(H3B2O5)3
d) CuHAsO4 e) Al(HSeO4)3 f) Ca(HTeO3)2 j) Ba(H2PO4)2 k) Co(HCO3)3 l) Sn(HMnO4)4
25.
Nombra las siguientes oxosales cidas con la nomenclatura Stock: a) NaHCO3 e) Ni2(HPO4)3 i) CuHAsO4 b) Fe(HSO4)3 f) KH2PO4 j) Pb(H2AsO4)2 c) Al(HSeO4)3 g) NaHTeO4 k) BaHSbO4 d) Mg(HMnO4)2 h) Ba(H2PO4)2 l) Hg(HCr2O7)2
Solucin: a) Hidrogenocarbonato de sodio. b) Hidrogenosulfato de hierro (III). c) Hidrogenoseleniato de
aluminio. d) Hidrogenomanganato de magnesio. e) Hidrogenofosfato de nquel (III). f) Dihidrogenofosfato de potasio. g) Hidrogenotelurato de sodio. h) Dihidrogenofosfato de bario. i) Hidrogenoarseniato de cobre (II). j) Dihidrogenoarseniato de plomo (II). k) Hidrogenoantimoniato de bario. l) Hidrogenodicromato de mercurio (II).
Alejandro Jimnez Cano
30
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Iones.
10
IONES
10.1 IONES MONOATMICOS Los metales tienen facilidad para ceder electrones y convertirse en iones positivos o cationes, con cambio los no metales captan electrones para quedar como iones negativos o aniones. IONES POSITIVOS Para nombrar iones positivos utilizaremos la nomenclatura de Stock, citando el nombre del metal y a continuacin la carga del in en nmeros romanos entre parntesis (indicando la valencia, la cul, si es nica, no se indica). H+ Mg+2 Ag+ Al+3 In hidrgeno. In magnesio. In plata. In aluminio. Na+ Ca+2 Fe+3 Cu+ In sodio. In calcio. In hierro (III). In cobre (I). K+ Zn+2 Fe+2 Cu+2 In potasio. In zinc. In hierro (II). In cobre (II).
IONES NEGATIVOS Para nombrar iones negativos utilizaremos la nomenclatura tradicional, en la que se cita el nombre del no metal seguido de la terminacin uro. La carga del no metal se corresponde con la valencia del no metal frente al hidrgeno. FITe-2 In fluoruro. In yoduro. In telururo. ClS-2 N-3 In cloruro. In sulfuro. In nitruro. BrSe-2 P-3 In bromuro. In seleniuro. In fosfuro.
10.2 IONES POLIATMICOS. Los cidos oxcidos se disocian en iones cuando se disuelven en agua. El anin recibe el nombre del cido oxcido del que proviene cambiando el sufijo y/o prefijo de una forma similar a como lo hacan al formar sales oxcidas. El catin es un in positivo monoatmico, que se nombra tal y como se explica en el apartado anterior. cido oxcido Anin Hipo- -oso Hipo- -ito -oso -ito -ico -ato Per- -ico Per- ato # Observa los siguientes ejemplos: a) cido hipocloroso b) cido ntrico c) cido sulfuroso d) cido permangnico HClO HNO3 H2SO3 HMnO4 H+ H+ 2H+ H+ *(ClO)*(NO3)*(SO3)-2 *(MnO4)In hipoclorito. In nitrato. In sulfito. In permanganato.
Alejandro Jimnez Cano
31
1 BACHILLERATO
Qumica I
Formulacin inorgnica / Iones.
Algunos cidos oxcidos pueden liberar sus iones H+ de forma escalonada. # Observa el siguiente ejemplo: cido fosfrico In dihidrogenofosfato In hidrogenofosfato. H3PO4 (H2PO4)*(HPO4)-2 H+ H+ H+ *(H2PO4)*(HPO4)-2 *(PO4)-3 In dihidrogenofosfato. In hidrogenofosfato. In fosfato.
** No es necesario escribir el anin entre parntesis pero as enfatizamos que la carga corresponde a la agrupacin de tomos y no slo al oxgeno. Caben destacar el in amonio: NH4+; y el in hidroxilo: OH10.3 DISOLUCIN DE CIDOS, HIDRXIDOS Y SALES. Cuando un cido, hidrxido o sal se disuelve en agua se disocia total o parcialmente en iones. Para realizar la disociacin correctamente hay que tener en cuenta el nmero de tomos de cada elemento en la molcula y mantener la neutralidad elctrica. cidos hidrcidos # HBr H+ y Br cidos oxcidos # HNO3 H+ y (NO3 )# H2SO4 2H+ y (SO4)-2 Hidrxidos # Al(OH)3 Al+3 y 3(OH)-
Oxosales # Ca(NO3)2 Ca+2 y 2(NO3)# Na2CO3 2Na+ y (CO3)-2
Sales binarias # NaCl Na+ y Cl# CaCl2 Ca+2 y 2Cl-2
# Ejercicio de iones: 26. Nombra los siguientes compuestos. Discialos y nombra los iones resultantes. a) Al(HTeO3)3 e) HgH2
Solucin:
b) FeCl3 f) H2SbO4 -
c) AuOH g) H2Cr2O7
d) Ni(H2PO4)3 h) Sn(OH)4
a) Hidrogenotelurito de aluminio. Al+3 (In aluminio) y 3HTeO3- (In hidrogenotelurito). b) Tricloruro de hierro. Fe+3 (In hierro (III)) y 3Cl- (In cloruro). c) Hidrxido de oro (I). Au+ (In oro (I)) y OH- (In hidroxilo). d) Dihidrogeno fosfato de nquel (III). Ni+3 (In nquel (III)) y 3H2PO4- (In dihidrogenofosfato). e) Hidruro de mercurio (II). Hg+2 (In mercurio (II)) y 2H- (In hidrgeno). f) In dihidrogenoantimoniato. 2H+ (In hidrgeno) y SbO4-3 (In antimoniato). g) cido dicrmico. 2H+ (In hidrgeno) y Cr2O7-2 (In dicromato). h) Hidrxido de estao (IV). Sn+4 (In estao (IV)) y 4OH- (In hidroxilo).
Alejandro Jimnez Cano
32
1 BACHILLERATO
Qumica I
Relacin de ejercicios de FORMULACIN INORGNICA
1.
Formula los siguientes compuestos inorgnicos: 1) Hidrxido de hierro (II). 2) Seleniuro de mercurio (II). 3) Carbonato de estroncio. 4) In fluoruro. 5) Hidrogenomanganato de magnesio. 6) Hidruro de estao (IV). 7) Ioduro de cobalto (II). 8) Amonaco. 9) Hidrogenosulfato de cobalto (II). 10) xido de cloro (III). 11) In trihidrogenodiantimonato. 12) cido mangnico. 13) Perxido de estroncio. 14) Trixido de dihierro. 15) Dihidrogenoarseniato de cobre (II). 16) Hidrxido de platino (II). 17) cido metafosfrico. 18) xido de radio. 19) cido metaantimonioso. 20) Cloruro de amonio. 21) Estibina. 22) Monxido de carbono. 23) cido crmico. 24) Sulfuro de titanio (IV). 25) Nitrato de sodio. 26) Hidrxido de rubidio. 27) Nitrito de estao (IV). 28) Hidrogenotelurito de calcio. 29) Sulfato de calcio. 30) In fosfuro. 31) cido selenioso. 32) Hidruro de bario. 33) Tribromuro de oro. 34) Hidrxido de mercurio (I). 35) cido hipocloroso. 36) Hidrogenoarseniato de cobre (II). 37) cido fluorhdrico. 38) Tetraxido de dinitrgeno. 39) Tricloruro de nquel. 40) Hidruro de rubidio. 41) In manganato. 42) Silicato de cesio. 43) Yoduro de hidrgeno. 44) Trixido de uranio. UO3 45) cido sulfuroso. 46) Tricloruro de oro. 47) Perxido de rubidio. 48) Hidrogenoantimoniato de cesio. 49) cido nitroso. 50) Piroarseniato de cobalto (III). 51) cido fosforoso. 52) Sulfuro de hidrgeno. 53) Seleniuro de amonio. 54) xido de mercurio (II). 55) Permanganato de oro (I). 56) Dihidrogenopirofosfato de estroncio. 57) Bromuro de magnesio. 58) In magnesio. 59) cido metaantimnico 60) xido de boro. 61) Hidrxido de cromo (II). 62) Hidrogenoseleniato de aluminio. 63) xido de titanio (IV). 64) In hidrogenodifosfato. 65) xido de silicio. 66) Sulfuro de plomo (II). 67) Tetrafluoruro de teluro. 68) xido de cobalto (III). 69) Hidrogenoselenito de aluminio. 70) Perxido de hidrgeno. 71) Sulfuro de diplata. 72) Heptafluoruro de yodo. 73) Hidruro de oro (III). 74) In mercurio (I). 75) Peryodato de hierro (III). 76) Hidrxido de oro (I). 77) cido piroarsenioso. 78) Ortoantimoniato de cobalto (III). 79) cido pirosilcico. 80) Sulfuro de amonio. 81) Hidruro de magnesio. 82) Hidrogenofosfato de nquel (III). 83) xido de plata. 84) cido carbnico. 85) Hidrxido de aluminio. 86) In carbonato. 87) Metaborato de magnesio. 88) cido brmico. 89) Hidrogenoantimoniato de bario. 90) Heptaxido de diyodo. 91) Hidruro de cobre (II). 92) Perxido de magnesio. 93) Hidruro de cadmio. 94) cido metabrico. 95) Hidrxido de magnesio. 96) Seleniuro de estao (IV). 97) Bromuro de platino (II). 98) Silano. 99) cido perydico. 100) Trihidrogenopiroborato de oro (III). 33
Alejandro Jimnez Cano
1 BACHILLERATO
Qumica I
Relacin de ejercicios de FORMULACIN INORGNICA
2.
Nombra los siguientes compuestos inorgnicos (una sola nomenclatura): 1) LiHTeO4 2) HClO3 3) (H2AsO4)4) Mn2O3 5) ZnH2 6) Co(OH)3 7) Ag2MnO4 8) HBrO2 9) H2O2 10) V2S3 11) RaSiO3 12) NH4I 13) HIO 14) AsH3 15) Au(HCO3) 3 16) AlCl3 17) Sb2O5 18) Hg2Se 19) ICl3 20) Br2O5 21) CoH3 22) (HSO4)23) HNO3 24) Ni(OH)3 25) PtSO4 26) H2CO3 27) CaO2 28) Sn(OH)4 29) BeH2 30) ZnO 31) AuH 32) H2SO4 33) Sn(NO3)4 34) N-3 35) FeI3 36) CuO 37) Zn(OH)2 38) H2TeO3 39) LiH 40) UO2 41) Cs2S 42) Zn+2 43) H3SbO3 44) RaHAsO4 45) Li3BO3 46) V2O3 47) Pt(OH)4 48) H3PO4 49) Cr(HCO3)2 50) BH3 51) H2Se 52) SnO2 53) NH4F 54) HPO2 55) Ni2Sb2O5 56) AuBr 57) Au2O 58) (H2SiO4)-2 59) Cu(H2AsO4)2 60) Au2CO3 61) NaCl 62) Cs2O2 63) Hg(H2PO4)2 64) H4Sb2O7 65) KOH 66) Be(IO3)2 67) VH5 68) Na+ 69) HAsO2 70) Pb(OH)2 71) CoCl3 72) Al(HSeO3)3 73) H3BO3 74) Ni2O3 75) KH 76) H2SiO3 77) Ca+2 78) CO2 79) HBr 80) CsOH 81) Li2O 82) RbH2PO4 83) H2Cr2O7 84) B2S3 85) Cl86) PtH2 87) SrBr2 88) SO2 89) (BrO4)90) Fe(HSO4)3 91) SnI2 92) PbS2 93) NH4Br 94) Mn(OH)4 95) Ca3(PO3)2 96) BaO2 97) Pt(HMnO4)4 98) HgH2 99) HMnO4 100) Zn(NO3)2
Alejandro Jimnez Cano
34
1 BACHILLERATO
Qumica I
Relacin de ejercicios de FORMULACIN INORGNICA
Solucin del ejercicio 1.
1) Fe(OH)2 2) HgSe 3) SrCO3 4) F- 5) Mg(HMnO4)2 6) SnH4 7) CoI2 8) NH3 9) Co(HSO4)210) Cl2O3 11) (H3Sb2O7)- 12) H2MnO4 13) SrO2 14) Fe2 O3 15) Cu(H2AsO4)2 16) Pt(OH)2 17) HPO3 18) RaO 19) HSbO2 20) NH4Cl 21) SbH3 22) CO 23) H2CrO4 24) TiS2 25) NaNO3 26) RbOH 27) Sn(NO2)4 28) Ca(HTeO3)2 29) CaSO4 30) P-3 31) H2SeO3 32) BaH2 33) AuBr3 34) HgOH 35) HClO 36) CuHAsO4 37) HF 38) N2O4 39) NiCl3 40) RbH 41) (MnO4)-2 42) Cs4SiO4 43) HI 44) 45) H2SO3 46) AuCl3 47) Rb2O2 48) Cs2HSbO4 49) HNO2 50) Co4(As2O7)3 51) H3PO3 52) H2S 53) (NH4)2Se 54) HgO 55) AuMnO4 56) SrH2P2O7 57) MgBr2 58) Mg+2 59) HSbO3 60) B2O3 61) Cr(OH)2 62) Al(HSeO4)3 63) TiO2 64) (HP2O7)-3 65) SiO2 66) PbS 67) TeF4 68) Co2O3 69) Al(HSeO3)3 70) H2O2 71) Ag2S 72) IF7 73) AuH3 74) Hg+ 75) Fe(IO4)3 76) AuOH 77) H4As2O5 78) CoSbO4 79) H6Si2O7 80) (NH4)2S 81) MgH2 82) Ni2(HPO4)3 83) Ag2O 84) H2CO3 85) Al(OH)3 86) (HCO3)- 87) Mg(BO2)2 88) HBrO3 89) BaHSbO4 90) I2O7 91) CuH2 92) MgO2 93) CdH2 94) HBO2 95) Mg(OH)2 96) SnSe2 97) PtBr2 98) SiH4 99) HIO4 100) Au(H3B2O5)3
Solucin del ejercicio 2.
1) Hidrogenotelurato de litio. 2) cido clrico. 3) In dihidrogenoarseniato. 4) Trixido de dimanganeso. 5) Hidruro de zinc. 6) Hidrxido de cobalto (III). 7) Manganato de plata. 8) cido bromoso. 9) Perxido de hidrgeno. 10) Sulfuro de vanadio (III). 11) Metasilicato de radio. 12) Yoduro de amonio. 13) cido hipoyodoso. 14) Arsina. 15) Hidrogenocarbonato de oro (III). 16) Tricloruro de aluminio. 17) xido de antimonio (V). 18) Seleniuro de cobre (I). 19) Tricloruro de yodo. 20) xido de bromo (V). 21) Hidruro de cobalto (III). 22) In hidrogenosulfato. 23) cido ntrico. 24) Hidrxido de nquel (III). 25) Sulfato de platino (II). 26) cido carbnico. 27) Perxido de calcio. 28) Hidrxido de estao (IV). 29) Hidruro de berilio. 30) xido de zinc. 31) Hidruro de oro (I). 32) cido sulfrico. 33) Nitrato de estao (IV). 34) In nitruro. 35) Ioduro de hierro (III). 36) Monxido de cobre. 37) Hidrxido de zinc. 38) cido teluroso. 39) Hidruro de litio. 40) Dixido de uranio. 41) Sulfuro de dicesio. 42) In zinc. 43) cido antimonioso. 44) Hidrogenoarseniato de radio. 45) Borato de litio. 46) xido de vanadio (III). 47) Hidrxido de platino (IV). 48) cido fosfrico. 49) Hidrogenocarbonato de cromo (II). 50) Borano. 51) Seleniuro de hidrgeno. 52) Dixido de estao. 53) Fluoruro de amonio. 54) cido metafosforoso. 55) Piroantimonito de nquel (II). 56) Monobromuro de oro. 57) Monxido de dioro. 58) In dihidrgenosilicato. 59) Dihidrogenoarseniato de cobre (II). 60) Carbonato de oro (I). 61) Cloruro de sodio. 62) Perxido de cesio. 63) Dihidrogenofosfato de mercurio (II). 64) cido piroantimnico. 65) Hidrxido de potasio. 66) Yodato de berilio. 67) Hidruro de vanadio (V). 68) In sodio. 69) cido metaarsenioso. 70) Hidrxido de plomo (II). 71) Tricloruro de cobalto. 72) Hidrogenoselenito de aluminio. 73) cido brico. 74) xido de nquel (III). 75) Hidruro de potasio. 76) cido metasilcico. 77) In calcio. 78) Dixido de carbono. 79) cido bromhdrico. 80) Hidrxido de cesio. 81) xido de litio. 82) Dihidrogenofosfato de rubidio. 83) cido dicrmico. 84) Trisulfuro de diboro 85) In cloruro. 86) Hidruro de platino (II). 87) Bromuro de estroncio. 88) Dixido de azufre. 89) In perbromato. 90) Hidrogenosulfato de hierro (III). 91) Ioduro de estao (II). 92) Sulfuro de plomo (IV). 93) Bromuro de amonio. 94) Hidrxido de manganeso (IV). 95) Fosfito de calcio. 96) Perxido de bario. 97) Hidrogenomanganato de platino (IV). 98) Hidruro de mercurio (II). 99) cido permangnico. 100) Nitrato de zinc.
Alejandro Jimnez Cano
35
You might also like
- NomenclaturaDocument17 pagesNomenclaturaVivi MoralesNo ratings yet
- Hid Roxi DosDocument5 pagesHid Roxi DosjoseNo ratings yet
- Que Pasa Cunado Chocan Los Atomos ActividadDocument6 pagesQue Pasa Cunado Chocan Los Atomos ActividadHumberto CortezNo ratings yet
- Polímeros NaturalesDocument65 pagesPolímeros NaturalesKatita Espinoza Calabran100% (2)
- Nomenclatura Inorganica 2021Document1 pageNomenclatura Inorganica 2021rafael linaresNo ratings yet
- Enlaces AtómicosDocument21 pagesEnlaces AtómicosJuan Salvador Jorquera MoralesNo ratings yet
- Resumen-De-Los-Principales-Casos-De-Factorizacion,-Con Teoria-Y-Ejemplos PDFDocument2 pagesResumen-De-Los-Principales-Casos-De-Factorizacion,-Con Teoria-Y-Ejemplos PDFJuan Guillermo Soto RincónNo ratings yet
- Clase 5 Constitución de Las AleacionesDocument29 pagesClase 5 Constitución de Las AleacionesDeboohZevallosNo ratings yet
- 513 Chávez Ocampos Indra Sherlín Act3QIIIDocument23 pages513 Chávez Ocampos Indra Sherlín Act3QIIISherlin ChávezNo ratings yet
- Las Reglas de CahnDocument5 pagesLas Reglas de CahnMarce Herrera BeltranNo ratings yet
- 3a Fisquim Modulo AnualDocument70 pages3a Fisquim Modulo AnualMariel IrustaNo ratings yet
- Nomenclatura InorgánicaDocument35 pagesNomenclatura InorgánicaRodrigo Vidal100% (1)
- Compuestos de Coordinacion.Document3 pagesCompuestos de Coordinacion.JnZNo ratings yet
- Ácidos OxácidosDocument5 pagesÁcidos Oxácidosscl11No ratings yet
- Profesoras Nombre Del Estudiante: Curso y División:: Instituto Nuestra Señora de La MercedDocument27 pagesProfesoras Nombre Del Estudiante: Curso y División:: Instituto Nuestra Señora de La MercedCele ZárateNo ratings yet
- Óxidos Básicos - QuimicaDocument6 pagesÓxidos Básicos - Quimicathania adela fernandez zuloetaNo ratings yet
- Taller Configuracion Electronica y T.P PDFDocument6 pagesTaller Configuracion Electronica y T.P PDFKiara Mosquera RodriguezNo ratings yet
- 3 Compuestos de Coordinacion. Parte 3Document52 pages3 Compuestos de Coordinacion. Parte 3PaolaAlejandraRodriguezNo ratings yet
- Ley PeriodicaDocument6 pagesLey PeriodicaJulian Arango100% (1)
- Ion de Compuestos TernariosDocument9 pagesIon de Compuestos TernariosLuis VacaNo ratings yet
- Trabajo Final Compuestos de CoordinacionDocument13 pagesTrabajo Final Compuestos de CoordinacionRikelbin PujolsNo ratings yet
- Tabla Periódica IngDocument30 pagesTabla Periódica IngLUIS FERNANDO HUANCA ADUVIRENo ratings yet
- Quimica Taller Reacciones Quimicas y EstequiometricasDocument6 pagesQuimica Taller Reacciones Quimicas y EstequiometricasLuis Yoani Berrio CardonaNo ratings yet
- Sistema Periódico y EnlaceDocument8 pagesSistema Periódico y EnlaceAngela Mata SanchezNo ratings yet
- Guía Nomenclatura InorgánicaDocument5 pagesGuía Nomenclatura InorgánicaCristian MoraNo ratings yet
- NMX B 028 1998Document8 pagesNMX B 028 1998Ernesto Ramirez VazquezNo ratings yet
- Qué Es EstequiometríaDocument3 pagesQué Es EstequiometríaNorkis Mejias100% (1)
- Tema 8 Formulación Inorgánica. Teoría y Hojas de EjerciciosDocument16 pagesTema 8 Formulación Inorgánica. Teoría y Hojas de EjerciciosCovadonga PerezNo ratings yet
- Tubos de Vacio y TransistoresDocument5 pagesTubos de Vacio y TransistoresDavid Sanabria Diaz0% (1)
- Ejercicios de Nomenclatura 2009-2Document3 pagesEjercicios de Nomenclatura 2009-2ShuletAR10No ratings yet
- Plasmodesmos, Estructura y FunciónDocument15 pagesPlasmodesmos, Estructura y FunciónD'imrPoloNo ratings yet
- Nomenclatura InorganicaDocument22 pagesNomenclatura InorganicaBryan Steven González Arévalo0% (1)
- Difracción de Rayos XDocument12 pagesDifracción de Rayos XAlfredo SolanoNo ratings yet
- UNIDAD 5 Concentración GravimétricaDocument24 pagesUNIDAD 5 Concentración GravimétricaAlexElesvanPurihuamanCubasNo ratings yet
- Taller Corrosion en MaterialesDocument10 pagesTaller Corrosion en MaterialesAlejandro RicardoNo ratings yet
- Los OxidosDocument18 pagesLos OxidosJaime Alberto Pacosillo SiñaniNo ratings yet
- Consulta Numero 4 - QuimicaDocument24 pagesConsulta Numero 4 - QuimicaSantiago Valencia GNo ratings yet
- Ácidos Oxácidos HidratadosDocument8 pagesÁcidos Oxácidos HidratadosRichard QuiguangoNo ratings yet
- Compuestos de CoordinaciónDocument27 pagesCompuestos de CoordinaciónMary MedinaNo ratings yet
- Ácidos Oxácidos y Sales OxisalesDocument1 pageÁcidos Oxácidos y Sales OxisalesRAMON HERIBERTO GUZMAN GONZALEZNo ratings yet
- Dorado Moreno Iván - Formulación y Nomenclatura Química InorgánicaDocument13 pagesDorado Moreno Iván - Formulación y Nomenclatura Química InorgánicacentroJOMNo ratings yet
- Ti Inspire CX Cas - Guía de PruebasDocument29 pagesTi Inspire CX Cas - Guía de PruebasAlexander Duque LeytonNo ratings yet
- Enlace IonicoDocument19 pagesEnlace Ionicoliliana martinez100% (1)
- Ejercicios EstequiometriaDocument2 pagesEjercicios EstequiometriakakaNo ratings yet
- Formulario Solicitud-Licencias-Art-114y115Document2 pagesFormulario Solicitud-Licencias-Art-114y115Luz PerezNo ratings yet
- Portafolio de Evidencias Quimica Parcial 3Document60 pagesPortafolio de Evidencias Quimica Parcial 3Andrea GarciaNo ratings yet
- Isotopos EstablesDocument51 pagesIsotopos EstablesJHOEL_GEONo ratings yet
- Tipos de IsomerìaDocument5 pagesTipos de IsomerìasinaiNo ratings yet
- Nomenclatura Iupac Organica Ja1Document19 pagesNomenclatura Iupac Organica Ja1jrodri011No ratings yet
- Los HidrocarburosDocument43 pagesLos HidrocarburosPatricia Diaz AranguizNo ratings yet
- QC03 - Tabla PeriódicaDocument19 pagesQC03 - Tabla PeriódicaJOSE EDWARD ORTEGA GALEANONo ratings yet
- Taller de QuimicaDocument8 pagesTaller de QuimicadavidNo ratings yet
- Formulación Química Orgánica PDFDocument22 pagesFormulación Química Orgánica PDFMar MarlenNo ratings yet
- Química Compuestos BinariosDocument3 pagesQuímica Compuestos Binariosjose hernandezNo ratings yet
- Organismos Autótrofos y Heterótrofos 6º PDFDocument15 pagesOrganismos Autótrofos y Heterótrofos 6º PDFPatriciaSanhuezaVillarrealNo ratings yet
- Guía de Ejercicios - MagnitudesDocument2 pagesGuía de Ejercicios - MagnitudesLuna MigdalNo ratings yet
- 12 FORMULACIÓN Y NOMENCLATURA ACTUALIZADA - OkDocument13 pages12 FORMULACIÓN Y NOMENCLATURA ACTUALIZADA - Okctf81873732No ratings yet
- Nomenclatura de BinariosDocument21 pagesNomenclatura de BinariosJuanNo ratings yet
- Separata Enlaces QuimicosDocument3 pagesSeparata Enlaces Quimicosjuss_1490No ratings yet
- Practica 3 NomenclaturaDocument10 pagesPractica 3 NomenclaturaPamatz Estrada I'rvinNo ratings yet
- Reanimacion Cardiopulmonar en Adultos PDFDocument10 pagesReanimacion Cardiopulmonar en Adultos PDFJavierNo ratings yet
- Embriología Glándula MamariaDocument7 pagesEmbriología Glándula MamariaJavierNo ratings yet
- Expo Farreras PDFDocument15 pagesExpo Farreras PDFJavierNo ratings yet
- Manual de Oxigenoterapia 2014Document142 pagesManual de Oxigenoterapia 2014Marcelo Alcalde Chavez100% (2)
- Preparacion ColonosDocument1 pagePreparacion ColonosJavierNo ratings yet
- BANCO DE PREGUNTAS CICATRIZACION-Javier ArequipaDocument1 pageBANCO DE PREGUNTAS CICATRIZACION-Javier ArequipaJavier100% (3)
- Via Clinica CA 2 Junio 2016Document102 pagesVia Clinica CA 2 Junio 2016Eduardo Cristian MB MisakiNo ratings yet
- Liquidos IV de MantenimientoDocument6 pagesLiquidos IV de MantenimientoJavierNo ratings yet
- 4tl4s Its MedicinafullDocument92 pages4tl4s Its MedicinafullCézhar Navarro Pardavé100% (1)
- Marcadores Tumorales PDFDocument14 pagesMarcadores Tumorales PDFJeremias EspejoNo ratings yet
- IRIS Perfil NocheDocument1 pageIRIS Perfil NocheJavierNo ratings yet
- Preguntas Licencia de La ANT Ecuador.Document38 pagesPreguntas Licencia de La ANT Ecuador.Fercho JaramilloNo ratings yet
- ACLS Manual de Bolsillo GUÍA de ATENCIÓN CARDIOVASCULAR de EMERGENCIA para Personal Del Equipo de Salud 2005 BookletDocument8 pagesACLS Manual de Bolsillo GUÍA de ATENCIÓN CARDIOVASCULAR de EMERGENCIA para Personal Del Equipo de Salud 2005 BookletJavierNo ratings yet
- Guias de TokioDocument8 pagesGuias de TokioCinthya Huiman ChasquibolNo ratings yet
- Simulacro 1Document15 pagesSimulacro 1Maverick 18No ratings yet
- Guia Aspirado Medula OseaDocument9 pagesGuia Aspirado Medula OseaJavierNo ratings yet
- Ada 2016Document14 pagesAda 2016JavierNo ratings yet
- Banco Preguntas 2014Document187 pagesBanco Preguntas 2014John Tapia80% (5)
- Clasificacion BacteriasDocument2 pagesClasificacion BacteriasMagdalena QuintanaNo ratings yet
- Profilaxis Ocular RNDocument7 pagesProfilaxis Ocular RNJavierNo ratings yet
- 2.abdomen Agudo PediatricoDocument3 pages2.abdomen Agudo PediatricoJavierNo ratings yet
- Preguntas Licencia de La ANT Ecuador.Document38 pagesPreguntas Licencia de La ANT Ecuador.Fercho JaramilloNo ratings yet
- Simulacro 1Document15 pagesSimulacro 1Maverick 18No ratings yet
- Uña EncarnadaDocument5 pagesUña EncarnadaJavierNo ratings yet
- Osteomielitis AgudaDocument7 pagesOsteomielitis AgudaJavierNo ratings yet
- SDMODocument15 pagesSDMOJavierNo ratings yet
- Comandos para Usar en MS-DosDocument1 pageComandos para Usar en MS-DosJavierNo ratings yet
- Act QuitoDocument1 pageAct Quitomariavivictoria79_1No ratings yet
- Guia MedicinaDocument25 pagesGuia MedicinaStefania MeraNo ratings yet
- Triptico VectoresDocument3 pagesTriptico Vectoresmarcelo garcia100% (1)
- Equilibrioenel PlanoDocument4 pagesEquilibrioenel Planodeapioth50% (2)
- MSDS Bentonita Sódica Natural PDFDocument6 pagesMSDS Bentonita Sódica Natural PDFJohnny AlvaroNo ratings yet
- Reporte Volcan Santa Ana 2Document13 pagesReporte Volcan Santa Ana 2Salvador AlvaradoNo ratings yet
- Algunos Criterios para La Seleccion y El Uso de Concreto LigeroDocument16 pagesAlgunos Criterios para La Seleccion y El Uso de Concreto LigeroAlejandro RodríguezNo ratings yet
- Guia Fs-12 (Imprenta) OndasDocument12 pagesGuia Fs-12 (Imprenta) OndasAvend SlainerNo ratings yet
- Metodos de Extraccion e Identificacion de TaninosDocument15 pagesMetodos de Extraccion e Identificacion de TaninosBiig JvliOo100% (25)
- Catalogo Conectores Es KRJDocument28 pagesCatalogo Conectores Es KRJtamia22lilaNo ratings yet
- Crucigrama CarlaDocument8 pagesCrucigrama CarlaDiego MartinezNo ratings yet
- Diseño Geométrico de Un Vuelo Fotográfico para Terreno Montañoso o AccidentadoDocument16 pagesDiseño Geométrico de Un Vuelo Fotográfico para Terreno Montañoso o AccidentadoJean Pierre Lucho Barrientos0% (1)
- Instituto Politécnico NacionalDocument16 pagesInstituto Politécnico NacionalBenji ValdezNo ratings yet
- Problemario de Trabajo y Energía CinéticaDocument2 pagesProblemario de Trabajo y Energía CinéticaCarlos Mauricio PerezNo ratings yet
- NTC 2050 y RETIEDocument4 pagesNTC 2050 y RETIEHugo HurtadoNo ratings yet
- Trabajo en El Plano InclinadoDocument5 pagesTrabajo en El Plano InclinadoMillonarios Con TDCNo ratings yet
- Transportacion VerticalDocument52 pagesTransportacion VerticalSantos Moises Jimenez MirandaNo ratings yet
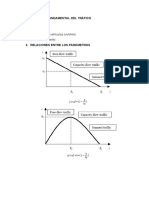
- Ecuación Fundamental Del TráficoDocument5 pagesEcuación Fundamental Del TráficoPATYNo ratings yet
- Banco de Preguntas PDFDocument14 pagesBanco de Preguntas PDFJonathanPicoNo ratings yet
- Evaluación Unidad 3 OkiDocument4 pagesEvaluación Unidad 3 OkiVerónicaAlejandraAriasRodriguezNo ratings yet
- Cap1 Matrices y Sistemas de Ecuaciones SinpausasDocument58 pagesCap1 Matrices y Sistemas de Ecuaciones SinpausasDaniel LezcanoNo ratings yet
- Isaac NewtonDocument4 pagesIsaac Newtonluca ramirezNo ratings yet
- Control de Calidad Shotcrete Jim Phillips - EPC ChileDocument39 pagesControl de Calidad Shotcrete Jim Phillips - EPC ChileGaby MuñozNo ratings yet
- Turbosina 110201Document7 pagesTurbosina 110201Alfonso MohaNo ratings yet
- Ley de FaradayDocument5 pagesLey de FaradayMontes MendozaNo ratings yet
- Escalas de Richter y MercalliDocument4 pagesEscalas de Richter y MercalliRodrigo RodrigoNo ratings yet
- Ejercicios Del Movimiento CircularDocument3 pagesEjercicios Del Movimiento CircularDavier Raul Bolanos Ceron100% (1)
- Tarea Tema 7 DifusiónDocument2 pagesTarea Tema 7 DifusiónLesly Lopez OceguedaNo ratings yet
- Sistemas EolicosDocument28 pagesSistemas Eolicossantigo9100% (1)
- 2018 Aprenda Tostar CAFE GmoVargas EnviadoDocument45 pages2018 Aprenda Tostar CAFE GmoVargas Enviadofabio alcalaNo ratings yet
- Manual Sobre El TIRO Con ARCODocument78 pagesManual Sobre El TIRO Con ARCOMaestro Sri Deva Fénix96% (24)