Professional Documents
Culture Documents
EXPERIMENTO 1 Solubilidad de Compuestos Organicos
Uploaded by
Julian OvalleCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
EXPERIMENTO 1 Solubilidad de Compuestos Organicos
Uploaded by
Julian OvalleCopyright:
Available Formats
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
PRACTICO 1 DETERMINACION DE SOLUBILIDAD DE COMPUESTOS ORGANICOS 1.- OBJETIVO GENERAL Determinar la solubilidad de algunos compuestos orgnicos en diversos reactivos y clasificarlos en los correspondientes grupos de solubilidad. 2.- OBJETIVOS OPERACIONALES En el desarrollo de Trabajo Prctico el alumno debe lograr los siguientes objetivos: Aprender a manipular muestras slidas y lquidas. Verificar las diferentes solubilidades de distintas sustancias orgnicas. Aprender a seguir una secuencia de anlisis de muestra.
3.- ACTIVIDAD EXPERIMENTAL 3.1.-Materiales y reactivos Reactivos: NaOH al 5%, ter, HCl al 5%, NaHCO3 al 5%, H2SO4 concentrado, H3PO4 al 85%. Materiales: Usuales de laboratorio. 3.2.- Generalidades
Los compuestos orgnicos en funcin de su solubilidad se pueden dividir en 7 grupos: a) Grupo 1: compuestos solubles en agua y en ter b) Grupo 2: compuestos solubles en agua e insolubles en ter. c) Grupo 3: compuestos insolubles en H2O pero solubles en NaOH diluido. Este grupo puede subdividirse en: A. Compuestos solubles en NaOH diluido y en NaHCO3 diluido. B. Compuestos solubles en NaOH diluido e insolubles en NaHCO3 diluido. d) Grupo 4: compuestos insolubles en agua pero solubles en HCL diluido. e) Grupo 5: Los hidrocarburos y compuestos que contienen C e H (no contienen N ni S) y que no forman parte de los grupos del 1 al 4 y
1
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
que son solubles en H2SO4 concentrado. Este grupo puede ser subdividido en 2 grupos: A. Compuestos solubles en H2SO4 concentrado y en H3PO4 al 85%. B. Compuestos solubles en H2SO4 concentrado pero insolubles en H3PO4 al 85%. f) Grupo 6: Todos los compuestos que no contienen N y S y que son insolubles en H2SO4 concentrado. g) Grupo 7: Los compuestos que contienen N y S y que no son clasificables del 1 al 4 grupo. La mayora de los compuestos de este grupo son solubles en H2SO4 concentrado. 3.3.- Procedimiento para determinar solubilidad
Todos los ensayos de solubilidad deben ser realizados a temperatura ambiente en tubos de ensayo. La cantidad a usar es 0,1 g si la sustancia es slida y 0,2 mL (5 gotas) si es lquida, por cada 3 mL de solvente. El slido debe estar finamente pulverizado para aumentar la velocidad de disolucin. a) Solubilidad en agua Tratar 0,1 g de la sustancia con porciones sucesivas de 1 mL de agua, agitando enrgicamente despus de cada adicin. Si el compuesto no se disuelve en 3 mL puede ser considerado como insoluble en agua. Si la sustancia es lquida se agrega 0,2 mL (5 gotas) de la sustancia en examen a 3 mL de agua y se agita. En ambos casos probar el contenido del tubo con papel tornasol para determinar su pH. b) Solubilidad en ter Si el compuesto es soluble en agua, se repite el ensayo con ter, usando un tubo seco. c) Solubilidad en NaOH al 5% Si el compuesto es insoluble en agua se ensaya su solubilidad en solucin de NaOH al 5%. Observar si aumenta la temperatura. Si el compuesto parece insoluble sacar algunas gotas de lquido sobrenadante y trasvasar a un tubo de ensayo. Agregar gota a gota HCL al 5 % hasta acidificar y observar si se forma precipitado o turbidez; en caso positivo el compuesto se clasifica en el grupo 3.
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
d) Solubilidad en NaHCO3 al 5% Si el compuesto es soluble en NaOH al 5% hacer el ensayo con NaHCO3 al 5 %. Observar si el compuesto se disuelve y si de inmediato se desprende CO2 (cido carboxlico, sulfnico, fenoles). Si se desprende despus de cierto tiempo (algn aminocido). e) Solubilidad en HCl al 5% A una cantidad de 0,1 g (0,2 mL) de sustancia agregar porciones sucesivas de 1 mL de HCl al 5%. Algunas bases orgnicas (por ejemplo, la naftilamina) dan cloruros que son solubles en agua pero que precipitan en exceso de HCl. Si el compuesto se disuelve va al grupo 4. Si el compuesto es insoluble sacar algunas gotas del lquido sobrenadante y agregar NaOH al 5% hasta basicidad y observar si se forma un precipitado, en caso positivo el compuesto se clasifica en el grupo 4. f) Solubilidad en H2SO4 concentrado Si la sustancia no es soluble en agua, en NaOH al 5%, ni en HCl al 5%, se prueba su solubilidad en H2SO4 concentrado. Agregar 0,1 g (0,2 mL.) de sustancia a 3 mL de H2SO4 concentrado. Si el compuesto no se solubiliza inmediatamente, agitar por un cierto tiempo pero no calentar. Observar si se produce un cambio de color (carbonizacin, desprendimiento de gas, polimerizacin). g) Solubilidad en H3PO4 al 85% Esta determinacin se hace si el compuesto es soluble en H2SO4 concentrado. Si el compuesto no se solubiliza rpido agitar por algn tiempo, pero no calentar.
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
4.- TEORIA DE LA SOLUBILIDAD 4.1.- Divisin de los compuestos orgnicos en grupos de solubilidad En las siguientes tablas se puede observar los 6 grupos de solubilidad, con diferentes compuestos que pertenecen a dichos grupos. Tabla 1. Grupos de solubilidad
Grupo / Caractersticas del grupo Compuestos Grupo 1 Solubles en agua y ter Alcoholes alifticos Aldehdos Cetonas cidos carboxlicos Esteres Fenoles Anhdridos Aminas Amidas Nitrilos Oxicidos (gliclicos) Grupo 2 Solubles en agua y no en ter Grupo 3 Solubles en NaOH al 5 % Grupo 4 Solubles en HCl al 5 %
Glicoles Aldehdos y cetonas polihidroxilados Sales de amina Sales de cidos carboxlicos cidos sulfnicos Algunas amidas, aminas y aminocidos cidos polibsicos, hidroxicidos Compuestos diamnicos, poliamnicos, aminoalcoholes
A.- Solubles en NaHCO3 al 5 %: cidos carboxlicos Nitrofenoles cidos sulfnicos B.- Insolubles en NaHCO3 al 5% Fenoles Algunas imidas Algunos nitrocompuestos Algunos enoles Algunas oximas
Aminas primarias Aminas secundarias alifticas y alifticas-aromticas Aminas terciarias alifticas y algunas alifticas aromticas Hidrazinas
Grupo / Caractersticas del grupo Compuestos
Grupo 5 No contienen N ni S Solubles en H2SO4 concentrado Hidrocarburos no saturados Algunos hidrocarburos aromticos polialquilados Alcoholes Aldehdos Cetonas Esteres de peso molecular relativamente elevado Anhdridos Lactonas Halogenos de acilo Quinonas
Grupo 6 No contienen N ni S Insolubles en H2SO4 Hidrocarburos alifticos saturados Hidrocarburos cclicos Hidrocarburos aromticos Eteres dianlicos Derivados halogenados de alquenos Algunos steres (bencil acetato)
Grupo 7 Contienen N y S Compuestos que no pertenecen a los grupos del 1 al 4 Nitrocompuestos terciarios Amidas y derivados de aldehdos y cetonas Nitrilos Azocompuestos, hidrazocompuestos, nitrosocompuestos Sulfnicos,sulfamdicos de amina secundaria y otros compuestos que contienen S Aminas aromticas
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
4.2.-Notas adicionales sobre grupos de solubilidad Figura 1. Diagrama de rbol de solubilidades
a) Grupo 1 Incluye los trminos mas bajos de las series homlogas con 4 a 5 tomos de C en cadena normal que pueden contener O y N en su estructura. Son solubles en agua por su bajo contenido en C. Si el compuesto es soluble tanto en agua como en ter, deber ser soluble en cualquier otro solvente, por lo tanto es innecesario otro ensayo de solubilidad.
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
b) Grupo 2 Los compuestos de los grupos 1 al 5 son usualmente solubles en lcali y en cidos diluidos. El comportamiento de las sales del grupo 2 de la tabla con cidos y bases diluidas puede dar informacin til. Con una sal de amina soluble en agua, el tratamiento con lcali diluido da una amina de olor caracterstico. Anlogamente la sal de un acido dbil soluble en agua es descompuesta por el HCl diluido o por el H2SO4 concentrado. La sal soluble en agua de un cido insoluble en agua (o de una base insoluble en agua) dar un precipitado si se trata con HCl diluido (o con NaOH diluido). Las sales de cidos sulfnicos y de bases cuaternarias no reaccionan con NaOH o HCl diluido. c) Grupo 3 El tribromofenol simtrico, el 2,4-dinitrofenol y el acido pcrico son solubles en solucin diluida de NaHCO3. d) Grupo 4 Teniendo presente que los cloruros de algunas aminas son poco solubles en agua fra, no debe inducir a error una aparente insolubilidad de un compuesto (que contiene N) en HCl diluido. La suspensin en HCl diluido debe ser filtrada y el filtrado debe ser alcalinizado. Un precipitado indicar que el compuesto deber ser clasificado en el grupo 4. Si no se forma ningn precipitado el compuesto es del Grupo 7. e) Grupo 5 Este grupo comprende todos los hidrocarburos insolubles en agua, los compuestos que contienen oxgeno y no contienen N o S y que son solubles en H2SO4 concentrado fro. Cualquier cambio durante la disolucin (color, carbonizacin excesiva, desprendimiento de gas o calor, polimerizacin, precipitacin de un compuesto) debe ser observada. f) Grupo 6 El H2SO4 concentrado diferenciacin siguiente: proporciona un ensayo simple para la
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
a) Parafinas saturadas, hidrocarburos aromticos simples. b) Hidrocarburos no saturados. G) Grupo 7
cclicos,
hidrocarburos
Este grupo comprende todos los compuestos que contienen N y S y que son insolubles en HCl diluido o en NaOH diluido.
5.- TEORIA DE SOLUBILIDAD 5.1.- Polaridad y solubilidad Cuando se disuelve un soluto, sus molculas o iones se distribuyen ms o menos al azar entre las molculas del solvente. En compuestos cristalinos como el cloruro de sodio, por ejemplo, la distancia promedio entre los iones sodio y cloruros es 2,8 A. En una solucin 1 M el solvente los mantiene a una distancia de aproximadamente 10 A. El trabajo necesario para separar dos placas con cargas opuestas disminuye al introducir una sustancia entre ellas, por el factor denominado constante dielctrica del medio. Las molculas de agua entre dos iones (o las placas cargadas de un condensador) son pequeos dipolos que orientan sus extremos de modo de neutralizar parcialmente las cargas inicas y as estabilizar el sistema. No es sorprendente entonces, que el agua con su alta constante dielctrica, de valor 80, facilite la separacin de los iones sodio y cloruro y que disuelva al NaCl, mientras que el ter (constante dielctrica 4,4) o hexano (constante dielctrica 1,9) son solventes muy pobres para sales de este tipo. Una alta constante dielctrica adems de la capacidad de formar puentes hidrgeno hacen del agua un buen solvente para sales y a la vez que un muy mal solvente para sustancias no polares En general, entonces, se puede esperar que un solvente polar disuelva fcilmente solo solutos polares y un solvente no polar slo disuelva solutos no polares. Esto se ha generalizado como lo semejante disuelve a lo semejante. Puesto que el agua es un compuesto polar, es un mal solvente para hidrocarburos saturados, no saturados y aromticos. Por otro lado, las sales de cidos orgnicos (RCO2Na, RSO3Na), aminas
7
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
hidrocloradas (RNH3Cl) y aminocidos (R-NH3+-CH-CO2-) son muy polares y son generalmente solubles en agua. Otros compuestos quedan entre estos dos extremos. Entre los ms frecuentes se puede mencionar los alcoholes, steres, teres, cidos, aminas, nitrilos, amidas, cetonas y aldehdos. En la mayora de las series homlogas de este tipo el lmite superior de solubilidad en agua se encuentra en las cercanas del miembro que contiene 5 tomos de carbono. Puesto que la mayora de las molculas orgnicas tienen tanto una parte polar y una no polar podra esperarse que la solubilidad dependiese del balance entre las dos partes. A medida que la parte hidrocarbonada de la molcula aumenta, la solubilidad en agua disminuye y aumenta su solubilidad en ter.
El aumento de las sustituciones de anillos aromticos en una molcula tambin aumenta su carcter apolar. As el -naftol y phidroxibifenol son menos solubles en agua que el fenol.
El grupo fenilo cuando esta presente como un sustituyente en cidos alifticos, alcoholes, aldehdos y compuestos similares tiene un efecto en la solubilidad aproximadamente equivalente a 4 tomos de carbono alifticos. Por ejemplo, alcohol benclico es tan soluble como el n- pentilalcohol.
La solubilidad de una sustancia es una medida del equilibrio entre la sustancia pura y su solucin. Tal equilibrio parece afectado no solo
8
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
por las interacciones ya discutidas, sino que tambin por las fuerzas intermoleculares en el soluto puro. Estas fuerzas son independientes de la polaridad u otras propiedades del solvente y sus fuerzas relativas pueden ser estimadas por una comparacin de los puntos de fusin y de ebullicin , puesto que lo procesos de fusin del slido o la ebullicin de un lquido involucra una separacin de molculas que esta relacionada con la separacin que ocurre en la disolucin. La relacin de puntos de fusin altos con solubilidad baja puede ser ilustrada por los ismeros maleico y fumrico. El acido fumrico sublima a 20C y es insoluble en agua, el acido maleico funde a 130C y es soluble en agua. En general, un aumento en el peso molecular lleva a un aumento en las fuerzas intermoleculares en un slido. Los polmeros y otros compuestos de alto peso molecular generalmente muestran bajas solubilidades en agua y ter, as, la glucosa es soluble en agua, pero sus polmeros, almidn y celulosa son insolubles. Muchos aminocidos son solubles en agua pero las protenas son generalmente insolubles. Aumentar el peso molecular de una molcula introducindole halgenos generalmente resulta en una disminucin de la solubilidad en agua lo que provoca que algunos compuestos solubles en agua cuando son sustituidos por halgenos se transformen en insolubles. El lmite mximo de 5 tomos de C para solubilidad en agua sigue de un principio muy general, que la semejanza estructural entre el soluto y el solvente es acompaada por un aumento de la solubilidad. Porque por la naturaleza polar del agua, los compuestos deben su solubilidad en ella casi completamente a los grupos polares que pueden contener. A medida que se asciende en una serie homologa, la parte hidrocarbonada (no polar) de la molcula aumenta continuamente mientras que la funcin polar permanece esencialmente invariable. Por lo tanto, al ascender hay una tendencia a disminuir la solubilidad en solventes polares tales como el agua. El hecho que el limite mximo de solubilidad en agua para varias series queda en las mismas cercanas , se debe a la semejanza de las polaridades de muchos grupos funcionales . La regin particular
9
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
(miembros con 5 tomos de carbono) en varias series en las que se alcanza el limite superior de solubilidad en agua est determinado por las proporciones arbitrarias de solvente y soluto escogido en este esquema de separacin. La tendencia de ciertos compuestos que contienen oxigeno para formar hidratos tambin contribuye a la solubilidad en agua. 5.2.- Efecto de cadenas laterales sobre la solubilidad Las ramificaciones de la cadena hidrocarbonada bajan las fuerzas intermoleculares y disminuye las atracciones intermoleculares. Por lo tanto no es sorprendente que un compuesto con cadenas laterales sea ms soluble que el correspondiente compuesto con cadenas no ramificadas. Esta es una regla muy general y es particularmente til en relacin con los compuestos alifticos simples, por ejemplo, la solubilidad de un compuesto iso difiere bastante de la de su ismero normal y se acerca a la del miembro normal precedente de la serie homologa en cuestin. En general, el ms ramificado de dos compuestos ismeros posee la mayor solubilidad. La posicin del grupo funcional en la cadena carbonada tambin afecta la solubilidad, por ejemplo, 3-pentanol es ms soluble que 2pentanol, que a su vez es ms soluble que 1-pentanol. Cuando se combina el efecto de las ramificaciones con el grupo funcional movindose hacia el centro de la molcula se nota un marcado aumento de la solubilidad. Normalmente la estructura mas compacta es la de mayor solubilidad al comparar compuestos del mismo tipo. 5.3.-Teora de solubilidad acido-base 5.3.1.- Efecto de la estructura en la acidez y basicidad En general el problema de decidir si un compuesto desconocido insoluble en agua se disolver en acido diluido o base diluida, es fundamentalmente cuestin de estimar aproximadamente su fuerza acida o bsica. Hay dos efectos principales que influyen en la acidez o basicidad, ellos son el efecto electrnico y el efecto estrico.
10
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
5.3.2.- Efectos electrnicos sobre la acidez o basicidad Se han realizado estudios sobre la correlacin cuantitativa de la estructura con la fuerza cida y bsica de compuestos orgnicos sustituidos. Estos efectos se han racionalizado sobre una base electrnica; una variedad de evidencia indica que las posiciones para y orto de compuestos bencnicos son mas sensibles a alteracin electrnica que la posicin meta. Para el caso del ion fenxido la teora de resonancia indica que las posiciones orto y para son centro de carga negativa parciales y as ellos pueden ser sustituidos por grupos polares, la sustitucin orto sin embargo siempre es interferida por efectos estricos.
La mayora de los cidos carboxlicos tienen constantes de disociacin en agua a 25 C de 10-6 o mayores y por lo tanto son fcilmente solubles en NaOH al 5%. Por otro lado, los fenoles que generalmente son menos cidos (la constante de disociacin del fenol es aproximadamente 10-10) aunque son solubles en solucin de NaOH son insolubles en solucin diluida de bicarbonato de sodio. La introduccin de grupos sustituyentes sin embargo puede cambiar la acidez. As el orto y para-nitrofenol tienen constantes de disociacin de aproximadamente 6*10-8, en otras palabras, la introduccin de un grupo nitro en orto o para aumenta la acidez del fenol en un factor de 600. Podra anticiparse que la adicin de dos grupos nitro, como 2,4-dinitrofenol aumenta la acidez de tal modo que el compuesto es soluble en NaHCO3 diluido. El efecto de aumentar la acidez de los grupos nitro se debe a la estabilizacin del anin fenxido por distribucin adicional de la carga negativa en el grupo nitro.
11
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
Influencias electrnicas similares afectan la basicidad de aminas. Aminas alifticas en solucin acuosa tienen constantes bsicas de aproximadamente 10-3 a 10-4 (cerca del amoniaco 10-5). La introduccin de un grupo fenilo, sin embargo, baja la basicidad. El efecto del anillo fenilo es estabilizar por resonancia el grupo amino, el grupo fenilo tambin disminuye la basicidad del nitrgeno inductivamente.
5.3.3.- Efectos estricos sobre acidez y basicidad Los fenoles orto sustituidos tienen reducida solubilidad en lcalis acuosos. La di-t-butilpiridina es significativamente ms dbil como base que la dimetilpiridina. Se piensa que el debilitamiento de las fuerzas bsicas de las aminas se debe a tensin estrica introducida cuando un protn es agregado al tomo de nitrgeno.
12
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
Las tensiones estricas pueden aumentar o disminuir la acidez de cidos carboxlicos. Por ejemplo, la sustitucin de grupos alquilos en el tomo de carbono alfa del cido actico tiende a disminuir la acidez por desestabilizacin de la base conjugada por inhibicin estrica de solvatacin. Los cidos benzoicos orto sustituidos son apreciablemente mas fuertes que los correspondientes ismero para. 5.3.4.- Solubilidad en HCl diluido Aminas alifticas, primarias, secundarias y terciarias forman sales polares, inicas con acido clorhdrico. Adems, las aminas alifticas son fcilmente solubles en cido clorhdrico. Los grupos arilos disminuyen la basicidad del tomo de nitrgeno; las aminas aromticas primarias aunque menos bsicas que las aminas alifticas primarias son solubles en acido clorhdrico diluido, mientras que las diarilaminas y triarilaminas no son solubles. Son tambin insolubles la difenilamina, trifenilamina y carbazol. Son solubles las arilalquilaminas que no contienen ms que un grupo arilo.
Las amidas disustituidas (RCONH2) que tienen un peso molecular lo suficientemente alto para ser insolubles en agua son solubles en acido clorhdrico diluido. Este comportamiento contrasta con el de las simples amidas (RCONH2) que son compuestos neutros.
Debe hacerse notar que algunas aminas pueden reaccionar con cido clorhdrico para formar hidrocarburos insolubles. Por ejemplo, ciertas arilaminas como -naftilamina forman hidrocloruros escasamente solubles en cido clorhdrico diluido.
13
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
Calentando la mezcla suavemente y diluyendo con agua se logra a veces disolucin. Tambin se puede disolver la suspensin en ter y tratar con HCl al 5 %, la formacin de un slido en la interfase indica una amina bsica. 5.3.5.- Solubilidad en soluciones de hidrxido de sodio al 5 % y bicarbonato de sodio al 5 % En la tabla compuestos: siguiente se muestra la solubilidad de algunos
Tabla 2. Clasificacin de solubilidad de algunos compuestos
Compuestos Estructura Grupo de solubilidad
Acidos carboxlicos Acidos sulfnicos Acidos sulfnicos Enoles Imidas Nitro Arenosulfonamidas B-dicarbonilcompuestos Oximas
RCO2H RSO3H RSO2H C=C-OH -C-NH-CCH-NO2 ArSO2NHR -C-CH-CC=N-OH
3A 3A 3A 3B 3B 3B 3B 3B 3B
14
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
Debe hacerse notar que aunque los compuestos 3-dicarbonilos son casi tan cidos como los fenoles, la velocidad para remover el protn del carbono puede ser relativamente lenta y la velocidad de disolucin de tales sustancias ser tan lenta que ellas aparecen como insolubles en bases. La presencia de grupos altamente electronegativos como trifluorometilos en el grupo carbonilo puede llevar a estos compuestos a clasificarse en el grupo 3 A. Los nitrocompuestos tienen una forma tautomrica que es casi tan fuerte como los cidos carboxlicos.
Aun un grupo nitro confiere suficiente acidez a una sustancia para hacerla soluble en hidrxido de sodio diluido. As el nitroetano tiene una Ka 3,5*10-9. El grupo p-nitrofenil hace la funcin -CONH- dbilmente cida en solucin acuosa. As, la p-nitro-acetanilida se disuelve en solucin de NaOH pero no en bicarbonato de sodio. Las sulfonamidas muestran la misma solubilidad que la p-nitro-acetanilida. Acidos grasos que contienen 12 o ms carbonos reaccionan lentamente con el lcali formando sales que son los jabones. La mezcla no es clara sino una dispersin coloidal opalescente, espumosa al agitarla. 5.3.6.- Solubilidad en cido sulfrico concentrado fro El acido sulfrico concentrado fro se usa con compuestos neutros insolubles en agua que no contienen otros elementos fuera de C, H y O. Si el compuesto es insaturado se sulfona fcilmente o si posee un grupo funcional que contiene oxgeno se disolver en cido sulfrico concentrado y fro. La disolucin en cido sulfrico frecuentemente va acompaada por una reaccin tal como sulfonacin, polimerizacin, deshidratacin o la adicin del acido sulfrico o uniones oleofnicas o acetilnicas.
15
UTFSM Sede Concepcin, 2009 2 Laboratorio de Anlisis Industrial I
Alcanos, cicloalcanos y sus derivados halogenados son insolubles en acido sulfrico. Hidrocarburos aromticos simples y sus derivados halogenados no sufren sulfonacin en estas condiciones y son insolubles. Sin embargo, la insercin de dos o ms grupos alquilos en el ncleo bencnico permite al compuesto sulfonarse fcilmente. Muchos alcoholes secundarios y terciarios al ser tratados con cido sulfrico concentrado se deshidratan rpidamente y dan olefinas que sufren polimerizacin. El polmero resultante es insoluble en el acido sulfrico concentrado. El alcohol benclico (y alcoholes similares) reaccionan con el cido sulfrico concentrado dando un precipitado coloreado.
16
You might also like
- Clasificacion de Compuestos Organicos de Acuerdo Con Su Solubilidad 2Document5 pagesClasificacion de Compuestos Organicos de Acuerdo Con Su Solubilidad 2LuisFierroGiraldo50% (2)
- Informe Grupos FuncionalesDocument12 pagesInforme Grupos FuncionalesEstefania Gonzalez GonzalezNo ratings yet
- Acidos CarboxilicosDocument7 pagesAcidos Carboxilicossussel baday100% (2)
- Práctica 7Document24 pagesPráctica 7ZHULEM NICKOL AYALA TINEONo ratings yet
- Informe 6Document6 pagesInforme 6daniellgb96No ratings yet
- PRACTICA 5-Sintesis de Una Amida-2016-1Document3 pagesPRACTICA 5-Sintesis de Una Amida-2016-1Orlando David Medinueta De AvilaNo ratings yet
- Marcha Sistematica para Cationes Sin El Empleo de h2sDocument5 pagesMarcha Sistematica para Cationes Sin El Empleo de h2sKelly N Martinez AlmenteroNo ratings yet
- Informe de Organica Pruebas de AlcoholesDocument13 pagesInforme de Organica Pruebas de AlcoholesYisett CantilloNo ratings yet
- Informe 1Document3 pagesInforme 1Jhon Alexander Suescún SepúlvedaNo ratings yet
- GUIA 2. Análisis Cualitativo de Grupos Funcionales-2016 1sDocument11 pagesGUIA 2. Análisis Cualitativo de Grupos Funcionales-2016 1sandres9410No ratings yet
- Informe N°05 de Química OrgánicaDocument20 pagesInforme N°05 de Química OrgánicaEda Erika AlfaroNo ratings yet
- Rub IdioDocument7 pagesRub IdioEfrain Trujillo ChambiNo ratings yet
- Reacciones Principales de Los AlcanosDocument32 pagesReacciones Principales de Los AlcanosLedwin PeraltaaNo ratings yet
- INFORME.7 y 8 QUIMICA ORGANICADocument15 pagesINFORME.7 y 8 QUIMICA ORGANICAyamileNo ratings yet
- Práctica I (Sesión1) - Identificando Una Muestra Problema 2022-1Document4 pagesPráctica I (Sesión1) - Identificando Una Muestra Problema 2022-1LAURA JULIANA GAMBOA RODRIGUEZNo ratings yet
- PRACTICA #11 Chanzapa SANPONIFICACIONDocument8 pagesPRACTICA #11 Chanzapa SANPONIFICACIONGABY GAMES YTNo ratings yet
- Informe 1 Quimica Organica 2 Propiedades de Los HidrocarburosDocument6 pagesInforme 1 Quimica Organica 2 Propiedades de Los HidrocarburosLiliana DuranNo ratings yet
- Filosofia Resumen Investigacion Cientifica y Caracter SistematicoDocument3 pagesFilosofia Resumen Investigacion Cientifica y Caracter Sistematicokatherine Chavez GonzalesNo ratings yet
- 6to INFORME PDFDocument10 pages6to INFORME PDFKarla HuamancajaNo ratings yet
- Informe 5. Lab BioqDocument8 pagesInforme 5. Lab BioqKELLY JOHANA CORREA SANTANo ratings yet
- Informe - Propiedades - Químicas - Alcoholes y Fenoles7Document2 pagesInforme - Propiedades - Químicas - Alcoholes y Fenoles7Rodrigo Esquivel JuradoNo ratings yet
- Taller Aldehídos y CetonasDocument2 pagesTaller Aldehídos y CetonasAlixón GNo ratings yet
- Tarea de QuimicaDocument20 pagesTarea de QuimicaBC NandoNo ratings yet
- Practica6Team1 Sintesis de NerolinaDocument14 pagesPractica6Team1 Sintesis de NerolinaHilda Ballin0% (1)
- INFORME Aldehidos y CetonasDocument7 pagesINFORME Aldehidos y CetonasAnita LopezNo ratings yet
- Pruebas Generales para Aminoacidos y para Proteinas Inf 2Document5 pagesPruebas Generales para Aminoacidos y para Proteinas Inf 2Martha L ValdésNo ratings yet
- Pre-Informe Nitración Del BencenoDocument8 pagesPre-Informe Nitración Del Bencenomiguel olivesNo ratings yet
- Informe 8Document8 pagesInforme 8Valentina Rodriguez SuarezNo ratings yet
- Síntesis y Caracterizacción Del Ácido AcetilsalicílicoDocument12 pagesSíntesis y Caracterizacción Del Ácido AcetilsalicílicoMartaYanesSánchezNo ratings yet
- Inf 08 Aldehidos y Cetonas.v2Document4 pagesInf 08 Aldehidos y Cetonas.v2Yajhaira DelgadoNo ratings yet
- Informe Laboratorio SolubilidadDocument4 pagesInforme Laboratorio SolubilidadLuisa0% (1)
- Equivalente de Neutralización de Un Ác. Org.Document4 pagesEquivalente de Neutralización de Un Ác. Org.Ashly De Jesus RodriguezNo ratings yet
- Traduccion Del PaviaDocument30 pagesTraduccion Del PaviaKarla Contreras de GonzalezNo ratings yet
- Informe Quimica9Document6 pagesInforme Quimica9Pepe Rojas YachasNo ratings yet
- Aldehc3addos y CetonasDocument18 pagesAldehc3addos y CetonasRoque100% (1)
- Cuestionario 1Document2 pagesCuestionario 1Rodrigo Rueda100% (1)
- Reporte 2 OrganicaDocument3 pagesReporte 2 OrganicaSilvia Betzabe OrdazNo ratings yet
- Alcoholes y FenolesDocument14 pagesAlcoholes y FenolesAxl PalominoNo ratings yet
- Clasificación de Compuestos Organicos Segun La SolubilidadDocument6 pagesClasificación de Compuestos Organicos Segun La SolubilidadEstefany MaldonadoNo ratings yet
- Practica de Formación de OsazonasDocument10 pagesPractica de Formación de OsazonasPabloNo ratings yet
- Informe Análisis OrgánicoDocument7 pagesInforme Análisis OrgánicoVanesiitha Marrugo SantanderNo ratings yet
- Sal de DiazonioDocument2 pagesSal de DiazoniorecluisNo ratings yet
- Informe de Marcha de Eter Química Orgánica Práctica N 5 Lucero GarciaDocument10 pagesInforme de Marcha de Eter Química Orgánica Práctica N 5 Lucero Garciamaria cabrera gasteloNo ratings yet
- Propiedades de Las SolucionesDocument20 pagesPropiedades de Las Soluciones.:("*"BLacK BuLLeT"*"):.80% (5)
- Laboratorio de Química OrgánicaDocument5 pagesLaboratorio de Química OrgánicaLadixRoseNo ratings yet
- Practica 8 QuimicaDocument9 pagesPractica 8 QuimicaCesar SuarezNo ratings yet
- Informe de Quimica OrganicaDocument9 pagesInforme de Quimica Organicacarlos benitezNo ratings yet
- Laboratorio 2 Titulación Potenciométrica de AminoácidosDocument7 pagesLaboratorio 2 Titulación Potenciométrica de AminoácidosNATHALIA VANESA BELALCAZAR CAICEDONo ratings yet
- Analisis Funcional de AlcoholesDocument9 pagesAnalisis Funcional de AlcoholesYube LlyNo ratings yet
- LAB. QUIMICA ORGANICA, 5 Extraccion de Agentes DesecantesDocument6 pagesLAB. QUIMICA ORGANICA, 5 Extraccion de Agentes DesecantesDayan Ocampo PatiñoNo ratings yet
- Informe NDocument7 pagesInforme NEver LuisNo ratings yet
- Caracterizacion de Alcoholes 1Document11 pagesCaracterizacion de Alcoholes 1Luis David ArgotiNo ratings yet
- Lección 1 Química Orgánica Iones EnolatoDocument3 pagesLección 1 Química Orgánica Iones EnolatoMishell Andrea Macías MonserrateNo ratings yet
- Reacciones de Indentificacion de La CafeinaDocument8 pagesReacciones de Indentificacion de La CafeinaJorge Luis Chambi LauraNo ratings yet
- Caracterizacion de HalurosDocument6 pagesCaracterizacion de HalurosVanessa Romero100% (1)
- Lab Acidos Carboxilicos y Derivados UdeaDocument4 pagesLab Acidos Carboxilicos y Derivados UdeaJose Luis Chasqui VelascoNo ratings yet
- Acidos Carboxilicos y Sus DerivadosDocument94 pagesAcidos Carboxilicos y Sus DerivadosJr Diego PaxiNo ratings yet
- SolubilidadDocument4 pagesSolubilidadAnita EspinosaNo ratings yet
- Clasificación de SustanciasDocument9 pagesClasificación de SustanciasEdith LCNo ratings yet
- Practica # 3 Ensayos Preliminares y Determinación de La Solubilidad de Compuestos OrgánicosDocument5 pagesPractica # 3 Ensayos Preliminares y Determinación de La Solubilidad de Compuestos OrgánicosXONICNo ratings yet
- Hier Base Speci As CervezaDocument3 pagesHier Base Speci As CervezaJulian OvalleNo ratings yet
- Nasa ThulDocument1 pageNasa ThulJulian OvalleNo ratings yet
- Manual de Referencia Aw 130Document234 pagesManual de Referencia Aw 130Julian OvalleNo ratings yet
- Nutrientres para LevadurasDocument1 pageNutrientres para LevadurasJulian OvalleNo ratings yet
- Expo ToxicilogiaDocument2 pagesExpo ToxicilogiaJulian OvalleNo ratings yet
- Ficha Tecnica Acido NitricoDocument2 pagesFicha Tecnica Acido NitricoWilson Heiner Rueda RamosNo ratings yet
- Carbonilo PDFDocument193 pagesCarbonilo PDFWalter Tejada ChaurraNo ratings yet
- Boletin Cluster Calzado Jun2013Document2 pagesBoletin Cluster Calzado Jun2013Julian OvalleNo ratings yet
- Hier Base Speci As CervezaDocument3 pagesHier Base Speci As CervezaJulian OvalleNo ratings yet
- Taller PreciptacionDocument2 pagesTaller PreciptacionJulian Ovalle0% (2)
- Análisis Químico 1Document9 pagesAnálisis Químico 1Jorge PirelaNo ratings yet
- Guia de Metodos de Analisis Por HPLC 2013-2Document10 pagesGuia de Metodos de Analisis Por HPLC 2013-2Julian OvalleNo ratings yet
- Síntesis Del Orto y para Nitro Fenol SEguimiento Con PreguntasDocument2 pagesSíntesis Del Orto y para Nitro Fenol SEguimiento Con PreguntasJulian OvalleNo ratings yet
- Taller N 1Document1 pageTaller N 1Julian OvalleNo ratings yet
- Ley-1258-08 Sociedad S.A.S PDFDocument12 pagesLey-1258-08 Sociedad S.A.S PDFcbecerr1No ratings yet
- Carpeta de Prsentacion Hoja de CocaDocument17 pagesCarpeta de Prsentacion Hoja de CocaJulian OvalleNo ratings yet
- Mate de Coca Energizante NaturalDocument6 pagesMate de Coca Energizante NaturalJulian Ovalle100% (1)
- CSB 1500 (0) Bulk-EsDocument1 pageCSB 1500 (0) Bulk-EsJulian OvalleNo ratings yet
- Beer y Bielas Recetario de CervezaDocument13 pagesBeer y Bielas Recetario de CervezaAndrade Ernesto Fidel100% (9)
- AcetamidaDocument4 pagesAcetamidaJulian OvalleNo ratings yet
- Cap¡tulo 01 - Un Breve Curso en Fabricacion de CervezaDocument6 pagesCap¡tulo 01 - Un Breve Curso en Fabricacion de CervezaJulian OvalleNo ratings yet
- Información Sobre La CocaínaDocument10 pagesInformación Sobre La CocaínaJulian OvalleNo ratings yet
- Calculos BeerDocument4 pagesCalculos BeerJulian OvalleNo ratings yet
- Laboratorio SolubilidadDocument1 pageLaboratorio SolubilidadJulian OvalleNo ratings yet
- Cifras Significativas EstadísticaDocument2 pagesCifras Significativas EstadísticaJulian OvalleNo ratings yet
- SolubilidadDocument1 pageSolubilidadJulian OvalleNo ratings yet
- Diferencia Química Organica e InorgánicaDocument6 pagesDiferencia Química Organica e InorgánicaJulian OvalleNo ratings yet
- Introduccin A La Qumica Analtica 1207079739869002 3Document36 pagesIntroduccin A La Qumica Analtica 1207079739869002 3Cesar Augusto Plasencia VegaNo ratings yet
- Proteinas TotalesDocument2 pagesProteinas TotalesMarlin Casanova GuajardoNo ratings yet
- Reacciones Caracteristicas Del Grupo IvDocument17 pagesReacciones Caracteristicas Del Grupo IvJohana VargasNo ratings yet
- Aldehidos y CetonasDocument5 pagesAldehidos y CetonasSantamaria Veliz OliviaNo ratings yet
- Exposición de Factores Que Afectan La Estabilidad de Los ComplejosDocument11 pagesExposición de Factores Que Afectan La Estabilidad de Los ComplejosJustin CascanteNo ratings yet
- Taller 1. EstequiometríaDocument14 pagesTaller 1. EstequiometríaCesar Diego Vargas MottaNo ratings yet
- Pectinas y Agar AgarDocument29 pagesPectinas y Agar Agaralfredo vilca segoviaNo ratings yet
- Taller 10 Unidad 3 EstequiometriaDocument5 pagesTaller 10 Unidad 3 EstequiometriaKaren GomezNo ratings yet
- 2BachQuiExa4Solucion PDFDocument4 pages2BachQuiExa4Solucion PDFAntonio José Vasco MerinoNo ratings yet
- Jabon Mi Japonesa Preferida... Con ACEITE DE ARROZDocument2 pagesJabon Mi Japonesa Preferida... Con ACEITE DE ARROZJose M RuizNo ratings yet
- Acido CitricoDocument7 pagesAcido CitricoAndy PhyNo ratings yet
- Practica N°3Document14 pagesPractica N°3Cielo AzulNo ratings yet
- Taller 1 Quimica Organica II Ago Dic 2016 - AldCetDocument5 pagesTaller 1 Quimica Organica II Ago Dic 2016 - AldCetchrisNo ratings yet
- Clasificacion de Los Hidrocarburos Cuarto de SecundariaDocument7 pagesClasificacion de Los Hidrocarburos Cuarto de SecundariaMilagros FabianNo ratings yet
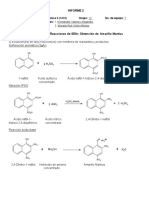
- Informe de La Práctica No. 2. Reacciones de SEAr, Obtención de Amarillo MartiusDocument8 pagesInforme de La Práctica No. 2. Reacciones de SEAr, Obtención de Amarillo MartiusAlejandra Hernández ValenzoNo ratings yet
- Exposiciòn NovenoDocument19 pagesExposiciòn NovenoJuan Pablo Acevedo SuarezNo ratings yet
- Determinación-De-Azúcares-Feling-Y-Fenol (2) 1Document4 pagesDeterminación-De-Azúcares-Feling-Y-Fenol (2) 1Vani VazquezNo ratings yet
- Reporte Heterociclos Inorgánicos TiotetrazolesDocument4 pagesReporte Heterociclos Inorgánicos TiotetrazolesJosue Hernandez MrkzNo ratings yet
- Formato Informe Laboratorio SumativaDocument6 pagesFormato Informe Laboratorio SumativaleninNo ratings yet
- ESQI GuionDocument15 pagesESQI Guionlucianobuglioni9323No ratings yet
- Sem. 3 Quimica ChininDocument2 pagesSem. 3 Quimica ChininRICHAR GUEVARA CHIQUILLANNo ratings yet
- Guía AlcanosDocument7 pagesGuía AlcanosErickson Sanchez50% (2)
- Importancia de Los AlcoholesDocument14 pagesImportancia de Los Alcoholesgero animationsNo ratings yet
- Quimica 3Document2 pagesQuimica 3Frank GaramediNo ratings yet
- Serie de Problemas QUIMICA ORGANICADocument80 pagesSerie de Problemas QUIMICA ORGANICARicardo SierraNo ratings yet
- Quim 1102Document2 pagesQuim 1102Allison Guerrero diazNo ratings yet
- Unidad 90 Guia 1 Quimica Tercero BguDocument9 pagesUnidad 90 Guia 1 Quimica Tercero Bgubyit s5No ratings yet
- Material para La Nomenclatura OrgánicaDocument4 pagesMaterial para La Nomenclatura OrgánicaMiguel CampeloNo ratings yet
- Nomenclatura y Caracteristicas de Alcanos NormalesDocument1 pageNomenclatura y Caracteristicas de Alcanos NormalesOmar CupidoNo ratings yet
- Laboratorio HidrolisisDocument4 pagesLaboratorio HidrolisisMarvin Paolo Rosas MendozaNo ratings yet
- Radicales 1Document1 pageRadicales 1Yadi UgenioNo ratings yet