Professional Documents
Culture Documents
Aluminum Base Alloys
Uploaded by
DaruzboyOriginal Description:
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Aluminum Base Alloys
Uploaded by
DaruzboyCopyright:
Available Formats
CHAPTER 4 ALUMINUM-BASE ALLOYS
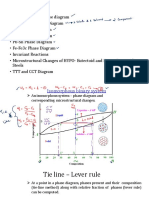
Aluminum, with its low density, was early an attractive candidate as the base for the development of engineering alloys. Although the strengths attained in these alloys are not as great as those attainable in steels, the strength-to-weight ratio is very favorable, and hence many commercial aluminum-base alloys are available. Most of these alloys have their strength increased by precipitation hardening, a process reviewed in Chapter 3. In this chapter, the physical metallurgy underlying the heat treatment of one commercial aluminum-base alloy, 2024, is examined in detail. The pertinent ternary and quaternary phase diagrams are used to describe the phase relations and to show why specific heat treatments are used. 4-1. Ternary Phase Diagrams The phase relations in ternary systems are usually presented in terms of isothermal sections through triangular composition-temperature phase diagrams. We will briefly examine te meaning of such sections here. Consider three components, A, B and C, which in pairs have the binary phase diagrams shown in Fig. 4-1, each being a simple eutectic system. To depict the phase relations for a ternary plot and show temperature as the variable in the vertical direction. We will assume here that the ternary system of A, B and C has eutectic diagram. That is, there is a ternary alloys which has a lowest melting point. The assumed diagram is shown in Fig. 4-2. Each of the terminal solid solutions has some solubility. Fig. 4-1. Three eutectic binary phase diagrams of the system A-B, B-C, and C-A. Fig. 4-2. Assumed ternary diagram for the system A-B-C. (From Phase Diagrams in Metallurgy, by F.N. Rhines. Copyright @ 1956, McGrawHill, New York. Used with the permission of McGraw-Hill Book Company) If a constant temperature plane is passed through the phase diagram, the intersection of this plane with the phase equilibria surfaces (e.g., solidliquid boundaries) generates an isothermal section. Those given by the temperatures shown in Fig. 4-2 are shown in Fig. 4-3. Note that three-phase equilibrium can exist over a range of temperatures in a ternary system, whereas it is limited to a fixed temperature in a binary system (e.g., two solids and a liquid at the eutetic temperature). Fig. 4-3. Isothermal sections from the ternary A-B-C phase diagram, at the temperatures indicated in Fig. 4-2. (From same source as Fig. 4-2; used with the permission of McGraw-Hill Book Company). If the composition of an alloy is in the three-phase region, the chemical composition of each phase is given by the apex at each corner. This is illustrated in Fig. 4-4. In the two-phase region the composition is given by a tie line, which must be experimentally located. This is illustrated also in Fig. 4-4. For example, the alloy which has the composition given by point 1 is in the + L region. The composition of the liquid (point 3) and the (point 2) must be connected by a straight line through point 1. From a mass balance the amount of each phase can be calculated. If the composition is at point 4, , L and are present, and the chemical composition of each phase is given by point 5, 6, and 7, respectively. Again , the amount of each phase can be calculated.
It is also useful to examine the projections of the liquidus, solidus and solvus, and these are ilustrated in Fig. 4-5 and 4-6, using the B rich corner of the ternary diagram in Fig. 4-2. Fig. 4-4. Isothermal section at temperature T5, used to illustrate the chemical composition of the phases in two-phase and three-phase region. Fig. 4-5 Illustration of the relation between the liquidus and solidus sufaces, and projection of their isotherms onto a plane. Fig. 4-6 Illustration of the relation between the solvus and its isotherms projected onto a plane. Fig. 4-7 Schematic quarternary isothermal phase diagram for the system A-B-C-D where the components are completely soluble. Fig. 4-8 Constant-composition sections from the quaternary diagrams shown in Fig. 4-7. If there are four components present, the presentation of phase equilibria is more complicated. One method is to present the composition-phase relations at a given temperature in a tetrahedron. This is illustrated in Fig. 4-7 for a hypothetical system in which the four components are completely soluble in each other. At the temperature for which the diagram applies, there is a single-phase region at the A-rich corner of the diagrams. A two-phase region ( + liquid) separates this region from the liquid region. It is difficult to analyze quantitatively data in such a figure. Instead it is more useful to present constant-composition sections from the tethahedron, as illustrated in Fig. 4-8. It is seen that these isothermal sections are similar in appearance to those of ternary systems. However, most binary system are sufficiently complicated that the quarternary diagram is difficult to present in any from other than the constant-composition sections.
4-2. Aluminum-Copper-Magnesium Alloys In the binary aluminum-copper system, the aluminum-rich terminal solid solution is in equilibrium with the intermetallic compound , which has approximately the formula CuAl2, although some solid solubility exists. (See Fig. 3-8). The addition of magnesium allows the formation of more intermetallic compounds, as illustrated Fig. 4-9 by the isothermal section at 4300C for the ternary system. Since the alloys of interest are aluminum-rich, only those phases in equlibrium with are of interest, and there are four possibilities. Although these are represented by compound formulas, in actuality there is some solid solubility. Fig. 4-9. Isotermal section at 4300C for the Al-Cu-Mg system. Note that there are several intermetallic compounds present. Four of these Mg2Al3, Mg32(Al,Cu)49, CuMgAl2 and CuAl2 can be in equlibrium with the phase. (Adapted from Metals Handbook, 8th Ed., Vol 8, American Society for Metals, Metals Park, Ohio, 1973) Fig. 4-10. Projections of the liquidus, solidus and solvus isotherms for the Al-rich end of the Al-CuMg system. The circle in each diagram denotes the alloy containing 4% Cu and 1% Mg, and the temperatures noted are for this composition. The letters a, b, and c refer to locations in Fig. 4-11. (Adapted from same source as Fig. 4-9)
Fig. 4-11. Illustration of the relation between the projection of the liqiudus, solidus and solvus isotherms and the three-dimensional phase diagram. The temperatures noted are for an aluminum alloy containing 4% Cu and 1% Mg. The liquidus, solidus and solvus isotherms are shown in Fig. 4-10. To illustrate the heat treatment of these alloys, we will consider an alloy containing 4% Cu and 1% Mg. This composition is located at the circle in each of the isothermal projections. The interpolated isotherms through this composition are indicated on the figures. To visualize the relation of this composition ti=o the isotherms, Fig. 4-11 shows the relation of the liquidus, solidus and solvus projections to the three-dimensional ternary phase diagram. It is seen that, for this composition, the alloy is liquid above 6500C (point a); in the two-phase liquid-solid region between 5700C (point b) and 6500C; in the single-phase region between 5700C and 5000C (point c); and in the three-phase region below 5000C. The three-phase relation is not shown in Fig. 4-11, but it is in Fig. 4-12, the isotherm at 4300C. It is seen that at this temperature this alloy has in equilibrium with CuAl2 and CuMgAl2. Fig. 4-12. Enlargement of the Al-rich portion of the Al-Cu-Mg isothermal section at 4300C. The alloy containing 4% Cu and 1% Mg is seen to be in the three-phase region in which , CuAl2 and CuMgAl2 are in equilibrium. Now for precipitation hardening, the first step in the heat treatment is to equilibrate the alloy in the region (Fig. 4-11); that is, to solution heat treat the alloy. This alloy must be heated between 500 and 5700C for sufficient time to homoginize the structure, which by experimentation would be found to be a few a hours. [However, the original casting may require up to 100 h to remove dendritic segregation (coring) and dissolve second-phase particles. See Chapter 2.]. After the solution heat treatment, the alloy must be cooled to 200C at a rate sufficient to suppress any precipitaion. For example, plate about 0.5 in. Thick (or less) can be quenched into cold water. The precipitation process begins immediately, and the rate depends upon the temperature at which the alloy is held after quenching from the solution treatment temperature. In this Al-Cu-Mg alloy, the rate at 200C is sfficiently great to cause prominent mechanical property changes, as shown in Fif. 4-13. (Precipitation hardening at room temperature is referred to as age hardening, or natural hardening.) note that the yield strength increases from about 12,000 psi for the solution-treated condition to about 38,000 psi after two years. Fig 4-13. Effect of aging at the 200C on the yield strength of Al-Cu-Mg alloys. (Adapted from W.L. Fink, D.W. Smith and L.A. Willey, in Age Hardening of Metals, American Society for Metals, Metals Park, Ohio, 1940) At 4300C, the alloy will contain at equilibrium about 3% CuAl2 and 5% CuMgAl2. (This is calculated by a mass balance from the data in Fig. 4-12.). Assuming that at equillibrium at 200C the Cu and Mg content of the is negligible, the amount of CuAl2 will be about 4% and CuMgAl2 about 4%. This is about the same as at 4300C can be used as an approximation of the amount present at 200C. Eximination of Fig. 4-12 shows that as the Mg content is increased to 1.5% Mg but the Cu content kept at 4%, the amount of CuAl2 decreases to less than 1% and that CuMgAl2 increases to 8%. Thus, as the Cu/Mg ratio decreases, CuMgAl2 formation becomes more important in determining the precipitation-hardening process. Note that the steps leading to the formation of this phase are more effective in precipitation hardening than those associated with the formation of CuAl2. This is seen in Fig. 4-13. Even though the binary alloy, in which only CuAl2 is involved, does harden appreciably, the addition of Mg causes significantly greater hardening.
In these ternary alloys, the precipitation mechanism is similar in scheme to that described in Chapter 3 for copper-aluminum alloys. First to form are GP zones, followed by a coherent transition phase. Eventually the equilibrium CuMgAl2 phase forms, then coarsens. If the Cu/Mg ratio is high, the formation of CuAl2 can occur, and its formation mechanism should be the same as described for the Al-Cu binary alloy. If the Cu/Mg ratio is such as to allow comparable amounts of both phases to form, the mechanism or formation of only a single GP zone, with the separate phases appearing later in the sequance. The precipitation details are not well established, even though the process involves the type of steps described in Chapter 5.
Aluminum-Copper-Magnesium Commercial Alloys A commonly used commercial alloy based on the Al-Cu-Mg ternary system is 2004, we will examine its heat treatment in detail. The chemical composition is within the following specification: 3.8-4.9% Cu, 1.2-1.8% Mg, 0.4-0.9% Mn, 0.50% max Si, 0.50% max Fe, 0.10% max Cr, 0.25% max Zn. Let us first examine this alloy as if it contained only Al, Cu and Mg, using an average composition of 4.5% Cu and 1.5% Mg. For such a ternary alloy, Fig. 4-10 shows a solidus of about 560oC and a solvus of about 520oC. For the 2024 alloy, the recommended solution treatment range is 488-499oC. This seems somewhat low, but the range of composition must be considered in specifying a temperature range for used with the alloy. Figure 4-14 shows the Cu and Mg ranges blocked out for the solidus and solvus. Note that if the Cu and Mg are both on the low side, the solidus will be about 560oC and the solvus about 500oC. However, if the Cu and Mg are both on the high side, the situation is different. To see this, we examine Fig. 4-15. The aluminum-rich section of the phase diagram is shown at 510oC, where the blocked-out area covers the composition limits of Mg and Cu. Note that for high Cu and Mg, liquid will be present with the ,and the solid phase CuMgAl2 may also be present. The ternary eutectic temperature for equilibrium , CuMgAl2, and CuAl2 is 508 oC. The diagram for 508 oC in Fig. 4-15(b) was derived from that for 510 oC in Fig. 4-15(a). Note that the liquid region has shrunk to a point corresponding to the ternary eutectic. If the temperature falls below 508 oC, this liquid phase disappears. Thus, at 508 oC in this general composition range the solidus and solvus are identical. This can be seen in Fig. 4-14, which shows the composition range blocked out on the solidus and solvus projections. For high Cu and Mg content, at 508 oC the alloy would fall within the phase fields involving , Cu Al2, CuMgAl2 and liquid. Fig 4-14. Solidus adn solvus projections with the Cu and Mg ranges for 2024 shown blocked out. (Adapted from same source as Fig. 4-9) Fig. 4-15. (a) Isotherm at 510 oC (adapted from H .W.L Philips, Annotated Equilibrium Diagrams of Some Aluminum Alloys Systems, The Institute of Metals, London, 1959). (b) Isotherm at 508 oC, the ternary eutectic temperature involving liquid, CuAl2 and CuMgAl2. Just below this temperature, the liquid shown by the point disappears. (c) Enlargement of the region shown in (b). For the 2024 alloy, two important facts are derived from this analysis. First, to avoid the possibility of localized melting in the alloy if the Cu and Mg are on high side, the solution treatment temperature is below 508 oC (e.g.,495 oC), and if the Cu and Mg content are on the high side of the allowable range, then the alloy will not be in a single-phase region but in a multiphase solid field. To visualize this, examine the isotherm at 430 oC in Fig. 4-16. It is seen that if Cu and Mg content are high the alloy will be in the -CuAl2 region or in the -CuAl2-CuMgAl2 region, depending upon the exact chemical
composition. Thus, solution treating the alloy between 430 and 508 oC will result in some solid phases present along with the . That is, the solution-treated condition may contain some CuAl2 or CuMgAl2 along with the . (Also, in the aged condition, both of these solid phases may form.) The lower solution temperature of 488 oC recommended for 2024 is based on the highest temperature consistent with minimizing the possibility of melting and yet obtaining maximum solution of solute. The recommended range also takes into account the uncertainty in temperature control and the temperature gradients that exist in commercial heat treating furnaces. Now the effects of the presence of Si, Mn and Fe must be considered. Figure 4-17 shows the projection of the aluminum-rich corner of the quaternary Al-Cu-Mg-Si phase diagram in the temperature range where only solid phases are present.the addition of Si will favor the formation of the quarternary compound Cu2Mg8Si5Al4. Figure 4-18 shows a section from the quartenary diagram at 502 oC for a fixed Cu content of 4%. The range of the allowable variation in Mg and Si content, could be in equilibrium with Mg2Si, CuMgAl2, CuAl2 and Cu2Mg8Si5Al4. Thus the addition of Si allows the formation of two more solid phases which more not present in the Al-Cu-Mg ternary system: Mg2Si and Cu2Mg8Si5Al4. Fig. 4-16. Isotherm at 430 oC. Enlargement of the Al-rich corner from Fig. 4-9. Fig. 4-17. Projection of the Al-rich corner of the Al-Cu-Mg-Si phase diagram for the solid condition. (From L.F. Mondolfo, Aluminum Alloys; Structure and Properties, Butterworths, London, 1976) Fig. 4-18. Section of the quaternary phase diagram for the Al-Cu-Mg-Si system at 502 oC and 4% Cu. The phase called Q is Cu2Mg8Si5Al4. (From same source as Fig. 17) Fig. 4-19. Projections of the Al-rich corner of the (a) Al-Cu-Mg-Mn, (b) Al-Cu-Mg-Fe and (c) Al-CuMn-Fe phase diagrams for the solid condition. (From same source as Fig. 4-17) The presence of Mn and Fe also allows the formation of additional intermetallic compounds. Figure 4-19(a) and (b) show the projection of the aluminum-rich corner of the Al-Cu-Mg-Mn and Al-Cu-MgFe diagrams in the solid range. Adding Mn promotes the formation of Cu3Mn2Al20, and adding Fe promotes Cu2FeAl7. Figure 4-9(c) shows the Al-Cu-Mn-Fe diagram. Increased Mn and Fe promote the formation of the phase which is a solid solution compound based on (CuFe) Al6 and MnAl6; it is usually designated as (Cu, Fe, Mn)Al6. Thus we see that in the 2024 commercial alloy several intermetallic phases may be present, depending upon the exact chemical composition and the heat treatment. It also depends quite sensitively upon how the alloy was cast, because the cooling rate from the liquid affects the phases formed in the eutectic reactions. In setting the upper limit of the solution treatment temperature, the possibility of a eutectic reaction between the and some of these other phases must be considered. However, it is found the lowest eutectic temperature is 505 oC (involving CuAl2, CuMgAl2 and Cu2FeAl7 and ), so that the upper limit of 499 oC is still valid. The microstructure of a 2024 alloy which has been annealed (cooled slowly from the solution treatment temperature) is shown Fig. 4-20. The large black particles are CuMgAl2, which were present at the solution treatment temperature. Also present in that condition were a few large gray particles of (Cu,Fe,Mn)Al6, due to the Fe and Mn in the alloy. However, the majority of the particles are CuMgAl2. The fine black praticles are also CuMgAl2, but they formed upon cooling slowly from
the solution treatment temperature. (Note that the particular etch used did not reveal the grain boundaries.) The microstructure in the solution-treated condition is shown in Fig. 4-21. The etch used revealed the grain boundaries, as well as some particles present at the solution treatment temperature. These were identified as CuMgAl2 along with some Cu2Mn3Al20 and Cu2FeAl7. Note that the grains are elongated, appearing similar to that of cold worked structure. This is caused by a nonuniform distribution of undissolved phases present at the solution temperature during annealing of the cold worked material. Upon completion of recrystallization, the grains begin to grow, but their boundary movement is inhibited by the particles present, and since their distribtion is nonuniform, the annealed grain structure is still elongated. Fig. 4-20. Microstructure of a 2024 alloy in the annealed condition (condition TO). Etched in 25% nitric acid. Optical micrograph; 500x.(Adapted from Metals Handbook, 8th Ed., Vol 7, American Society for Metals, Metals Park, Ohio, 1972) During precipitation, the structure is too fine to properly resolve with optical microscopy. Electron microscopy reveals that the precipitation process is similar to that described in Chapter 3 for Al-Cu alloys; however, the details of the precipitation process do depend upon the exact chemical composition of the alloy. In all cases, though, GP zones and transition phases from which are responsible for hardening. Eventually, the equilibrium phases appear. Fig. 4-21. Microstructure of 2024 alloy in the solution heat treated colndition (condition T3). Optical micrograph; 500x. The dark particles are CuMgAl2, Cu2Mn3Al20 and Cu2FeAl2. Etched in Kellers reagent. (From same source as Fig. 4-20) Fig. 4-22. Effect of aging time at 20, 0 and -17 oC on the mechanical properties of 2024 alloy. (From Solid Solution, American Society for Metals, Metals Park, Ohio, 1958) Fig. 4-23. Effect of aging time and temperature on the mechanical properties of 2024 alloy. The initial condition was the natural aged state (temper T4). (From same source as Fig. 4-23) Fig. 4-24. Effect of Fe additions on the age hardening at 150 OC of Al-Cu alloys. (From H.Y. Hunsicker, in Age Hardening of Metals, American Society for Metals, Metals Park, Ohio, 1940) Fig. 4-25. Isothermal section at 500 oC for the Al-Cu-Fe system. (Adapted from H.W.L. Phillips, J. Inst. Metals, Vol 82, p 197, 1953/54) The effect of the precipitation process on the mechanical properties of a 2024 alloy is illustrated in Fig. 4-22 and 4-23. Aging at low temperature hardens the alloy in a manner very similar to that for Al-Cu-Mg ternary alloy (Fig. 4-13). Elevated temperature precipitation is much more effective in hardening this alloy. The data in Fig. 4-23 shoh that the strength can be increased from about 40,000 to about 55,000 psi by aging at about 200 oC (400 oF) for a few hours. For the 2024 alloy, a recommended aging treatment is to heat for 11 to 13 h in range 185 to 196 OC (365 to 385 OF). Figure 4-23 shows that this time is in the range of the maximun in the strength. The mechanical properties upo aging do not vary greatly with variation in chemical composition within the allowable range for 2024 alloy from those shown in Fig. 4-22 and 23. However, the effects of Fe deserves specific attention since its presence can lower the hardening response. Figure 4-24 shows that the the addtion of 1.0% Fe to an Al-4.5 Cu alloy almost eliminates any hardening.
Examination of the Al-Cu-Fe ternary 500 oC isotherm (Fig. 4-25) shows why the iron has such an effect: the solubility of Fe in is quite low, and the intermetallic compound based on the approximate formula Cu2FeAl7 forms. Figure 4-26 is an enlargement of the aluminum-rich corner. The line at constant Cu content of 4.5% is shown, and the composition of 4.5% Cu and 1.0% Fe is in the + region. The tie line through this composition, extending from the phase to the compound (Cu2FeAl7)3, reveals that the Cu content of the is 2.2%. Thus, although the alloy contains 4.5% Cu, the compound Cu2FeAl7 takes about half of the cooper out of the solution. Upon rapid cooling to 20 oC, the alloy consists of particles of the compound in an matrix, but the contains only 2.2% Cu. Upon aging, very little additional Cu2FeAl7 will from since its solubility in is very low at 500 OC. The phase boundaries shift to favor the precipitation of CuAl2, which is the phase which froms in the binary Al-Cu alloy. However, even though the ternary alloy contains 4.5% Cu, upon aging it behaves like a binary alloy containing about 2.2% Cu. This is responsible for the very low age hardening of the iron-containing alloys shown in Fig. 4-25, and for the iron content of the 2024 alloy being held to 0.5% or less. Fig.4-26. Enlargement of the Al-rich corner of the Al-Cu-Fe ternary phase diagram at 500 OC.
BAB 4 PADUAN ALUMINIUM - DASAR
Aluminium , dengan kepadatan yang rendah , adalah awal kandidat yang menarik sebagai dasar untuk pengembangan paduan rekayasa . Meskipun kekuatan dicapai dalam paduan ini tidak begitu besar seperti yang dicapai pada baja , rasio kekuatan -to-weight sangat menguntungkan , dan karenanya banyak paduan aluminium - dasar komersial yang tersedia . Sebagian besar paduan ini memiliki kekuatan mereka meningkat pengerasan presipitasi , proses terakhir dalam Bab 3 . Dalam bab ini , metalurgi fisik yang mendasari perlakuan panas dari satu paduan aluminium - dasar komersial , 2024, diperiksa secara rinci . The bersangkutan terner dan kuartener diagram fasa yang digunakan untuk menggambarkan hubungan fase dan untuk menunjukkan mengapa pengobatan panas spesifik yang digunakan . 4-1 . Ternary Tahap Diagram Hubungan fase dalam sistem terner biasanya disajikan dalam hal bagian isotermal melalui segitiga suhu komposisi fase diagram . Kami akan secara singkat memeriksa te arti bagian seperti di sini. Perhatikan tiga komponen , A , B dan C , yang di pasang telah diagram fasa biner ditunjukkan pada Gambar . 4-1 , masing-masing menjadi sistem eutektik sederhana . Untuk menggambarkan hubungan fase untuk plot ternary dan suhu menunjukkan sebagai variabel dalam arah vertikal . Kami akan menganggap di sini bahwa sistem terner dari A , B dan C memiliki diagram eutektik . Artinya , ada paduan terner yang memiliki titik leleh terendah . Diagram diasumsikan ditunjukkan pada Gambar . 42 . Setiap larutan padat terminal memiliki beberapa kelarutan . Gambar . 4-1 . Tiga eutektik diagram fasa biner dari sistem AB , BC , dan CA . Gambar . 4-2 . Diasumsikan diagram terner untuk sistem A - B - C . ( Dari Tahap Diagram di Metalurgi , oleh FN Rhines . Copyright @ 1956, McGrawHill , New York . Digunakan dengan izin dari McGraw -Hill Book Company ) Jika sebuah pesawat suhu konstan dilewatkan melalui diagram fasa , persimpangan pesawat ini dengan permukaan kesetimbangan fase ( misalnya , batas solidliquid ) menghasilkan bagian isotermal . Yang diberikan oleh suhu ditunjukkan pada Gambar. 4-2 ditunjukkan pada Gambar . 4-3 . Perhatikan bahwa tiga fase kesetimbangan dapat ada pada rentang suhu dalam sistem terner , sedangkan terbatas pada suhu tetap dalam sistem biner ( misalnya , dua padatan dan cairan pada suhu eutetic ) . Gambar . 4-3 . Bagian isotermal dari terner ABC diagram fasa , pada suhu yang ditunjukkan pada Gambar . 4-2 . ( Dari sumber yang sama seperti Gambar 4-2 ; . Digunakan dengan izin dari McGraw Hill Book Company ) . Jika komposisi paduan berada di kawasan tiga fase , komposisi kimia dari setiap tahap diberikan oleh puncak di setiap sudut . Hal ini diilustrasikan pada Gambar . 4-4 . Di wilayah dua - fase komposisi diberikan oleh garis dasi , yang harus eksperimen berada. Hal ini digambarkan juga pada Gambar . 44 . Misalnya, paduan yang memiliki komposisi yang diberikan oleh titik 1 adalah dalam + L daerah . Komposisi cairan ( point 3 ) dan ( point 2 ) harus terhubung oleh garis lurus melalui titik 1 . Dari keseimbangan massa jumlah setiap fase dapat dihitung . Jika komposisi adalah pada titik 4 , , L dan
yang hadir , dan komposisi kimia dari setiap tahap ditentukan oleh titik 5 , 6 , dan 7 , masingmasing. Sekali lagi , jumlah masing-masing fase dapat dihitung . Hal ini juga berguna untuk mengetahui proyeksi likuidus , solidus dan solvus , dan ini ilustrated pada Gambar . 4-5 dan 4-6 , menggunakan sudut B kaya diagram terner pada Gambar . 4-2 . Gambar . 4-4 . Bagian isotermal pada suhu T5 , digunakan untuk menggambarkan komposisi kimia dari fase dalam dua - fase dan wilayah tiga fase . Gambar . 4-5 Ilustrasi hubungan antara likuidus dan solidus sufaces , dan proyeksi isoterm mereka ke pesawat . Gambar . 4-6 Ilustrasi hubungan antara solvus dan isoterm yang diproyeksikan ke pesawat. Gambar . 4-7 Skema kuarterner diagram fase isotermal untuk sistem ABCD dimana komponen benarbenar larut . Gambar . 4-8 bagian Konstan - komposisi dari diagram kuartener ditunjukkan pada Gambar. 4-7 . Jika ada empat komponen ini, penyajian kesetimbangan fasa lebih rumit . Salah satu metode adalah untuk menyajikan hubungan komposisi - fase pada suhu tertentu dalam tetrahedron . Hal ini diilustrasikan pada Gambar . 4-7 untuk sistem hipotetis di mana empat komponen benar-benar larut dalam satu sama lain . Pada suhu yang diagram berlaku , ada fase tunggal wilayah di - kaya Sebuah sudut diagram . Sebuah wilayah dua fase ( + cairan ) memisahkan wilayah ini dari wilayah cair . Sulit untuk menganalisis data kuantitatif pada gambar tersebut . Sebaliknya itu adalah lebih berguna untuk menyajikan bagian konstan - komposisi dari tethahedron , seperti diilustrasikan pada Gambar . 4-8 . Hal ini terlihat bahwa bagian isotermal mirip dalam penampilan dengan yang sistem terner . Namun, sistem biner kebanyakan cukup rumit bahwa diagram kuarterner sulit untuk hadir di setiap dari selain bagian konstan - komposisi .
4-2 . Aluminium - Tembaga - Magnesium Paduan Dalam sistem aluminium - tembaga biner , larutan padat terminal kaya aluminium berada dalam kesetimbangan dengan senyawa intermetalik , yang memiliki sekitar rumus CuAl2 , meskipun beberapa kelarutan padat ada. ( Lihat Gambar . 3-8 ) . Penambahan magnesium memungkinkan pembentukan senyawa intermetalik yang lebih , seperti yang diilustrasikan Gambar . 4-9 oleh bagian isotermal pada 4300C untuk sistem terner . Karena paduan bunga - kaya aluminium , hanya fase dalam equlibrium dengan yang menarik , dan ada empat kemungkinan . Walaupun hal ini diwakili oleh rumus senyawa , dalam kenyataannya ada beberapa kelarutan padat . Gambar . 4-9 . Bagian isotermal pada 4300C untuk sistem Al - Cu - Mg . Perhatikan bahwa ada beberapa senyawa intermetalik hadir . Empat dari ini - Mg2Al3 , MG32 ( Al , Cu ) 49 , CuMgAl2 dan CuAl2 - bisa di equlibrium dengan fase . ( Diadaptasi dari Logam Handbook , 8th Ed . , Vol 8 , American Society untuk Logam , Logam Park, Ohio , 1973) Gambar . 4-10 . Proyeksi dari likuidus , solidus dan solvus isoterm untuk akhir Al - kaya sistem Al Cu - Mg . Lingkaran di setiap diagram menunjukkan paduan yang mengandung 4 % Cu dan 1 % Mg ,
dan suhu dicatat adalah untuk komposisi ini . Huruf a, b , dan c mengacu pada lokasi pada Gambar . 4-11 . ( Diadaptasi dari sumber yang sama seperti Gambar . 4-9 ) Gambar . 4-11 . Ilustrasi hubungan antara proyeksi liqiudus , solidus dan solvus isoterm dan diagram fase tiga dimensi . Suhu dicatat adalah untuk paduan aluminium yang mengandung 4 % Cu dan 1 % Mg . Likuidus , solidus dan solvus isoterm ditunjukkan pada Gambar . 4-10 . Untuk menggambarkan perlakuan panas dari paduan ini , kami akan mempertimbangkan paduan yang mengandung 4 % Cu dan 1 % Mg . Komposisi ini terletak di lingkaran di masing-masing proyeksi isotermal . Isoterm yang diinterpolasi melalui komposisi ini ditunjukkan pada angka-angka . Untuk memvisualisasikan hubungan komposisi ti ini = o isoterm , Gambar . 4-11 menunjukkan hubungan antara likuidus , solidus dan solvus proyeksi untuk tiga - dimensi diagram fasa terner . Hal ini terlihat bahwa , untuk komposisi ini , paduan cair di atas 6500C ( butir a) ; di wilayah cair-padat dua fase antara 5700C ( butir b) dan 6500C , dalam satu fase daerah antara 5700C dan 5000C ( titik c ) , dan di wilayah tiga fase di bawah 5000C . Tiga - fase hubungan tidak ditampilkan pada Gambar . 4-11 , tetapi pada Gambar . 4-12 , isoterm pada 4300C . Hal ini terlihat bahwa pada suhu ini paduan ini telah dalam kesetimbangan dengan CuAl2 dan CuMgAl2 . Gambar . 4-12 . Pembesaran bagian Al - kaya bagian isotermal Al - Cu - Mg pada 4300C . Paduan yang mengandung 4 % Cu dan 1 % Mg terlihat berada di wilayah tiga fase di mana , CuAl2 dan CuMgAl2 berada dalam kesetimbangan . Sekarang untuk pengerasan presipitasi , langkah pertama dalam perlakuan panas adalah untuk menyeimbangkan paduan di wilayah (Gambar 4-11 ) , yaitu , untuk solusi panas mengobati paduan . Paduan ini harus dipanaskan antara 500 dan 5700C untuk waktu yang cukup untuk homoginize struktur , yang oleh eksperimen akan ditemukan beberapa jam . [ Namun , casting asli mungkin memerlukan hingga 100 jam untuk menghilangkan segregasi dendritik ( coring ) dan melarutkan partikel fase kedua . Lihat Bab 2 . ] . Setelah pengobatan solusi panas , paduan harus didinginkan hingga 200C pada tingkat yang cukup untuk menekan precipitaion apapun. Misalnya, piring sekitar 0,5 inci tebal ( atau kurang ) dapat dicelup ke dalam air dingin . Proses pengendapan dimulai segera , dan tingkat tergantung pada suhu di mana paduan diadakan setelah pendinginan dari suhu pengobatan solusi . Dalam paduan Al - Cu - Mg ini , tingkat di 200C adalah sfficiently besar untuk menyebabkan perubahan sifat mekanik yang menonjol , seperti yang ditunjukkan pada Fif . 4-13 . ( Pengendapan pengerasan pada suhu kamar disebut sebagai usia pengerasan , atau pengerasan alami . ) Mencatat bahwa kekuatan luluh meningkat dari sekitar 12.000 psi untuk kondisi solusi - diperlakukan untuk sekitar 38.000 psi setelah dua tahun . Gambar 4-13 . Efek penuaan pada 200C pada kekuatan luluh dari Al - Cu - Mg paduan . ( Diadaptasi dari WL Fink , DW Smith dan LA Willey , di Umur Pengerasan Logam , American Society untuk Logam , Logam Park, Ohio , 1940) Pada 4300C , paduan akan berisi pada kesetimbangan sekitar 3 % dan 5 % CuAl2 CuMgAl2 . ( Ini dihitung dengan keseimbangan massa dari data pada Gambar . 4-12 . ) . Dengan asumsi bahwa pada equillibrium pada 200C Cu dan Mg isi dapat diabaikan , jumlah CuAl2 akan menjadi sekitar 4 % dan CuMgAl2 sekitar 4 % . Ini hampir sama seperti di 4300C dapat digunakan sebagai perkiraan dari jumlah yang ada di 200C . Eximination Gambar. 4-12 menunjukkan bahwa kandungan Mg meningkat menjadi 1,5 % Mg tapi isi Cu disimpan di 4 % , jumlah CuAl2 menurun hingga kurang dari 1 % dan
CuMgAl2 meningkat menjadi 8 % . Dengan demikian , sebagai rasio Cu / Mg menurun , pembentukan CuMgAl2 menjadi lebih penting dalam menentukan proses presipitasi - pengerasan . Perhatikan bahwa langkah-langkah yang mengarah pada pembentukan fase ini lebih efektif dalam pengerasan presipitasi dibandingkan terkait dengan pembentukan CuAl2 . Ini terlihat pada Gambar . 4-13 . Meskipun paduan biner , di mana hanya CuAl2 terlibat , tidak mengeras lumayan , penambahan Mg menyebabkan pengerasan signifikan lebih besar . Dalam paduan terner , mekanisme curah hujan mirip dalam skema dengan yang dijelaskan dalam Bab 3 untuk paduan tembaga - aluminium . Pertama ke bentuk adalah zona GP , diikuti oleh fase transisi koheren . Akhirnya bentuk kesetimbangan fasa CuMgAl2 , kemudian coarsens . Jika rasio Cu / Mg tinggi , pembentukan CuAl2 dapat terjadi , dan mekanisme pembentukannya harus sama seperti yang dijelaskan untuk Al - Cu paduan biner . Jika rasio Cu / Mg adalah seperti untuk memungkinkan jumlah yang sebanding dari kedua fase untuk membentuk , mekanisme dan pembentukan hanya zona GP tunggal , dengan fase terpisah muncul kemudian di sequance tersebut . Rincian curah hujan yang tidak mapan , meskipun proses melibatkan jenis langkah-langkah yang dijelaskan dalam Bab 5 .
Aluminium - Tembaga - Magnesium Paduan Komersial Sebuah paduan komersial yang umum digunakan berdasarkan sistem terner Al - Cu - Mg adalah 2004, kami akan memeriksa perlakuan panas secara rinci . Komposisi kimia dalam spesifikasi sebagai berikut : 3,8-4,9 % Cu , 1,2-1,8 % Mg , Mn 0,4-0,9 % , 0,50% max Si , 0,50% max Fe , 0,10 % max Cr , 0,25 % Zn max . Mari kita memeriksa paduan ini seolah-olah itu hanya berisi Al , Cu dan Mg , menggunakan komposisi rata-rata 4,5 % Cu dan 1,5 % Mg . Untuk seperti paduan terner , Gambar . 4-10 menunjukkan solidus sekitar 560oC dan solvus sekitar 520oC . Untuk 2024 alloy , berbagai pengobatan solusi yang disarankan adalah 488 - 499oC . Hal ini tampaknya agak rendah , tetapi berbagai komposisi harus dipertimbangkan dalam menentukan rentang suhu untuk digunakan dengan paduan . Gambar 4-14 menunjukkan Cu dan Mg rentang diblokir untuk solidus dan solvus . Perhatikan bahwa jika Cu dan Mg keduanya di sisi rendah , solidus akan menjadi sekitar 560oC dan solvus tentang 500oC . Namun, jika Cu dan Mg keduanya pada sisi yang tinggi , situasinya berbeda . Untuk melihat ini , kita meneliti Gambar . 4-15 . Bagian yang kaya aluminium dari diagram fasa ditunjukkan pada 510oC , dimana area diblokir -out meliputi batas komposisi Mg dan Cu . Perhatikan bahwa untuk Cu tinggi dan Mg , cairan akan hadir dengan , dan fase padat CuMgAl2 juga dapat hadir . Suhu eutektik terner untuk keseimbangan , CuMgAl2 , dan CuAl2 adalah 508 oC . Diagram untuk 508 oC pada Gambar . 4-15 ( b ) yang berasal dari itu untuk 510 oC pada Gambar . 4-15 ( a) . Perhatikan bahwa wilayah cair telah menyusut ke titik yang sesuai dengan eutektik terner . Jika suhu turun di bawah 508 oC , fase cair ini menghilang . Dengan demikian, pada 508 oC dalam kisaran komposisi umum ini solidus dan solvus identik . Hal ini dapat dilihat pada Gambar . 4-14 , yang menunjukkan kisaran komposisi diblokir pada proyeksi solidus dan solvus . Untuk tinggi Cu dan Mg konten , pada 508 oC paduan akan jatuh dalam bidang fase yang melibatkan , Cu Al2 , CuMgAl2 dan cair . Gambar 4-14 . Solidus adn proyeksi solvus dengan Cu dan Mg berkisar selama 2024 menunjukkan diblokir . ( Diadaptasi dari sumber yang sama seperti Gambar . 4-9 )
Gambar . 4-15 . ( a) Isoterm pada 510 oC ( diadaptasi dari H . WL Philips , Annotated Equilibrium Diagram Beberapa Aluminium Paduan Systems, The Institute of Metals , London , 1959) . ( b ) Isoterm pada 508 oC , suhu eutektik terner melibatkan cair , CuAl2 dan CuMgAl2 . Tepat di bawah suhu ini , cairan yang ditunjukkan oleh titik menghilang . ( c ) Pembesaran wilayah ditunjukkan pada ( b). Untuk 2024 alloy , dua fakta penting yang berasal dari analisis ini . Pertama , untuk menghindari kemungkinan pencairan lokal di paduan jika Cu dan Mg berada di sisi yang tinggi , suhu pengobatan solusinya adalah di bawah 508 oC ( misalnya , 495 oC ) , dan jika Cu dan konten Mg berada di sisi yang tinggi rentang yang diijinkan , maka paduan tidak akan berada dalam wilayah satu fase tetapi dalam bidang padat multifase . Untuk memvisualisasikan ini , memeriksa isoterm pada 430 oC pada Gambar . 4-16 . Hal ini terlihat bahwa jika Cu dan konten Mg yang tinggi paduan akan berada di wilayah - CuAl2 atau di wilayah - CuAl2 - CuMgAl2 , tergantung pada komposisi kimia yang tepat . Dengan demikian , solusi mengobati paduan antara 430 dan 508 oC akan menghasilkan beberapa fase padat hadir bersama dengan tersebut . Artinya, kondisi solusi - diperlakukan mungkin mengandung beberapa CuAl2 atau CuMgAl2 bersama dengan tersebut . (Juga , dalam kondisi tua , kedua fase padat bisa terbentuk . ) Semakin rendah suhu larutan dari 488 oC direkomendasikan untuk 2024 didasarkan pada suhu tertinggi konsisten dengan meminimalkan kemungkinan pencairan dan belum memperoleh solusi maksimum zat terlarut . Rentang direkomendasikan juga memperhitungkan ketidakpastian dalam kontrol suhu dan gradien suhu yang ada di panas komersial mengobati tungku . Sekarang efek dari kehadiran Si , Mn dan Fe harus dipertimbangkan . Gambar 4-17 menunjukkan proyeksi sudut - kaya aluminium dari kuaterner Al - Cu - Mg - Si diagram fasa pada rentang temperatur di mana hanya fase padat penambahan present.The Si akan mendukung pembentukan senyawa kuarterner Cu2Mg8Si5Al4 . Gambar 4-18 menunjukkan bagian dari diagram quartenary pada 502 oC untuk Cu konten tetap dari 4 % . Kisaran variasi yang diijinkan di Mg dan konten Si , bisa berada dalam kesetimbangan dengan Mg2Si , CuMgAl2 , CuAl2 dan Cu2Mg8Si5Al4 . Dengan demikian penambahan Si memungkinkan pembentukan dua fase padat yang lebih tidak hadir dalam sistem terner Al - Cu - Mg : Mg2Si dan Cu2Mg8Si5Al4 . Gambar . 4-16 . Isoterm pada 430 oC . Pembesaran dari sudut Al - kaya dari Gambar . 4-9 . Gambar . 4-17 . Proyeksi sudut Al - kaya diagram fasa Al - Cu - Mg - Si untuk kondisi padat . ( Dari LF Mondolfo , Aluminium Paduan , Struktur dan Properties , Butterworths , London , 1976) Gambar . 4-18 . Bagian dari diagram fasa kuaterner untuk sistem Al - Cu - Mg - Si pada 502 oC dan 4 % Cu . Fase yang disebut Q adalah Cu2Mg8Si5Al4 . ( Dari sumber yang sama seperti Gambar . 17 ) Gambar . 4-19 . Proyeksi dari sudut Al - kaya ( a) Al - Cu - Mg - Mn , ( b ) Al - Cu - Mg - Fe dan ( c ) Al - Cu - Mn - Fe diagram fase untuk kondisi padat . ( Dari sumber yang sama seperti Gambar . 4-17 ) Kehadiran Mn dan Fe juga memungkinkan pembentukan senyawa intermetalik tambahan . Gambar 419 ( a) dan ( b ) menunjukkan proyeksi sudut - kaya aluminium dari Al - Cu - Mg - Mn dan Al - Cu Mg - Fe diagram dalam kisaran padat . Menambahkan Mn mempromosikan pembentukan Cu3Mn2Al20 , dan menambahkan Fe mempromosikan Cu2FeAl7 . Gambar 4-9 ( c ) menunjukkan diagram Al - Cu - Mn - Fe . Peningkatan Mn dan Fe mempromosikan pembentukan fase yang
merupakan senyawa larutan padat berdasarkan ( CuFe ) AL6 dan MnAl6 , biasanya ditunjuk sebagai ( Cu , Fe , Mn ) AL6 . Jadi kita melihat bahwa di 2024 paduan komersial beberapa fase intermetalik mungkin ada, tergantung pada komposisi kimia yang tepat dan perlakuan panas . Hal ini juga tergantung cukup sensitif pada bagaimana paduan itu diusir , karena laju pendinginan dari cairan mempengaruhi fase terbentuk dalam reaksi eutektik . Dalam menetapkan batas atas suhu pengobatan solusi , kemungkinan reaksi eutektik antara dan beberapa di antaranya tahapan lain yang harus dipertimbangkan . Namun, ditemukan suhu eutektik terendah adalah 505 oC ( melibatkan CuAl2 , CuMgAl2 dan Cu2FeAl7 dan ) , sehingga batas atas 499 oC masih berlaku . Struktur mikro dari paduan 2024 yang telah anil ( didinginkan perlahan-lahan dari suhu pengobatan solusi ) ditunjukkan Gambar . 4-20 . Partikel-partikel hitam besar yang CuMgAl2 , yang hadir pada suhu pengobatan solusi . Juga hadir dalam kondisi yang beberapa partikel abu-abu besar ( Cu , Fe , Mn ) AL6 , karena Fe dan Mn dalam paduan . Namun, sebagian besar partikel CuMgAl2 . The praticles hitam halus juga CuMgAl2 , tetapi mereka terbentuk pada saat pendinginan perlahan dari suhu pengobatan solusi . ( Perhatikan bahwa etsa tertentu yang digunakan tidak mengungkapkan batas butir . ) Struktur mikro dalam kondisi solusi - diperlakukan ditunjukkan pada Gambar . 4-21 . Etsa yang digunakan mengungkapkan batas butir , serta beberapa partikel hadir pada temperatur perlakuan solusi . Ini diidentifikasi sebagai CuMgAl2 bersama dengan beberapa Cu2Mn3Al20 dan Cu2FeAl7 . Perhatikan bahwa biji-bijian yang memanjang , muncul mirip dengan struktur bekerja dingin . Hal ini disebabkan oleh distribusi seragam fase larut hadir pada suhu larutan selama anil bahan bekerja dingin . Setelah menyelesaikan rekristalisasi , butir mulai tumbuh , tetapi gerakan batas mereka dihambat oleh partikel ini, dan karena distribtion mereka seragam , struktur butir yang anil masih memanjang . Gambar . 4-20 . Mikrostruktur dari 2024 paduan dalam kondisi anil ( kondisi TO) . Terukir dalam asam nitrat 25 % . Optical mikrograf ; 500x ( . Diadaptasi dari Logam Handbook , 8th Ed , Vol 7 , American Society untuk Logam , Logam Park, Ohio , 1972) . Selama curah hujan , struktur terlalu baik untuk benar menyelesaikan dengan mikroskop optik . Mikroskop elektron menunjukkan bahwa proses pengendapan mirip dengan yang dijelaskan dalam Bab 3 untuk Al - Cu paduan , namun rincian dari proses pengendapan yang tergantung pada komposisi kimia yang tepat dari paduan . Dalam semua kasus , meskipun, GP zona dan fase transisi dari yang bertanggung jawab untuk pengerasan . Akhirnya , fase kesetimbangan muncul. Gambar . 4-21 . Mikrostruktur 2024 paduan dalam larutan perlakuan panas colndition ( kondisi T3 ) . Optical mikrograf ; 500x . Partikel-partikel gelap CuMgAl2 , Cu2Mn3Al20 dan Cu2FeAl2 . Terukir dalam reagen Keller . ( Dari sumber yang sama seperti Gambar . 4-20 ) Gambar . 4-22 . Pengaruh waktu penuaan pada 20 , 0 dan -17 oC pada sifat mekanik dari paduan 2024 . ( Dari Larutan Padat , American Society untuk Logam , Logam Park, Ohio , 1958) Gambar . 4-23 . Pengaruh waktu aging dan temperatur terhadap sifat mekanik paduan 2024 . Kondisi awal adalah alam negara usia ( temper T4 ) . ( Dari sumber yang sama seperti Gambar . 4-23 )
Gambar . 4-24 . Pengaruh penambahan Fe pada pengerasan usia 150 OC dari Al - Cu paduan . ( Dari HY Hunsicker , di Umur Pengerasan Logam , American Society untuk Logam , Logam Park, Ohio , 1940 ) Gambar . 4-25 . Bagian isotermal pada 500 oC untuk sistem Al - Cu - Fe . ( Diadaptasi dari HWL Phillips , J. Inst . Logam , Vol 82 , p 197 , 1953-1954 ) Efek dari proses presipitasi pada sifat mekanik dari 2.024 paduan diilustrasikan pada Gambar . 4-22 dan 4-23 . Penuaan pada suhu rendah mengeras paduan dalam cara yang sangat mirip dengan yang untuk Al - Cu - Mg alloy terner (Gambar 4-13 ) . Peningkatan curah hujan suhu jauh lebih efektif dalam pengerasan paduan ini . Data pada Gambar . 4-23 shoh bahwa kekuatan dapat ditingkatkan dari sekitar 40.000 menjadi sekitar 55.000 psi oleh penuaan di sekitar 200 oC ( 400 oF ) selama beberapa jam . Untuk 2024 alloy , pengobatan penuaan disarankan adalah panas selama 11 sampai 13 jam dalam kisaran 185-196 OC ( 365-385 OF ) . Gambar 4-23 menunjukkan bahwa saat ini berada di kisaran maximun dalam kekuatan . Sifat mekanis upo penuaan tidak bervariasi dengan variasi komposisi kimia dalam rentang yang diijinkan untuk 2024 paduan dari yang ditunjukkan pada Gambar . 4-22 dan 23 . Namun, efek dari Fe layak untuk mendapatkan perhatian khusus karena kehadirannya dapat menurunkan respon pengerasan . Gambar 4-24 menunjukkan bahwa dengan penambahan 1,0 % Fe ke Al - 4.5 Cu paduan hampir menghilangkan pengerasan apapun. Pemeriksaan Al - Cu - Fe terner 500 oC isoterm (Gambar 4-25 ) menunjukkan mengapa besi memiliki efek seperti itu : kelarutan Fe dalam cukup rendah , dan senyawa intermetalik berdasarkan bentuk-bentuk rumus Cu2FeAl7 perkiraan . Gambar 4-26 adalah pembesaran sudut yang kaya aluminium . Garis konstan Cu isi dari 4,5% ditunjukkan , dan komposisi 4,5% Cu dan 1,0 % Fe dalam + wilayah . Garis dasi melalui komposisi ini , membentang dari fase untuk senyawa ( Cu2FeAl7 ) 3 , mengungkapkan bahwa kandungan Cu dari adalah 2,2 % . Jadi, meskipun paduan mengandung 4,5% Cu , senyawa Cu2FeAl7 memakan waktu sekitar setengah dari tembaga keluar dari solusi . Setelah pendinginan cepat hingga 20 oC , paduan terdiri dari partikel senyawa dalam matriks , tetapi hanya 2,2 % Cu . Setelah penuaan , sangat sedikit Cu2FeAl7 tambahan akan dari sejak kelarutannya dalam sangat rendah pada 500 OC . Batas-batas fase bergeser mendukung pengendapan CuAl2 , yang merupakan fase yang froms dalam biner Al - Cu alloy . Namun, meskipun paduan terner mengandung 4,5% Cu , setelah penuaan itu berperilaku seperti paduan biner yang mengandung sekitar 2,2 % Cu . Ini bertanggung jawab untuk pengerasan usia yang sangat rendah dari paduan besi yang mengandung ditunjukkan pada Gambar. 4-25 , dan untuk kadar besi dari 2.024 paduan diadakan untuk 0,5 % atau kurang . Gbr.4 - 26 . Pembesaran sudut Al - kaya dari Al - Cu - Fe diagram fasa terner pada 500 OC .
You might also like
- 6 0LDies PDFDocument101 pages6 0LDies PDFscodavnx100% (1)
- Phase Equilibria and Phase TransformationDocument57 pagesPhase Equilibria and Phase TransformationAzhan Haqimi100% (1)
- Athene S Theory of Everything PDFDocument19 pagesAthene S Theory of Everything PDFAdriana Ealangi0% (1)
- Iron-IronCarbide Phase DiagramDocument3 pagesIron-IronCarbide Phase Diagramumangmodi32No ratings yet
- NC, CNC and RoboticsDocument100 pagesNC, CNC and RoboticsGovt Job update - JagadishNo ratings yet
- Ternary Phase DiagramsDocument10 pagesTernary Phase Diagramskikiomen4No ratings yet
- Welding Technology English (Cont.)Document143 pagesWelding Technology English (Cont.)Long Beautéophile100% (1)
- Chemistry Leuco DyesDocument312 pagesChemistry Leuco Dyeskarel470% (1)
- Determination of Lead-Tin Phase Diagram Using Cooling CurvesDocument5 pagesDetermination of Lead-Tin Phase Diagram Using Cooling CurvesSandra de la Merced100% (1)
- Phase Diagrams - Equilibrium Microstructural Development: 38 WT % PBDocument45 pagesPhase Diagrams - Equilibrium Microstructural Development: 38 WT % PBpetember100% (1)
- The Law of CosinesDocument12 pagesThe Law of CosinesLei Xennia YtingNo ratings yet
- AFS Thermal Analysis of CupsDocument12 pagesAFS Thermal Analysis of Cupsyash_ganatraNo ratings yet
- TYPD ExercisesDocument10 pagesTYPD ExercisesConstance Lynn'da GNo ratings yet
- Formal Lab 2Document38 pagesFormal Lab 2sreyes4100% (1)
- Lead Tin Phase Diagram ExperimentDocument5 pagesLead Tin Phase Diagram ExperimentOliver Tabell100% (2)
- S. Ostanin Et Al - Ab Initio Study of The Phase Separation of Argon in Molten Iron at High PressuresDocument3 pagesS. Ostanin Et Al - Ab Initio Study of The Phase Separation of Argon in Molten Iron at High PressuresDrebuioNo ratings yet
- Chapter 4-Phase DiagramDocument16 pagesChapter 4-Phase Diagramtky96No ratings yet
- Chapter 2 - TTA - TTT - DiagramsDocument13 pagesChapter 2 - TTA - TTT - DiagramsPrasad Mhatre100% (1)
- Diagram MeDocument22 pagesDiagram MeAkira SaidNo ratings yet
- Biomaterials II Lec 5Document13 pagesBiomaterials II Lec 5m9trdk92ksNo ratings yet
- Phase Diagram - : Dr. Aneela Wakeel 02-01-2018Document42 pagesPhase Diagram - : Dr. Aneela Wakeel 02-01-2018Hassan KhanNo ratings yet
- Metallurgical EngineeringDocument49 pagesMetallurgical EngineeringMatab ThamerNo ratings yet
- 2 5391019718461098174Document7 pages2 5391019718461098174Motaz TharwatNo ratings yet
- Capili Jefferson 9Document13 pagesCapili Jefferson 9Christian Al EncarnacionNo ratings yet
- Question & Answer Set-7Document12 pagesQuestion & Answer Set-7eeng.ali651550% (2)
- FL&O Section 10Document24 pagesFL&O Section 10Muhammad FaizNo ratings yet
- On Equilibrium Phase Diagram of The Iron - Carbon System: Prof. Evgeny V. SidorovDocument6 pagesOn Equilibrium Phase Diagram of The Iron - Carbon System: Prof. Evgeny V. SidorovRamon BrownNo ratings yet
- Unit - III: Me432P: Material EnggDocument37 pagesUnit - III: Me432P: Material Engghans groupNo ratings yet
- Ch08 Metals and AlloysDocument26 pagesCh08 Metals and Alloysabin vkNo ratings yet
- Metals and Alloys StudyDocument26 pagesMetals and Alloys Studyabin vkNo ratings yet
- Capili Jefferson 10Document5 pagesCapili Jefferson 10Christian Al EncarnacionNo ratings yet
- TTOPIC 6 Phase PDFDocument19 pagesTTOPIC 6 Phase PDFSaud AssiriNo ratings yet
- Molybdonem Phase Diagraphsm CR CoDocument6 pagesMolybdonem Phase Diagraphsm CR CotheosaundersNo ratings yet
- Chapter 8 (Heat Treatment)Document12 pagesChapter 8 (Heat Treatment)Shekinah KanindaNo ratings yet
- Task 4: Thermal Equilibrium DiagramDocument3 pagesTask 4: Thermal Equilibrium DiagramMisbah Tehseen100% (1)
- 5 Raja 444230Document12 pages5 Raja 444230medane_saad6707No ratings yet
- Copper NickelDocument5 pagesCopper NickelFahri Ali ImranNo ratings yet
- Materials and Metallurgy (ME-209) Phase DiagramsDocument24 pagesMaterials and Metallurgy (ME-209) Phase DiagramsMuhammad AmirNo ratings yet
- CHAPTER 3 Phase Diagram TTT HT - 1stDocument25 pagesCHAPTER 3 Phase Diagram TTT HT - 1stAriff AziziNo ratings yet
- 1.1 Diagramas de FasesDocument60 pages1.1 Diagramas de FasesAlex Pelinco ApazaNo ratings yet
- Materials Science and Engineering Properties 1st Edition Charles Gilmore Solutions Manual 1Document36 pagesMaterials Science and Engineering Properties 1st Edition Charles Gilmore Solutions Manual 1brendacastanedabatxnmfoze100% (20)
- Cu Al Fe PDFDocument4 pagesCu Al Fe PDFreyhanNo ratings yet
- Assignment WEEK 5 SolutionsDocument5 pagesAssignment WEEK 5 SolutionsPeeka Prabhakara RaoNo ratings yet
- Iron Carbon Phase Diagram TEDDocument6 pagesIron Carbon Phase Diagram TEDAnonymous dh6DITNo ratings yet
- 00400011a3 Papers 00400011A3 00400011A30172 PDFDocument13 pages00400011a3 Papers 00400011A3 00400011A30172 PDFandyNo ratings yet
- 2009 Models For The Thermodynamic Properties, Density and Viscosity of Molten SaltsDocument12 pages2009 Models For The Thermodynamic Properties, Density and Viscosity of Molten SaltsAdrian CaraballoNo ratings yet
- Lecture 1 - Smart Materials - IntroductionDocument8 pagesLecture 1 - Smart Materials - IntroductionOmar Adel MohammedNo ratings yet
- Zn-Fe-Al Phase Diagram Low TempDocument16 pagesZn-Fe-Al Phase Diagram Low Tempbdavis33100% (1)
- Lab 7 - Phase DiagramsDocument7 pagesLab 7 - Phase Diagramsabd333No ratings yet
- Cast Steel: The Iron-Carbon Equilibrium Diagram: AbstractDocument5 pagesCast Steel: The Iron-Carbon Equilibrium Diagram: Abstractchacha4500No ratings yet
- Characterization of The Weld Structure in A Duplex Stainless Steel Using Color MetallographyDocument11 pagesCharacterization of The Weld Structure in A Duplex Stainless Steel Using Color MetallographyAndrea CalderaNo ratings yet
- 1 Physical Metallurgy - Solid SolutionDocument28 pages1 Physical Metallurgy - Solid SolutionVinod Patil50% (2)
- RR416DKM19F2014Document2 pagesRR416DKM19F2014HasmitthaNo ratings yet
- 4Document63 pages4ARJUN PESARU 19BME0161No ratings yet
- Re Austenitisation MartensiteDocument4 pagesRe Austenitisation MartensiteAndress SsalomonnNo ratings yet
- 104 PhaseDiags QS2AnsDocument6 pages104 PhaseDiags QS2Ansnilanga123No ratings yet
- Written Report Chapter 9Document8 pagesWritten Report Chapter 9Engineer ZephyrusNo ratings yet
- CH 11Document9 pagesCH 11Muchammad FauziNo ratings yet
- Guevara & Irons (2011) Part IDocument12 pagesGuevara & Irons (2011) Part IaarondenboerNo ratings yet
- Topic 4 Extension Questions: 4 Bonding and StructureDocument1 pageTopic 4 Extension Questions: 4 Bonding and Structurelianchen251110No ratings yet
- Chem 5Document10 pagesChem 50No ratings yet
- MO Theory Stuff PDFDocument20 pagesMO Theory Stuff PDFbits_who_am_i100% (1)
- Emm HandoutsDocument58 pagesEmm HandoutsDr.A.Maniram KumarNo ratings yet
- Supercapacitors Based on Carbon or Pseudocapacitive MaterialsFrom EverandSupercapacitors Based on Carbon or Pseudocapacitive MaterialsNo ratings yet
- Amorphous Semiconductors: Structural, Optical, and Electronic PropertiesFrom EverandAmorphous Semiconductors: Structural, Optical, and Electronic PropertiesNo ratings yet
- Applications of 8086Document38 pagesApplications of 8086Ajay PeterNo ratings yet
- All About FTP Must ReadDocument7 pagesAll About FTP Must ReadPINOY EUTSECNo ratings yet
- Act MCQDocument10 pagesAct MCQKARTHICKNo ratings yet
- Spray-Agglomeration of NPK-fertilizer in A Rotating Drum Granulator PDFDocument8 pagesSpray-Agglomeration of NPK-fertilizer in A Rotating Drum Granulator PDFKhoa TrầnNo ratings yet
- Metron PS-410 Patient SimulatorDocument2 pagesMetron PS-410 Patient SimulatorismailshajjiNo ratings yet
- PT 849 Req D PatchesDocument34 pagesPT 849 Req D PatchesxwNo ratings yet
- Manual EOS UtilityDocument122 pagesManual EOS Utilityjaimegarcia20No ratings yet
- DRG ch4Document33 pagesDRG ch4Muhammad Ashiqur Rahaman NoorNo ratings yet
- Ptical Oxygen Sensor: ATA HeetDocument14 pagesPtical Oxygen Sensor: ATA HeetZoran ConstantinescuNo ratings yet
- KinematicsDocument5 pagesKinematicsUnicornpop PopNo ratings yet
- Video Display DevicesDocument66 pagesVideo Display DevicesshabanaNo ratings yet
- Application Note: Vishay General SemiconductorDocument4 pagesApplication Note: Vishay General SemiconductorMamoon AlrimawiNo ratings yet
- 932qlg65vteb PDFDocument4 pages932qlg65vteb PDFMariaNo ratings yet
- Chap 9 PracDocument8 pagesChap 9 Pracyiiluk'Moo SineNo ratings yet
- Time ResponseDocument105 pagesTime ResponseFrogie HuniebieNo ratings yet
- Digital Microelectronic Digital Microelectronic Circuits Circuits ( (Document24 pagesDigital Microelectronic Digital Microelectronic Circuits Circuits ( (Gowtham HariNo ratings yet
- Norma JIC 37Document36 pagesNorma JIC 37guguimirandaNo ratings yet
- Neural-Network-Based Maximum Power Point Tracking Methods For Photovoltaic Systems Operating Under Fast Changing EnvironmentsDocument12 pagesNeural-Network-Based Maximum Power Point Tracking Methods For Photovoltaic Systems Operating Under Fast Changing EnvironmentsAbderrezak BadjiNo ratings yet
- Lecture 2 - Inverse Laplace TransformsDocument3 pagesLecture 2 - Inverse Laplace TransformsAmirah MapandiNo ratings yet
- Mongo DB Basic CommandsDocument15 pagesMongo DB Basic CommandsgauriNo ratings yet
- Data Communication: By:Eng - Alaa I.HaniyDocument8 pagesData Communication: By:Eng - Alaa I.Haniypömo cNo ratings yet
- Cooling Solutions About UsDocument18 pagesCooling Solutions About UsBlender RemixNo ratings yet
- Molten Salt Heat Storage PDFDocument20 pagesMolten Salt Heat Storage PDFchuckhsu1248No ratings yet
- Complex Numbers SpreadsheetDocument2 pagesComplex Numbers SpreadsheetrodwellheadNo ratings yet