Professional Documents
Culture Documents
L8 QF 10 11 PDF
Uploaded by
Francisco PestanaOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
L8 QF 10 11 PDF
Uploaded by
Francisco PestanaCopyright:
Available Formats
Leccin 8 Qumica Fsica (Curso 2010-11)
LECCIN 8: TOMOS POLIELECTRNICOS Objetivos de la Leccin. Funciones de onda simtricas y antisimtricas. Principio de exclusin de Pauli. El tomo de He. Determinantes de Slater. Orbitales aproximados de Slater. Principio de Construccin y Configuracin electrnica. Momento angular en tomos polielectrnicos. Interacciones spin-orbital. Estructura energtica y espectros de tomos polielectrnicos. Apndice 8.1: Construccin de trminos espectroscpicos. Apndice 8.2: Efecto Zeeman. Cuestiones. Problemas.
OBJETIVOS DE LA LECCIN. En la leccin 2 se dejo pendiente uno de los postulados de la Mecnica Cuntica, aquel que afectaba a sistemas con ms de una partcula. Este principio, denominado de antisimetra, o principio de exclusin de Pauli, ser estudiado en esta leccin. El principio de antisimetra, fija el tipo de funciones de onda vlidas en sistemas polielectrnicos. La aplicacin de este principio a funciones de onda construidas segn la aproximacin de electrones independientes, y que posteriormente sern utilizadas para el clculo de energa mediante mtodos aproximados, permite deducir que las energas de los estados dependen de la repulsin entre electrones, as como del valor de los nmeros cunticos L y S. La influencia de los nmeros cunticos L y S en la energa de los estados puede analizarse de forma conjunta a travs del nmero cuntico J. Dicho anlisis se efecta de forma cualitativa a travs de las denominadas interacciones Spin-Orbital, o interacciones L-S, a partir de las cuales se definen los denominados trminos espectroscpicos, equivalentes a los niveles de energa del tomo. Por ltimo, se analizan algunos ejemplos donde se estudiar la estructura electrnica y los espectros de algunos tomos polielectrnicos sencillos.
169
Leccin 8 Qumica Fsica (Curso 2010-11)
FUNCIONES DE ONDA SIMTRICAS Y ANTISIMTRICAS Las funciones de onda para el tomo de helio, segn la aproximacin de electrones independientes, tiene la forma = (q1)(q2), donde y representan dos orbitales cualesquiera del tomo de hidrgeno, y q1 y q2, son las coordenadas de los dos electrones (ri en el caso ms simple). Hasta donde hemos visto, no existe nada que nos impida colocar dos, o ms electrones, en el mismo orbital. Para que nuestro razonamiento sea general, vamos a suponer que y son diferentes, y para analizar un ejemplo, supondremos que = 1s y = 2s. El cuadrado de , nos proporciona la probabilidad de encontrar a cada uno de los electrones en determinadas regiones del espacio, q1 y q2 (o r1 y r2).
2 2 P (1, 2 ) = ( ) d = ( 1s,2s ) d = 1s ( r1 ) d1 2s ( r2 ) d2 = P1s ( r1 ) P2s ( r2 ) 2 2
(8.1)
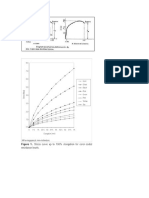
Es decir, la probabilidad total es el producto de las probabilidades individuales de cada electrn en el correspondiente orbital atmico. Vamos a suponer, que queremos calcular la probabilidad de encontrar al electrn 1 a una distancia r1 del ncleo, y simultneamente al electrn 2 a una distancia r2. La probabilidad total, ser por tanto el producto P(1,2) = P1s(r1) P2s(r2). En la Figura 8.1-a, se muestran las representaciones de P1s(r1), y P2s(r2), y se indican con flechas los valores de estas funciones para dos distancias concretas r1 y r2, indicando dichas distancias con lneas verticales rosas.
a)
Probabilidad
15
b)
P1s (r1) P2s (r2) Probabilidad
15
P2s (r1)
10
10
P1s (r2)
5
r1
r2
r (D )
r1
r2
r (D )
Figura 8.1
Arbitrariamente hemos asignado el electrn 1 al orbital 1s, pero nada nos obliga a ello. Vamos a suponer ahora que el electrn 1 est situado en el orbital 2s, mientras que el 2 lo est en el 1s. De hecho las probabilidades de encontrar a los electrones a esas distancias, y en dichos orbitales son diferentes de cero. La asignacin realizada ahora se indica mediante; = (q2)(q1) En este caso, la probabilidad ser,
2 2 P ( 2,1) = ( ) d = ( 2s,1s ) d = 1s ( r2 ) d2 2s ( r1 ) d1 = P1s ( r2 ) P2s ( r1 ) 2 2
(8.2)
En la Figura 8.1-b, se indican los valores de P1s(r2) y P2s(r1) a las mismas distancias que en el
170
Leccin 8 Qumica Fsica (Curso 2010-11)
caso anterior. Evidentemente, como puede deducirse de la Figuras 8.1, P(1,2) P(2,1). Es decir, la probabilidad total es diferente en funcin de cmo distribuyamos los electrones en los diferentes orbitales, lo cual es absurdo, ya que los electrones no cambian de sitio, solo los asignamos, arbitrariamente, a un orbital u otro. En cualquier caso, la funciones = 1s,2s = 1s(r1) 2s(r2), y = 2s,1s = 1s(r2) 2s(r1), son degeneradas, ya que al ser un sistema formado por partculas independientes, la energa es la suma de las energas de los orbitales atmicos 1s y 2s. Es decir, tenemos dos funciones que poseen la misma energa, pero que dan lugar a diferentes probabilidades, luego, Cual es la funcin correcta?. De hecho, la pregunta anterior no tiene sentido y deberamos mejor preguntar; Es posible distinguir a un electrn del otro?, llevan una etiqueta los electrones que nos indican en todo momento, que pertenecen al orbital 1s o al 2s?. Evidentemente, no. Antes de resolver el problema veamos por qu ha surgido dicho problema: Todo parte de que no se puede resolver de forma analtica la ecuacin de Schrdinger de tomos polielectrnicos, H = E, por lo que se utilizan soluciones aproximadas, del tipo 0 = (qi), (aproximacin de electrones independientes), de forma que cada electrn es introducido en un orbital atmico del hidrgeno, y al hacer esto, estamos distinguiendo a los electrones, es decir, estamos ponindoles etiqueta, y por lo tanto estamos cometiendo un error. Aunque en Mecnica Clsica las partculas son distinguibles, en Mecnica Cuntica dos partculas idnticas son indistinguibles. La necesidad de que las partculas cunticas sean indistinguibles, se traduce en el principio que nos dice que; Las propiedades de todo sistema cuntico deben permanecer invariantes
ante el intercambio de dos partculas idnticas. Segn esto, cuando en la funcin de onda del tomo
de He se intercambian de posicin los electrones 1 y 2, las propiedades del sistema no deberan modificarse, y, evidentemente esto no ocurre con las dos funciones anteriores, ya que las probabilidades que predicen dichas funciones son diferente. Luego, las funciones = 1s,2s = 1s(r1) 2s(r2), y = 2s,1s = 1s(r2) 2s(r1), no son funciones aceptables para describir correctamente la probabilidad de encontrar a los electrones en el tomo de He. Volvamos a una situacin general, donde , y , son dos orbitales atmicos cualesquiera, representando = (q1)(q2) una situacin en la que introducimos al electrn 1 en el orbital , y el 2, en el , mientras que , representa la situacin inversa, en la que electrn 1 se introduce en el orbital , y el 2, en el . Segn lo comentado con anterioridad, estas funciones no son aceptables ya que; ()2 ()2. Funciones aceptables son las que cumplen que ( q1 ,q 2 ) = ( q 2 ,q1 )
2 2
( q1 ,q 2 ) = ( q 2 ,q1 )
(8.3)
Esta relacin la tiene que cumplir, no solo la funcin real desconocida, sino tambin cualquier funcin aproximada que utilicemos (aproximacin de electrones independientes). Si en la ecuacin (8.3)(parte derecha), el signo es positivo, se dice que la funcin es simtrica, y si es negativo, antisimtrica. Aunque las funciones y no son aceptables, sin embargo, si lo son combinaciones
171
Leccin 8 Qumica Fsica (Curso 2010-11)
lineales de ellas
s = + a = s ( q1 ,q 2 ) = s ( q 2 ,q1 ) a ( q1 ,q 2 ) = a ( q 2 ,q1 )
(8.4)
Estas dos funciones si son aceptables desde el punto de vista de que los electrones son partculas indiscernibles. Adems, son funciones degeneradas con y . A esta forma de introducir degeneracin se le denomina degeneracin por intercambio. El sentido fsico de estas expresiones consiste en permitir que todos los electrones, al ser indistinguibles, puedan situarse en todos los orbitales atmicos. La funcin de onda total se construye a partir del producto de la funcin orbital o espacial (solucin de la ecuacin de Schrdinger), y de la funcin de spin
n,� ,m,s,ms = n,� ,m s,ms = orbital spin = ( ) spin
(8.5)
Para un electrn dado, solo existen dos funciones de spin, que corresponden a los valores de ms = 1/2. A estas funciones se las denomin en la Leccin 6 mediante + y -. La funcin de onda total debe poseer simetra con respecto al intercambio de electrones, luego, dado que la parte espacial posee simetra, s o a, la parte de spin tambin debe poseer simetra. Con dos funciones y dos electrones, es posible construir 4 funciones que posean simetra, estas son
+ (1) ( 2 ) (1) + ( 2 ) antisimetrica (1) ( 2 ) simetrica
(8.6)
+ (1) + ( 2 ) simetrica + (1) ( 2 ) + (1) + ( 2 ) simetrica
La funcin de onda total se construye multiplicando la parte espacial por la de spin, luego, en nuestro sistema de dos electrones, vamos a tener 8 funciones posibles, 4 simtricas y 4 antisimtricas. Las 4 funciones simtricas son:
( (
) + (1) ( 2 ) (1) + ( 2 )
+ ) + (1) + ( 2 ) + ) (1) ( 2 )
+ ) + (1) ( 2 ) + (1) + ( 2 )
(8.7)
Mientras que las 4 antisimtricas son:
( (
+ ) + (1) ( 2 ) (1) + ( 2 )
) + (1) + ( 2 ) ) (1) ( 2 )
) + (1) ( 2 ) + (1) + ( 2 )
(8.8)
Cualquiera de estas 8 funciones cumple el requisito exigido por la ecuacin (8.3).
172
Leccin 8 Qumica Fsica (Curso 2010-11)
PRINCIPIO DE EXCLUSIN DE PAULI
El principio de exclusin de Pauli nos dice que; un sistema formado por varios electrones solo puede estar representado por funciones de onda antisimtricas. Es decir, que de las 8 funciones anteriores, solo son vlidas, para describir el comportamiento del tomo de He, las 4 combinaciones antisimtricas, Total(q1,q2) = - Total(q2,q1). Estas son
+ ) + (1) ( 2 ) (1) + ( 2 )
[1]
(8.9)
[ 2] + (1) ( 2 ) + (1) + ( 2 ) [3] ( ) [ 4] ( ) (1) ( 2 )
) + (1) + ( 2 )
En la primera de estas funciones [1], la parte espacial es simtrica, y los electrones poseen valores de ms opuestos, se dice en este caso que los electrones son paralelos, o estn apareados ( ). El valor de ms total es Ms = ms(1) + ms(2) = 1/2 - 1/2 = 0 (usaremos letras maysculas, Ms, para indicar la suma de los valores de ms correspondientes a electrones individuales). Como Ms vara entre S, el spin total ser S = 0. La multiplicidad de un estado se defini en la leccin 6 como la relacin 2S+1, en nuestro caso 2S+1=1 (singlete). Adems, para este caso no existe ninguna restriccin para que = , es decir, los dos electrones pueden situarse en el mismo orbital atmico (parte espacial), y por lo tanto, pueden tener los mismos nmeros cunticos n, y m, ya que ms es diferente. Fijmonos ahora en las funciones [2]-[4] de la ecuacin (8.9), para estas tres funciones la parte espacial es antisimtrica, por lo que si = , la funcin de onda es cero. Es decir, la funcin de onda no existe si los dos electrones poseen los mismos nmeros cunticos n, y m. Estas tres funciones deben ser analizadas conjuntamente ya que poseen la misma parte espacial. En la funcin [2], Ms = ms (1) + ms(2) = +1/2 +1/2 =1, en la [3], Ms = +1/2 +(-1/2) =0, mientras que en la [4], Ms = -1/2 -1/2 = -1. Es decir, Ms = 0,1, por lo que S = 1. Se dice en este caso, que los electrones son antiparalelos o estn desapareados ( ), la multiplicidad es 2S+1 = 3 (hay tres estados degenerados, estado triplete). En este ltimo caso, los dos electrones poseen el mismo valor de ms, y como , se llega a la conclusin de que los dos electrones no pueden tener sus 4 nmeros cunticos iguales, ya que en dicho caso, la funcin de onda es cero. Esta es una conclusin del principio de exclusin de Pauli, que con frecuencia se suele enunciar como el propio principio. Supongamos que las funciones de onda simtricas son tambin vlidas para el tomo de He. Elijamos para ello, por ejemplo, la segunda de las funciones de la ecuacin (8.7). En esta funcin, los dos electrones poseen el mismo valor de ms, y adems, nada impide que = , es decir, los dos electrones pueden tener sus 4 nmeros cunticos iguales, en contra de la evidencia experimental. El hecho de que el movimiento de los electrones deba estar representado por funciones de onda antisimtricas tiene que ver con el valor de su spin. Las partculas que poseen spin semientero se denominan Fermiones (electrn, neutrn etc.), y estas partculas llevan asociadas funciones de onda
173
Leccin 8 Qumica Fsica (Curso 2010-11)
antisimtricas, o lo que es lo mismo, dos partculas no pueden tener los mismos nmeros cunticos, y por lo tanto no pueden situarse en el mismo estado. Las partculas con spin entero se denominan Bosones (fotn), y estas llevan asociadas en su movimiento funciones de onda simtricas, por lo que para ellas no se cumple el principio de exclusin de Pauli, es decir dos o ms partculas pueden tener todos sus nmeros cunticos iguales, pudiendo situndose en el mismo estado. Un ejemplo es la luz monocromtica. Las conclusiones del principio de exclusin son de enorme importancia, pero hay que recordar que necesitamos este principio para corregir las funciones de onda obtenidas mediante la aproximacin de electrones independientes. Estas funciones no son las funciones reales del tomo. Si se pudiera resolver la ecuacin de Schrdinger para tomo polielectrnicos este principio no sera necesario, ya que estara implcito en las soluciones obtenidas.
174
Leccin 8 Qumica Fsica (Curso 2010-11)
EL TOMO DE HELIO
Vamos a analizar los primeros niveles de energa del tomo de He, partiendo de la aproximacin de electrones independientes. En el estado fundamental, la configuracin electrnica es
1s 2 , lo que implica que debemos utilizar una parte espacial simtrica y por tanto, una de spin
antisimtrica. Dicha funcin tendr la forma
0 = N 1s (1) 1s ( 2 ) + 1s ( 2 ) 1s (1) + (1) ( 2 ) (1) + ( 2 ) = = 1s (1) 1s ( 2 ) + (1) ( 2 ) (1) + ( 2 )
(8.10)
Donde la constante de normalizacin, en la ltima de las expresiones, vale 1, suponiendo que los orbitales atmicos estn a su vez normalizados. En este estado los electrones estn apareados ( ), es decir S = 0. Vamos a aplicar el mtodo de variaciones para calcular la energa aproximada de este estado. La funcin de spin no depende de las coordenadas, actuando como una constante que para simplificar no escribiremos, por lo tanto E 0 = 0 H 0 d = 0 H 0 0 d + Las integrales del tipo:
2 (1) 1s ( 2 ) 0 d = 2E1s + 1s d =2E1s + J1s,1s r12 r12 2 2
(8.11)
(1) ( 2 )
2
r12
d =J ,
(8.12)
se denominan integrales de Coulomb. Estas son integrales bielectrnicas. En el apndice 7.1 se describi como se determinan. En la Tabla 8.1, se proporcionan los valores para algunas integrales sencillas de este tipo.
J,
5 Z 8 17 Z 81 59 Z 243
1s
1s 1s
1s
2s 2p
K, J1s,1s
16 Z 729 112 Z 6561
1s
1s 1s
1s
2s 2p
Tabla 8.1
Las integrales de Coulomb tienen unidades de energa, y en la tabla estn expresadas en unidades atmicas. Si se substituye en la ecuacin 8.11, la energa aproximada del estado fundamental del He ser: E 0 = 2E1s + J1s,1s = 2 Z2 5 10 + Z = 4 + = 2.75 2n 2 8 8 u.a. (8.13)
Experimentalmente la energa es 2.905 u.a, como ya sabemos. En la Figura 8.2, se muestra
175
Leccin 8 Qumica Fsica (Curso 2010-11)
un diagrama, en el que se representan las energas de los primeros estados del tomo de He.
1s 12p1 1s 12s 1
S=0 E2S=-2.124
2S = 21P1
3 S=1E2T=-2.135 2T = 2 P2,1,0 E =-2.146 1S = 21 S0 S=0 1S
S=1 E =-2.176 = 23S 1T 1 1T S=0
E0=-2.905
1s 2
0 = 11S0
Figura 8.2
La primera configuracin electrnica excitada del He es; 1s1 2 s1 . Al ser los orbitales diferentes tenemos dos opciones que consisten en usar funciones de onda espaciales simtricas, o antisimtricas. Llamemos 1T, a la funcin que se construye con una parte espacial antisimtrica, por lo que S =1, y los electrones estn desapareados (estado triplete, ). Esta funcin, que en realidad son tres funciones, tiene la forma:
+ (1) + ( 2 ) 1 1T = ( 1s (1) 2s ( 2 ) 1s ( 2 ) 2s (1) ) + (1) ( 2 ) + (1) + ( 2 ) 2 1 2 ( ) ( ) (8.14)
El fator 1/21/2, es la constante de normalizacin. Por otro lado, llamaremos 1S, a la funcin que posee la parte espacial simtrica, y de spin antisimetrica, por lo que S = 0 ( , estado singlete).
1S =
1 + (1) ( 2 ) (1) + ( 2 ) ( 1s (1) 2s ( 2 ) + 1s ( 2 ) 2s (1) ) 2
(8.15)
Segn la aproximacin de electrones independientes, los estados 1T, y 1S, son degenerados, sin embargo, cuando se aplica el mtodo de variaciones, sus energas son diferentes, as, ignorando la parte de spin, para 1T; E1T = 1T H1T d = 1T H 0 1T d + Vamos a analizar la ltima de estas integrales:
2 1T 1 ( 1s (1) 2s ( 2 ) 1s ( 2 ) 2s (1) ) 1 (1) 2s ( 2 ) d = 1s d + r12 d = 2 r12 2 r12 2 2 2 2 1T 2 d = E1s + E 2S + 1T d r12 r12
(8.16)
1 1s ( 2 ) 2s (1) 2 (1) 2s ( 2 ) 1s ( 2 ) 2s (1) d 1s d 2 r12 2 r12
2 2
(8.17)
Las dos primeras integrales son idnticas, y son del tipo de las integrales de Coulomb, analizadas en la ecuacin (8.12)
176
Leccin 8 Qumica Fsica (Curso 2010-11)
2 1s (1) 2 2s ( 2 )
r12
d =
2 2 1s ( 2 ) 2s (1)
r12
d = J1s,2s
(8.18)
Por otra parte, a las integrales del tipo:
K = (1) ( 2 ) ( 2 ) (1) r12 d (8.19)
se las denomina integrales de intercambio. En la Tabla 8.1, se muestran algunos valores para estas integrales bielectrnicas, que se resuelven mediante el mismo procedimiento al descrito en el apndice 7.1. Volviendo a la ecuacin (8.16) E1T = 1T H 0 1T d +
2 1T d =E1s + E 2S + J1s,2s K1s,2s r12
(8.20)
Por otra parte, si realizamos la misma operacin con la funcin 1S, tendremos que
E1S = 1S H 1S d = 1S H 0 1S d +
12S
r12
d = E1s + E2 S +
12S
r12
(8.21)
La ltima integral, puede escribirse como:
2 2 2 1S 1 ( 1s (1) 2s ( 2 ) + 1s ( 2 ) 2s (1) ) 1 1s (1) 2s ( 2 ) d = d = d + r12 2 r12 2 r12 2
1 1s ( 2 ) 2s (1) 2 (1) 2s ( 2 ) 1s ( 2 ) 2s (1) d + 1s d = J1s,2s + K1s,2s 2 r12 2 r12
2 2
(8.22)
Por lo tanto,
E1S = E1s + E2 S + J1s ,2 s + K1s ,2 s
datos de la Tabla 8.1, se obtiene que:
4 4 E1T = + 0.420 0.044 = 2.124 uaE. Experimentalmente 2.176 2 8 4 4 E1S = + 0.420 + 0.044 = 2.036 uaE. Experimentalmente 2.146 2 8
(8.23)
Resultado diferente al obtenido para 1T. Teniendo en cuenta que En = -Z2/2n2, y a partir de los
(8.24)
Por lo tanto, la configuracin electrnica 1s1 2 s1 , conduce a dos niveles de energa, en funcin de que el spin total sea S = 1, o S = 0. En la Figura 8.2, se representan las energas experimentales de estos estados, que son ligeramente diferentes a las calculadas mediante el mtodo de variaciones. Para la siguiente configuracin electrnica, 1s12p1, se pueden construir dos nuevas funciones que llamaremos 2T, y 2S. La forma de estas funciones es: 2T 2S + (1) + ( 2 ) = 1s (1) 2p ( 2 ) 1s ( 2 ) 2p (1) ) + (1) ( 2 ) + (1) + ( 2 ) ( 2 (1) ( 2 ) 1 = + (1) ( 2 ) (1) + ( 2 ) ( 1s (1) 2p ( 2 ) + 1s ( 2 ) 2p (1) ) 2 1
(8.25)
Aplicando el mtodo de variaciones, como anteriormente, sus energas aproximadas sern:
177
Leccin 8 Qumica Fsica (Curso 2010-11)
4 4 E 2T = E1s + E 2p + J1s,2p K1s,2p = + 0.486 0.034 = 2.049uaE Exper. 2.135 2 8 (8.26) E 2S = E1s + E 2p + J1s,2p + K1s,2p = 1.980uaE Exper. 2.124 En la Figura 8.2, se esquematizan estos diferentes niveles de energa. Con respecto al tomo de hidrgeno, la energa electrnica en el He est afectada por tres fenmenos nuevos: * La repulsin electrnica, * El spin total. * El valor del nmero cuntico . Es sorprendente que, a pesar de que la ecuacin de Schrdinger no predice la aparicin del spin, la energa que se obtiene si es funcin del spin. Este fenmeno surge del empleo de funciones de onda que poseen parte espacial simtrica (S = 0), o antisimtrica (S = 1). Un procedimiento cualitativo para analizar conjuntamente la influencia de y S en la energa, lo que se denomina interacciones spin-orbital, se analizar al final de esta leccin. Otra cuestin relacionada con lo anterior consiste en que puede generalizarse que; para una configuracin dada, el estado ms estable es siempre el de mayor spin (regla de Hund). Fijmonos, por ejemplo, en las ecuaciones (8.14) y (8.15), las cuales vamos a escribir de la forma: 1S = N ( 1s (1) 2s ( 2 ) + 1s ( 2 ) 2s (1) ) 1T = N ( 1s (1) 2s ( 2 ) 1s ( 2 ) 2s (1) ) S =1 S=0 (8.27)
Donde N es una constante que incluye la funcin de spin. En la Figura 8.3, se muestran las representaciones de la funcin probabilidad (el cuadrado de las funciones), para ambas funciones frente a r1 y a r2. En la pgina web: http://www.uco.es/organiza/departamentos/quimica-fisica/quimicafisica/MC/QFL8a.htm, se describe el mtodo para realizar esta representacin.
(R1S)2
(R1T)
r1 = r 2
Figura 8.3
178
Leccin 8 Qumica Fsica (Curso 2010-11)
En dicha figura, se observa que la probabilidad de encontrar a los dos electrones juntos, es decir para r1 . r2 (lnea roja en la figura), es cero para el estado 1T, y diferente de cero para 1S. Es decir, cuando S = 1, existe una repulsin entre los electrones, adicional a la repulsin de carga (hueco de Fermi), que hace que sea imposible encontrar a los electrones prximos uno a otro, este fenmeno estabiliza al orbital. Sin embargo, cuando S = 0, existe una cierta atraccin entre los electrones, debido al acoplamiento de sus spines, por lo que como consecuencia de la repulsin entre cargas, el estado es ms inestable, y es por lo tanto de mayor energa que cuando S = 1. .
179
Leccin 8 Qumica Fsica (Curso 2010-11)
DETERMINANTES DE SLATER
Cuando existen ms de dos electrones, no podemos construir funciones antisimtricas a mano, dado lo enormemente laborioso que resulta. Un mtodo general de escribir funciones de onda antisimtricas es mediante determinantes en los que se utilizan directamente las funciones spin-orbital. As, la funcin 0 del He, puede escribirse: 0 = 1 1s (1) + (1) 1s (1) (1) 2 1s ( 2 ) + ( 2 ) 1s ( 2 ) ( 2 ) (8.28)
En la primera columna, se coloca un spin-orbital 1s+, y en la segunda el otro spin-orbital 1s-, y en cada fila se aade un electrn. En general, la funcin de onda antisimtrica para el estado fundamental de un tomo, con n electrones, se puede escribir como
1s ( 2 ) + ( 2 ) 0 = 1s ( 3) + ( 3) n � 1 1s (1) + (1) 1s ( 2 ) ( 2 ) 1s ( 3) ( 3) � 1s (1) (1) 2s ( 2 ) + ( 2 ) � n ( 2 ) ( 2 ) 2s ( 3) + ( 3) � n ( 3) ( 3) � � � 2s (1) + (1) � n (1) (1)
(8.29)
1s ( n ) + ( n ) 1s ( n ) ( n ) 2s ( n ) + ( n ) � n ( n ) ( n )
La funcin cambia de signo si se intercambian dos filas (electrones) de posicin, lo que indica su carcter antisimtrico, y es cero, si dos columnas son iguales, es decir, si utilizamos dos spinorbitales con los 4 nmeros cunticos idnticos. La forma de expresar funciones antisimtricas de estados excitados de tomos es ms compleja, y se necesitan en general sumar varios determinantes.
180
Leccin 8 Qumica Fsica (Curso 2010-11)
ORBITALES APROXIMADOS DE SLATER
Los orbitales de Slater (STO) son funciones analticas de fcil manejo que se obtienen a partir del concepto de carga nuclear efectiva. Este concepto, de forma muy simplificada, consiste en suponer que los electrones internos apantallan la carga del ncleo, de forma que en la interaccin entre el electrn y el ncleo no interviene su carga real, sino la denominada carga nuclear efectiva, la cual se determina a partir de una serie de relaciones ms o menos empricas, procedentes de clculos variacionales. Los orbitales de Slater, en unidades atmicas, tienen la forma, n,� ,m = Nr n*1e rZ*/ n* Y�m (8.30) donde N, es una constante de normalizacin, n*, es el nmero cuntico principal efectivo, Z*, es la carga nuclear efectiva, e Ym, son las funciones armnicos esfricos. El valor de n*, se determina sustituyendo el nmero cuntico principal n = 1, 2, 3, 4, 5, 6, .., por n = 1, 2, 3, 3.7, 4, 4.2, .., y siendo Z* = Z Sn,, donde Sn,, es la denominada constante de apantallamiento. Esta, se calcula clasificando los orbitales atmicos en los siguientes grupos (1s) (2s,2p) (3s,3p) (3d) (4s,4p) (4d) (4f) (5s,5p).... El valor de Sn,, para un electrn dado, es la suma de las siguientes contribuciones: 1) 0.35 por cada electrn que exista en el mismo grupo que el considerado, salvo si es el grupo (1s) en cuyo caso se suma 0.3. 2) Si el electrn considerado es s o p, se suma 0.85 por cada electrn en el grupo inmediatamente inferior, y 1 por cada electrn ms interno. Para el resto de los grupos se suma 1 por cada electrn interno. La energa del tomo puede tambin determinarse, de forma aproximada, mediante la relacin
E = ( Z* i )
i
2 ( n* i )
(8.31)
Por ejemplo, para el He, Z1s* = 2-0.3 = 1.7, luego EHe = -2 (1.7)2/2 = -2.89 uaE (experimentalmente EHe = -2.905). Para el Li, Z1s* = 3-0.3 = 2.7, Z2s* = 3-20.85 = 1.3, luego ELi = -2 (2.7)2/2-(1.3)2/8 = -7.501 uaE (experimentalmente EHe = -7.478). Analicemos una cuestin interesante en el caso del tomo de Li. Cuando la configuracin electrnica es la fundamental (1s22s1), la energa del electrn en el orbital 2s es E2s = -(1.3)2/8 = -0.211 uaE. Pero si la configuracin electrnica es; 1s12s2, la constante de apantallamiento de los electrones 2s ser 0.85+0.35 = 1.2, luego Z2s* = 3-1.2 = 1.8, y por lo tanto, la energa de un electrn en un orbital 2s es E2s = -(1.8)2/8 = -0.405 uaE. Es decir, la energa del electrn en un orbital 2s no es constante como suceda en el tomo de hidrgeno. Dicha energa depende de la poblacin del resto de los orbitales (configuracin electrnica), y por tanto de la energa de repulsin. Los orbitales de Slater (OTS o STO en Ingles), se utilizan con frecuencia en sustitucin de los orbitales atmicos (OA) del hidrgeno, para construir orbitales moleculares mediante combinaciones lineales (CLOST, en vez de CLOA). La razn es que es ms fcil resolver las integrales que aparecen con los OTS. Tambin es frecuente utilizar orbitales atmicos gaussianos (OTG o GTO en Ingles).
181
Leccin 8 Qumica Fsica (Curso 2010-11)
PRINCIPIO DE CONSTRUCCIN Y CONFIGURACIN ELECTRNICA
El principio de construccin (Aufbau), fue enunciado por Niels Bohr, y permite determinar la configuracin electrnica del tomo en su estado fundamental. Este principio nos dice que: Para
construir la configuracin electrnica de un tomo se llenan sus orbitales en orden creciente de n+ , y cuando n+ coincide, se llena primero el orbital de menor n. Sin embargo, este principio falla al
menos para diez tomos, y existen unos 20 tomos para los que no se tiene una certeza clara de su configuracin electrnica. Este principio ha sido completado con la regla de Hund, que nos dice que un tomo toma la configuracin con el mayor nmero de electrones desapareados.
Un caso tpico en el que no se cumple el anterior principio es el del tomo de Cr(Z=24), cuya configuracin electrnica es [Ar]4s13d5. Los tomos anteriores y posteriores en la tabla peridica tienen una configuracin; V(Z=23): [Ar]4s23d3, y Mn(Z=25): [Ar]4s23d5. Segn el principio de construccin, un orbital 4s (n+ = 4), debe llenarse antes que un orbital 3d (n+ = 5). La razn por la que se llena antes el orbital 4s que el 3d, se debe a que la energa de
repulsin entre los electrones situados en orbitales 3d, que estn ms localizados en el espacio, es mayor que la energa de repulsin entre electrones situados en orbitales 4s, que estn menos localizados.
Clculos tericos, mediante el mtodo de Hartree, analizado en la leccin anterior, confirman que para el tomo de Cr la configuracin electrnica [Ar]4s13d5, con 6 electrones desapareados, es de menor energa que la configuracin [Ar]4s23d4, con 4 electrones desapareados. Este fenmeno es interpretado mediante las denominadas interacciones spinorbital, que se analizarn ms adelante, aunque no puede predecirse de forma general, por lo que deben efectuarse clculos para resolver la ecuacin de Schrdinger. La regla de Hund lo predice en muchas ocasiones, aunque no en todas. Hay que recalcar, que la configuracin electrnica del Cr [Ar]4s13d5, con solo 4 electrones desapareados, por ejemplo:
2 1 1 0 4s1 3d z 3d1 2 3d 2 xy 3d xz 3d yz , es de mayor energa que la configuracin [Ar]4s 3d , con 4 x y2
electrones desapareados.
La configuracin electrnica de un tomo es una representacin basada en la aproximacin de electrones independientes, donde a cada electrn se le asignan 4 nmeros cunticos, procedentes de las soluciones del tomo de hidrgeno. Una configuracin electrnica no es equivalente a un nivel de energa, como ocurra en el tomo de hidrgeno. En tomos polielectrnicos la situacin energtica es mucho ms compleja, ya que la configuracin electrnica no tiene en cuenta, ni la repulsin entre electrones, ni las interacciones entre los momentos angulares orbital y de spin (interacciones spinorbital).
182
Leccin 8 Qumica Fsica (Curso 2010-11)
� � El momento angular orbital total de un tomo polielectrnico L , se define como la suma � � �� vectorial de los momentos angulares orbitales individuales de cada electrn L = i � i . A partir de
esta definicin es posible construir los operadores L2 y Lz. Puede demostrarse que estos operadores conmutan con el Hamiltoniano del tomo polielectrnico, [H,L2] = 0 y [H,Lz] = 0, lo que nos indica que las observables correspondientes a estos operadores, se conservan, o sea, estn cuantizadas.
MOMENTO ANGULAR EN TOMOS POLIELECTRNICOS
Figura 8.4
Las propiedades de L2 y Lz, son idnticas a las estudiadas para electrones individuales, es decir L2 = L(L+1)2, y Lz = ML, siendo L un nmero entero mayor o igual que cero (0, 1, 2..), el cual se representa por una letra mayscula (S, P, D ...). Adems ML, toma valores desde L hasta L, de unidad en unidad. Sin embargo, los operadores i2 y z, individuales de cada electrn (se utiliza letras pequeas para no confundirlos con los totales), no conmutan con el operador H, debido a la existencia de los trminos 1/rij de repulsin entre electrones, y por lo tanto, las observables correspondientes no se conservan, o lo que es lo mismo, no estn cuantizadas. Asignar nmeros cunticos individuales a cada electrn, es decir, asignar una configuracin electrnica al tomo, es una aproximacin matemtica (aproximacin de electrones independientes), de la que partimos para obtener soluciones ms prximas a las reales. La energa real del tomo no depende de dichos nmeros cunticos individuales, sino de los nmeros cunticos totales L y ML, y como veremos, tambin S y MS. Los nmeros cunticos individuales de cada electrn y por tanto las configuraciones electrnicas, nos sirven para hacernos una idea mental aproximada de la situacin de los electrones en el tomo, y adems, nos permiten determinar de una forma relativamente sencilla los nmeros cunticos L y S totales. Vamos a analizar cmo se construyen los nmeros cunticos totales del tomo: Supongamos un tomo en el que existen dos electrones, uno con 1 =3, y otro con 2 = 1. En cada caso, m =0, 1, .. . Los valores de no pueden ser sumados, ya que estn relacionados con el mdulo de vectores,
183
Leccin 8 Qumica Fsica (Curso 2010-11)
sin embargo, los valores de mi si pueden ser sumados tal cual, ya que corresponden a la proyeccin de dichos vectores sobre un eje comn, el eje z. Definiremos ML = m1 + m2, por lo que existirn tantos valores de ML como combinaciones posibles de m1 y m2. Todos los valores posibles de ML se muestran en Tabla 8.2.
Tabla 8.2
Los valores de ML posibles pueden combinarse en tres series que varan entre 4, 3, y 2, de unidad en unidad. Estas tres series nos indican que existen tres valores posibles de L, que son, 4, 3, y 2. Es decir, L toma valores comprendidos entre (1 + 2) y |1 - 2|, de unidad en unidad. En general, �� � �� � puede demostrarse que siempre que sumemos dos vectores � 1 y � 2 , cuyos mdulos estn � � cuantizados por las cantidades [1(1+1)]1/2 y [2(2+1)]1/2, el vector resultante L , tiene tambin su mdulo cuantizado por la cantidad [L(L+1)]1/2, donde L es un nmero entero, que puede tomar todos los valores comprendidos entre (1 + 2) y |1 - 2|, de unidad en unidad. �� �� � � � La misma regla se cumple si sumamos dos vectores s1 y s 2 , � y s . As, si tenemos dos electrones con s1 = 1/2 y s2 = 1/2, S toma valores comprendidos entre s1 + s2 y |s1 - s2|, de unidad en unidad, es decir, S = 0 y 1. Si en el tomo existe otro electrn, los nmeros cunticos 3 y s3, del tercer electrn, se adicionan siguiendo las mismas reglas, al resultado de adicionar los dos anteriores. Veamos un ejemplo con el spin. As, el resultado de adicionar el spin de dos electrones es; S1,2 = 1 y 0. Este resultado se adiciona a s3 = 1/2, de forma que S toma valores comprendidos desde S12 + s3 hasta |S12 s3|. Como existen dos valores de S12, tendremos dos opciones: S = 3/2 y 1/2 (1+1/2....1-1/2), y S= 1/2 (1/2+0). En la prctica solo hay dos valores , S = 3/2 y 1/2(repetido). Como vimos para el tomo de hidrgeno, los momentos angulares de spin y orbital llevan asociados momento magnticos que interaccionan entre s. Estas interacciones afectan notablemente a la estructura energtica del tomo.
184
Leccin 8 Qumica Fsica (Curso 2010-11)
INTERACCIONES SPIN-ORBITAL
Las interacciones entre los momentos magnticos, orbital (L) y de spin (S) son muy complejas, y dependen del tamao del tomo. As para tomos ligeros (aproximadamente la mitad de la tabla peridica), dominan las interacciones denominadas de spin-orbital o de Russell-Saunders, que son las nicas que veremos aqu. Sin embargo, para tomos pesados, dominan otros tipos de interacciones denominadas acoplamientos j-j. Los datos experimentales indican que la energa de los electrones en tomos polielectrnicos ligeros, depende del momento angular total del tomo � � � � J = L+S (8.32) El mdulo de J, esta cuantizado mediante la relacin ya conocida � J = � J ( J + 1)
(8.33)
donde J es un nmero cuntico entero, o semientero, que toma valores positivos o cero, comprendidos entre L + S, y |L S|, de unidad en unidad. La proyeccin del vector J sobre un eje, esta cuantizada mediante otro nmero cuntico, MJ, tal que MJ = ML + MS, de forma que MJ toma valores comprendidos entre J y J, de unidad en unidad. Si LS, el nmero de valores de J (L+S, L+S-1....LS), es 2S+1. A esta magnitud se le denomina multiplicidad, y representa el nmero de valores de J, para unos valores dados de L y S. Cuando S > L, el valor 2S+1, no representa el nmero de valores de J. La energa de cada estado depende de los tres nmeros cunticos L, S y J, as como del nmero cuntico principal n, y por esta razn se construyen los denominados trminos espectroscpicos. n 2S+1 L J 0 1 2 3 4 5 6 � L= S P D F G H I � (8.34)
Como ejemplo, supongamos una configuracin electrnica np1 np1, donde n n, por lo que los electrones poseen ya un nmero cuntico diferente. A estos electrones, se les denominan no equivalentes. Para nuestros dos electrones, 1 = 1, 2 = 1, s1 =1/2 y s2 = 1/2. Por lo tanto, L = (1 + 2) ... |1 - 2| = 2, 1, 0, y S = 1,0. Luego, existirn trminos correspondientes a todas las posibles combinaciones de estos nmeros cunticos: D, D, P, P, S y S. Los valores de J estn comprendidos entre L+S .. |L-S|, luego D3,2,1, D2, P2,1,0, P1, S1 y S0. De una forma cualitativa, la energa de los trminos espectroscpicos, para una configuracin electrnica dada, puede clasificarse segn las denominadas reglas de Hund. Estas son: 1. La energa del estado es menor cuanto mayor sea S. 2. A igualdad de S, la energa es menor cuanto mayor sea L. 3. Si la configuracin electrnica es menor de semi-llena, la energa ser mnima cuanto menor sea J. Si es igual o mayor que semi-llena, la energa ser mnima cuanto mayor sea J.
3 1 3 1 3 1 3 1 3 1 3 1
185
Leccin 8 Qumica Fsica (Curso 2010-11)
En la Figura 8.5, se muestra el diagrama cualitativo de energa de los 10 trminos espectroscpicos, o 10 niveles de energa que aparecen para la anterior configuracin.
Figura 8.5
Cada uno de los 10 niveles de configuracin esta degenerado en MJ, existiendo 2J+1 valores para cada trmino. El nmero de valores de MJ, se muestra asimismo en la columna de la derecha de la Figura 8.5. Es decir, existen 10 niveles de energa y 36 estados. A cada una de las combinaciones posibles de los nmeros cunticos individuales de los electrones, se le denomina microestado. Para una configuracin p1, existen 6 microestados, es decir, 6 formas diferentes de asignar nmeros cunticos al electrn (3 valore de m y dos de ms). Como nuestra configuracin es np1np1, (electrones no equivalentes), y por lo tanto los electrones ya tienen un nmero cuntico diferente, el nmero de microestados ser 66 = 36. El nmero de microestados ha de coincidir con el nmero de estados totales obtenidos a partir de los trminos espectroscpicos. En realidad, utilizar los nmeros cunticos individuales, , m, s, y ms, es equivalente a utilizar los nmeros L, S, J y MJ, solo modificamos la forma de combinarlos, aunque conviene expresar los estados en funcin de los nmeros cunticos totales ya que la energa depende de ellos. En la Tabla 8.3, se muestran los trminos correspondientes a otras configuraciones de electrones no equivalentes.
Tabla 8.3
Supongamos ahora, que la configuracin es np2. A estos electrones se les denomina equivalentes, ya que poseen dos nmeros cunticos iguales (n y ). Bajo estas condiciones, es necesario tener en cuenta el principio de exclusin de Pauli. El nmero de microestados para
186
Leccin 8 Qumica Fsica (Curso 2010-11)
electrones equivalentes puede determinarse mediante la relacin: Microestados = m! 6! = = 15 ( m n )!n! 4!2! (8.35)
donde m es el nmero de electrones que caben en el orbital (6 en nuestro caso) y n, el nmero de electrones que existen (2 en nuestro caso). Luego una configuracin p2, da lugar a 15 microestados. Los 15 microestados, o formas de asignar nmeros cunticos, de la configuracin p2 se muestran en la Tabla 8.4. Con estos microestados puede determinarse todos los posibles valores de ML y MS, sumando directamente los valores m y ms individuales de los electrones (ver columnas 4 y 5 de la tabla). Una vez que se tienen los valores de ML y MS, se agrupan en diferentes series que nos permitan calcular L y S, dado que dichos nmeros cunticos varan entre +L y -L (ML), y entre +S y S (MS), de unidad en unidad.
mR=1 0 -1 ML =3 mR 2 MS =3 ms 0 0 0 1 1 -1 -1 0 0 0 0 1 0 -1 0
1 0 1 0 1 0 1 0 0 -1 -1 -1 -1 -2
Tabla 8.4
As, existe una serie de 5 microestados (sombreado oscuro en la tabla anterior), para los que MS = 0 y ML = 0, 1, 2, por lo que para este conjunto de microestados S = 0 y L = 2. Por lo tanto J = 2. Luego a estos 5 microestados le corresponde el trmino 1D2. Existen adems, un conjunto de 9 microestados, que han sido sealados por un sombreado claro. Estos 9 microestados pueden clasificarse en tres grupos a su vez. En uno de ellos, ML = 0, 1, y MS =1 (triple raya entre las columnas 4 y 5 de la tabla). En otro ML = 0, 1, y MS = 0 (doble raya en la
187
Leccin 8 Qumica Fsica (Curso 2010-11)
tabla), y en el ltimo ML =0, 1, y MS = -1 (raya simple en la tabla). Es decir, en este conjunto de 9 microestados, ML = 0, 1, y MS = 0, 1, luego, L = 1 y S = 1, por lo que J = 2,1,0, y por lo tanto, existen tres trminos espectroscpicos 3P2,1,0. Por ltimo, queda un microestado para el que MS = 0 y ML = 0, luego S = 0 y L = 0, de forma que J = 0, a lo que le corresponde el trmino 1S0. Aplicando las reglas de Hund, podemos ordenar los trminos por orden creciente de energa, de una forma cualitativa, tal como se muestra en la Figura 8.6.
Figura 8.6
Cuando se compara este diagrama de energa con el descrito anteriormente para electrones no equivalentes (Figura 8.5), se observa que aparecen menos trminos, lo que se debe al principio de exclusin de Pauli. La configuracin electrnica p2 conduce por lo tanto a 5 niveles de energa, siendo el trmino fundamental, el P0. En la Tabla 8.5, se muestran los trminos espectroscpicos correspondientes a otras configuraciones de electrones equivalentes.
3
Tabla 8.5
El mtodo descrito para calcular los trminos espectroscpicos es enormemente engorroso y en la prctica no se utiliza, pinsese que para una configuracin f3, existen 364 microestados. En el apndice 8.1, se describe un procedimiento emprico para construir los trminos espectroscpicos de cualquier configuracin electrnica. Existen dos casos particulares que merecen ser mencionados:
188
Leccin 8 Qumica Fsica (Curso 2010-11)
En primer lugar, una capa completa no contribuye a los momentos angulares orbital y de spin, ya que para ella L = 0 y S = 0. Por esta razn, los electrones internos, correspondientes a capas llenas, no participan en el trmino espectroscpico. As, por ejemplo, para construir los trminos espectoscpicos de un tomo con una configuracin electrnica 1s22s2p63s1, solo es necesario considerar sus capas semillenas, es decir, 3s1, donde, S = 1/2, L = 0, y J = 1/2, siendo su trmino espectroscpico, por tanto: S1/2. En segundo lugar, si bien es complejo calcular todos los trminos espectroscpicos de una configuracin electrnica dada, es sencillo, sin embargo, calcular el trmino espectroscpico fundamental para cualquier configuracin electrnica. Nos basta con aplicar las reglas de Hund, y buscar los microestados que la cumplan; en primer lugar con (MS)maximo = S, y a continuacin con (ML)mximo = L. Veamos por ejemplo cmo aplicar esto para una configuracin p3. La primera regla de Hund nos dice, que el estado es de menor energa cuanto mayor es S. Como MS vara entre S de unidad en unidad, debemos buscar, para dicha configuracin el valor mximo posible MS. El valor mximo de Ms lo tendramos cuando los tres electrones se colocan desapareados en el orbital. Esto se ilustras en la Figura 8.7-a, donde se representa un microestado con MS = 3/2. La forma de representar los microestados, es dibujar tantas casillas como valores de m existen, en nuestro caso, 1, 0 y -1, y dentro de cada casilla, dibujar una flecha hacia arriba, por cada electrn con ms = +1/2, o una flecha hacia abajo, por cada electrn con ms = -1/2. Pero con MS = 3/2, solo existe un microestado, el dibujado en la Figura, para el cual ML =0, luego S=3/2 y L=0, por lo tanto J=3/2. Luego el trmino fundamental es 4S3/2. a)
2
-1
b)
-1
-2
Figura 8.7
Para una configuracin d , el valor mximo posible de MS = 2 (ver Figura 8.7-b). Para este valor de MS el valor mximo de ML permitido es ML=2, luego S=2 y L=2, como la capa esta menos de semillena, J= 0, luego el trmino fundamental es 5D0.
189
Leccin 8 Qumica Fsica (Curso 2010-11)
ESTRUCTURA ENERGTICA Y ESPECTROS DE TOMOS POLIELECTRNICOS
Los espectros de tomos polielectrnicos solo pueden ser interpretados si se conoce cul es la estructura energtica del tomo, es decir, cules son sus niveles de energa. Para determinar los niveles de energa de un tomo, aunque sea solo de forma cualitativa, necesitamos determinar los trminos espectroscpicos para todas sus posibles configuraciones electrnicas. Como ejemplo analicemos el tomo de He, el cual en su estado fundamental posee una configuracin 1s2, luego le corresponde un trmino espectroscpico 11S0. La energa de los diferentes trminos del tomo se ilustra en la Figura 8.8.
Figura 8.8
La primera configuracin electrnica excitada del He es 1s1, 2s1, o en general, 1s1ns1, con n > 1. Para todos estos casos 1 =0 y 2 =0, luego L=0. Al existir dos electrones no equivalentes, S puede tomar dos valore S = 0, 1, luego J = 0, 1, por lo que tenemos trminos espectroscpicos n1S0 y n3S1. Al helio con spin cero se le denomina para-helio, mientras que al que tiene spin 1, orto-helio. La siguiente configuracin electrnica excitada del He es 1s12p1, o tambin en general, 1s1 np1, donde n > 1. Para todos estos casos 1 =0 y 2 =1, luego L=1. Al existir dos electrones no equivalentes S puede tomar dos valore S = 0,1, luego para S= 0, J =1, por lo que el trmino espectroscpico es n1P1. Para S = 1, J = 2, 1, 0, luego existen tres trminos , n3P2,1,0. De la misma forma, para una configuracin electrnica 1s1nd1, los trminos espectroscpicos sera n1D2 y n3D3,2,1. Para una configuracin 1s1nf1, los trminos espectroscpicos seran n1F3 y n3F4,3,2, etc. La energa de estos estados se muestra en la Figura 8.8. Asimismo, en la Figura 8.2, si
190
Leccin 8 Qumica Fsica (Curso 2010-11)
indica la energa de los primeros estados energticos del tomo, relacionndose la nomenclatura utilizada al comienzo de la leccin, con la basada en los trminos espectroscpicos. Cuando al tomo de He se le comunica una energa de 24.5 e.v. = 198305 cm-1, tiene lugar el primer potencial de ionizacin del tomo. No todos los saltos posibles estn permitidos mediante absorcin y emisin de radiacin. Las reglas de seleccin para tomos polielectrnicos son las siguientes: *Para el electrn que salta de una configuracin electrnica a otra = 1. * Para el conjunto de los nmeros cunticos, S = 0, L = 0, 1, y J = 0, 1, salvo el salto de J = 0, a J = 0, que est prohibido. Segn estas reglas, en el espectro de absorcin solo aparecen los trnsitos desde 11S0 n1P1. Sin embargo, los espectros de emisin son mucho ms complejos, ya que el retorno del electrn al estado fundamental no tiene por qu ser en un solo paso, sino en cascada. En la Figura 8.8, se muestran algunos de los posibles saltos espectroscpicos del espectro de emisin. Veamos un ejemplo ms complejo, como es el del tomo de carbono. En la Figura 8.9, se ilustra el diagrama de energa de algunos de sus estados.
Figura 8.9
La configuracin electrnica del estado fundamental del carbono es 2s2p2, luego, para una configuracin p2, los trminos son 3P, 1D y 1S. Nosotros podemos predecir cualitativamente el orden pero no la energa exacta sin efectuar clculos. El carbono en su estado fundamental se sita en un trmino 3P (2 electrones desapareados). Una primera configuracin electrnica excitada es, 2s2p13s1, es decir p1s1, para la que tenemos
191
Leccin 8 Qumica Fsica (Curso 2010-11)
trminos, 1P y 3P. La siguiente configuracin electrnica excitada es 2s2p13p1, es decir p1p1 (no equivalentes), para la que tenemos trminos S, P y D con multiplicidad 1 y 3. Sin embargo, experimentalmente, tambin es posible la configuracin 2s1p3. Esta es una configuracin electrnica denominada mixta, con electrones equivalentes, los p3 y no equivalentes, s1. Los trminos de esta configuracin no aparecen en la tabla 8.3, sin embargo, son fciles de calcular. Los trminos de la configuracin p3 si aparecen en dicha tabla, siendo 4S (S=3/2, L=0), 2D (S = 1/2, L=2) y 2P (S= y L=1). Estos son los nmeros cunticos correspondientes a los 3 electrones p equivalentes. El del cuarto electrn (2s1) se adiciona a los anteriores sin ninguna restriccin, ya que es no equivalente, como para este electrn 4 = 0, el L total coincide con el de los electrones p3 y el s4 = 1/2, por lo que habra que adicionarlo a los anteriores, siguiendo las reglas habituales. As, para L = 0, S = {2,1}, para L = 2, S = {1,0} y para L=1, S = {1,0}, lo que conduce a trminos 5S, 3S, 3D, 1D, 3P y
1
P.
Como puede observarse de la Figura 8.9, las reglas empricas de Hund no son infalibles, y, por ejemplo, para la configuracin 2s1p3 el trmino 1D, es de menor energa que el
3
S, o para la 2s2p13p1, el orden de los trminos es 1P, 3D, 3S, 3P, 1D y 1S. A medida que el peso atmico
del tomo aumenta, y sobre todo para configuraciones excitadas, la reglas de Hund son cada vez menos fiables. Adems, el orden relativo de los trminos de una configuracin con respecto a otra es imposible de predecir sin efectuar clculos numricos. Con el fin de interpretar los espectros de tomos polielectronicos se recurre a dos mtodos experimentales. Uno de ellos consiste en la realizacin de espectros en presencia de campos magnticos. En este caso, la energa se hace funcin de MJ, de forma semejante a como ocurra con el tomo de hidrgeno, observndose el desdoblamiento de ciertas lneas espectrales (efecto Zeeman). La energa de interaccin entre un campo magntico externo, B, y el momento magntico total del tomo viene dada por
� � E int eraccion = g B M J B (8.36)
donde B, es el magnetn de Bohr, y g es una relacin entre los nmeros cunticos L, S y J, dada por: 3J(J + 1) + S(S + 1) L(L + 1) g= (8.37) 2J(J + 1) La deduccin terica de esta expresin, se realiza en el Apndice 8.2. Otro mtodo al que se recurre para interpretar espectros, es la realizacin de estos en presencia de campos elctricos. En presencia de un campo elctrico, la energa de los estados se hace funcin de |MJ| (efecto Stark).
192
Leccin 8 Qumica Fsica (Curso 2010-11)
APNDICE 8.1: CONSTRUCCIN DE TRMINOS ESPECTROSCPICOS.
Existe un mtodo emprico sencillo para determinar los trminos espectroscpicos de una configuracin de electrones equivalentes dada. Supongamos la configuracin np2, y construyamos mediante tablas todos los valores posibles de ML y MS. Estos se muestran en la Figura 8.10.
ms1 ms2 1/2 1/2 1/2 m1 1 0 -1 m2 1 0 1 2 1 0
-1/2 0 -1 0 1 0 -1
Figura 8.10
MS
ML
-1 0 -1 -2
Existen 4 valores de MS, y 9 de ML, de forma que 49 = 36 microestados, como ya sabamos. Pero de estos 36 microestados, solo son posibles 15, a consecuencia del principio de exclusin de Pauli. Supongamos que el spin total es S = 1 (MS = 1, 0, -1)(). Cuando esto ocurre, los dos electrones poseen 3 nmeros cunticos iguales, n, y ms, por lo que los electrones deben tener el nmero cuntico, m diferente, por lo que en la tabla de valores de ML, debemos eliminar los trminos de la diagonal, que se construyen con idnticos valores de m para los dos electrones. Esto se ilustra en la Figura 8.11, donde se muestra la tabla de valores de ML, para S = 1, en la que los valores de la diagonal han sido tachados.
S= 1 m1 1 0 -1 m2 1 2 1 0 0 1 0 -1 -1 0 -1 -2
S =0 m1 1 0 -1 m2 1 2 1 0 0 1 0 -1 -1 0 -1 -2
Figura 8.11
Tras eliminar estos valores, nos queda que ML toma valores de 1 0 y -1, por lo que L=1, y como S=1, tendremos trminos; 3P2, 3P1, 3P0. Solo se toma un lado de la diagonal, ya que de lo contrario se discrimina entre electrones. Estos 3 trminos corresponden a 9 microestados, 3 valores de
193
Leccin 8 Qumica Fsica (Curso 2010-11)
ML 3 de MS. Si ahora suponemos S = 0 (cuadro de la derecha en la Figura 8.11), en este caso, los electrones ya tienen un nmero cuntico diferente (ms), por lo que no existe ninguna restriccin en cuanto a los valores de ML. Si bien, se eliminan de la tabla los valores ya utilizados (regla emprica), es decir, 1, 0 y -1 (valores tachados). Por lo tanto ML = {2, 1, 0, -1, -2} y {0}, por lo que L = 2 y 0, por lo que tenemos trminos 1D2 y 1S0. Estos trminos corresponden a 6 microestados, que con los 9 de antes son 15. Veamos otro ejemplo, supongamos una configuracin nd1nd1 (electrones no equivalentes nn). Como 1 = 2 y 2 = 2, L = 4, 3, 2, 1, 0, y S = 1, 0. En este caso, todas las combinaciones son posibles, por lo que existiran trminos 1S, 1P, 1D, 1F, 1G, 3S, 3P, 3D, 3F, 3G, con los correspondientes valores de J que no haremos. Supongamos ahora que los electrones son equivalentes, (n = n) (nd2). Como en el caso anterior el spin total es 1 o 0. Se construye la tabla de valores de ML (ver Figura 8.12). Si S = 1, hay que eliminar los valores de la diagonal (ya que en caso contrario los electrones tendran su 4 nmeros cunticos iguales), por lo que, los valores de ML que nos quedan (en blanco en la Figura), seran; ML = {3,2,1,0,-1,-2,-3} y {1,0,-1}, luego L = 3 y 1. Lo que implica trminos 3F y 3P. Por otra parte cuando S = 0, los electrones ya tienen un nmero cuntico diferente (ms), por lo que no existen restricciones, en este caso L = {4,3,2,1,0}, pero hay que eliminar los valores utilizados con S = 1, por lo que L = 4,2,0, o sea, 1S, 1D y 1G.
S =1 m1 m2 2 1 0 -1 -2 2 4 3 2 1 0 1 3 2 1 0 -1 0 2 1 0 -1 -2 -1 1 0 -1 -2 -3 -2 0 -1 -2 -3 -4
Figura 8.12
Estas reglas se pueden utilizar con ms electrones, adicionando primero dos electrones, al resultado el tercero, y as sucesivamente.
194
Leccin 8 Qumica Fsica (Curso 2010-11)
APNDICE 8.2: EFECTO ZEEMAN
Con el fin de interpretar los espectros de tomos polielectronicos, se recurre a diferentes mtodos experimentales. Uno de ellos es la realizacin de espectros en presencia de campos magnticos (efecto Zeeman). En estos casos, la energa de los estados se hace funcin de MJ, de forma semejante a como ocurra con el tomo de hidrgeno, observndose el desdoblamiento de ciertas lineas espectrales. En la Figura 8.13, se muestra un equema donde se representan algunos de los vectores definidos a continuacin.
Figura 8.13
Los momentos magnticos orbital y de spin tienen la forma
��� � � L = B L �
�� � � S = 2 B S �
(8.38)
donde B = e/2mc, es el magneton de Bohr. El momento magntico total ser:
��� � � � T = B L + 2S �
(8.39)
El vector J (momento angular total), se defini como
� � � � J = L+S
(8.40)
Por lo que los vectores J y T no estn en la misma direccin, como se observa en la Figura 8.13. Supongamos que aplicamos un campo magntico B. La energa de interaccin entre dicho campo y el momento magntico total del tomo ser:
��� � � � � � � � E = T B = B B L + 2S �
(8.41)
Esta interaccin interesa expresarla en funcin de J y MJ, y no de T directamente. Por ello, se introduce el siguiente cambio:
195
Leccin 8 Qumica Fsica (Curso 2010-11)
�2 � � � � � � � � J + J S � J J + J S � � � � � � � � JJ L + 2S = J + S = J + S � � = J= J �2 �2 JJ J J
(8.42)
Adems, si se tiene en cuenta que � � � � � � LL = J S
� � � � � � = J J + S S 2J S
(8.43)
Por lo que
�2 �2 � �2 � � J +S L J S = 2
Luego
(8.44)
�2 �2 �2 � �2 �2 1 �2 1 �2 1 � J + J + S L � 3J + S L � � � � � 2 2 2 J= L + 2S = J gJ = �2 �2 J 2J
(8.45)
Donde, teniendo en cuenta la relacin entre los mdulos al cuadrado de cada vector, y los nmeros cunticos correspondientes J, L y S, es posible expresar el factor numrico que multiplica al vector J, como:
�2 �2 � �2 3J + S L 3� 2 J(J + 1) + � 2S(S + 1) � 2 L(L + 1) g= = = �2 2� 2 J(J + 1) 2J = 3J(J + 1) + S(S + 1) L(L + 1) 2J(J + 1)
(8.46)
Al factor g, se le denomina factor g de land, y su valor depende nicamente de los tres nmeros cunticos L, S y J. Por lo tanto, la energa de interaccin entre el campo magntico externo y el momento magntico del tomo ser:
E=
� � � � � � � � B � � � B L + 2S = g B B J = g B B J cos() = � � � � � � �M� � � B � B � =g B J cos( ) = g B J �J = g B M J B � � J
(8.47)
Es decir, la accin del campo magntico rompe la degeneracin en MJ, apareciendo tantos niveles de energa como valores de MJ existen. Por lo tanto, cuando se realiza un espectro en presencia de un campo magntico, se observa el desdoblamiento de las lneas espectrales, lo cual se conoce como efecto Zeeman. En la Figura 8.14, se muestra un ejemplo correspondiente a la transicin entre los estados 2S1/2 2P1/2. Esta transicin, que aparece como una banda en el espectro, se desdobla en 4 bandas en presencia de un campo magntico externo. Una representacin esquemtica de dicho desdoblamiento, se muestra tambin en la Figura 8.14.
196
Leccin 8 Qumica Fsica (Curso 2010-11)
Figura 8.14
197
Leccin 8 Qumica Fsica (Curso 2010-11)
CUESTIONES
1) Justificar por qu en sistemas polielectrnicos, las funciones de onda deben ser antisimtricas. 2) En base al principio de antisimetra, explicar porqu es imposible que un tomo posea una configuracin electrnica ns3. 3) Definir, lo ms brevemente posible, que se entiende por configuracin electrnica de un tomo, e indicar porqu, en general, estas no coinciden con los niveles de energa de los tomos. 4) Bajo la aproximacin de electrones independientes, la funcin de onda espacial de cierto estado del tomo de He puede escribirse como; = N[1s(1)2s(2) + 1s(2)2s(1)]. Normalizar la funcin, sabiendo que los orbitales 1s y 2s estn normalizados, y que d = d1d2. Escribir la funcin spin-orbital completa, e indicar el trmino espectroscpico de dicho estado. 5) Segn la aproximacin de electrones independientes las configuraciones 1s12s1 y 1s12p1 son degeneradas. )Cuantos niveles de energa corresponden a dichas configuraciones y como se denominan?. )A que fenmenos fsicos debe achacarse el hecho de que las configuraciones electrnicas 1s12s1 y 1s12p1 no correspondan a un solo nivel de energa? 6) En la aproximacin de electrones independientes, la parte espacial de los estados electrnicos del tomo de He tienen la forma: = N[(1)(2) (2)(1)]. Para dos casos genricos en los que = y , construye todos los spin-orbitales que pueden existir, e indica cual es el spin en cada caso. 7) Explica lo ms brevemente posible porqu deben utilizarse los determinantes de Slater para construir las funciones de onda de los tomos poli-electrnicos. 8) Indicar si las siguientes funciones de onda correspondientes a diferentes configuraciones del tomo de He, son correctas o no. En caso de que no lo sean indicar porqu, y en caso de que lo sean indicar el spin correspondiente. I) = N 1s (1) 1s ( 2 ) 1s ( 2 ) 1s (1) + (1) + ( 2 ) II) = N 1s (1) 2s ( 2 ) 1s ( 2 ) 2s (1) + (1) ( 2 ) + + ( 2 ) (1) III) = N1s (1) 2s ( 2 ) + (1) ( 2 ) + ( 2 ) (1)
IV) = N 1s (1) 2s ( 2 ) + 1s ( 2 ) 2s (1) + (1) ( 2 ) + ( 2 ) (1) V) = N1s (1) 1s ( 2 ) + (1) ( 2 ) + + ( 2 ) (1)
PROBLEMAS
1) a) Construir la funcin de onda antisimtrica de orden cero del boro, cuya configuracin electrnica es, 1s22s2p1. Indicar si la energa que se obtiene al aplicar la teora de variaciones a la funcin anterior, es mayor, menor o igual, que la energa experimental del tomo. b) En unidades atmicas la energa del electrn en un tomo hidrogenoideo es En = -Z2 /2n2, donde Z es la carga nuclear. Determinar la energa de los electrones del tomo de boro, segn la aproximacin de electrones independientes, e indicar si la energa obtenida es mayor, menor o igual, que la energa experimental del tomo. Utilizar como energa experimental del tomo, la que se obtiene segn el mtodo aproximado de Slater. 2) Sea un sistema cuntico, en el cual existen infinitos estados no degenerados con energa En =n2h2/8ma2, donde n = 1, 2, 3, ... . Supngase adems, que en el sistema existen tres partculas idnticas no interaccionantes. Determinar la energa mnima del sistema cuando las partculas son Fermiones y cuando son Bosones. 3) Deducir el trmino espectroscpico fundamental de las siguientes configuraciones electrnicas. d3 f3, f9, s1d2, p2d2, p5, 4) Determinar la configuracin electrnica que corresponde a los trminos atmicos fundamentales: 3F2, 4S3/2, 6 S5/2, 7F0.
198
Leccin 8 Qumica Fsica (Curso 2010-11)
5) Explicar porqu son errneos los siguientes smbolos de los niveles de un tomo. asimismo, qu valores de J, pueden tomar los siguientes trminos 1S, 2P, 3P, 3D y 4D.
S1, 2D7/2 y 0P1. Indicar,
6) Todos los trminos espectroscpicos de cierta configuracin electrnica son: 2P1/2, 2P3/2, 2D3/2, 2D5/2, 4S3/2. a) Determinar de qu configuracin se trata, y cul es el trmino fundamental. b) Ordenar los trminos por orden creciente de energa e indicar que transiciones estn permitidas desde el trmino fundamental a los restantes. 7) En la Figura 8.15, se muestran algunas de las transiciones electrnicas observadas para el tomo de oxgeno.
3
8 6 4 2
3 1
S D
Figura 8.15
a) Indicar que trminos, de los representados, pertenecen a la configuracin electrnica fundamental de dicho tomo. b) La primera configuracin electrnica excitada del tomo de O es 1s22s2p33s1. Determinar el trmino espectroscpico fundamental de esta configuracin e indicar si el trmino 3S, pertenece o no a dicha configuracin. c) Indicar las transiciones permitidas, mediante absorcin de radiacin, entre los estados representados en la figura. d) Las emisiones de radiacin desde 1D 3P ( = 630 nm, rojo), y 1S 1D ( = 557.7 nm, verde), son observadas en la luz que forman las Auroras Boreal y Austral. )Contradice esta observacin las conclusiones del apartado anterior?. Razonar en cualquier caso la respuesta.
8) Indica el nmero de microestados, los trminos espectroscpicos, y el trmino fundamental, correspondientes a una configuracin p1d1. 9) Normalizar la siguiente funciones y demostrar que son ortogonales entre si. s = N 1s (1) 2s ( 2 ) + 1s ( 2 ) 2s (1)
a = N 1s (1) 2s ( 2 ) 1s ( 2 ) 2s (1)
199
You might also like
- Mecánica Cuántica y Configuración ElectrónicaDocument60 pagesMecánica Cuántica y Configuración ElectrónicaWILBERT.AYMA.CC.No ratings yet
- Átomos Con Muchos Electrones para PrecentarDocument16 pagesÁtomos Con Muchos Electrones para PrecentarEdwin José Castro SánchezNo ratings yet
- Principio de Exclusión de Pauli M. CuanticaDocument9 pagesPrincipio de Exclusión de Pauli M. Cuanticanick1340ableNo ratings yet
- Números Cuánticos y Configuración ElectrónicaDocument8 pagesNúmeros Cuánticos y Configuración ElectrónicaPamelaNo ratings yet
- Clases de Química InorgánicaDocument42 pagesClases de Química InorgánicaRobert Cazar100% (3)
- Números cuánticos y sus aplicacionesDocument11 pagesNúmeros cuánticos y sus aplicacionesJaimeNo ratings yet
- Números Cuanticos y Configuración Electrónica PDVDocument15 pagesNúmeros Cuanticos y Configuración Electrónica PDVPaula Astudillo VegaNo ratings yet
- Guia de Numeros Cuanticos y ConfiguracionDocument11 pagesGuia de Numeros Cuanticos y ConfiguracionPATRICIA3812No ratings yet
- Determinantes de Slater 2Document2 pagesDeterminantes de Slater 2Jorge Mario RodriguezNo ratings yet
- Quimica Numeros CuanticosDocument5 pagesQuimica Numeros CuanticosLex LunaNo ratings yet
- Numeros Cuanticos y Configuracion ElectronicaDocument26 pagesNumeros Cuanticos y Configuracion ElectronicaArelis GonzalezNo ratings yet
- Números CuantcosDocument10 pagesNúmeros CuantcosJuan Carlos Cantoral VilchezNo ratings yet
- SommerfeldDocument3 pagesSommerfeldAlberto RANo ratings yet
- CementitaDocument9 pagesCementitaLeonel RuizNo ratings yet
- Numeros CuanticosDocument11 pagesNumeros Cuanticosgedave2712No ratings yet
- Estructura MateriaDocument8 pagesEstructura MateriaMiguel Angel Criado AlonsoNo ratings yet
- AtomospolielectronicosDocument11 pagesAtomospolielectronicosegaqfbNo ratings yet
- Configuración ElectrónicaDocument5 pagesConfiguración ElectrónicaMoMoNo ratings yet
- Clase 3 Modelos Atomicos U2Document23 pagesClase 3 Modelos Atomicos U2Milagros RamirezNo ratings yet
- Enlaces químicos y estructura atómicaDocument155 pagesEnlaces químicos y estructura atómicaMarioswald De JesusNo ratings yet
- Presentación Teoría MecanocuánticaDocument34 pagesPresentación Teoría MecanocuánticaSofia Pilar Mondaca SepúlvedaNo ratings yet
- Resumen - Principio de AntisimétriaDocument10 pagesResumen - Principio de AntisimétriaLuis RomeroNo ratings yet
- Números CuanticosDocument10 pagesNúmeros CuanticosMartha DiestraNo ratings yet
- Configuración Electrónica GráficaDocument13 pagesConfiguración Electrónica Gráficabiologia1713No ratings yet
- Configuracion ElectronicaDocument12 pagesConfiguracion ElectronicaAlexander Capcha MuñozNo ratings yet
- Tecnológico Nacional de MéxicoDocument7 pagesTecnológico Nacional de MéxicoLUISS ZZZZZZZNo ratings yet
- QG - Semana 3 - CVHDocument26 pagesQG - Semana 3 - CVHTJEKEYKURFKRYRKNo ratings yet
- Tema 3. El ÁtomoDocument11 pagesTema 3. El ÁtomoSam Gonzales100% (1)
- Ejercicios Numeros CuanticosDocument8 pagesEjercicios Numeros CuanticosBrians RovaNo ratings yet
- Reglas de Distribución Electónica y Números CuánticosDocument11 pagesReglas de Distribución Electónica y Números CuánticosCesar Danilo Garcia SosaNo ratings yet
- Guía de Clase Números Cuánticos y OrbitalesDocument4 pagesGuía de Clase Números Cuánticos y OrbitalesIan SolisNo ratings yet
- Resolución Examen Unidad 2 PDFDocument6 pagesResolución Examen Unidad 2 PDFDanielNo ratings yet
- Valores de Los 4 Números Cuánticos para Los Siete Niveles Atómicos.Document9 pagesValores de Los 4 Números Cuánticos para Los Siete Niveles Atómicos.Miguel Angel SanchezNo ratings yet
- CONFIGURACION-Electronica FinalDocument17 pagesCONFIGURACION-Electronica FinalsofiaNo ratings yet
- Configuración electrónica: distribución de electrones en átomosDocument30 pagesConfiguración electrónica: distribución de electrones en átomosJorge MéndezNo ratings yet
- Estructura y Modelo Atómico de La Materia CeDocument73 pagesEstructura y Modelo Atómico de La Materia CeElizabeth J. Bórquez-SegoviaNo ratings yet
- Quimica-009-Niveles de Energia Sub Niveles Orbitales y ElectronesDocument7 pagesQuimica-009-Niveles de Energia Sub Niveles Orbitales y ElectronesMoroni45No ratings yet
- Configuracion Electronica GraficaDocument13 pagesConfiguracion Electronica GraficaMarbel HdezNo ratings yet
- Ecuación de SchrodingerDocument8 pagesEcuación de SchrodingerVideosNo ratings yet
- Configuración Electrónica (O Periódica) : Modelo Atómico GeneralDocument15 pagesConfiguración Electrónica (O Periódica) : Modelo Atómico GeneralDaimely GonzalezNo ratings yet
- Identificación de Los Numeros CuanticosDocument15 pagesIdentificación de Los Numeros CuanticosJervin Gómez100% (1)
- Clase1 36601Document20 pagesClase1 36601dfsadsvgfdsNo ratings yet
- Mecánica Cuántica Electrones OrbitalesDocument5 pagesMecánica Cuántica Electrones OrbitalesMarcos Anguita SNo ratings yet
- QC03Números Cuánticos y Configuración ElectrónicaDocument15 pagesQC03Números Cuánticos y Configuración ElectrónicaDiego SosaNo ratings yet
- Configuracion ElectronicaDocument7 pagesConfiguracion ElectronicaNAHOMY ALEXANDRA MEZA ALFARONo ratings yet
- Ecuacion de OndaDocument23 pagesEcuacion de OndaNewtoniXNo ratings yet
- Los Números Cuánticos PDFDocument30 pagesLos Números Cuánticos PDFMilma CermeñoNo ratings yet
- Unidad4 pt3Document45 pagesUnidad4 pt3Alvaro GuerreroNo ratings yet
- Configuracion Electronica (24 D)Document24 pagesConfiguracion Electronica (24 D)Daimo Diego Lopez AnicetoNo ratings yet
- Configuracion ElectronicaDocument27 pagesConfiguracion Electronicadavid felipe medina ramirezNo ratings yet
- Microestados InorganicaDocument10 pagesMicroestados Inorganicamurillo123No ratings yet
- Lectura 2.2-Números Cuánticos EspolDocument7 pagesLectura 2.2-Números Cuánticos EspolLeyver MartinezNo ratings yet
- Tema 1 TeoriadelaspropiedadesDocument33 pagesTema 1 Teoriadelaspropiedadespedimeh524No ratings yet
- Configuración Electrónica de Un ÁtomoDocument13 pagesConfiguración Electrónica de Un ÁtomoernestolavNo ratings yet
- Configuración electrónica átomosDocument8 pagesConfiguración electrónica átomosEloy Alembert Fernandez HonoratoNo ratings yet
- 1.-Numeros Cuanticos XX CLASEDocument33 pages1.-Numeros Cuanticos XX CLASEBrander GómezNo ratings yet
- Adaptación Estructura Atómica Sistema PeriódicoDocument24 pagesAdaptación Estructura Atómica Sistema PeriódicoMiguel Angel Criado AlonsoNo ratings yet
- Experiencias sobre circuitos eléctricos en serie operados por corriente directaFrom EverandExperiencias sobre circuitos eléctricos en serie operados por corriente directaNo ratings yet
- Guía de MatematicaDocument21 pagesGuía de MatematicaFelix Honorio Ramires TorresNo ratings yet
- Ejemplo de Redistribución de La InformaciónDocument1 pageEjemplo de Redistribución de La InformaciónFrancisco PestanaNo ratings yet
- Tema3 Disoluciones PDFDocument40 pagesTema3 Disoluciones PDFEsther Salazar VásquezNo ratings yet
- Elaboración de Jarabes, Vinos y LicoresDocument21 pagesElaboración de Jarabes, Vinos y Licoresaot1979100% (1)
- Cuadro Resumen Informacion Nutricional PDFDocument1 pageCuadro Resumen Informacion Nutricional PDFFrancisco PestanaNo ratings yet
- Tema 2 PDFDocument23 pagesTema 2 PDFFrancisco PestanaNo ratings yet
- Elaboracion de Productos Lacteos 2-2Document19 pagesElaboracion de Productos Lacteos 2-2aot1979No ratings yet
- Cuantiosas Veces Habrás Escuchado El Tan Resonante NombreDocument14 pagesCuantiosas Veces Habrás Escuchado El Tan Resonante NombreFrancisco PestanaNo ratings yet
- El PH de Los Alimentos y La Seguridad AlimentariaDocument6 pagesEl PH de Los Alimentos y La Seguridad AlimentariaFrancisco PestanaNo ratings yet
- Ejercicios Resueltos de Volumetria PDFDocument431 pagesEjercicios Resueltos de Volumetria PDFLaura Guarguati100% (5)
- Cocina BasicaDocument191 pagesCocina Basicaapi-374896193% (44)
- Ferment Os 3Document8 pagesFerment Os 3Alex DavidNo ratings yet
- 2 CENAM Uso de Certificado de CalibraciónDocument6 pages2 CENAM Uso de Certificado de CalibraciónFrancisco PestanaNo ratings yet
- Manual de Estudios de GastronomíaDocument146 pagesManual de Estudios de GastronomíaFrancisco Pestana100% (1)
- Esferificaciones de Patata - WWW - CocinistaDocument3 pagesEsferificaciones de Patata - WWW - CocinistaFrancisco Pestana100% (1)
- Gestion Por Procesos IsoDocument9 pagesGestion Por Procesos IsoFrancisco PestanaNo ratings yet
- Vitamina A RetinolDocument4 pagesVitamina A RetinolFrancisco PestanaNo ratings yet
- Ejercicios Resueltos de Quimica Calculos Quimicos 2º BachilleratoDocument14 pagesEjercicios Resueltos de Quimica Calculos Quimicos 2º BachilleratoMarcelo Andrés Ochagavía Subercaseux100% (1)
- Providencia 162 2016 Productos Cosmeticos ArtesanalesDocument17 pagesProvidencia 162 2016 Productos Cosmeticos ArtesanalesFrancisco PestanaNo ratings yet
- Ley Orgánica de Precios JustosDocument8 pagesLey Orgánica de Precios JustosRenbel CelisNo ratings yet
- Apendiceb PDFDocument5 pagesApendiceb PDFFrancisco PestanaNo ratings yet
- Formulas de Jabones LiquidosDocument7 pagesFormulas de Jabones LiquidosFrancisco PestanaNo ratings yet
- (CEM) Calibración de Balanzas MonoplatoDocument42 pages(CEM) Calibración de Balanzas Monoplatoalbertonunez@udc.esNo ratings yet
- Quimica General-Problemas - Unidad de EstequiometriaDocument45 pagesQuimica General-Problemas - Unidad de Estequiometriachicho640490% (29)
- Pesas Patrones-Norma Peruana (OIML 111)Document134 pagesPesas Patrones-Norma Peruana (OIML 111)Francisco PestanaNo ratings yet
- Aspectos Practicos de La Validaciion Incertidumbre en Mediciones QuimicasDocument150 pagesAspectos Practicos de La Validaciion Incertidumbre en Mediciones Quimicasdéborah_rosales100% (1)
- Pesas Patrones-Norma Peruana (OIML 111)Document134 pagesPesas Patrones-Norma Peruana (OIML 111)Francisco PestanaNo ratings yet
- TERMOFLUIDOSDocument4 pagesTERMOFLUIDOSDavid Ag GaNo ratings yet
- Fallas en Interruptores TermomagnéticosDocument2 pagesFallas en Interruptores TermomagnéticosMike Estrada0% (2)
- Estudio de La Carbonatación Acelerada en Probetas de Hormigón Armado (Argentina)Document9 pagesEstudio de La Carbonatación Acelerada en Probetas de Hormigón Armado (Argentina)Wellington Henrique Freitas SilvaNo ratings yet
- Matemáticas 1° SecundariaDocument6 pagesMatemáticas 1° SecundariaLuis Eduardo Lara HenriquezNo ratings yet
- ARRANQUEDocument20 pagesARRANQUEDenis Bazan LlepenNo ratings yet
- Informe Final ResistenciasDocument11 pagesInforme Final Resistencias955753039100% (3)
- Efecto de Las ExplosionesDocument3 pagesEfecto de Las ExplosionesAlice BaskervilleNo ratings yet
- Materiales dúctiles y sus propiedadesDocument3 pagesMateriales dúctiles y sus propiedadesvicky mNo ratings yet
- Cuadernillo ING. - SIDERURGIA-II - SERGIO PDFDocument90 pagesCuadernillo ING. - SIDERURGIA-II - SERGIO PDFFelixRobertoAlvarezFlorezNo ratings yet
- Actividad 2 Robotica Carlos UrbietaDocument7 pagesActividad 2 Robotica Carlos UrbietaCarlos UrbietaNo ratings yet
- Enlace Quimico SantillanaDocument2 pagesEnlace Quimico SantillanaLiliana Martinez ChamorroNo ratings yet
- Floyd - Principios de Circuitos Electricos, 2007, 8a EdDocument5 pagesFloyd - Principios de Circuitos Electricos, 2007, 8a EdIng Castillo SanchezNo ratings yet
- Festival Academico 2013, Etapa EstatalDocument20 pagesFestival Academico 2013, Etapa EstatalM. en C. Arturo Vázquez CórdovaNo ratings yet
- Torsión en Barras CircularesDocument4 pagesTorsión en Barras CircularesDamn Lord YeahNo ratings yet
- Quimica 6Document6 pagesQuimica 6Quimica TecnologiaNo ratings yet
- George Lucas La Guerra de Las Galaxias Una Nueva EsperanzaDocument265 pagesGeorge Lucas La Guerra de Las Galaxias Una Nueva Esperanzakronprinz_adam0% (1)
- Campos VectorialesDocument31 pagesCampos VectorialesYoberth EspinozaNo ratings yet
- Cap-9 Final TomasiDocument13 pagesCap-9 Final TomasiJ Alberto Gómez70% (10)
- Ejercicios Sales TernariasDocument2 pagesEjercicios Sales Ternarias521124150% (2)
- Resistencias Sección Transversal y VariablesDocument14 pagesResistencias Sección Transversal y VariablesAnonymous hR3e8SsNo ratings yet
- Primer Informe de Laboratorio de Preparacion MecanicaDocument6 pagesPrimer Informe de Laboratorio de Preparacion MecanicaMax SuniNo ratings yet
- Analisis Granulometrico Agregado Fino y GruesoDocument32 pagesAnalisis Granulometrico Agregado Fino y GruesoYeltsin Huatangari Alarcon100% (1)
- Ensayos tecnológicos acero: chispa, plegado, embutición y forjaDocument10 pagesEnsayos tecnológicos acero: chispa, plegado, embutición y forjaNildaEncisoMarquezNo ratings yet
- Examen Psicotecnico 2009Document38 pagesExamen Psicotecnico 2009Jose Abella100% (2)
- Reglamento - Interno - Uso de Explosivos PDFDocument6 pagesReglamento - Interno - Uso de Explosivos PDFMag Aguilar100% (1)
- Avance ProgramaticoDocument4 pagesAvance ProgramaticoChristian LacarriereNo ratings yet
- Conducción en Condiciones AdversasDocument50 pagesConducción en Condiciones AdversasSalvatore MillerNo ratings yet
- Práctica 4 MOMENTOS DE INERCIA DIFERENTES CUERPOSDocument5 pagesPráctica 4 MOMENTOS DE INERCIA DIFERENTES CUERPOSDavid UzhcaNo ratings yet
- Ecuaciones de Movimiento Coordenadas Normal y TangencialDocument5 pagesEcuaciones de Movimiento Coordenadas Normal y Tangencialjonathan vargasNo ratings yet
- Actuadores y SensoresDocument22 pagesActuadores y SensoresJohn Edward BenjumeaNo ratings yet