Professional Documents
Culture Documents
Examenes de Quimica 2
Uploaded by
Gabriel EmilianoCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Examenes de Quimica 2
Uploaded by
Gabriel EmilianoCopyright:
Available Formats
INTEC rea de Ciencias Bsicas y ambientales Sub-rea de Qumica Examen final de Qumica II A 209 Nombre_____________________________________________________Matricula__________________Sec.______ I. Seleccione la respuesta correcta.
(Valor 5 puntos) 1. Cuando la reaccin directa e inversa ocurren simultneamente, se obtiene: a) el estado de equilibrio, b) el estado ajustado, c) el estado neutro, d) el estado estndar 2. En una celda electroqumica o pila los electrones viajan de un electrodo al otro a travs de: a) la celda b) el puente salino c) un circuito externo d) la solucin de electrolito. 3. En la siguiente reaccin redox: CuCl2 + Zn Zncl2 + Cu. a) el Cu se reduce b) el Cl se oxida c) el Cu se oxida d) el Zn acta con agente oxidante. 4. Un carbono que este unido a otros cuatros tomos de carbono se llama: a) saturado b) cuaternario c) secundario d) primario. 5. La serie de etapas por las que pasan los reaccionantes para convertirse en productos se llama: a) principio de Chatelier b) efecto de ion comn c) equilibrio qumico d) mecanismos de reaccin II- Coloque falso o verdad segn considere el enunciado: (valor: 5 puntos) 1. Un electrolito es dbil si disuelto en agua no conduce la corriente elctrica___________ 2. Una solucin es bsica cuando [H+] > [OH-] _____________ 3. El grupo de los Halgenos es el conjunto de elementos no metlicos mas reactivo de la tabla peridica________ 4. En una cuba electroltica los iones se mueven a travs del puente salino____________ 5. El dopado de los metales se realiza con el objeto de que estos sean mejores conductores_____________ III- PROBLEMAS. Deben hacerse todos los planteos para que la respuesta sea valida. (Valor: 10 puntos) 1- Calcular Hfo para el nitrato de plomo (II) (Pb(NO3)2(l)) a partir de la siguiente reaccin: Pb(OH)2(s) + 2HNO3(l) Pb(NO3)2(l) + 2H2O (l) H= -421.6Kj b) Cuanto calor se libera por la reaccin de 2.5g de hidrxido de plomo con 1. 35g de acido ntrico? 2- Escribe la formula semi-desarrollada de los siguientes compuestos orgnicos: a) 3etil,4-metil,1-octeno b)4,4-dicloro,3-isopropil,1-hexino c)2,3,3-trimetilpentano d) 1,4-dibromo,2,6-dimetilbenceno e)3,5,6-trimetil,4-isopropil-1heptino 3-Nombre los siguientes compuestos: CH3 CH3 a) CH3-CC-CH-CH2-CH-CCH b) CH3-CHCH-CH-CH2-CH-CH3 CH2CH3 CH2 CH2-CH3 d) CH3-CHCH-CH-CH2-CHCH2 CH(CH3)2
c) CHC-CH2-CCH
CH2-CH3 e) CH3-CH2-CH-CHCH-C-CH2-CH3 CH3 CH3
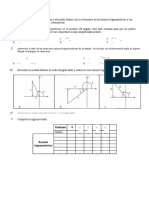
4-100mililitros de solucin 1M conteniendo Cr3+ se somete a una corriente de 5A durante 1hora. A-Que cantidad de cromo se deposita en el ctodo? B-Cual es la concentracin final de la solucin? 5- Determine la Ke a 400oC para la reaccin N2O4(g) 2NO2(g) , si la reaccin se inicial con 0.450moles de N2O4 en 2.0 litros y en el equilibrio queda 36% de este?
INTEC rea de Ciencias Bsicas y ambientales Examen final de Qumica II B 209 Nombre___________________________________________________Matricula____________________Sec.______ I. Seleccione la respuesta correcta. (Valor: 5 puntos) 1. En la siguiente reaccin redox: CuCl2 + Zn Zncl2 + Cu. a) el Zn se oxida b) el Cl se oxida c) el Cu se oxida d) el Zn acta como agente oxidante. 2. Un carbono que esta unido a dos tomos de hidrgeno se llama: a) saturado b) cuaternario c) secundario d) primario. 3. Dado:3A B, si la vel. de desaparicin de A es 1.2M/seg, la velocidad de formacin de B es: a) 0.3M/seg b) 3.6M/seg c) 1.2M/seg d) 0.4M/seg 4. Es la formula general de los alquenos: a)CNH2N b) CNH2N-2 c) CNH2N+2 d) C1/NH2N-2 : 5. Si el pH de una solucin de NaOH es 10, la concentracin de OH- es: a) 104M b) 10-4M c) 10-10M d) 1010M II- Coloque falso o verdad segn considere los siguientes enunciados: (valor: 5 puntos) 1. El compuesto de mayor produccin a nivel mundial es el acido sulfrico_______________ 2. Al hierro colado se le conoce tambin como hierro fundido_____________ 3. En una pila los iones se mueven a travs del puente salino______________ 4. Los elementos ms electropositivos de la tabla peridica son los halgenos_____________ 5. Cuando el valor de Ke es muy pequeito en la solucin se tiene poco productos_____________ III- PROBLEMAS. Deben hacerse todos los planteos para que la respuesta sea vlida. (Valor: 10 puntos) 1- Escribe la formula semi-desarrollada de los siguientes compuestos orgnicos: a) 3etil,4-metil,1-octeno b) 3-isopropil,1-hexino c) 2,3,3-trimetilpentano d) 1,4-dibromo,2,6-dimetilbenceno e) 3,5,6-trimetil,4-isopropilheptano 2- Nombre los siguientes compuestos CH3 a) CH3-CC-CH-CH2-CH-CH2-CH3 CH2CH3
CH3 b) CH3-CHCH-CH-CH2-CH-CH3 CH2 CH2-CH3
c) CHC-CH2-CCH
d) CH3-CHCH-CH-CH2-CHCH2 CH(CH3)2
CH2-CH3 e)CH3-CH2-CH-CHCH-C-CH2-CH3 CH3 CH3
3- Dado el sistema hipottico: 3A + 2B 2C + D, de donde se obtuvo el siguiente cuadro: Experimento A, M B, M vel. Inicial de formacin de D, M/min 1 1.00 10-2 1.0010-2 6.0010-3 -2 -2 2 2.00 10 3.0010 1.4410-1 -2 -2 3 1.00 10 2.0010 1.2010-2 a-cual es la ley de velocidad del sistema? b-cual es el valor de la constante de velocidad? c-Cual es el orden de la reaccin? 4- Cuantas horas tardara depositar 100g de Cr metlico en el ctodo y liberar 100g de Cl2(g) en el nodo de una cuba electroltica que contiene CrCl3 fundido, con una corriente de 5A? ( Escriba las semireacciones) 5-El pH de una solucin amoniacal de limpieza domestica es 10.2. Calcule el valor de las concentraciones de todas las especies qumicas del sistema: NH3 + H2O NH4+ + OH- (Kb= 1.8x10-5 y [H2O]= constante).
INTEC rea de Ciencias Bsicas y ambientales Examen final de Qumica II C 209 Nombre___________________________________________________Matricula____________________Sec.______ I. Seleccione la respuesta correcta. (Valor: 10 puntos) 1. En la siguiente reaccin redox: CuCl2 + Zn Zncl2 + Cu. a) el Zn se reduce b) el Cl se oxida c) el Cu se oxida d) el Zn acta como agente reductor. 2. Un carbono que est unido a tres tomos de hidrgeno se llama: a) terciario b) cuaternario c) secundario d) primario. 3. Dado:4A 5B, si la vel. de desaparicin de A es 2.8M/seg, la velocidad de formacin de B es: a) 2.95M/seg b) 3.25M/seg c) 4.125M/seg d) 3.50M/seg 4. La serie de etapas por las que pasan los reaccionantes para convertirse en productos se llama: a) principio de Chatelier b) efecto de ion comn c) equilibrio qumico d) mecanismos de reaccin 5. Cul de las siguientes es la formula general de los alquinos? a)CNH2N b) CNH2N-2 c) CNH2N+2 d) C1/NH2N-2 : 6. Para una reaccin endotrmica, si se aumenta la temperatura, la Ke: a) aumenta, b) disminuye c) no se afecta d) se hace cero 7. En los procesos redox denominados pilas las reacciones qumicas producen: a) metales por reduccin b) corriente elctrica c) metales por oxidacin d) un equivalente en cada electrodo 8. Si el pH de una solucin de HCl es 0, la concentracin de la solucin es: a) 10-14 M b) 10-1M c) 101M d) 100M 9. El estado de oxidacin del Cr en el KCrO4 es: a) +6 b) +7 c) +8 d) +4 10. En una pila los electrones giran a travs de: a) los polos b) las celdas c) el circuito externo d) el puente salino II- Resuelva los siguientes ejercicios (DEBE REALIZAR TODO EL PLANTEO PARA QUE SEA VALIDO): (10 puntos) 1. La reaccin N2O4(g) 2NO2(g) se inicia con 0.450mol de N2O4 en un recipiente de 2 litros. Cuando alcanza el equilibrio se encuentran 0.110 mol de NO2 en el recipiente. Cul es el valor de Ke? B- Cuales son las concentraciones en equilibrio? 2. Utilice los valores de la tabla para H y determine cul es el Hr para: SF6(g) + 3H2O(l) 6HF(g) + SO3(g) Hr =?
3- Nombre los siguientes compuestos segn la IUPAC: CH3 CH3 a) CH3-CC-CH-CH2-CH-CH2-CH3 b) CH3-CHCH-CH-CH2-CH-CH3 CH2CH3 CH2 CH2-CH3 d) CH3-CHCH-CH-CH2-CHCH2 CH(CH3)2 4- Escriba las formulas semidesarrolladas para: a) 1, 2, 4 triclorobenceno
c) CHC-CH2-CCH
CH2-CH3 e)CH3-CH2-CH-CHCH-C-CH2-CH3 CH3 CH3
b) 3-isopropil, 4, 4-dimetil-1-hexeno
c) 3-terbutil, 2,2-dimeti- 6propil undecano
d) paranitrobenceno
5- Prediga si la siguiente reaccin redox se verifica espontneamente en el sentido que indica la flecha. Si no lo es arrglela de modo que si lo sea y luego represente dicha celda usando la notacin de una celda y calcule fem? B- escriba las semireacciones y la ecuacin global balanceada: Be++(ac) + Au(s) Be(s) + Au+++(ac)
INTEC rea de Ciencias Bsicas y ambientales Examen final de Qumica II D 209 Nombre___________________________________________________Matricula____________________Sec.______ I. Seleccione la respuesta correcta. (valor: 10 puntos) 1. El estado que se observa cuando los valores de: T= 0 oC, P= 1atm. y la M= 1mol/litro es: a) el estado normal b) el estado ajustado c) el estado neutro d) el estado estndar 2. Cuando el pH= 5.5se puede decir que es una solucin: a) de cido fuerte b) de base fuerte c) de acido dbil d) de base dbil 3. En la siguiente reaccin redox: CuCl2 + Zn Zncl2 + Cu. a) el Zn se reduce b) el Cl se oxida c) el Cu se oxida d) el Cl es un espectador 4. Un carbono que est unido a un solo tomos de hidrgeno se llama: a) terciario b) cuaternario c) secundario d) primario. 5. Dado:3A 4B, si la vel. de desaparicin de A es 0.9M/seg, la velocidad de formacin de B es: a) 3M/seg b) 1.2M/seg c) 0.12M/seg d) 0.8M/seg 6. Los hidrocarburos encuentran su principal utilidad como: a) agente reductores b) iniciadores de polmeros c) combustibles d) catalizadores de alto rendimiento 7. Cul de las siguientes es la formula general de los alcanos? a)CNH2N b) CNH2N-2 c) CNH2N+2 d) C1/NH2N-2 : 8. Si una reaccin es exotrmica, al aumentar la temperatura la Ke: a) aumenta, b) disminuye c) no se afecta d) se hace cero. 9. Cul de estos compuestos se produce de forma natural por la descomposicin bacteriana de la vegetacin subacutica? a) propano b) etano c) gasolina d) metano. 10. Si el pH de una solucin es 8.5, la solucin es de: a) base fuerte b) acido dbil c) acido fuerte d) base dbil II- Resuelva los siguientes ejercicios (DEBE REALIZAR TODO EL PLANTEO PARA QUE SEA VALIDO): (10 puntos) 1. El HCN tiene una Ka = 4.9x10-10 cul es el grado (%) de ionizacin de este acido en una solucin 0.0850M? B- Cual es el pH de la solucin? 2. Utilice los datos de la tabla correspondiente para calcular Hro en: SiO2(s) + 3C(s) SiC(s) + 2CO(g) B-Cual es la cantidad de calor que se obtiene por la reaccin de 2.5 g de SiO2 con 1.35g de Carbono? 3- Nombre los siguientes compuestos segn la IUPAC: CH3 CH3 a) CH3-CC-CH-CH2-CH-CH2-CH3 b) CH3-CHCH-CH-CH2-CH-CH3 CH2CH3 CH2 CH2-CH3 d) CH3-CHCH-CH-CH2-CHCH2 CH(CH3)2 4- Escriba las formulas semidesarrolladas para: a) 1, 2, 4 triclorobenceno c) 3-terbutil, 2,2-dimeti-6-propil, undecano Hro=?
c) CHC-CH2-CCH
CH2-CH3 e)CH3-CH2-CH-CHCH-C-CH2-CH3 CH3 CH3
b) 3-isopropil, 4, 4-dimetil-1-hexeno d) meta di nitrobenceno e) para etil, isopropil benceno
5- La reaccin 2A producto se inicia con [A] es 0.250M. A t= 9.9seg, [A] es 0.225M y a t= 10.45seg. [A] es 0.202M. Determine: a) La velocidad de reaccin en estos intervalos de t? b) Cual ser la concentracin de A a los 15seg? c) Que tiempo tardara la concentracin de A para colocarse en 0.100M? (asuma que la Vr se mantiene constante en el ultimo intervalo)
INTEC rea de Ciencias Bsicas y ambientales Examen final de Qumica II E 209 Nombre______________________________________________________Matricula____________________Sec.______ I. Seleccione la respuesta correcta. (valor: 5 puntos) 1- Cual de los siguientes elementos se obtiene comercialmente a partir del agua de mar? a) A b) Ca c) Mg d) K 2. La base conjugada para el HCes: a) C- b) H+ c) H- d) OH3-Cual de los siguientes es un factor que no afecta la Ke: a) concentracin b) presin c) temperatura d) masa 4-La especie que aparece en una etapa del mecanismo de una reaccin y no en la reaccin global es un: a) catalizador b) espectador c) intermediario d) electrolito dbil 5- Para una solucin dbilmente cida cual de las siguientes es la relacin entre los iones de H+ y de OH-? a) H3O+ OH- b) H3O+ OH- c) H3O+ = OH- d) H3O+ = 0 II- Coloque verdad o falso. (valor: 5 puntos) 1- Si un cido tiene una Ki alta se dice que es dbil________ 2- El gas propano se obtiene de forma natural por descomposicin de la materia vegetal _________ 3- Un electrodoes una superficie sobre la que se lleva a cabo una semireacion de una celda __________ 4- Las propiedades metalicas crecen de izquirda a derecha en la tabla periodica________ 5- La conduccion electrolitica se realiza por el movimiento de los electrones a traves de un liquido________ II- Resuelva los siguientes ejercicios (DEBE REALIZAR TODO EL PLANTEO PARA QUE SEA VALIDO): (10 puntos) 1. Calcular Hfo para: 2C(grafito) + H2(g) C2H2(g) , a partir de los elementos, dada las ecuaciones: a- C(grafito) + O2(g) CO2(g) Hro = -393.5Kj/mol b- H2(g) + 1/2O2(g) H2O(l) Hro = -285.5Kj/mol c- 2C2H2(g) + 5O2(g) 4CO2(g) + 2H2O(l) Hro = -2598.8Kj/mol 2. Para el siguiente par redox Ag / Cd, : a) haga el diagrama de pila y calcule el potencial b) escriba las semireacciones y la reaccin global 3- Nombre los siguientes compuestos segn la IUPAC: CH3 CH3 a) CH3-CC-CH-CH2-CH-CH2-CH3 b) CH3-CHCH-CH-CH2-CH-CH3 CH2CH3 CH2 CH2-CH3 d) CH3-CHCH-CH-CH2-CHCH2 CH(CH3)2 4- Escriba las formulas semidesarrolladas para: a) 1, 2, 4 triclorobenceno
c) CHC-CH2-CCH
CH2-CH3 e)CH3-CH2-CH-CHCH-C-CH2-CH3 CH3 CH3
b) 3-isopropil, 4, 4-dimetil-1-hexeno
c) 3-terbutil, 2,2-dimeti- 6propil undecano
d) paranitrobenceno
5-Si 15g de NH2NH2 se disuelven en 10 litros de agua pura, cual es el pH (Kb = 3.0x10 -6)? Como cambia el pH de esta solucin si se le adicionan 20 g de NH2NH3Cl?
INTEC rea de Ciencias Bsicas y ambientales Examen final de Qumica II F 209 Nombre______________________________________________________Matricula____________________Sec.______ I. Seleccione la respuesta correcta. (valor: 10 puntos) 1. La superficie donde ocurre una semireaccion redox, se llama: a) celda electroltica b) potencial normal c) celda electroqumica d) electrodo 2. La funcin de una solucin buffer, cuando se agrega algo de cido o base fuerte, es: a) volverse cido b) volverse bsico c) volverse neutro d) mantenerse prcticamente igual. 3. En la siguiente reaccin redox: CuCl2 + Zn Zncl2 + Cu. a) el Zn se reduce b) el Cl se oxida c) el Cu se oxida d) el Zn acta como agente reductor. 4. Un carbono que esta unido a dos tomos de hidrgeno se llama: a) saturado b) cuaternario c) secundario d) primario. 5. Dado:2A B, si la vel. de desaparicin de A es 0.90M/seg, la velocidad de formacin de B es: a) 1.80M/seg b) 0.90M/seg c) 0.30M/seg d) 0.45M/seg 6. Un recipiente conteniendo material de reaccin y electrodos sumergidos en este, se conoce como: a) celda de Down b) celda de Daniels c) celda galvnica d) celda electroltica 7. Es la formula general de los alquenos: a)CNH2N b) CNH2N-2 c) CNH2N+2 d) C1/NH2N-2 : 8. Cual de las siguientes situaciones se obtiene en un sistema en equilibrio al agregar un catalizador? a) aumenta la vel. directa b) disminuye la vel. inversa c) disminuye la concentracin de reactivos d) no afecta el equilibrio 9. Cuando se tiene un equilibrio heterogneo no se toman en cuenta para la expresin de Ke los: a) cidos fuertes b) bases dbiles c) elementos en estado estndar d) slidos y lquidos puros 10.Si el pH de una solucin de NaOH es 10, la concentracin de la solucin es: a) 104M b) 10-4M c) 10-10M d) 1010M II- Resuelva los siguientes ejercicios (DEBE REALIZAR TODO EL PLANTEO PARA QUE SEA VALIDO): (10 puntos) 1. La reaccin 3Fe(S) + 4H2O(g) Fe3O4(S) + 4H2(g) se inicia con 15g de H2O en un recipiente de 4 litros y suficiente Fe. El equilibrio se establece a 850oC. La Ke= 0.980. Cules son las concentraciones de H y de H2O en el equilibrio? 2. Utilice los valores de la tabla para H y determine cul es el Hr para: SF6(g) + 3H2O(l) 6HF(g) + SO3(g) Hr =?
3- Nombre los siguientes compuestos segn la IUPAC: CH3 CH3 a) CH3-CC-CH-CH2-CH-CH2-CH3 b) CH3-CHCH-CH-CH2-CH-CH3 CH2CH3 CH2 CH2-CH3 d) CH3-CHCH-CH-CH2-CHCH2 CH(CH3)2 4- Escriba las formulas semidesarrolladas para: a) 1, 2, 4 triclorobenceno
c) CHC-CH2-CCH
CH2-CH3 e)CH3-CH2-CH-CHCH-C-CH2-CH3 CH3 CH3
b) 3-isopropil, 4, 4-dimetil-1-hexeno
c) 3-terbutil, 2,2-dimeti- 6propil undecano
d) paranitrobenceno
5- Prediga si la siguiente reaccin redox se verifica espontneamente en el sentido que indica la flecha. Si no lo es arrglela de modo que si lo sea y luego represente dicha celda usando la notacin de una celda y calcule fem? B- escriba las semireacciones y la ecuacin global balanceada: Be++(ac) + Au(s) Be(s) + Au+++(ac)
INTEC rea de Ciencias Bsicas y ambientales Examen final de Qumica II G 209 Nombre_______________________________________________Matricula____________________Sec.______ I-Coloque falso (F) o verdadero (V) (5ptos.): a- El aumento de la presin es uno de los factores que favorecen la velocidad de una reaccin _________ b-El valor de la constante especifica de velocidad, K, depende de la concentracin de los productos____ _ c-Un catalizador aumenta la velocidad de la reaccin directa, pero tambin la de la inversa _______ d-La Ke para una reaccin endotrmica aumenta si se aumenta la temperatura_____ e-Una solucin con un pH =3 tiene mayor concentracin de H + que otra con un pH =1_______ II. Seleccione la respuesta correcta. (valor: 5 puntos) 1- Cual de las siguientes es la base conjugada del HNO2: a) H+ b) NO2+ c) H- d) NO2 2- Cuando en un sistema en equilibrio se aumenta la presin, el equilibrio se desplaza hacia el producto que ocupa: a) mayor volumen b) menor volumen c) igual volumen d) no se desplaza 3- Si el pH de una solucin de NaOH es 10, la concentracin de la solucin es: a) 104M b) 10-4M c) 10-10M d) 1010M 4- Una sustancia que acta como cido y como base se llama: a) anftera o anfiprotica b) cido conjugado c) base conjugada d) solucin reguladora 5-Cual de los siguientes hidrocarburos se obtiene por descomposicin bacteriana de la vegetacin subacutica: a)C2H4 b) C3H8 c) C2H2 d) CH4 II- Resuelva los siguientes ejercicios (DEBE REALIZAR TODO EL PLANTEO PARA QUE SEA VALIDO): (10 puntos) 1. Cul es el valor de Ka de un acido dbil monoprotico (HA), cuya solucin tiene una concentracin de 0.0650M y el pH es 3.45? 2. Utilice la tabla de valores del potencial de reduccin para formar una pila con el par redox Li/Sn. Cules son las semireacciones y la reaccin global? Cul es el potencial de la pila? 3- Nombre los siguientes compuestos segn la IUPAC: CH3 CH3 a) CH3-CC-CH-CH2-CH-CH2-CH3 b) CH3-CHCH-CH-CH2-CH-CH3 CH2CH3 CH2 CH2-CH3 d) CH3-CHCH-CH-CH2-CHCH2 CH(CH3)2 4- Escriba las formulas semidesarrolladas para: a) 1, 2, 4 triclorobenceno
c) CHC-CH2-CCH
CH2-CH3 e)CH3-CH2-CH-CHCH-C-CH2-CH3 CH3 CH3
b) 3-isopropil, 4, 4-dimetil-1-hexeno
c) 3-terbutil, 2,2-dimeti- 6propil undecano 5- Use las abcd-
d) paranitrobenceno
siguientes ecuaciones para hallar Hfo del HBr(g) a 25oC:
Br2(l) Br2(g) Hro = 3110kj/mol HBr(g) H(g) + Br(g) Hro = 339.1Kj/mol Br2(g) 2Br(g) Hro = 164792Kj/mol H2(g) 2H(g) Hro = 4066494Kj/mol
INTEC rea de Ciencias Bsicas y ambientales Examen final de Qumica II H 209 Nombre_______________________________________________Matricula____________________Sec.______ I. Seleccione la respuesta correcta. (Valor: 5puntos) 1.Si el carbn arde ms rpido en oxigeno que en aire, el factor que afecta la velocidad en este caso es : a) la temperatura b) la concentracin c) la naturaleza de los reactivos d) la presin 2. La superficie donde ocurre una semireaccion redox, se llama: a) celda electroltica b) potencial normal c) celda electroqumica d) electrodo 3. En la siguiente reaccin redox: CuCl2 + Zn Zncl2 + Cu. a) el Zn se reduce b) el Cl se reduce c) el Cu se reduce d) ninguna es correcta 4 Cul es la expresin de la constante de equilibrio que es correcta para la reaccin: Fe2O3(s) + 3H2(g) 2Fe(s) + 3H2O(g) a) Ke = Fe2O3 H23 / Fe2 H2O 3 b) Ke = H2 / H2O c) H2O3 / H23 d) Ke = Fe2 H2O3 / Fe2O3 H23 5. Cual es mas reactivo de los siguientes hidrocarburos?: a) benceno b) propano c) penteno d) ciclobutano II- Ponga verdadero (V) o falso(F). (Valor 5 puntos) 1- Para los compuestos en su estado estndar el valor de Hof es cero (Hof = 0 )_______ 2- El proceso de Haber es utilizado en la obtencin del amoniaco________ 3- El desecho que se produce en la preparacin de la MENA es la GANGA__________ 4-Los elementos ms electropositivos en la tabla peridica son los alcalinos_________ 5- En la reaccin donde HPRODUCTOS < HREACTIVOS se libera energa____________ III- Resuelva los siguientes ejercicios (DEBE REALIZAR TODO EL PLANTEO PARA QUE SEA VALIDO): (10 puntos) 1. La reaccin N2O4(g) 2NO2(g) se inicia con 0.450mol de N2O4 en un recipiente de 2 litros. Cuando alcanza el equilibrio se encuentran 0.110 mol de NO2 en el recipiente. Cul es el valor de Ke? B- Cuales son las concentraciones en equilibrio? 2. Utilice los valores de la tabla para H y determine cul es el Hr para: SF6(g) + 3H2O(g) 6HF(g) + SO3(g) Hr =?
3- Nombre los siguientes compuestos segn la IUPAC: CH3 CH3 a) CH3-CC-CH-CH2-CH-CH2-CH3 b) CH3-CHCH-CH-CH2-CH-CH3 CH2CH3 CH2 CH2-CH3 d) CH3-CHCH-CH-CH2-CHCH2 CH(CH3)2
CH2-CH3 e) CH3-CH2-CH-CHCH-C-CH2-CH3 CH3 CH3
c) CHC-CH2-CCH
f) 4- Escriba las formulas semidesarrolladas para: a) 1, 2, 4 triclorobenceno b) 3-isopropil, 4, 4-dimetil-1-hexeno
c) 3-terbutil, 2,2-dimeti- 6propil undecano
d) paranitrobenceno
5- Los datos cinticos que figuran en la siguiente tabla corresponden a la reaccin: 2NO (g) + O2(g) 2NO2(g) NO, M O2, M Velocidad inicial de formacin del NO2, M/s 0.010 0.010 2.5x10 -3 0.010 0.020 5.0x10-3 0.030 0.020 45x10 -3 a) Escriba la ecuacin de velocidad b) Cual es el valor de la constante de velocidad?
You might also like
- Temas Selectos de QuimicaDocument4 pagesTemas Selectos de QuimicaIsaias Sanches LopezNo ratings yet
- Examen Química 1Document6 pagesExamen Química 1Izamary Lizarraga DuarteNo ratings yet
- FILA A Prueba Nomenclatura InorganicaDocument5 pagesFILA A Prueba Nomenclatura InorganicaANA MARIA MARIHUAN100% (1)
- Examen Quimica 1Document2 pagesExamen Quimica 1Josué DassaevNo ratings yet
- Examen Final de Quimica IIDocument7 pagesExamen Final de Quimica IIMariajoseMorenoAlbaNo ratings yet
- Examen Parcial Quimica 2 Primer ParcialDocument2 pagesExamen Parcial Quimica 2 Primer ParcialOswaldo Anduaga100% (3)
- Cuestionario Átomos y MoléculasDocument7 pagesCuestionario Átomos y MoléculasJesús Pérez ArcosNo ratings yet
- Tercer Examen Parcial Quimica 2Document3 pagesTercer Examen Parcial Quimica 2Koko QfbNo ratings yet
- Prueba HidrocarburosDocument4 pagesPrueba HidrocarburosNicole Alejandra Abarca CamposNo ratings yet
- Modelo de Examen QuimicaDocument1 pageModelo de Examen QuimicaEmanuel LeguizamonNo ratings yet
- Evaluación Calculos EstequiométricosDocument1 pageEvaluación Calculos EstequiométricosMALEJA SANTANANo ratings yet
- Taller compuestos nitrogenadosDocument5 pagesTaller compuestos nitrogenadosOscar Niño BernalNo ratings yet
- CETEC Morelos: Temas Selectos de Química IIDocument15 pagesCETEC Morelos: Temas Selectos de Química IIVictorNo ratings yet
- PRUEBA DE QUÍMICA 3° Medio EQUILIBRIO QUÍMICODocument5 pagesPRUEBA DE QUÍMICA 3° Medio EQUILIBRIO QUÍMICOCarolina Torres Armijo50% (4)
- Actividades Sobre Balance QuímicoDocument3 pagesActividades Sobre Balance QuímicoRoland M ReyesNo ratings yet
- Balancear ecuaciones redoxDocument3 pagesBalancear ecuaciones redoxClaudia HernandezNo ratings yet
- Examen Ordinario RespuestasDocument9 pagesExamen Ordinario Respuestaswastl054100% (1)
- Examen Semestral de QuimicaDocument4 pagesExamen Semestral de QuimicaAnna SanferNo ratings yet
- Prueba Ley de Hess Fila BDocument4 pagesPrueba Ley de Hess Fila BClaudiaNo ratings yet
- Examen VelocDocument5 pagesExamen VelocCarmen Ramirez CavagnolaNo ratings yet
- Prueba Segunta y Tercera Ley de La TermodinamicaDocument3 pagesPrueba Segunta y Tercera Ley de La TermodinamicaDiego Ignacio Parra ZentenoNo ratings yet
- Examen Quimica Tercer BimestreDocument2 pagesExamen Quimica Tercer BimestreTeodoro Medellin Chávez100% (1)
- Guia de Discusion de Termoquimica y Cinetica, 2013Document10 pagesGuia de Discusion de Termoquimica y Cinetica, 2013Albert GuardadoNo ratings yet
- Práctica N°10 Balanceo Por RedoxDocument1 pagePráctica N°10 Balanceo Por RedoxMiguel Gómez CuroNo ratings yet
- RedoxDocument10 pagesRedoxRodrigo Ignacio Muñoz SotoNo ratings yet
- Qui MicaDocument15 pagesQui MicaESTUDIANTE JOSE DAVID MARTINEZ RODRIGUEZNo ratings yet
- Guia Tipos de Reacciones I MedioDocument3 pagesGuia Tipos de Reacciones I MedioAnonymous PShSARDzgYNo ratings yet
- Poligrafiado DigitalesDocument55 pagesPoligrafiado DigitalesGloria VargasNo ratings yet
- 04 Disoluciones Test PDFDocument18 pages04 Disoluciones Test PDFkarinNo ratings yet
- Preguntas y Problemas Fisica Medica II BDocument6 pagesPreguntas y Problemas Fisica Medica II BCarolina Herasme100% (1)
- Segundo Examen Parcial Quimica 2Document3 pagesSegundo Examen Parcial Quimica 2Koko Qfb50% (2)
- Prueba Química REDOX 2020alternDocument4 pagesPrueba Química REDOX 2020alternDiego Ignacio Parra Zenteno100% (1)
- GUIA ONCE 2010 Estequiometria y GasesDocument12 pagesGUIA ONCE 2010 Estequiometria y Gasesquimicacombia554590% (10)
- Reacciones Quimicas 4 TODocument6 pagesReacciones Quimicas 4 TOwilliam100% (1)
- Examen Final Ciencias 3roDocument8 pagesExamen Final Ciencias 3roarmandoNo ratings yet
- Examen Física Primer Periodo Parte 1Document3 pagesExamen Física Primer Periodo Parte 1Edison Alexander Tenjo RamosNo ratings yet
- EjerciciosComposicionPorcentualFormulaEmpiricaDocument2 pagesEjerciciosComposicionPorcentualFormulaEmpiricaMALEJA SANTANA100% (1)
- Taller Balanceo Por Ión-ElectrónDocument2 pagesTaller Balanceo Por Ión-ElectrónSANTIAGO JIMENEZ TRIANANo ratings yet
- Ejercicios Quimica GeneralDocument10 pagesEjercicios Quimica Generaldanna kangNo ratings yet
- Química Orgánica I - Prueba 1Document2 pagesQuímica Orgánica I - Prueba 1Valeriita Marisol BasantesNo ratings yet
- EVALUACIÓN de Formula Minima y Molecular GRADO DECIMODocument1 pageEVALUACIÓN de Formula Minima y Molecular GRADO DECIMOLisbethOrtegaAguasNo ratings yet
- 1 BIOL ActDocument52 pages1 BIOL ActE.F C.L.No ratings yet
- .... Examen de Tercer PeriodoDocument11 pages.... Examen de Tercer PeriodoAngie Daniela Morales CuellarNo ratings yet
- Guía Examen Quimica 2 Primer ParcialDocument12 pagesGuía Examen Quimica 2 Primer ParcialLuis_Alberto_P_42450% (2)
- Examen Extraordinario Química OrgánicaDocument3 pagesExamen Extraordinario Química OrgánicaFernando Torres PérezNo ratings yet
- Taller Compuestos AromaticosDocument3 pagesTaller Compuestos AromaticosAnonymous GdWMlV46bUNo ratings yet
- Prueba Formativa RedoxDocument4 pagesPrueba Formativa Redoxclaudiolineros89No ratings yet
- Corrección Prueba 1Document8 pagesCorrección Prueba 1Stephanie Ibarra ReyNo ratings yet
- Taller de Oxidos e HidroxidosDocument2 pagesTaller de Oxidos e HidroxidosMartha Viviana Tejada Gallego100% (1)
- Ejercicios 2. Hibridaciòn y Funciones OrganicasDocument4 pagesEjercicios 2. Hibridaciòn y Funciones OrganicasMili Romero CuevaNo ratings yet
- Balanceo de Ecuaciones Nivelacion 10Document2 pagesBalanceo de Ecuaciones Nivelacion 10jose GuzmanNo ratings yet
- Recuerda las reglas de la tabla periódicaDocument7 pagesRecuerda las reglas de la tabla periódicaElvi MurilloNo ratings yet
- Guia Grupos FuncionalesDocument12 pagesGuia Grupos FuncionalesFelipe Alejandro JaraNo ratings yet
- Examen Mol y Número de AvogadroDocument1 pageExamen Mol y Número de Avogadrojavier quesada100% (2)
- Test de Ideas PreviasDocument2 pagesTest de Ideas PreviasDaniel Felipe AlbaNo ratings yet
- 9-BIOLOGIA-taller Virtual Biologia 9 PDFDocument4 pages9-BIOLOGIA-taller Virtual Biologia 9 PDFPARRA CANABATE OSCAR MAURICIONo ratings yet
- Temas Selectos de Quimica Segundo ParcialDocument3 pagesTemas Selectos de Quimica Segundo ParcialIsaac GarzaNo ratings yet
- 2do Parcial Quimica-I 2023-1Document3 pages2do Parcial Quimica-I 2023-1Jimena Ramírez OsornoNo ratings yet
- Boletín SelectividadDocument41 pagesBoletín Selectividadlunares77775No ratings yet
- Ingeniería de Transito: Elementos, Conductor y PercepciónDocument15 pagesIngeniería de Transito: Elementos, Conductor y PercepciónGabriel EmilianoNo ratings yet
- Tubo de VenturiDocument7 pagesTubo de VenturiGabriel EmilianoNo ratings yet
- Tema I-Introd CarreterasDocument7 pagesTema I-Introd CarreterasGabriel EmilianoNo ratings yet
- Hidrograma UnitarioDocument6 pagesHidrograma UnitarioGabriel EmilianoNo ratings yet
- Unidad I IntroduccionDocument48 pagesUnidad I IntroduccionGabriel EmilianoNo ratings yet
- PC Juan PayeroDocument8 pagesPC Juan PayeroGabriel EmilianoNo ratings yet
- Practica 4 Geologia Resumen.Document9 pagesPractica 4 Geologia Resumen.Gabriel EmilianoNo ratings yet
- Der Echos RealesDocument33 pagesDer Echos RealesRenzo Ezequiel GuerreroNo ratings yet
- Practica 1 Lab Termo de Sust PurDocument9 pagesPractica 1 Lab Termo de Sust Purlogan123No ratings yet
- Laboratorio Circuitos Eléctricos N6 Ingeniería Mecánica UNIDocument32 pagesLaboratorio Circuitos Eléctricos N6 Ingeniería Mecánica UNIÐanıel PaucarNo ratings yet
- Informe Flujo CompresibleDocument19 pagesInforme Flujo CompresibleJuan David GómezNo ratings yet
- Moldeo por fusión y sus procesos claveDocument32 pagesMoldeo por fusión y sus procesos claveArturo SáezNo ratings yet
- LAB 3 Fenol AguaDocument2 pagesLAB 3 Fenol AguaSebastián MachucaNo ratings yet
- Diferencia entre sistemas isostáticos e hiperestáticosDocument10 pagesDiferencia entre sistemas isostáticos e hiperestáticosdiego ururi67% (3)
- Asimetría y medidas de asimetríaDocument11 pagesAsimetría y medidas de asimetríaCyber TeenNo ratings yet
- Cap - Iv.tipos de PerforadorasDocument35 pagesCap - Iv.tipos de PerforadorasJonathan VilcaNo ratings yet
- Acustica - Di MarcoDocument498 pagesAcustica - Di MarcoAlekos Dat100% (2)
- Impilso Cantidad de Movimiento PDFDocument4 pagesImpilso Cantidad de Movimiento PDFLuis Salazar100% (1)
- Práctica 1 - Electricidad y MagnetismoDocument6 pagesPráctica 1 - Electricidad y MagnetismoMontse IniestraNo ratings yet
- Tesis Master Cristina Ubeda BernabeDocument68 pagesTesis Master Cristina Ubeda BernabeRoger Chira SedanoNo ratings yet
- 2°#fuerzas ElásticasDocument6 pages2°#fuerzas Elásticasteradata05912967% (3)
- NTC1610Document19 pagesNTC1610Charles GuzmanNo ratings yet
- Investigacion Mantenimiento U-1Document50 pagesInvestigacion Mantenimiento U-1Victoria CocteconNo ratings yet
- ElectromagnetoDocument10 pagesElectromagnetoChekkoo Alonso NeriNo ratings yet
- Diseño de MOLINO DE BOLASDocument123 pagesDiseño de MOLINO DE BOLASEDUARDONo ratings yet
- Taller 6 Razones TrigonometricasDocument2 pagesTaller 6 Razones TrigonometricasCarlos Eduardo Beltrán Castro0% (1)
- Experimento 6 Determinacion Del Calor de Sbulimacion Del Yodo Mediante Un Metodo OpticoDocument5 pagesExperimento 6 Determinacion Del Calor de Sbulimacion Del Yodo Mediante Un Metodo OpticoAlfredo Castaño PuertaNo ratings yet
- PROPORCIONALIDADDocument42 pagesPROPORCIONALIDADKBrado Morales100% (1)
- INFORME Modificacion ExpedienteDocument7 pagesINFORME Modificacion ExpedienteRonald Chauca HuamanNo ratings yet
- CaidasDocument2 pagesCaidasAgustin Valencia RequeNo ratings yet
- Orden Trabajo InformeDocument1 pageOrden Trabajo InformeJean RamosNo ratings yet
- Vigas Teoria ElasticaDocument19 pagesVigas Teoria ElasticaAnybazAngieNo ratings yet
- Circunferencia y ParabolaDocument13 pagesCircunferencia y ParabolaingleuceNo ratings yet
- 2 Problemas Mov Armc3b3nico AmortiguadoDocument2 pages2 Problemas Mov Armc3b3nico AmortiguadoJavier Andres0% (1)
- Guia de Geometria Analitica Plan 2017Document2 pagesGuia de Geometria Analitica Plan 2017Victoria NavarroNo ratings yet
- Notación científica y cifras significativasDocument23 pagesNotación científica y cifras significativasantonioNo ratings yet
- Leyes de Newton y movimiento de partículasDocument13 pagesLeyes de Newton y movimiento de partículasDanieo h Solis delgadoNo ratings yet
- Influencia de la zeolita de Cabo de Gata en morteros de cementoDocument20 pagesInfluencia de la zeolita de Cabo de Gata en morteros de cementoRoux GandyNo ratings yet