Professional Documents
Culture Documents
Transformaciones de Fase en Los Aceros
Uploaded by
judal57Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Transformaciones de Fase en Los Aceros
Uploaded by
judal57Copyright:
Available Formats
1.
Transformaciones en estado slido en el sistema Fe-C
Los metales constituyen ms de la mitad de los elementos qumicos conocidos en la actualidad y son de relevante importancia debido al sinfn de aplicaciones industriales para las que son utilizados. Todos los metales puros y aleaciones que se forman con ellos se dividen en ferrosos y no ferrosos. Concentraremos la atencin en los primeros, a los cuales pertenecen el hierro y las aleaciones en base de hierro, los que constituyen cerca del 95% de la produccin mundial de metales. Se entiende por metal puro a aquel metal que contiene impurezas por debajo del 0.01%. La metalurgia moderna permite obtener metales de alta pureza (99.9999%). No obstante, las impurezas, an en muy pequeas cantidades, pueden influir en forma esencial sobre las propiedades del metal. Las aleaciones tienen resistencia mecnica y dureza ms altas que los metales puros, hacindolas ms requeridas para muchos usos industriales. En particular, los aceros, los cuales son bsicamente aleaciones de hierro y carbono, combinan buena resistencia (o carga de rotura), tenacidad, dureza y relativo bajo costo. Se entiende por tenacidad a la resistencia del metal a la deformacin y a la rotura. Por otro lado, se define plasticidad a la facultad del metal de experimentar una deformacin remanente (residual) sin destruirse. La bajaplasticidad o ausencia de la misma se denomina fragilidad. Se entiende por dureza a la propiedad del metal de oponer resistencia a la deformacin plstica, la cual puede ser determinada por varios mtodos distintos (dureza Brinell, dureza Rockwell, dureza Vickers, etc.). Por ejemplo, para determinar la dureza Brinell, una superficie plana del metal es apretada contra una bola de acero duro de 2.5, 5 10 mm de dimetro. Se denomina el nmero de dureza Brinell (HB) a la relacin entre la carga transmitida a travs de la bola y la superficie de la huella esfrica dejada por la bola sobre la superficie del metal. Este mtodo es usado para aceros con durezas inferiores a los 450 HB. Para metales ms duros suele determinarse la dureza por el mtodo Rockwell (HRC), por el cual se usa un cono de diamante con un ngulo de 120. Es el mtodo ms utilizado en la industria debido a la rapidez de medicin y al pequeo tamao de la huella dejada sobre la superficie del metal. El cambio de las dimensiones y de la forma de una pieza bajo la accin de fuerzas aplicadas recibe el nombre de deformacin. Las deformaciones pueden estar ocasionadas por fuerzas exteriores aplicadas al cuerpo o por fuerzas internas que surgen durante los procesos fsico-qumicos que transcurren en el propio cuerpo. Las tensiones temporales surgen bajo la accin de una carga exterior y desaparecen despus de quitar la misma, mientras que las tensiones internas se equilibran dentro del mismo cuerpo sin que acten fuerzas exteriores. Estas ltimas se deben a la distribucin no uniforme de las deformaciones en el interior del cuerpo, las cuales aparecen como resultado de la distribucin desigual de temperaturas en el interior del metal. Estas tensiones
trmicas aparecen durante el calentamiento y enfriamiento rpidos, en los cuales se producen dilataciones y contracciones irregulares de las capas exteriores e interiores del metal. Estas tensiones se originan como consecuencia de las transformaciones de fase durante el tratamiento trmico [1].
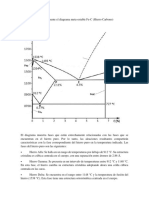
1.1 Fases en estado slido en el sistema Fe-C Para poder entender las distintas fases de los aceros, es necesario describir los puntos crticos del Fe puro. Para ello puede tomarse una muestra de Fe lo ms puro posible y dejarlo enfriar muy lentamente. Se observa que el Fe solidifica instantneamente a 1538 C. Al continuar descendiendo la temperatura no se observa nada anormal en el proceso de enfriamiento hasta los 1394 C. All disminuye la velocidad de enfriamiento debido a un desprendimiento espontneo de calor. A los 912 C se produce un nuevo desprendimiento ocasionando otra disminucin en la velocidad de enfriamiento. El mismo fenmeno se observa una vez ms (esta vez a 750 C) antes de llegar a la temperatura ambiente. Las temperaturas a las cuales se producen estos fenmenos se llaman puntos crticos, denominados Ar4, Ar3 y Ar2, respectivamente. El primero corresponde a un cambio alotrpico del Fe cuando pasa del estado Fe- al estado Fe-. El segundo est asociado a la transformacin de Fe- en Fe- no magntico. Finalmente, el ltimo punto crtico corresponde a la transformacin de Fe- no magntico en Fe- magntico. El porcentaje de carbono en los aceros ordinarios o de bajo carbono oscila entre un 0.03 % y un 0.30 %, y el porcentaje de manganeso lo hace entre un 0.25 % y un 1 %. Tambin pueden hallarse presentes otros elementos como el silicio e impurezas como el azufre, el fsforo, etc., pero en muy bajas proporciones. En un primer anlisis, estos aceros pueden considerarse como aleaciones binarias de Fe-C para luego agregarle los efectos de los otros elementos. Los constituyentes simples del sistema Fe-C son: austenita, ferrita y cementita. Los dos primeros se caracterizan por ser soluciones slidas, de insercin octadrica de C en Fe- y Fe-, respectivamente. La cementita (Fe3C) es una compuesto intermetlico con estructura ortorrmbica. En la Fig. 1.1 se muestran las fases presentes en las aleaciones Fe-C enfriadas muy lentamente, a varias temperaturas y composiciones de hierro con carbono hasta del 6.67 %. Este diagrama de fases no es estrictamente un diagrama de equilibrio puesto que la cementita, pese a ser muy estable, puede llegar a descomponerse en fases ms estables del hierro y en carbono (grafito) [2].
Austenita- La solucin slida intersticial amagntica de C en Fe- es llamada austenita y tiene una estructura cristalina FCC. La mxima solubilidad slida del C en austenita es del 2.11 % a 1148 C, disminuyendo a un 0.8 % a 723 C. Su dureza es de 180 a 200 HB. No es posible obtener austenita- a la temperatura ambiente por enfriamiento lento, aunque s es posible en algunos aceros aleados (con 12% de Mn, o 8% de Ni, etc.). La austenita- es amagntica como el Fe-. Es blanda, dctil y tenaz, y sus caractersticas mecnicas varan con la composicin. Como valores medios aproximados pueden tomarse 300 HB de dureza y entre 880 y 1100 MPa de carga de rotura. Ferrita- Se llama as a la solucin slida intersticial de carbono en Fe-, la cual tiene una estructura BCC. El C es muy poco soluble en Ferrita-, alcanzando una mxima solubilidad slida del 0.09 % a 1495 C. Ferrita- Esta fase es una solucin slida de carbono en la red cristalina del Fe- (BCC). El carbono es muy poco soluble en Ferrita-, alcanzando una mxima solubilidad slida del 0.0218 % a 727 C, disminuyendo a un 0.008 % a 20 C. Los tomos de carbono se disponen en los intersticios de la red de Fe-. La Ferrita- es magntica por debajo de los 770 C y amagntica por arriba de esta temperatura. Se suele distinguir entre la Ferrita- y la Ferrita- segn sea o no magntica. Como cristalogrficamente se trata del mismo constituyente, normalmente se habla simplemente de Ferrita. Es el constituyente ms blando de los aceros, teniendo una dureza promedio aproximada de 90 HB con unos 300 MPa de carga de rotura.
Cementita (Fe3C) Termodinmicamente es inestable, y en determinadas condiciones puede descomponerse dando 3Fe + grafito. Las condiciones cinticas requeridas para que tenga lugar esta descomposicin, requieren un nmero tan elevado de horas que, en la prctica, no se presenta nunca en los aceros binarios Fe-C. Sin embargo por prolongada permanencia a miles de horas a temperatura superiores a los 450 C, los aceros de bajo carbono o dbilmente aleados (por ejemplo C<0.15%, Mn<0.5%), grafitizan por descomposicin de cementita en ferrita + grafito. Es un compuesto frgil y es el constituyente ms duro de los aceros, con una dureza promedio aproximada de 68 HRC. Se presenta en celdas ortorrmbicas y es ferromagntica por debajo de los 210 C [3].
1.2 Cintica de la transformacin de la austenita Las microestructuras de los aceros son el resultado de la transformacin de la austenita durante un enfriamiento lento, la cual est asociada a la transformacin alotrpica por movimiento de los tomos de Fe a una difusin de C. Con C en solucin slida la transformacin de Fe- a Fe tiene lugar por encima de los 1394 C, siendo tanto ms alta esta temperatura cuanto mayor sea el contenido de C que el Fe presenta en solucin slida, dentro de ciertos lmites.
La transformacin austenita a ferrita se inicia por debajo de 912 C, siendo tanto ms baja esta temperatura cuando ms alto sea el contenido de C en la austenita. Para contenidos de C superiores a 0.77% la estabilizacin de la fase es tal que su transformacin alotrpica en no tiene lugar por lento enfriamiento hasta alcanzar los 727 C, cualquiera que sea el contenido de C superior a 0.77%.
Para ilustrar esto pueden analizarse los siguientes ejemplos de transformacin por enfriamiento lento: Austenita de 0.3% C Austenita de 1% C Austenita de 0.77% C Pudiendo observarse las transformaciones de fase claramente en la Fig. 1.1.
Fig. 1.1: Diagrama metaestable Fe-C
Austenita de 0.3% C A temperaturas superiores a los 912 C, la aleacin se halla por completo en estado . Disminuyendo la temperatura por debajo de 912 C, la austenita sigue an sin transformarse, siendo necesario llegar hasta una temperatura A3 para que pueda iniciarse la transformacin . Este comienzo de transformacin tiene lugar con incremento de volumen, lo cual permite determinar esta temperatura por medidas dilatomtricas. La transformacin no se realiza plenamente a A3, sino que a esta temperatura comienza la nucleacin de ferrita en las juntas del grano austentico, con migracin de C por difusin hacia el interior del grano. El centro del grano, por su mayor contenido en C, requerir una temperatura an menor para poder transformarse en . Al descender la temperatura, aumentar la proporcin de ferrita en los contornos del grano y disminuir la proporcin de austenita no transformada, enriquecida en C.
A 727 C quedar an sin transformar una tercera parte de la austenita original, la cual tiene ahora un contenido de C del 0.77% y es conocida como austenita binaria eutectoide. La transformacin de esta austenita se describe ms adelante.
Austenita de 1% C Al enfriar esta austenita desde altas temperaturas, la contraccin de la red cristalina da lugar a que el C disuelto aumente la distorsin del cristal, y a una dada temperatura Acm, la red se har inestable. Los tomos de C expulsados de la malla formarn la cementita, la cual comienza a nuclearse en las juntas del grano austentico, por reaccin con los tomos de Fe. El centro del grano austentico queda empobrecido en C y ser necesaria una disminucin de temperatura para que pueda producirse una nueva migracin de C hacia los contornos del grano. Este proceso contina durante el enfriamiento hasta que se alcanzan los 727 C, temperatura para la cual hay un 4% en peso de cementita en los contornos del grano, y la austenita remanente tiene un contenido en C del 0.77%.
Austenita de 0.77% C Una austenita con contenido inicial de C igual a 0.77% no experimenta ninguna transformacin por enfriamiento lento hasta alcanzar los 727 C. A esta temperatura, el C en solucin slida sobresaturada e inestable, emigra y empieza a formar ncleos de cementita en los contornos del grano de la austenita. Las zonas prximas a los grmenes de cementita se empobrecen en C y se transforman alotrpicamente en grmenes de ferrita. Los grmenes de cementita continan creciendo a expensas del C absorbido de la austenita contigua. El resultado es un conjunto de lminas de cementita flanqueadas por otras de ferrita que forman un constituyente complejo denominado perlita. La reaccin austenita ferrita + cementita recibe el nombre de reaccin eutectide. Los aceros binarios Fe-C se denominan Hipoeutectides o Hipereutectides segn si su contenido de C sea menor o mayor al 0.77%, respectivamente. Si una muestra de acero ordinario (de bajo carbono) en condiciones austenticas se enfra rpidamente hasta la temperatura ambiente, por ejemplo templndola en agua, su estructura cambiar de austenita a martensita.
La temperatura a la cual comienza esta transformacin se denomina inicio de martensita (MS) y la temperatura a la cual la transformacin termina se denomina fin de martensita (MF). La temperatura MS para aleaciones Fe-C disminuye a medida que aumenta el porcentaje en peso del carbono, y son distintos los tipos de martensitas que se forman dependiendo de este porcentaje.
Si bien la dureza de la martensita aumenta con este porcentaje debido a la alta concentracin de dislocaciones en las redes, su tenacidad disminuye.
1.3 Descomposicin isotrmica de la austenita Las transformaciones isotrmicas de aceros eutectoides a las temperaturas entre 723 C y alrededor de 550 C producen microestructuras perlticas. A medida que la temperatura de la transformacin disminuye en este intervalo, la perlita adopta morfologas diferentes que suelen conocerse por los nombres de perlita gruesa, perlita fina (sorbita) y trostita.
Perlita gruesa: se forma entre 650 C y 727 C, est constituida por lminas alternas de ferrita y cementita separadas entre s de 0.25 m a 0.5 m y su resistencia es de unos 800 MPa.
Perlita fina: se forma entre 600 C y 650 C, est constituida por lminas alternas de ferrita y cementita separadas entre s de 0.1 m a 0.2 m y su resistencia est entre 900 MPa y 1400 MPa. Trostita: se forma entre 500 C y 600 C, tiene una estructura muy fina, prcticamente irresoluble al microscopio ptico, con distancia interlaminares del orden 0.1 m. y su resistencia est entre 1400 MPa y 1750 MPa. Su dureza est comprendida entre 400 HB y 500 HB. Si el acero eutectoide se enfra en el rango de 550 C a 250 C y se transforma de forma isotrmica, se produce una estructura intermedia entre perlita y martensita llamada bainita, como se ve en la Fig. 1.2. Su dureza oscila entre 40 HRC y 60 HRC. Algunos aceros presentan una neta frontera de temperatura entre las transformaciones perltica y baintica, pudindose definir una temperatura BS. Por debajo de ella la frontera vara linealmente con los porcentajes de elementos aleantes. La Fig. 1.3 muestra el diagrama de enfriamiento continuo para un acero no aleado eutectoide. Si la velocidad de enfriamiento es muy lenta, se obtiene perlita gruesa. Esto puede suceder si se deja la pieza en el horno, dejando que se enfre con l. Si la velocidad es un poco mayor, por ejemplo enfriando con aire esttico, se obtiene perlita blanda o fina. Y si la velocidad es tan alta que la curva de enfriamiento no corta en ningn punto a la curva del diagrama TTT (transformacin tiempo-temperatura), se obtiene estructura martenstica (acero templado). Se denomina velocidad crtica de temple (VC) a la mnima velocidad de enfriamiento requerida para evitar la transformacin de la austenita en otros constituyentes antes de alcanzar la temperatura MS.
Fig. 1.2: Diagrama de transformacin isotrmica para un acero de carbono ordinario eutectide mostrando su relacin con el diagrama de fases Fe-Fe3C.
Fig. 1.3: Diagrama de enfriamiento continuo para un acero no aleado eutectide
Existen varias diferencias evidentes entre los diagramas isotrmicos para un acero eutectoide y para otro Hipoeutectides. Una de estas diferencias es que las curvas TTT del acero Hipoeutectides estn desplazadas hacia la izquierda, por lo cual no es posible templar este acero dentro de la regin de la austenita para producir una estructura completamente de martensita, como puede observarse en la Fig. 1.4.
Fig.1.4: Diagrama de transformacin isotrmica de una acero Hipoeutectides que contienen 0.47% C y 0.57 % Mn, austenizado a una temperatura de 843 C.
En general cualquier elemento que forme solucin slida con la austenita ya sea de sustitucin (Mn, Ni,Cr, etc.) o bien de insercin (B, N, etc.) retrasa las transformaciones isotrmicas tanto perlticas como bainticas, debido a que ejercen una barrera para la difusin del C. Para aceros Hipoeutectides, la influencia del carbono es similar a la de cualquier elemento, por lo que las transformaciones perlticas y bainticas tardan ms en realizarse cuanto mayor sea el contenido de carbono.
Referencias 1. V. Zev: "Tratamiento trmico de metales", Editorial Mir Mosc, 1986. 2. W.F. Smith: "Fundamentos de la Ciencia e Ingeniera de Materiales", Mac Graw-Hill, 1993. 3. J.A. Pero-Sanz Elorz: "Ciencia e Ingeniera de Materiales - Metalurgia Fsica: estructura y propiedades", Dossat, 1992. 4. G. Snchez Sarmiento, M. A. Morelli y J. Vega: "Improvements to the SAE J406 Hardenability Predictor". R. Cols et al, Editors: Proceedings of the 1st. International Automotive Heat Treating Conference, ASM International, Puerto Vallarta, Mxico, 12-15, Julio de 1998, pp 401414. 5. G. Snchez Sarmiento, G.E. Totten, G.M. Webster y E. Mues: "Computational determination of heat transfer coefficients of aqueous polyalkylene glycols bath solutions in quenching
operations", Proceedings of the 16th ASM Heat Treating Conference and Exposition , Cincinnati, Ohio, USA, March 12-16, 1996. 6. G. Snchez Sarmiento, C. Barragn, E. Mues y C.Bunte: "Aplication of computer models to the determination of the heat transfer coefficients of UCON quenchant soluctions in heat treating operations". Proceedings of the 2nd International Conference on Quenching and the control of Distorsion, Cleveland, Ohio, November 4-7, 1996. 7. G. Strang y G. Fix: "An analysis of the finite element method", 1973. 8. F. G. Basombro y B. Cruz: "Ecuacin cuasiarmnica con derivada temporal. Su resolucin por el mtodo de Faedo-Galerkin con elementos finitos (programas CTR y CTR1)". CNEA-NT 30/78. Centro Atmico Bariloche. Marzo de 1977. 9. G. Snchez Sarmiento, A. Gastn y J. Vega: "INDUCTER-B: A finite element phase transformation model of induction heat treating of steels sensitive to its chemical composition", Proceedings of the 1st. International Conference on Induction Heat Treating, Indianapolis, USA, 5-18, September 1997. 10. P. K. Agarwal y J. K. Brimacombe: "Mathematical model of heat flow of austenite - perlite transformation in eutectoid carbon steel rods for wire", Metall. Transc., 12 B, 121-133 (1980). 11. G. Snchez Sarmiento, M. Castro: "INC-PHATRAN: Modelo computacional para la simulacin del proceso de tratamiento trmico - Manual del Usuario". Julio de 2001.
You might also like
- Transformaciones de Los Aceros en Estado SólidoDocument37 pagesTransformaciones de Los Aceros en Estado SólidoAle GeiNo ratings yet
- Diagrama Aceros FundicionesDocument19 pagesDiagrama Aceros FundicionesevarlysNo ratings yet
- Aleaciones de CobreDocument24 pagesAleaciones de CobrePablo ValloryNo ratings yet
- Propiedades Mecanicas de Los Microconstituyentes Del AceroDocument16 pagesPropiedades Mecanicas de Los Microconstituyentes Del AceroFreire SonNo ratings yet
- Corrosión TrabajoDocument10 pagesCorrosión TrabajoFernando LópezNo ratings yet
- Fe+C FasesDocument10 pagesFe+C FasesCristian ZavaletaNo ratings yet
- Metalurgia de La SoldaduraDocument43 pagesMetalurgia de La SoldaduraCarlos German Mamani PizarroNo ratings yet
- 2201-Mendoza Rodriguez-Tecmatdiagrama de Fases de Hierro CarbonoDocument31 pages2201-Mendoza Rodriguez-Tecmatdiagrama de Fases de Hierro CarbonoAlexis Mendoza RodriguezNo ratings yet
- Nomenclatura de La Estructura Del BuqueDocument122 pagesNomenclatura de La Estructura Del Buquepatricio-1703No ratings yet
- Metalurgia Soldabilidad Aceros (Modo de Compatibilidad)Document66 pagesMetalurgia Soldabilidad Aceros (Modo de Compatibilidad)Andres PozoNo ratings yet
- Aleaciones HierroDocument14 pagesAleaciones HierroGerman OrtegaNo ratings yet
- Informe de Diagrama de Hierro de Carbono y Otras DefinicionesDocument9 pagesInforme de Diagrama de Hierro de Carbono y Otras DefinicionesneyzaNo ratings yet
- Acero y Sus Tratamientos TermicosDocument10 pagesAcero y Sus Tratamientos TermicosMayra Fierro100% (1)
- Equipo 5Document48 pagesEquipo 5nbeyrutNo ratings yet
- Diagrama HierroDocument8 pagesDiagrama Hierropineda1505No ratings yet
- Diagrama Hierro-CarbonoDocument28 pagesDiagrama Hierro-CarbonoEDISON IDROVONo ratings yet
- Diagrama Fe CDocument12 pagesDiagrama Fe CDei DavisNo ratings yet
- Acerotratamientoscorrosion PDFDocument19 pagesAcerotratamientoscorrosion PDFpudetoNo ratings yet
- Diagrama Hierro-CarbonoDocument5 pagesDiagrama Hierro-CarbonoMichelle RosadoNo ratings yet
- FERRITADocument35 pagesFERRITARuben Paguay100% (2)
- DIAGRAMA Fe-CDocument18 pagesDIAGRAMA Fe-CSebastian AlbornosNo ratings yet
- Aleaciones FerrosasDocument21 pagesAleaciones FerrosasCamilo AulestiaNo ratings yet
- Diagrama IsomorfoDocument5 pagesDiagrama IsomorfoJordan Muñoz Garcia50% (2)
- Unidad 2Document39 pagesUnidad 2Daniel FerminNo ratings yet
- Diagrama Hierro CarbonoDocument20 pagesDiagrama Hierro CarbonoJhon AcevedoNo ratings yet
- Aleaciones de HierroDocument15 pagesAleaciones de HierroJONTERNo ratings yet
- Practica 6Document10 pagesPractica 6Daniel TorresNo ratings yet
- Apuntes MaterialesDocument44 pagesApuntes Materialeswjosel100% (1)
- Tratamientos Termicos Estudiar MasDocument23 pagesTratamientos Termicos Estudiar MasJose CastroNo ratings yet
- Lab Tratamientos TermicosDocument10 pagesLab Tratamientos TermicosDiego Cornejo MoralesNo ratings yet
- Introducción de La MetalografiaDocument37 pagesIntroducción de La MetalografiaRody Williams Curasma VillalvaNo ratings yet
- Diagrama Hierro CarbonoDocument14 pagesDiagrama Hierro CarbonoAnibal Vp100% (1)
- Diagramas de Fase en El Diagrama Hierro CarbonoDocument27 pagesDiagramas de Fase en El Diagrama Hierro CarbonoJorge Enrique SalazarNo ratings yet
- Diagrama Fe-C y Sus AleacionesDocument26 pagesDiagrama Fe-C y Sus AleacionesGerman Felipe ColiboroNo ratings yet
- Tecnología Del AceroDocument8 pagesTecnología Del AceroArthur VelasquezNo ratings yet
- DIAGRAMA Fe IntroducciónDocument13 pagesDIAGRAMA Fe IntroducciónCARLOS ALFREDO ASCANOA BEJARANONo ratings yet
- MetalografiaDocument7 pagesMetalografiaAnonymous DFBpy30ANo ratings yet
- APUNTES DE ALEACIONES Fe-CDocument30 pagesAPUNTES DE ALEACIONES Fe-Cfranciscobermudez211202No ratings yet
- Diagrama Hierro CarbonoDocument23 pagesDiagrama Hierro CarbonoMariano PoloiuiopolNo ratings yet
- Fe CDocument0 pagesFe CStefanny DánicaNo ratings yet
- 10.2 Diagrama Fe-CDocument13 pages10.2 Diagrama Fe-CRoberto López PáezNo ratings yet
- 06 Metalurgia Del AceroDocument47 pages06 Metalurgia Del Aceroquerero7No ratings yet
- Diagrama de Fases Hierro CarbonoDocument16 pagesDiagrama de Fases Hierro CarbonoMichel BenzoNo ratings yet
- ACEROSDocument30 pagesACEROSSuair DiazNo ratings yet
- El Hierro Tecnicamente PuroDocument10 pagesEl Hierro Tecnicamente PuroValhia Loarte SanaNo ratings yet
- Unidad 2 Fundamentos Materiales Clase 7Document55 pagesUnidad 2 Fundamentos Materiales Clase 7bryanNo ratings yet
- Taller Metales y AleacionesDocument12 pagesTaller Metales y AleacionesBrayan AriasNo ratings yet
- Diagrama TTT y Fases Del Fe CDocument10 pagesDiagrama TTT y Fases Del Fe CHayram PatracaNo ratings yet
- Principios Basicos de MetalurgiaDocument12 pagesPrincipios Basicos de Metalurgiaroberto vioesNo ratings yet
- DIAGRAMA HIERRO CARBONO Fe) PDFDocument11 pagesDIAGRAMA HIERRO CARBONO Fe) PDFCarlos Armando Valdivia TrigosoNo ratings yet
- Ley Diagrama VeranoDocument11 pagesLey Diagrama VeranoJOAN RODOLFO PURIS CoNDORNo ratings yet
- Ensayo Diagrama Hierro CarbonoDocument14 pagesEnsayo Diagrama Hierro CarbonoRíos AlbertoNo ratings yet
- PROBLEMAS Fe CDocument18 pagesPROBLEMAS Fe CRoberto PayaNo ratings yet
- Transformacion Bajo Enfriamiento ContinuoDocument4 pagesTransformacion Bajo Enfriamiento ContinuoGian Herrera herreraNo ratings yet
- Clasificación Aceros y Tratamientos TérmicosDocument7 pagesClasificación Aceros y Tratamientos TérmicosÁlvaro Díaz AlfaroNo ratings yet
- Ingeniería de procesos siderúrgicos: La experiencia de AHMSAFrom EverandIngeniería de procesos siderúrgicos: La experiencia de AHMSANo ratings yet
- Bladesmithing: Secretos del tratamiento térmico de la forja de cuchillosFrom EverandBladesmithing: Secretos del tratamiento térmico de la forja de cuchillosNo ratings yet
- Oficios Artísticos. Forja: Las técnicas de la forja explicadas paso a pasoFrom EverandOficios Artísticos. Forja: Las técnicas de la forja explicadas paso a pasoRating: 5 out of 5 stars5/5 (1)
- Soldadura en el montaje de tuberías. FMEC0108From EverandSoldadura en el montaje de tuberías. FMEC0108Rating: 3.5 out of 5 stars3.5/5 (3)
- Bladesmithing; Cuchillería a partir de chatarra: Cómo fabricar cuchillos con ballestas, cables, clavos de vías férreas y limasFrom EverandBladesmithing; Cuchillería a partir de chatarra: Cómo fabricar cuchillos con ballestas, cables, clavos de vías férreas y limasNo ratings yet
- Procedimiento Instalacion de Pararrayos Compressed PDFDocument7 pagesProcedimiento Instalacion de Pararrayos Compressed PDFDaniela Angelica Ali BellidoNo ratings yet
- Endurecimiento Por DeformaciónDocument10 pagesEndurecimiento Por Deformaciónuriel9515No ratings yet
- Metodo FangerDocument6 pagesMetodo FangerJulioAdahiltonVideaCarmonaNo ratings yet
- Cinetica Solido Trabajo Conservacion Grupo 7 WordDocument50 pagesCinetica Solido Trabajo Conservacion Grupo 7 WordCristhian Nc0% (1)
- Inversión de Onda Senoidal PuraDocument31 pagesInversión de Onda Senoidal PuraHugo PomaresNo ratings yet
- El Experimento de La Presión y La VelaDocument4 pagesEl Experimento de La Presión y La VelaALVARO100% (1)
- Diferencias de Iluminacion Entre Cine Television y VideoDocument4 pagesDiferencias de Iluminacion Entre Cine Television y VideoJose Luis Vacaflor100% (1)
- Taller de CarpinteriaDocument35 pagesTaller de CarpinteriaurielrockNo ratings yet
- Sulfato Suelos 16.12 (2) .XlsokDocument5 pagesSulfato Suelos 16.12 (2) .XlsokGean Carlos Tuesta VillacortaNo ratings yet
- Capitulo 2 Materia y EnergiaDocument20 pagesCapitulo 2 Materia y Energiaresumen futNo ratings yet
- Cadenas de RodillosDocument13 pagesCadenas de RodillosalfredoNo ratings yet
- Telurio Revisado PDFDocument4 pagesTelurio Revisado PDFAmy NakamatsuNo ratings yet
- Nivelación TopográficaDocument9 pagesNivelación Topográficajuan100% (1)
- Apuntes Q IIDocument79 pagesApuntes Q IIIsidro Gonzalez ParraNo ratings yet
- 10 Fiscia CEPRE - Setiembre - Diciembre 2013Document4 pages10 Fiscia CEPRE - Setiembre - Diciembre 2013William Taipe100% (1)
- 109 111 TrigoDocument3 pages109 111 TrigosdafdfsfdsafhfghgfNo ratings yet
- Tema5. Fuentes de Corriente y Cargas Activas.Document14 pagesTema5. Fuentes de Corriente y Cargas Activas.saiwor100% (3)
- Cojines WeberDocument52 pagesCojines Weberjose100% (1)
- TransformadorDocument26 pagesTransformadormarylianaNo ratings yet
- Mecánica Automotriz - Unidad 7Document22 pagesMecánica Automotriz - Unidad 7Tony VIDALESNo ratings yet
- Manual Tecnico RWTMDocument47 pagesManual Tecnico RWTMJoseph War100% (3)
- Tarea Preparatoria 1er Parcial Resistencia de Los MaterialesDocument2 pagesTarea Preparatoria 1er Parcial Resistencia de Los MaterialesSamuel Contreras0% (1)
- Generacion de Los Rayos XDocument14 pagesGeneracion de Los Rayos XwilsonNo ratings yet
- Accidentes de Transito-TeoríaDocument8 pagesAccidentes de Transito-TeoríaCeic Civil Tres DNo ratings yet
- Guia Producto Marlon STDocument41 pagesGuia Producto Marlon STMailson Apaza KatataNo ratings yet
- Proyección DiedricaDocument26 pagesProyección DiedricaLendys Jose Melean ReañoNo ratings yet
- Definicion de Amperes Voltage IntencidadDocument18 pagesDefinicion de Amperes Voltage IntencidadRoberto Mamani HuillcaNo ratings yet
- Tipos de PercepcionDocument5 pagesTipos de PercepcionSami MoralesNo ratings yet
- ProalgDocument4 pagesProalgAnonymous unHFWYTFNo ratings yet