Professional Documents
Culture Documents
Chemistry Paper 3
Uploaded by
A. SuhaimiOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Chemistry Paper 3
Uploaded by
A. SuhaimiCopyright:
Available Formats
SULIT 2 4541/3 2
1 A group of students carried out an experiment to investigate the effect of type of electrodes
when aqueous copper(II) chloride solution is electrolysed.
The electrolysis was first carried out by using carbon electrodes.
Both the electrodes were weighed.
Copper(II) chloride solution was electrolysed for 45 minutes.
Then both the carbon electrodes were weighed again.
The experiment was repeated by replacing carbon electrodes with copper electrodes.
Sekumpulan pelajar menjalankan eksperimen untuk mengkaji kesan jenis elektrod apabila
larutan akueus kuprum(II) klorida dielektrolisis.
Elektrolisis dimulakan dengan menggunakan elektrod karbon.
Kedua-dua elektrod karbon itu ditimbang.
Larutan kuprum(II) klorida dielektrolisis selama 45 minit.
Kemudian kedua-dua elektrod karbon ditimbang semula.
Eksperimen itu diulang dengan menggantikan elektrod-elektrod karbon dengan elektrod-
elektrod kuprum.
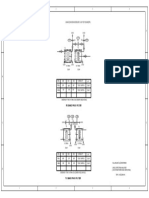
Diagram 1.1 shows the set-up of apparatus used for the electrolysis of copper(II) chloride
solution using carbon electrodes.
Rajah 1.1 menunjukkan susunan radas bagi elektrolisis larutan kuprum(II) klorida
menggunakan elektrod-elektrod karbon.
Beginning of the experiment After 45 minutes
Permulaan eksperimen. Selepas 45 minit
A A
Carbon electrodes
Copper(II) chloride solution
(blue in colour)
Diagram 1.1
4541/3 [Lihat sebelah
SULIT
SULIT 3 4541/3 3
Diagram 1.2 shows the set-up of apparatus for the electrolysis of copper(II) chloride
solution using copper electrodes.
Rajah 1.2 menunjukkan susunan radas bagi elektrolisis larutan kuprum(II) klorida
menggunakan elektrod-elektrod kuprum.
Beginning of the experiment After 45 minutes
Permulaan eksperimen. Selepas 45 minit
A A
Copper electrodes
Copper(II) chloride solution
(blue in colour)
Diagram 1.2
(a) Write the observation and inference obtained at the carbon anode and both the
copper electrodes during the electrolysis.
Tuliskan pemerhatian dan inferens yang diperolehi pada anod karbon dan kedua-
dua elektrod kuprum semasa elektrolisis itu.
Type of electrodes Observations Inference
Jenis elektrod Pemerhatian Inferens
Carbon anode
Anod karbon
Copper anode
Anod kuprum
Copper cathode
Katod kuprum
[6 marks]
4541/3 [Lihat sebelah
SULIT
SULIT 4 4541/3 4
(b) Based on the experiment, state
Berdasarkan eksperimen, nyatakan
(i) the manipulated variable.
pemboleh ubah yang dimanipulasikan.
…………………………………………………………………………..………………
(ii) the responding variable.
pemboleh ubah yang bergerak balas.
…………………………………….…………………………………………………….
(iii) the constant variable.
pemboleh ubah yang dimalarkan.
…………………………………………………………………………………………..
[3 marks]
(c) State the hypothesis for the experiment.
Nyatakan hipotesis bagi eksperimen ini.
…………………………………………………………………………………………
…………………………………………………………………………………………
[3 marks]
(d) Based on the experiment in Diagram 1.1, state the colour change of the copper(II)
chloride solution after 45 minutes.
Berdasarkan eksperimen dalam Rajah 1.1,nyatakan perubahan warna larutan
kuprum(II) klorida selepas 45 minit.
…………………………………………………………………………………………
…………………………………………………………………………………………
[3 marks]
(e) Classify all the ions present in copper(II) chloride solution into cations and anions.
Kelaskan semua ion yang hadir dalam larutan kuprum(II) klorida kepada kation dan
anion.
[3 marks]
4541/3 [Lihat sebelah
SULIT
SULIT 5 4541/3 5
2 A student carried out an experiment to determine the end-point for the titration of 25.0 cm3 of
1.0 mol dm-3 sodium hydroxide solution with 1.0 mol dm-3 hydrochloric acid. Phenolphthalein is
used as the acid-base indicator. Hydrochloric acid is added until the end-point of titration is
reached.
Table 1 shows the three burette readings for the titrations that have been conducted.
Seorang pelajar menjalankan satu eksperimen untuk menentukan takat akhir bagi pentitratan
antara 25 cm3 1.0 mol dm-3 larutan natrium hidroksida dengan 1.0 mol dm-3 asid hidroklorik.
Fenolftalein digunakan sebagai penunjuk asid – bes. Asid hidroklorik ditambah sehingga takat
akhir pentitratan tercapai.
Jadual 1 menunjukkan tiga bacaan buret bagi pentitratan yang telah dijalankan.
Titration no. I II III
0 13 25
Initial burette
reading 1 14 26
Bacaan awal
burette
2 15 27
……………...... ……………...... ……………...... 25
12 25 38
26
Final burette 13 26 39
reading
27
Bacaan akhir
burette
14 27 40
……………...... ……………...... ……………......
Table 1
4541/3 [Lihat sebelah
SULIT
SULIT 6 4541/3 6
4541/3 [Lihat sebelah
SULIT
SULIT 7 4541/3 7
(a) Record the burette readings for the three titrations in the spaces provided in Table 1.
Rekodkan bacaan buret untuk ketiga-tiga pentitratan di ruang yang disediakan dalam
Jadual 1
[3 marks]
(b) Construct a table and record the initial burette reading, final burette reading and the volume
of acid used for each titration.
Bina satu jadual dan rekodkan bacaan awal buret, bacaan akhir buret dan isipadu asid
yang digunakan untuk setiap pentitratan.
[3 marks]
(c) Calculate the average volume of hydrochloric acid used in the experiment.
Hitungkan isipadu purata asid hidroklorik yang digunakan dalam eksperimen tersebut.
[3 marks]
(d) If the experiment is repeated by replacing 1.0 mol dm-3 of hydrochloric acid with
1.0 mol dm-3 of sulphuric acid, predict the volume of sulphuric acid needed to reach the end-
point of titration.
Jika eksperimen itu diulang dengan menggantikan 1.0 mol dm-3 asid hidroklorik dengan
1.0 mol dm-3 asid sulfurik, ramalkan isipadu asid sulfurik yang diperlukan untuk mencapai
takat akhir pentitratan.
………………………………………...………………………………………………………..
[3 marks]
(e) Give the operational definition for the end-point of titration.
Beri definisi secara operasi bagi takat akhir pentitratan.
.....................................................................................................................................................
.....................................................................................................................................................
[3 marks]
4541/3 [Lihat sebelah
SULIT
SULIT 8 4541/3 8
3 The equation represents the decomposition of hydrogen peroxide.
Persamaan di bawah mewakili tindak balas penguraian hidrogen peroksida.
2H2O2 2H2O + O2
The rate of decomposition of hydrogen peroxide can be increased by adding
manganese(IV) oxide powder which acts as a catalyst.
Plan a laboratory experiment to investigate the effect of catalyst on the decomposition of
hydrogen peroxide.
Kadar penguraian hidrogen peroksida boleh ditingkatkan dengan menambah serbuk
mangan(IV) oksida yang bertindak sebagai mangkin.
Rancang satu eksperimen dalam makmal untuk mengkaji kesan mangkin ke atas kadar
penguraian hidrogen peroksida.
Your planning should include the following:
Perancangan anda hendaklah mengandungi perkara-perkara berikut:
(a) Problem statement
Pernyataan masalah
(b) All the variables
Semua pembolehubah
(c) Statement of the hypothesis
Pernyataan hipotesis
(d) List of substances and apparatus
Senarai bahan dan radas
(e) Procedure of the experiment
Prosedur eksperimen
(f) Tabulation of data
Penjadualan data
[17 marks]
END OF QUESTION PAPER
4541/3 [Lihat sebelah
SULIT
You might also like
- Effect of Electrodes on Copper Chloride ElectrolysisDocument27 pagesEffect of Electrodes on Copper Chloride ElectrolysisHafizoh HarunNo ratings yet
- Section A: SPM Chemistry Set 5 Paper 2Document18 pagesSection A: SPM Chemistry Set 5 Paper 2Jaaizah JaafarNo ratings yet
- Bengkel Ambang SPM 2009 Kertas 3Document28 pagesBengkel Ambang SPM 2009 Kertas 3rajhiniNo ratings yet
- Paper 3 2009Document13 pagesPaper 3 2009Muhammad AzmilNo ratings yet
- Determining Concentration of HCl Through TitrationDocument11 pagesDetermining Concentration of HCl Through Titrationkhangsiean89No ratings yet
- SPM Mid Year 2008 SBP Chemistry Paper 3Document10 pagesSPM Mid Year 2008 SBP Chemistry Paper 3ChinWynn.comNo ratings yet
- Electrochemistry Paper 2Document27 pagesElectrochemistry Paper 2Siti Aishah ZolkanainNo ratings yet
- Electrochemical Series ExperimentDocument10 pagesElectrochemical Series Experimentteruna21No ratings yet
- Jawab Semua Soalan.: Set 1 Set IIDocument7 pagesJawab Semua Soalan.: Set 1 Set IIFadzil RashidNo ratings yet
- Cambridge Ordinary LevelDocument24 pagesCambridge Ordinary LevelDennis MuzilaNo ratings yet
- Kimia P3 SBP Mid Year SPM 2008Document30 pagesKimia P3 SBP Mid Year SPM 2008adeebsparkNo ratings yet
- Kimia3 (1) MRSMDocument12 pagesKimia3 (1) MRSMMuhammad NaharNo ratings yet
- Cambridge O Level: CHEMISTRY 5070/42Document16 pagesCambridge O Level: CHEMISTRY 5070/42Maryam ShahidNo ratings yet
- Chemist f5 Paper 3 2015Document7 pagesChemist f5 Paper 3 2015putri_latifahNo ratings yet
- Set 1 Paper 2Document22 pagesSet 1 Paper 2fadliehaliemNo ratings yet
- Rate of Reaction Experiment Sodium ThiosulphateDocument9 pagesRate of Reaction Experiment Sodium ThiosulphateMiesya87No ratings yet
- University of Cambridge International Examinations General Certificate of Education Ordinary LevelDocument20 pagesUniversity of Cambridge International Examinations General Certificate of Education Ordinary LevelDennis MuzilaNo ratings yet
- 0620 s18 QP 43Document16 pages0620 s18 QP 43mostafa barakatNo ratings yet
- KIMIA Kertas 2 4541/2: Elektrod PemerhatianDocument2 pagesKIMIA Kertas 2 4541/2: Elektrod PemerhatiandranasridNo ratings yet
- Gerak Gempur Chemistry Paper 3Document8 pagesGerak Gempur Chemistry Paper 3Arvinth Guna SegaranNo ratings yet
- Worksheet On KineticsDocument4 pagesWorksheet On KineticsOlesha Janae CarterNo ratings yet
- Heat of Neutralization Experiment ResultsDocument4 pagesHeat of Neutralization Experiment Resultssuzana22No ratings yet
- Electrolysis of Copper (II) Chloride Solution (40Document17 pagesElectrolysis of Copper (II) Chloride Solution (40Fika KarimNo ratings yet
- Structure and Properties of AtomsDocument35 pagesStructure and Properties of Atomsija0% (2)
- Maklumat Untuk Calon: Information For CandidateDocument9 pagesMaklumat Untuk Calon: Information For CandidateJue MayaNo ratings yet
- ExamDocument16 pagesExamquimicosorioNo ratings yet
- Empirical and Molecular Formulas of Chemical CompoundsDocument31 pagesEmpirical and Molecular Formulas of Chemical Compoundsintan noraisyahNo ratings yet
- Chemistry, C6A Electrolysis (S)Document30 pagesChemistry, C6A Electrolysis (S)Farah Aisyah Ahmad100% (1)
- Chem Prac 2Document12 pagesChem Prac 2ali zaibNo ratings yet
- November 2015 (v1) QP - Paper 3 CIE Chemistry IGCSEDocument12 pagesNovember 2015 (v1) QP - Paper 3 CIE Chemistry IGCSEManya KakrooNo ratings yet
- SULIT 4541/2 Kimia Kertas 2 2017Document26 pagesSULIT 4541/2 Kimia Kertas 2 2017Arvin DiNozzoNo ratings yet
- Kimia Form5 k3Document6 pagesKimia Form5 k3Sabri IbrahimNo ratings yet
- Cambridge Ordinary LevelDocument20 pagesCambridge Ordinary LevelAziha MahmudNo ratings yet
- Paper 3 CHEM Form 4 P1 2016Document7 pagesPaper 3 CHEM Form 4 P1 2016Phang Hui KienNo ratings yet
- Chemistry Paper 2 Questions PDF August 24 2011-12-50 PM 472kDocument22 pagesChemistry Paper 2 Questions PDF August 24 2011-12-50 PM 472kJamaludin Abu KassimNo ratings yet
- Cambridge International General Certificate of Secondary EducationDocument16 pagesCambridge International General Certificate of Secondary EducationDark GreenNo ratings yet
- SPM 2004 BM Bi K2Document19 pagesSPM 2004 BM Bi K2henfinNo ratings yet
- 2009 HCI Prelim P2Document15 pages2009 HCI Prelim P2Felicia LimNo ratings yet
- Kertas 2 Pep Akhir Tahun Ting 4 Terengganu 2018 - SoalanDocument19 pagesKertas 2 Pep Akhir Tahun Ting 4 Terengganu 2018 - SoalaniswaniswanNo ratings yet
- Observing and Making Inference in Science ExperimentsDocument23 pagesObserving and Making Inference in Science ExperimentsRoslizawani WanieyNo ratings yet
- Bengkel Ambang SPM 2009 Kertas 3Document27 pagesBengkel Ambang SPM 2009 Kertas 3Shida BaharNo ratings yet
- 2021 CJC H2 CHEM Prelim P2 QPDocument20 pages2021 CJC H2 CHEM Prelim P2 QPclarissa yeoNo ratings yet
- 09 JJ H2 Prelim P2Document15 pages09 JJ H2 Prelim P2etherfoxxNo ratings yet
- Soalan Struktur Dan EseiDocument31 pagesSoalan Struktur Dan EseiShukor Sudin100% (1)
- Latihan PDPR Kimia SPM 2021 Pada 21 AprilDocument8 pagesLatihan PDPR Kimia SPM 2021 Pada 21 Aprilexo kaihunNo ratings yet
- Ulangkaji Soalan Midyear f5 - ActualDocument20 pagesUlangkaji Soalan Midyear f5 - ActualnurulizzahNo ratings yet
- Section A Chemistry RevisionDocument27 pagesSection A Chemistry RevisionAzalida Md YusofNo ratings yet
- Cambridge International General Certificate of Secondary EducationDocument12 pagesCambridge International General Certificate of Secondary EducationJaden HalkNo ratings yet
- STPM Percubaan 2008 Sabah Chemistry Paper 2Document13 pagesSTPM Percubaan 2008 Sabah Chemistry Paper 2ChinWynn.com100% (1)
- An SEO-Optimized Title for a Chemistry Experiment DocumentDocument8 pagesAn SEO-Optimized Title for a Chemistry Experiment Documentamin_zamanNo ratings yet
- Module 5A Electrochemistry I - PKIIIDocument6 pagesModule 5A Electrochemistry I - PKIIIMohd HafiezNo ratings yet
- SPM Chemistry Paper 2Document19 pagesSPM Chemistry Paper 2AnneLeongNo ratings yet
- Kertas 2Document21 pagesKertas 2NURUL SALEHAH BINTI MOHD YUSOF MoeNo ratings yet
- Cambridge International AS & A Level: CHEMISTRY 9701/52Document12 pagesCambridge International AS & A Level: CHEMISTRY 9701/52Emmanuel Antwi-BuasiakoNo ratings yet
- Endohedral Metallofullerenes: Fullerenes with Metal InsideFrom EverandEndohedral Metallofullerenes: Fullerenes with Metal InsideNo ratings yet
- International Thermodynamic Tables of the Fluid State: Propylene (Propene)From EverandInternational Thermodynamic Tables of the Fluid State: Propylene (Propene)No ratings yet
- Novel Carbon Materials and Composites: Synthesis, Properties and ApplicationsFrom EverandNovel Carbon Materials and Composites: Synthesis, Properties and ApplicationsXin JiangNo ratings yet
- Unusual Structures and Physical Properties in Organometallic ChemistryFrom EverandUnusual Structures and Physical Properties in Organometallic ChemistryNo ratings yet
- Physical quantity S.I. unitDocument7 pagesPhysical quantity S.I. unitA. SuhaimiNo ratings yet
- Introduction To PhysicsDocument30 pagesIntroduction To PhysicsA. SuhaimiNo ratings yet
- Worksheet (Vernier Calipers / Micrometer Screw Gauge)Document6 pagesWorksheet (Vernier Calipers / Micrometer Screw Gauge)A. SuhaimiNo ratings yet
- Exercise 1Document1 pageExercise 1A. SuhaimiNo ratings yet
- Jadual SpotchekDocument1 pageJadual SpotchekA. SuhaimiNo ratings yet
- Ting 4 P2 Trial 2015 Fizik SPMDocument72 pagesTing 4 P2 Trial 2015 Fizik SPMA. SuhaimiNo ratings yet
- PK 1 F 42016Document21 pagesPK 1 F 42016A. SuhaimiNo ratings yet
- Score: . ./24 X 100 . %Document2 pagesScore: . ./24 X 100 . %A. SuhaimiNo ratings yet
- Pressure Forces and EffectsDocument72 pagesPressure Forces and EffectsA. SuhaimiNo ratings yet
- Exercise 4Document2 pagesExercise 4A. SuhaimiNo ratings yet
- Exercise 3Document2 pagesExercise 3A. SuhaimiNo ratings yet
- Chapter 5 Teleskop MikroskopDocument39 pagesChapter 5 Teleskop MikroskopA. SuhaimiNo ratings yet
- Understanding Science and TechnologyDocument10 pagesUnderstanding Science and TechnologyA. SuhaimiNo ratings yet
- Metre Rule /pembaris Meter: Measuring Instrument Smallest Scale Division Accuracy The MeasurementDocument3 pagesMetre Rule /pembaris Meter: Measuring Instrument Smallest Scale Division Accuracy The MeasurementA. SuhaimiNo ratings yet
- SPM 2014 Trial Exam T4 Revision QuestionsDocument15 pagesSPM 2014 Trial Exam T4 Revision QuestionsA. Suhaimi100% (1)
- Ramalan Paper 2 Bahagian B C Fizik SPM 2014 Analisis Sejak 2004Document3 pagesRamalan Paper 2 Bahagian B C Fizik SPM 2014 Analisis Sejak 2004A. SuhaimiNo ratings yet
- PP1 Bahagian A 2017Document15 pagesPP1 Bahagian A 2017A. SuhaimiNo ratings yet
- Get Logik - Class 6Document4 pagesGet Logik - Class 6A. SuhaimiNo ratings yet
- Ramalan Paper 2 Bahagian B C Fizik SPM 2014 Analisis Sejak 2004Document3 pagesRamalan Paper 2 Bahagian B C Fizik SPM 2014 Analisis Sejak 2004A. SuhaimiNo ratings yet
- Skima TrialDocument2 pagesSkima TrialA. SuhaimiNo ratings yet
- RSL Sains Sem 3 Non Tek.Document9 pagesRSL Sains Sem 3 Non Tek.A. SuhaimiNo ratings yet
- Elektrik K2BhgCK3BhgB PelajarDocument2 pagesElektrik K2BhgCK3BhgB PelajarA. SuhaimiNo ratings yet
- Modul KSK Semester 1 Dan 3 Tahun 2014Document1 pageModul KSK Semester 1 Dan 3 Tahun 2014A. SuhaimiNo ratings yet
- Tip Kertas 3Document9 pagesTip Kertas 3A. SuhaimiNo ratings yet
- Inovasi 4 Electricity - Electromotive Force Emf Form 5 Scheme 2015Document7 pagesInovasi 4 Electricity - Electromotive Force Emf Form 5 Scheme 2015A. SuhaimiNo ratings yet
- Bab1FizikSPM Pelajar EditDocument17 pagesBab1FizikSPM Pelajar EditA. SuhaimiNo ratings yet
- Jadual BerkalaDocument2 pagesJadual BerkalaA. SuhaimiNo ratings yet
- Elektrik K2BhgCK3BhgB PelajarDocument2 pagesElektrik K2BhgCK3BhgB PelajarA. SuhaimiNo ratings yet
- Fizik Kertas 3 LatihanDocument11 pagesFizik Kertas 3 LatihanA. SuhaimiNo ratings yet
- Elektrik K2BhgCK3BhgB Skema SahajaDocument2 pagesElektrik K2BhgCK3BhgB Skema SahajaA. Suhaimi100% (1)
- ABB 4 Pole Contactor, 230V, 40ADocument1 pageABB 4 Pole Contactor, 230V, 40ASEERALANNo ratings yet
- Chainsaw SparesDocument2 pagesChainsaw SpareswanttobeanmacccNo ratings yet
- Air SuspensionDocument27 pagesAir SuspensionStanly JohnsonNo ratings yet
- COILDATADocument1 pageCOILDATABarış TaşkınNo ratings yet
- Ups Installation and Maintenance ManualDocument141 pagesUps Installation and Maintenance ManualMuntasir100% (1)
- H2S ScavengerDocument7 pagesH2S ScavengerRizwan FaridNo ratings yet
- Marine Seawater ValvesDocument8 pagesMarine Seawater ValvesPhornlert WanaNo ratings yet
- Industrial Sliding DoorsDocument40 pagesIndustrial Sliding DoorsAnonymous CPEha1db7UNo ratings yet
- PSC Unit 4 PPT - Part 3Document35 pagesPSC Unit 4 PPT - Part 3Rino VidNo ratings yet
- Et200s Im151 1 Standard Manual en-US en-USDocument66 pagesEt200s Im151 1 Standard Manual en-US en-USJesús Zacarías ZapataNo ratings yet
- Structural Analysis With The Finite Element Method. Linear StaticsDocument1 pageStructural Analysis With The Finite Element Method. Linear StaticsluchogilmourNo ratings yet
- Denison Hydraulics Goldcup Digital Hi-Iq Control: Electronic Control Card User Manual Software Version 2.2BDocument62 pagesDenison Hydraulics Goldcup Digital Hi-Iq Control: Electronic Control Card User Manual Software Version 2.2BHassan Haghighi TajvarNo ratings yet
- IJCSEIERDFEB20174Document10 pagesIJCSEIERDFEB20174TJPRC PublicationsNo ratings yet
- 150-4059 - Rockbreaker Installation Manual PDFDocument26 pages150-4059 - Rockbreaker Installation Manual PDFDanny Joel Espinoza CastañedaNo ratings yet
- Abbreviations GuideDocument12 pagesAbbreviations GuideHosein AsgariNo ratings yet
- Jacoby TarboxDocument7 pagesJacoby TarboxBayu Permana RydhaNo ratings yet
- Solid Mechanics: Amit Sir (M-Tech (STRUCTURE), BE, Diploma in Civil), 7020059691/7385990691Document9 pagesSolid Mechanics: Amit Sir (M-Tech (STRUCTURE), BE, Diploma in Civil), 7020059691/7385990691Nikita GonnadeNo ratings yet
- Father of The Lightweight Concrete IndustryDocument4 pagesFather of The Lightweight Concrete IndustryProfessor Dr. Nabeel Al-Bayati-Consultant EngineerNo ratings yet
- Iec61000 4 7 (Ed2.0) en - DDocument8 pagesIec61000 4 7 (Ed2.0) en - Dtwinvbooks100% (1)
- Driver Control Master NXT Service Manual 092137-8Document53 pagesDriver Control Master NXT Service Manual 092137-8Piero Capretti0% (1)
- VAS5054ADocument3 pagesVAS5054AKarim ElmahrokyNo ratings yet
- If Steam Drum Under Vacuum Then What Will HappenDocument2 pagesIf Steam Drum Under Vacuum Then What Will HappenyogacruiseNo ratings yet
- 50 KvaDocument4 pages50 KvariogadNo ratings yet
- Dynamic Architecture Journal ArticleDocument11 pagesDynamic Architecture Journal Articlesakshi soniNo ratings yet
- Trays and Packed TowersDocument71 pagesTrays and Packed TowersArt G. Enzi100% (1)
- Article 5 - How To Purge Husqvarna Hydrostatic TransmissionDocument3 pagesArticle 5 - How To Purge Husqvarna Hydrostatic TransmissionSofia AlyaNo ratings yet
- 10 Ways To Speed Up Torrent DownloadsDocument5 pages10 Ways To Speed Up Torrent DownloadsricoffanyNo ratings yet
- Notification ACF One Range Officer RajasthanDocument2 pagesNotification ACF One Range Officer RajasthanAshok SainiNo ratings yet
- SY155WDocument4 pagesSY155WLutfi DstrNo ratings yet
- Ms Acess 2Document80 pagesMs Acess 2Mebrie1No ratings yet