Professional Documents
Culture Documents
Manual Metodos Hidrobiológicos
Uploaded by
Beltrán BriceñoOriginal Description:
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Manual Metodos Hidrobiológicos
Uploaded by
Beltrán BriceñoCopyright:
Available Formats
Universidad del Zulia Facultad Experimental de Ciencias Departamento de Biologa Unidad Acadmica de Ecologa Acutica
METODOS HIDROBIOLGICOS
Manual de Trabajos Prcticos
Elaborado por: Dr. Jos El Rincn Ramirez Coordinador de la Asignatura
Maracaibo, Noviembre 13 de 2000
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
Contenido
Contenido Presentacin Usuarios Orientaciones Didcticas Objetivos Ejercicio Practico N 1: Preparacin de Soluciones Ejercicio Practico N 2: Determinacin del Oxgeno Disuelto Ejercicio Practico N 3: Determinacin de Alcalinidad, Dureza Total y Calcio en Aguas Naturales Ejercicio Practico N 4: Determinacin de Nitrgeno Inorgnico (Nitratos, nitritos y amonio) y Orgnico Ejercicio Practico N 5: Determinacin de Fsforo Inorgnico en Aguas Naturales Ejercicio Practico N 6: Determinacin Granulomtrica de los sedimentos Ejercicio Practico N 7: Determinacin de Pigmentos Fotosintticos Ejercicio Practico N 8: Determinacin de Biomasa y Abundancia Bacteriana en Aguas Naturales Ejercicio Prctico N 9 Caracterizacin del Habitat Lacustre: Determinacin de Parmetros Fsicos, Qumicos y Biolgicos Bibliografa
2 3 4 5 6 7 12 17
22
28 32 36 39
42
47
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
Presentacin
Este manual es el resultado de la recopilacin de los ejercicios prcticos desarrollados durante la docencia de la asignatura Mtodos Hidrobiolgicos dictada por el autor en la Unidad Acadmica de Ecologa Acutica en el Departamento de Biologa de la Facultad de Ciencias de la Universidad del Zulia. La idea fundamental de este documento es el de proveer las herramientas metodolgicas fundamentales para abordar el estudio cientfico de los diferentes cuerpos de agua, tanto marinos como continentales. De tal manera, que el manual comprende experiencias para la determinacin de las caractersticas fsicas, qumicas y biolgicas de los ambientes acuticos. La informacin presentada aqu es el resultado de una compilacin de literatura en otros idiomas diferentes al espaol, por lo que este manual viene a cubrir la deficiencia de materiales escritos en el idioma castellano. As mismo, se han desarrollado una serie de adaptaciones a los mtodos para adecuarlos a las condiciones tropicales particulares, por lo que este manual resultar til para todos aquellos que desarrollan investigaciones en ros, lagos, estuarios y ambientes marinos de nuestro Pas.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
USUARIOS
Los ejercicios prcticos han sido planteados con un lenguaje sencillo, claro, apropiado para alumnos del sexto o sptimo semestre de la Licenciatura en Biologa. Va dirigido a lectores con algn conocimiento general de la Ecologa y de los ambientes acuticos. En algunos casos, se consider necesario definir algunos trminos o conceptos bsicos. Los fundamentos de los mtodos fueron descritos con amplitud de manera de poder informar al lector acerca de los conceptos tericos y conceptuales que sirven de base a cada uno de los mtodos descritos.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
Orientaciones Didcticas
Este manual est diseado para su uso en cursos introductorios de mtodos ecolgicos, limnologa, biologa acutica, etc. Un conocimiento elemental de biologa, qumica y lgebra se requiere en muchos de los ejercicios, por lo que se recomienda que el estudiante haya cursado estas asignaturas antes de iniciarse con los mtodos hidrobiolgicos. Cada seccin consiste de un ejercicio prctico o mtodo para el estudio de un determinado parmetro. Los ejercicios no representan un simple recetario de cocina, sino que se muestran los principios y fundamentos de cada procedimiento, explicando como recolectar muestras, almacenar muestras y datos, analizar los datos, enfatizando las posibles fuentes de error. Se recomienda al profesor la lectura inicial de los fundamentos a fin de poder tener una mejor comprensin de los rudimentos tericos que sirven de basamento a cada uno de los procedimientos metodolgicos. Similarmente, se recomienda que las muestras para el desarrollo de los mtodos sean obtenidas a partir de cuerpos de agua con el cual el estudiante este familiarizado, a fin de vincularlo a los problemas ambientales que presenta su entorno y estimular su inters por el estudio ecolgico y el planteamiento de soluciones.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
OBJETIVOS
Al finalizar el curso el estudiante estar en capacidad de: Conocer los principios fundamentales de los diferentes mtodos comnmente empleados en la investigacin de la biologa y ecologa de los ambientes acuticos. Identificar diferentes ambientes acuticos de la regin y los mtodos para su estudio. Aplicar los diferentes mtodos estudiados a partir de muestras obtenidas en el campo. Discutir las ventajas y desventajas de los diferentes mtodos hidrobiolgicos. Desarrollar destrezas y habilidades en la manipulacin segura del instrumental, reactivos y equipos relacionados con los mtodos hidrobiologicos.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
Ejercicio Prctico No. 1:
PREPARACIN DE SOLUCIONES
INTRODUCCIN En un ecosistema acutico el componente abitico est constituido bsicamente por las propiedades fsicas y qumicas del agua, las cuales condicionan la existencia del componente bitico, integrado por todos los organismos vivos que habitan en el cuerpo de agua. En particular, las caractersticas qumicas del ecosistema acutico son determinadas comnmente mediante mtodos qumicos, lo cual implica la preparacin de soluciones a concentraciones que requieren de una alta precisin y exactitud. Las soluciones pueden definirse como mezclas de una o mas sustancias (ya sean slidas, lquidas o gaseosas) dentro de un medio disolvente (por lo general un lquido). Todas las sustancias que intervienen se distribuyen uniformemente unas con respecto a las otras. Sin embargo, las proporciones pueden variar de varias maneras. El trmino soluto se utiliza para referirse a la sustancia disuelta. El medio disolvente se conoce con el nombre de solvente. Las soluciones que se conocen corrientemente son: a) Diluidas, b) Concentradas, c) Saturadas y d) Sobresaturadas. Las soluciones diluidas son aquellas que poseen una cantidad pequea cantidad de soluto para un solvente. En las soluciones concentradas la proporcin del soluto es relativamente alta (por ejemplo 300 gramos en 500 ml de H20). Por su parte, en las soluciones saturadas las molculas de soluto disuelto estn en equilibrio dinmico con las molculas sin disolver. Si agregamos soluto hasta obtener un resto insoluble en el agua, obtendremos una solucin saturada.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
La concentracin de las soluciones se acostumbra a expresarla como peso de soluto sobre unidad de volumen del solvente. Una solucin normal es el Peso Equivalente del soluto por litro de solucin un miliequivalente en 1 mililitro (Solucin 1N = PE/1000ml). Ejemplos: Una solucin 1N de NaOH, PM = Na (23) + O (16) + H (1) = 40 gramos PE = PM/N OH- = 40/1 = 40 gramos. En este caso el Peso Molecular es igual al Peso Equivalente. Una solucin 1N de NaOH se prepara disolviendo 40 gr de NaOH en 1000ml de agua. Es conveniente que el estudiante recuerde como se preparan soluciones stock, standard y patrones de concentraciones conocidas, ya que son requeridas para elaborar las curvas de calibracin, necesarias para conocer las concentraciones de las muestras. OBJETIVOs: - Identificar el instrumental bsico para preparar soluciones qumicas en el laboratorio. - Conocer las normas de seguridad que deben implementarse al momento de trabajar con reactivos qumicos. - Calcular las concentraciones y diluciones requeridas en la preparacin de diferentes soluciones. - Preparar diferentes soluciones para su ulterior utilizacin en la determinacin de los parmetros qumicos del ecosistema acutico. MATERIALES: BALONES VOLUMTRICOS DE 50, 100, 250 Y 500 ML MATRACES ERLENEMEYER DE 250 ML CILINDROS GRADUADOS DE 100 ML BURETAS (25 50 ML) EMBUDO DE VIDRIO VIDRIOS DE RELOJ PROPIPETAS DE 10, 25 Y 50 ML PIPETAS VOLUMTRICAS DE 5, 10, 25 Y 50 ML. SOPORTE UNIVERSAL CON PINZAS PARA BURETAS.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
- GOTEROS Reactivos: - Agua Destilada - Sulfato de Manganeso (MnSO4- mono, di, tetrahidratado). - 500 grs NaOH ( 700grs KOH) - 135 grs de NaI ( 150 grs. de KI) - NaN3 (10 gramos). - Almidn (5 grs). - Tiosulfato de Sodio (Na2S2O3.5H2O) 30 grs. - Biyodato de potasio - KH(IO3)2 5 gramos - Na-EDTA.2H2O - CaCO3 - NH4Cl - Amonaco Concentrado - Negro de Eriocromo T - HCl 36N - K2Cr2O7 5 gr - Yoduro de Potasio 500 gr - Fenolftaleina 2 gr. - Alcohol Isoproplico 95% 1 Litro - Naranja de metilo 1.0 gr. - Verde de bromocresol 1 gr. - Naranja de metilo 1 gr. PROCEDIMIENTO: 1. PREPARACIN DE SOLUCIONES PARA LA DETERMINACIN DE O2 DISUELTO 1.1. Reactivo de Sulfato Manganoso: Disuelva 400g de MnSO 4.2H2O ( 364g de MnSO4.H2O) en 1 litro de agua destilada. En este ejercicio prctico se prepararan 500 ml. Calcule el peso que debe tomar del MnSO4. 1.2. Reactivo de Ioduro Alcalino: Disuelva 500 grs de NaOH ( 700 g de KOH) y 135g de NaI ( 150g de KI) en 1 litro de agua destilada. 1.3. Solucin de Almidn soluble: 2g en 100ml de agua destilada. Calentar hasta transparencia. Pueden agregarse 0.5ml de formol para preservar.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
10
1.4. Solucin de Tiosulfato de Sodio 0,025N (Na2S2O3.5H2O) (PM=248,19). Una solucin 1N de Tiosulfato contiene el peso molecular de esa sustancia en un litro de solucin; una solucin 0,025N ser igual a 248,19 x 0,025 = 6,2048 g/L. Llevar 6,2g de Tiosulfato puro a 1 Litro con agua destilada recin hervida y enfriada. Agregar algunas gotas de cloroformo para preservar. Guardar en botella ambar en oscuridad. 1.5. Estandarizacin del Tiosulfato de Sodio: La solucin de tiosulfato de sodio debe ser estandarizada cada vez que se vaya a utilizar. Los reactivos necesarios son: 1) solucin standard 0.25N de dicromato de potasio: 0,6129g de K2Cr2O7 en 500 ml de agua destilada recin hervida y enfriada. 2) Solucin de Yoduro de Potasio al 25%: Disolver 25g de KI en 100 ml de agua destildada. Procedimiento: Colocar en un erlenmeyer 100 ml de agua destilada hervida y enfriada. Agregar 3 ml de la solucin de KI al 25%. Agreagar, por medio de una pipeta volumtrica 50 ml de la solucin de dicromato de potasio. Agregar 10ml de HCl concentrado. Titular el I2 liberado con la solucin estndar 0,025N de tiosulfato; cuando el color amarillo desaparece casi por completo agregar 2 ml de de la solucin de almidn y continuar la titulacin hasta la desaparicin del color ( el color final puede ser ligeramente verdoso debido a sales de cromo. El factor de correccin para el tiosulfato es : Ml dicromato/ml tiosulfato= 50/x Por ejemplo, si la titulacin requiri 48.8 ml de tiosulfato 0,025N, el factor ser: 50/48.8= 1.024 2. PREPARACIN DE REACTIVOS PARA LA DETERMINACIN DE LA DUREZA TOTAL DE LAS AGUAS. 2.1. Reactivo de EDTA 0,01M. Se disuelven 0,3723 grs. de NaEDTA.2H2O en 100 ml de agua destilada. Estandarice esta solucin titulando con una solucin estndar de carbonato de calcio la cual se preparar pesando 1.00 gr. De CaCO 3 desecado a 110 C durante una hora y media y se lleva a un matraz de 500ml con poca agua. Se agrega gota a gota HCl diluido en igual volumen de agua destilada (1 + 1 HCl) hasta que se disuelva
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
11
todo el carbonato, no debindose requerir para ello mas de 3 ml de cido. Se aaden 200 ml de agua destilada y ser hierve por unos minutos para eliminar el CO2. Enfre y ajuste a un pH de 5.0 si es necesario utilizando HCl (1 +1) NH4OH 3N. Transfiera la mezcla a un baln aforado de 500 ml y enrase con agua destilada (1.0 ml = 1.0mg CaCO3 = 0,4008mg Ca). 2.2. Mezcla amortiguadora del pH: Mezclar 67,5gr. de cloruro de amonio con 570 ml de amonaco concentrado y diluir a 1 litro. 2.3. Indicador: Pesar 0,8 gr. de Negro de Eriocromo T y 100 gr. de NaCl. Mezcle y macere en un mortero hasta que la mezcla quede homognea en un color rosado plido y las partculas sean bastante finas. 3. PREPARACIN DE REACTIVOS PARA LA DETERMINACIN DE LA ALCALINIDAD EN LAS AGUAS. 3.1. Agua libre de dixido de carbono: Hervir por 15 minutos y enfriar a temperatura ambiente. El pH debe ser superior a 6.0. 3.2. Solucin de fenolftalena: Disuelva 0.5 gr. de fenolftalena en 50 ml de alcohol isoproplico o etlico. Aada 50 ml de agua y mezcle. 3.3. Solucin stock de acido sulfurico : Diluya 3 ml de H 2SO4 concentrado en 1 litro de agua destilada, esto producir una solucin 0.1N aprox. 3.4. Solucin estndar de cido sulfrico: Diluya 200 ml de la solucin 0.1N en 1 litro de agua destilada libre de CO2. 3.5. Solucin indicadora de naranja de metilo: Disuelva 0.5g de naranja de metilo en 1 litro de agua destilada. 3.6. Indicador mixto de verde de bromocresol y rojo de metilo: Se disuelven 0,1 g de verde de bromocresol y 0,02 gr. de naranja de metilo en 100ml de alcohol etlico o isoproplico 95%.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
12
Ejercicio Prctico No. 2:
DETERMINACIN DEL OXIGENO DISUELTO
INTRODUCCIN De todos los mtodos qumicos disponibles para la investigacin en ambientes acuticos, la determinacin del oxgeno disuelto es uno de los ms frecuentemente utilizados y ms importantes. El Oxgeno Disuelto provee de valiosa informacin acerca de las reacciones biolgicas y bioqumicas que tienen lugar en el agua; es una medida de uno de los factores ambientales que afectan la vida acutica y de la capacidad del agua para el procesamiento de los ingresos de materia orgnica. El oxgeno en forma de gas se disuelve libremente en las aguas dulces. Este puede provenir de la atmsfera o como un producto de la fotosntesis de las algas y plantas acuticas, y es utilizado en reacciones bioqumicas respiratorias y en reacciones qumicas inorganicas. La concentracin de oxgeno disuelto en el agua depende tambin de la temperatura, presin, y concentraciones de varios iones. La forma ms conveniente para medir el oxgeno disuelto es utilizando un oxigenmetro y un electrodo. Estos tienen la desventaja de ser muy costosos, requieren una calibracin muy frecuente, y son poco precisos para concentraciones de O2 entre 0 y 1 mg/L . Un gran nmero de mtodos colorimtricos han sido propuestos para la determinacin del oxgeno disuelto, pero muchos de ellos han sido bastante imprecisos, particularmente a bajas concentraciones. Aunque un gran nmero de mtodos qumicos han sido empleados para medir el oxgeno disuelto, el mtodo de Winkler, o alguna modificacin de este, es el ms frecuentemente utilizado en limnologa.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
13
El mtodo de Winkler fue introducido en 1888 por L.W. Winkler de Budapest y hasta ahora sigue siendo concebido como un mtodo muy preciso. El mtodo depende de la oxidacin de hidrxido manganoso (manganeso bivalente) por el oxgeno disuelto en el agua, resultando en la formacin de un compuesto tetravalente. Cuando el agua que contiene el compuesto tetravalente es acidificada, se libera Iodo libre a partir de la oxidacin de ioduro de potasio. El iodo libre es qumicamente equivalente a la cantidad de oxgeno disuelto presente en las muestras y es determinado por titulacin contra una solucin estandar de tiosulfato de sodio (p. ejem. 0.005 M). las reacciones que tienen lugar por la adicin de los reactivos (KI, KOH, MnSO4, y H2SO4) al agua son las siguientes: El sulfato manganoso reacciona con la mezcla hidrxido de potasio-ioduro de potasio para producir un precipitado blanco de hidroxido manganoso: MnSO4 + 2KOH Mn(OH)2 + K2SO4
Cuando este precipitado blanco es obtenido, no hay ms oxgeno disuelto en la muestra. Un precipitado marrn indica que el oxgeno estuvo presente y reaccion con el hidrxido manganoso, formando oxido mangnico bsico: 2Mn(OH)2 +O2 2MnO(OH)2
Con la adicin de cido sulfrico, este precipitado se disuelve, formando sulfato mangnico: 2MnO(OH)2 + 4H2SO4 2Mn(SO4)2 + 6H2O
Hay una reaccin inmediata entre Mn(SO4)2 y el ioduro de potasio aadido previamente, liberando iodo y resultando en la tpica coloracin del iodo (marrn parduzca) del agua. 2MnO(SO4)2 + 4 KI 2MnSO4 + 2K2SO4 + 2I2
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
14
El nmero de moles de Iodo liberados por esta reaccin es equivalente al nmero de moles de oxgeno presentes en la muestra. La cantidad de iodo es determinado al titular una porcin de la solucin con una solucin estandar de tiosulfato de sodio: 4Na2S2O3 + 2I2 2Na2S4O6 + 4NaI
EQUIPOS, MATERIALES Y REACTIVOS: Materiales Botellas para DBO Erlenmeyer de 250 ml Buretas de 50 ml Pipetas Agitador Magntico Reactivos: a. Solucin de sulfato de manganeso 480 grs. de MnSO4.4H2O 400 grs. de MnSO4.2H2O 364 grs. de MnSO4. H2O b. Solucin alcali-ioduro-azide 500 grs. de NaOH ( 700 grs. de KOH) 135 grs. de NaI ( 150 grs. de KI) En un litro de agua destilada aadir 10 gramos de NaN3 (Azide) disuelto en 40 ml de agua destilada. c. H2SO4 concentrado 36N c. Almidn: 5 gramos de almidn disueltos en agua fra, agregar agua hirviendo en agitacin, diluir a 1 Litro. Usar el sobrenadante. Preservar agregando unas pocas gotas de tolueno. d. Solucin stock de Tiosulfato de sodio 0.10N. Disolver 24.82 gramos de Na2S2O3.5H2O en ebullicin, enfriar y aforar a 1 litro.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
15
e. Estndar de Tiosulfato: Diluir 250 ml de tiosulfato a 1 litro o disolviendo 6.205 gramos de Na2S2O3.5H2O en agua recien hervida y diluir a 1 litro. Preservar aadiendo 5 ml de cloroformo. f. Estandarizacin: El tiosulfato de sodio se puede estandarizar en una solucin equivalente de biyodato de potasio KH(IO3)2. Preparar un stock de biyodato equivalente al stock de tiosulfato (0.1N) pesando 3.249 gms. La solucin de biyodato equivalente al tiosulfato 0.025N es de 812.4 mg/l de KH(IO3)2 250 ml del stock en 1 litro. PROCEDIMIENTOS: Procedimiento de Estandarizacin Disolver aproximadamente 2 gramos de KI en un frasco erlenmeyer en 10-150 ml. de agua destilada. Aada 10 ml. de H2SO4 (1:9). Aada exactamente 20.0 ml de la solucin estandar de biyodato. Diluya a 200 ml con agua destilada y titule con la solucin de tiosulfato el yodo liberado agregando almidn al final de la titulacin. Cuando las soluciones son equivalentes se deben gastar 20 ml. de la solucin de tiosulfato 0.025N. Determinacin del Oxgeno Disuelto: A la muestra, colectada en botellas de 250 o 300 ml, se debe aadir 2 ml. de sulfato de manganeso, seguidos de 2 ml de alcaliazide, bien debajo de la superficie del lquido. Tape cuidadosamente y agite por inversin la botella por lo menos 30 veces. Permita que el precipitado se sedimente. Cuando el precipitado se asiente y se vea claro el sobrenadante vuelva a invertir la botella. despus de 2 minutos destape cuidadosamente la botella e inmediatamente aada 2.0 ml de H2SO4 dejando correr el cido por las paredes del cuello de la botella, tape de nuevo y mezcle por inversin hasta la disolucin completa. Tome un volumen correspondiente a 200 ml de la muestra y titule con el tiosulfato 0.025N hasta obtener un color amarillo palido. Aada 2 ml de la solucin de almidn y continue la titulacin hasta la desaparicin del color azul.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
16
Para 200 ml de la muestra original, 1 ml de tiosulfato de sodio 0.025N es= 1 mg/L de Oxgeno disuelto puede aplicarse la formula siguiente: ppm de OD = (ml de tiosulfato) (normalidad tiosulfato)(8000) (ml de muestra) ( ml de la botella-2) (ml de la botella) reporte valores de 2 decimales
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
17
Ejercicio Prctico No. 3:
Determinacin de Alcalinidad, Dureza Total y Calcio en Aguas Naturales
DETERMINACIN DE LA ALCALINIDAD 1.1. Fundamentos La alcalinidad es la capacidad del agua para aceptar protones y por lo general se debe a los componentes de bicarbonato (HCO3-), carbonato (CO3=) e hidrxido (OH-)de aguas naturales o tratadas. Los valores de carbonato y bicarbonato se pueden calcular por titulacin de la alcalinidad con un cido inorgnico valorado, al punto de equivalencia del bicarbonato (pH 8,3) y, posteriormente al punto de equivalencia del cido carbnico (pH 4-5). a. Determinacin de Alcalinidad a la fenolftaleina Reactivos: - HCl 0,1N - Indicador de Fenolftaleina Material Requerido: - Erlenmeyer de 250 ml - Cilindro graduado de 100 ml - Bureta de 25 ml - Gotero Procedimiento: Se mide con el cilindro graduado 100 ml de la muestra y se agregan 6-7 gotas del indicador de fenolftaleina. Si la muestra problema vira al rojo, titular inmediatamente con HCl 0,1N hasta incoloro. Si no hay cambio de color se procede con la determinacin del bicarbonato.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
18
b. Determinacin de Alcalinidad Total: Reactivos: - Acido clorhdrico 0,1N: Se prepara con 8,3 ml de HCl concentrado y se afora a 1000 ml con agua destilada. - Indicador mixto de bromocresol y rojo de metilo: 0,1 gr de verde de bromocresol y 0,02 gr de rojo de metilo se disuelven en 100 ml de alcohol etlico o isoproplico 95%. Material requerido: - Erlenmeyer de 250 ml - Cilindro graduado de 100 ml - Bureta de 25 ml - Goteros Procedimiento: A la misma muestra en la cual se determin la alcalinidad a la fenolftaleina se agregan 3 gotas del indicador mixto. La muestra toma un color verde azulado e inmediatamente se titula sobre una superficie blanca con HCl 0,1N hasta una coloracin rosa claro. Clculos: Alcalinidad Fenolftaleina = (mg/L CaCO3)
A x N x 50.000 Vol. Muestra (ml)
B x N x 50.000
Alcalinidad Total =
Vol. Muestra (ml)
Donde: A = ml de HCl gastados durante la titulacin a la fenolftaleina B = ml de HCl totales gastados hasta el punto final con el indicador mixto. N = Normalidad del cido Nota: la alcalinidad por bicarbonatos expresada como mg/L de HCO3 puede ser obtenida dividiendo la alcalinidad total entre 0.82, directamente a travs de la siguiente relacin:
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
19
mg HCO3/L = ml HCl gastado x Norm. HCL x 61 x 1000 Volumen de muestra (ml)
DETERMINACIN DE DUREZA TOTAL Fundamentos: La concentracin de calcio mas magnesio expresada como equivalente de CaCO3 corresponde a la Dureza Total. Otros metales divalentes tambin contribuyen a la dureza, pero sus concentraciones son generalmente insignificantes en las aguas naturales. Los iones Calcio y Magnesio forman complejos estables con la sal disdica del cido etilendiaminotetracetico (CaEDTA y MgEDTA). El punto final de la titulacin es indicado con un segundo agente acomplejante, el Negro de Eriocromo T. Si se agrega una pequea cantidad de Negro de Eriocromo T a una muestra tamponada a pH 10, se forma un complejo soluble de color rojo vinoso. En la titulacin el EDTA disocia el complejo de Ca y Mg con Negro de Eriocromo T y los iones de Calcio y Magnesio forman un complejo mas estable con EDTA. Cuando todo el calcio y magnesio se ha acomplejado con EDTA, el color de la solucin es azul. Ca++ + Mg++ + Ca y Mg Negro de Eriocromo T + EDTA ---- CaEDTA + MgEDTA + Negro de Eriocromo T (Azul) Procedimiento: Se toman 50 ml de la muestra y se coloca en un erlenmeyer de 250 ml al que se agrega 1 ml de solucin amortiguadora de pH y nua punta de esptula del indicador Negro de Ericromo T. Se valora con la solucin de EDTA hasta que el indicador vire de rojo vinoso a azul. Al estar cerca del punto final es necesario un goteo lento y agitacin vigorosa de la muestra. Clculos: Los resultados expresados en ppm (mg/L) de CaCO3 se calculan a travs de la siguiente expresin:
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
20
Dureza Total (mg/L de CaCO3) = ml EDTA x M EDTA x 100,1 x 1000 Volumen de la muestra (ml)
DETERMINACIN DE CALCIO Fundamentos: El calcio puede ser lixiviado prcticamente de todos los tipos de rocas, pero es mucho ms abundante en regiones con depsitos de calizas, dolomitas o yeso. El calcio es importante para la productividad biolgica de las aguas. Es un componente fundamental de la pared celular de muchas plantas acuticas y de las estructuras de sostn de muchos animales tales como los tejidos seos de los peces y las conchas de los moluscos. El titulante EDTA utilizado en la determinacin de calcio es el mismo que el empleado en la determinacin de dureza y reacciona tanto con el calcio como con el magnesio. Para determinar solo Calcio, se eleva el pH suficientemente de manera que el magnesio precipita como hidrxido de magnesio, y se utiliza un indicador especfico para calcio. Material requerido: - Erlenmeyer de 250 ml - Cilindro graduado de 50 ml - Bureta de 25 ml. - Esptula Reactivos: - Hidrxido de Sodio 1N: se disuelven 4 gr en agua destilada y cuando se enfre se diluye hasta 100 ml. - Indicador de Murexide: Mezcle con ayuda de un mortero 0.2 gr del indicador de murexide y 100 gr de NaCl. - EDTA 0.01 M Procedimiento: 1. Tome una muestra que contenga menos de 10 mg de Ca. Usualmente una muestra de 50 ml es
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
21
adecuada, pero si la alcalinidad total es superior a 250 mg/L, probablemente se requiere tomar una alcuota de la muestra y diluir a 50 ml con agua destilada. 2. Aada 1 2 ml de la solucin de NaOH para producir un pH de 13 14. Agite. 3. Aada la punta de la esptula del indicador en polvo. La solucin debe tornarse rojiza. 4. Titule con el EDTA hasta que se produzca el vire de rojo a azul. Clculos: mg Ca por Litro =
A x B x 400,8 Vol. Muestra (ml)
Donde: A = ml de EDTA gastados B = Molaridad del EDTA Nota si se utilizan 50 ml de muestra y la molaridad del EDTA es 0,01M entonces: mg Ca/Litro = A x 8,016
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
22
Ejercicio Prctico No. 4:
DETERMINACIN DE NITRGENO INORGNICO (NITRATOS, NITRITOS Y AMONIO) Y NITRGENO ORGNICO
Nitratos y Nitritos: El mejor mtodo (hasta la fecha) para la determinacin del NO3N en el agua es a travs de la reduccin del nitrato a nitrito en una solucin alcalina-buffer, y pasando la muestra a travs de una columna que contiene limaduras de cadmio metlico. Luego el nitrito (NO2-N) es determinado por un sensible mtodo de diazotizacin que resulta en un color rosa cuya absorbancia obedece las leyes de Beer hasta casi 500 g NO3-N o NO2-N/L. Las concentraciones de nitrito de la muestra original pueden ser determinadas con bastante precisin antes de la reduccin del NO3-N a NO2-N por la misma tcnica de diazotizacin. Este mtodo de reduccin del nitrato requiere columnas de vidrios especiales para una anlisis eficiente. Este mtodo permite procesar ocho (8) muestras por columna por hora. Cuatro columnas pueden fcilmente ser operadas simultneamente. Almacenamiento de la muestra: Las muestras deben ser filtradas a travs de filtros de fibra de vidrio para combustin a 500C (por ejemplo Whatman GF/F, 0,6-0,7 m de tamao de poro). Se asume que el filtrado solo contiene materiales disueltos. El filtrado puede ser almacenado a 4 5 C pero debe ser analizado dentro de 24 horas. Aparatos y Reactivos: 1. Columnas de Reduccin: Estas deben ser construidas de vidrio de boro-silicato de acuerdo a ciertas dimensiones estandarizadas. En el fondo de la columna se coloca lana de vidrio. 2. Cadmio metlico: Las limaduras de cadmio metlico (> 99,9% de pureza) deben ser tamizadas para obtener tamaos de partculas entre 0,5 y 2,0 mm. Aproximadamente 40 g de limaduras de cadmio son lavadas con HCL 2N (85 ml de HCl
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
23
3.
4.
5.
6.
7.
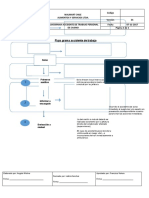
concentrado diluido hasta 500 ml con agua destilada) en un embudo de separacin y lavado con agua destilada. El Cd es entonces tratado con aproximadamente 100 ml de una solucin de sulfato cprico (20g de CuSO4.5H 2O disuelto en un litro de agua destilada) y agitado hasta que desparezca el color azul desaparezca debido a que el cobre se deposita sobre el cadmio. Las limaduras de Cd-Cu sern luego lavadas con agua destilada cuidadosamente; evite exponer el cadmio al aire. Con las columnas llenas de agua, se aade el Cd-Cu evitando que queden atrapadas burbujas en la columna. Enjuague cada columna con una solucin de 50 ml de agua destilada ms 5 ml de una solucin buffer de la siguiente composicin: 100g de cloruro de amonio, 20g de tetraborato de sodio, y 1 g de EDTA disdico dihidrato disuelto en agua destilada hasta hacer un litro. El flujo del enjuague debe ser a una velocidad de 6ml/min. Solucin de Sulfanilamida: Se disuelven 5g de sulfanilamida en una solucin de 50ml de HCL concentrado y 300 ml de agua destilada. Diluya hasta 500ml. Solucin de N-(1-naftil) etilen diamina dihidrocloruro: se disuelven 0,5 g de dihidrocloruro en 500 ml de agua destilada. Almacene en botella ambar Estandar de Nitratos: Disuelva 0,722g de KNO3 (secado por 1 hora a 110 C) en agua destilada y lleve a un litro: (1,00ml = 100g NO3-N) Estandar de Nitritos: Disuelva 0,4929 g de NaNO2 (secado por una hora a 110 C) en agua destilada y lleve a un litro: (1,00ml = 100g NO2-N).
Procedimiento: Ver FlujoDiagrama. Amonio: Fundamentos: Excepto en condiciones muy alcalinas (pH > 9.0), gran parte del amonio (NH3) existe en la forma inica (NH 4+) en las aguas continentales. Sus concentraciones son por lo general muy bajas debido a que es asimilado rpidamente por algas, bacterias y plantas acuticas. El contenido de la muestra puede variar rapida y
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
24
marcadamente. De manera que la muestra debe ser analizada tan pronto como sea posible despues de ser tomada en el campo. El mtodo para la determinacin de amonio ms recomendado en el mtodo del fenol-hiplocorito usando nitropusiato como catalizador. El amonio reacciona con el fenol y el hipoclorito bajo condiciones alcalinas para formar un complejo azul indophenol. El color desarrollado es proporcional a la concentracin de amonio dentro de un rango dado (0 a 1000 g NH4-N/L). La sensibilidad es buena, con una desviacij estandar de alrededor de 2 5 g/L. Reactivos: 1. Buffer: Na3PO4 ( K3PO4) en una solucin al 5% (p/v). 2. Solucin stock de Fenol: Se disuelven 500 g de fenol en metanol y se lleva a 800 ml con metanol. Se almacena en botellas ambar y bajo refrigeracin 3. NaOH 20% : Se disuelven 270 g de NaOH en agua desmineralizada y se lleva a un litro. 4. Solucin A : Se toman 15 ml de la solucin stock de fenol y 0,02 g de nitroprusiato de sodio (Na2Fe (CN)5NO . 2H2O) y se diluyen en 100 ml con agua. 5. Solucin B : Se mezclan volmenes iguales de (15 ml) de hipoclorito de sodio (cloro comercial al 5% puede ser suficiente) y de NaOH al 27% y se lleva a 50 ml con agua destilada. 6. Almacene ambas soluciones A y B en botellas ambar en un refrigerador, despues de enfriadas a temperatura ambiente. 7. Estandar de amonio: Se disuelven 3,819 g de NH4Cl seco en agua destilada y deionizada y se lleva a 1 Litro. 1,00 ml=1000g NH$-N. Se hacen diluciones en serie para los diferentes estandars. Procedimiento: Utilizando cilindros graduados de 50 ml. 1. Dispense 50 ml de agua destilada y desionizada (blanco), los estandars de amonio, y las muestras en cilindros graduados de 50 ml. 2. Aada 2ml de del buffer de fosfato; mezcle (un vortex mezcla bastante bien). Ignore cualquier precipitado que se forme. 3. Aada 5 ml de la Solucin A; mezcle bien.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
25
4. Aada 2,5 ml de la Solucin B; mezcle bien. 5. Permita una hora para que se desarrolle el color (debe ser estable a temperatura del laboratorio por 24 h). 6. Lea la densidad ptica a 630 nm, sustrayendo la densidad ptica del blanco, use celdas de longitud apropiada para la intensidad de color observadas (1-cm para altos niveles de amonio; 5-cm para el rango de 0 a 200 g NH4-N/L; 10 cm para menos de 20 g/L. 7. Prepare una curva estandar de densidades pticas versu la concentracin de tus estandares corregidos. Las concentraciones de la muestra pueden ser leidas directamente desde el grfico. Cuando la curva estandar es lineal (debe serlo) las concentraciones de las muestras se calculan directamente: Odb = absorbancia del agua destilada ms los reactivos (blanco) Ods = absorbancia de los estandars y las muestras ms los reactivos Concentracin del estndar: (g NH4-N/L) -------------------- =
F= factor de extincin
Ods del estandar -ODb
Nitrgeno Orgnico: Fundamentos: Una gran fraccin del nitrgeno total en las aguas continentales ocurre como nitrgeno orgnico en forma particulada y especialmente en forma disuelta. Se dispone de un nmero de tcnicas analticas para la determinacin de nitrgeno orgnico disuelto y particulado. Las fracciones particulada y disuelta del nitrgeno orgnico usualmente son separadas en aparatos de vidrio con filtros de fibra de vidrio (Whatman GF/F, o.6-0.7 m). El nitrgeno es entonces analizado por diferentes tcnicas. El nitrgeno de la fraccin particulada es convertido a amonio por el clsico mtodo Kjeldahl, despus de tratamiento con acido sulfrico. El amonio resultante es luego concentrado por destilacin y titulado.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
26
Alternativamente, la materia orgnica puede ser calcinada a altas temperaturas en un analizador C-H-N, en este caso el nitrgeno orgnico es convertido a N2 libre y luego analizado por cromatografa de gas. Las concentraciones de nitrgeno orgnico disuelto son ms difciles de determinar en el agua. Se ha empleado la tcnica del micro-Kjeldahl, pero los lmites de sensibilidad frecuentemente exceden las bajas concentraciones encontradas en aguas naturales. Recientemente los compuestos de nitrgeno orgnico y amonio han sido analizados por descomposicin y oxidacin fotoltica con radiacin ultravioleta de alta intensidad. Cuando las muestras contienen muy bajas concentraciones de nitrgeno orgnico disuelto es preferible utilizar mtodos automatizados (Espectrofotmetros de AA y emisin de llama, espectrofotmetros de emisin de plasma, cromatografa inica, cromatografa lquida de alta resolucin (HPLC), espectrofotmetro de flujo continuo, etc)
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
27
Flujodiagrama para la Determinacin de Nitratos Estandares
Colocar 50 ml En cilindro graduado
Blancos Colocar 50 ml en Cilindro graduado
Muestras
Colocar 50 ml En cilindro graduado
Aadir 5 ml de la solucin B vigorosamente Aadir 10 ml de la muestra con el buffer a la columna, permitir que corra y descartar el efluente
Aadir el resto de la muestra con el buffer, colectar 2 ml en el mismo cilindro, descarte. Se colectan 25 ml
Tan pronto como sea posible se aaden 0,5 ml de la solucin de sulfonilamida a los 25 ml de la muestra eluida
g NO3-N/L = F [Ods muestra (Odb + Odo)], Donde : Odb = absorbancia del agua deslidada mas los reactivos, el blanco. Odo = absorbancia de la muestra sin naftiletilendiamina (solo si existe una coloracin marrn) Ods = abosrbancia de estandares o muestras mas reactivos F=concentracin del estandar (gNO3/L)/ Ods del estandar - ODb
Despus de 5 min pero antes de 8 min se aaden 0,5 ml de la solucin del naftiletilendiamina y mezcle cuidadosamente
Entre 10 min y 2 hr, mida el coeficiente de extincin a una longitud de onda de 543 nm
Intercale las muestras de agua, los estandares y los blancos. Utilice al menos tres soluciones estandar Prof. JOS ELI RINCN RAMREZ
Cuando la curva estandard es lineal las concentraciones de las muestras pueden ser calculadas por un factor de la unidad de extincin Prepare una curva estandar de OD versus concentracin para los estandares corregidos (Odcorr=Ods-Odb)
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
28
Ejercicio Prctico No. 5
Determinacin de Fsforo Inorgnico en Aguas Naturales
Introduccin: El intenso inters ecolgico en el Fsforo proviene de su importante rol en el metabolismo de la biosfera. En comparacin a otros nutrientes esenciales y componentes estructurales de la biota (C, N, O, S), el fsforo es menos abundante y comnmente limita la productividad biolgica de los ecosistemas acuticos. Gran parte del fsforo de las aguas se encuentra en la fase particulada de la biota, principalmente algas y plantas acuticas. Diferentes compuestos lbiles de bajo peso molecular son secretados por esta fase particulada conformando una fraccin coloidal transitoria de elevado peso molecular. Parte de esta fraccin coloidal y una porcin del fsforo particulado se pierde de la zona productiva por sedimentacin, y parte es hidrolizado como ortofosfato soluble. Este ltimo es rpidamente asimilado por la biota y es usualmente bajo en la zona trofognica. Determinacin de Fsforo Soluble Reactivo Fundamentos: La medicin de los ortofosfatos solubles est basada en la reaccin de estos compuestos con el molibdato de amonio en medio cido, seguida por una reduccin del cido fosfomolibdico a un complejo azul. Lo anterior depende de al presencia de estos compuestos de fsforo como ortofosfatos. Se utiliza el mtodo de Murphy y Riley (1962): Los fosfatos reaccionan con el molibdato de amonio y forman un complejo como amonio molibdofosfato. Despus de una reduccin controlada se produce un complejo azul de molibdeno.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
29
NH4+ + PO4-3 (MoO3.MoO2)4H2
MoO4
--
(NH4)3 P (Mo3O10)4
H3
PO4
Al agregar el molibdato en cido sulfrico y una solucin de cido ascrbico se forma un complejo amarillo de cido fosfomolibdico (molibdofosfato de amonio). H2SO4 + (NH4+) MoO4.4H2O + PO4-3 - (NH4+) (MoO10)4 amarillo Con el agente reductor (cido ascrbico) el complejo cido se reduce a azul de molibdeno; al efectuar esta reaccin se agrega un catalizador, que en este caso es tartrato antimonil potsico.
(NH4+)3 P (Mo3O10)4 + Acido Ascrbico
H3PO4(4MoO2)2 + C6H5O6
La cantidad de azul de molibdeno formado es directamente proporcional a la concentracin de fsforo como ortofosfato presente en la muestra.
Almacenamiento de las muestras: las muestras de agua deben ser filtradas inmediatamente a travs de filtros de fibra de vidrio (GF/F, 0,6-0,7 m) y almacenadas a 5C. Los anlisis deben ser hechos dentro de 2 horas y preferiblemente a la media hora de la coleccin de la muestra. Cuando el anlisis requiere ser dilatado la muestra puede ser congelada a 20C. Reactivos: 1. Solucin de molibdato de amonio: Se disuelven 15 g de paramolibdato de amonio (NH4)6Mo7O24.4H2O en agua
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
30
2.
3.
4.
5.
6.
destilada y se lleva a 500 ml. Se almacena en botellas de polietileno ambar. Acido Sulfrico: Aadir 140 ml de cido sulfrico concentrado a 900 ml de agua destilada. Almacene en botella con tapa de vidrio. Solucin de Acido Ascrbico: Se disuelven 27g de L-Acido Ascrbico en 500 ml de agua destilada. Se debe preparar diariamente o almacenar congelado en una botella plstica. La solucin es estable por unos pocos das si es refrigerada. Solucin de Tartrato antimonil potsico: Disuelva 0,34 de tartrato antimonil potsico [K(SbO)C4H4O6.H2O] en 250 ml de agua destilada, caliente si es necesario. Almacene en botella de vidrio. Reactivo compuesto: Mezcle 100 ml de molibdato de amonio, 250 ml de cido sulfrico, 100 ml de cido ascrbico, y 50 ml de tartrato antimonil potsico. Prepare diariamente para su uso y descarte el exceso. Soluciones Estandar de Fosfato: Disuelva 0,2197 (105C,24h) de fosfato dihidrgeno de potasio (KH2PO4) en agua destilada y diluya a 1 litro. Almacene en botellas ambar con 1 ml de cloroformo: 1,00 = 50,0 g PO4-P. Diluya con agua destilada para realizar los estandares apropiados.
Procedimiento: Ver Flujograma
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
31
Flujograma para la Determinacin de Ortofosfatos
Estandares Colocar 100 ml en cilindro con tapa esmerilada
Blancos Colocar 100 ml en cilindro con tapa esmerilada
Muestras Colocar 100 ml en cilindro con tapa esmerilada
Agregar 10 ml del reactivo Compuesto, mezcle vigotrosamente.
Despus de 10 minutos pero dentro de 2 horas mida el coeficiente de extincin en una celda de 1 cm a una longitud de onda de 885nm. Ajuste el espectrofotmetro a cero con agua destilada.
Mida la absorbancia del blanco y corrija para cualquier desarrollo de color con los reactivos. Odcorr = Odmuestra-ODblanco
Prepare la curva estandar de cuatro soluciones estandar (pej. 10, 50, 100 y 500 g/l). Calcule el factor F como sigue: F = concentracin del estndar/(Odestandar Odblanco) g/l PO4-P = F [Odmuestra (Odblanco + Odturb)]
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
32
Ejercicio Prctico No. 6:
Determinacin Granulomtrica de los Sedimentos
Introduccin: El substrato de los cuerpos de agua constituye el habitat de un grupo de animales colectivamente llamado Bentos. Es por ello que la determinacin de las caractersticas del sedimento: arcilla, limo, arena, grava, etc.,deben ser registradas en cualquier evaluacin fsica de este componente del habitat acutico. Los ros, debido a la fuerza erosiva de la corriente, pueden carecer de sedimento fino, predominando fundamentalmente los tipos rocosos, gravosos o arenosos. En ambientes lnticos, el sedimento puede estar constituido principalmente por partculas finas de menor dimetro, y predominan los tipos de limo, arcilla y arena. Para clasificar a los constituyentes del suelo segn su tamao de partcula se han establecido muchas clasificaciones granulomtricas. Bsicamente todas aceptan los trminos de grava, arena, limo y arcilla, pero difieren en los valores de los lmites establecidos para definir cada clase. De todas estas escalas granulomtricas, son la de Atterberg o Internacional (llamada as por haber sido aceptada por la Sociedad Internacional de la Ciencia del Suelo) y la americana del USDA (Departamento de Agricultura de los Estados Unidos) las ms ampliamente utilizadas. Ambas clasificaciones se reproducen en la siguiente figura:
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
33
El trmino textura se usa para representar la composicin granulomtrica del suelo o del sedimento. Cada trmino textural corresponde con una determinada composicin cuantitativa de arena, limo y arcilla. En los trminos de textura se prescinde de los contenidos en gravas; se refieren a la fraccin del suelo que se estudia en el laboratorio de anlisis de suelos y que se conoce como tierra fina. Por ejemplo, un suelo que contiene un 25% de arena, 25% de limo y 50% de arcilla se dice que tiene una textura arcillosa. Los trminos texturales se definen de una manera grfica en un diagrama triangular que representa los valores de las tres fracciones. Las partculas no estn sueltas sino que forman agregados y hemos de destruir la agregacin para separar las partculas individuales. Por ello antes de proceder a la extraccin de las diferentes fracciones hay una fase previa de preparacin de la muestra. En esta fase previa existen diversos mtodos para separar a las partculas del suelo, unos son mtodos fsicos (trituracin suave, agitacin lenta, agitacin rpida, ultrasonidos, lavado y coccin) y otros son tcnicas qumicas (oxidacin de la materia orgnica con agua oxigenada, ataque cido de los carbonatos y compuestos de Fe con ClH, dispersin de las arcillas con hexametafosfato sdico o amonaco). Como los agentes agregantes pueden ser muy distintos, normalmente no sirve uno slo de estos mtodos sino que se monta una cadena de tratamientos. La extraccin final de las fracciones se realiza por tamizado para las arenas, mientras que la sedimentacin en fase acuosa es el mtodo normal de separacin de los limos y de las arcillas. Si se necesita subfraccionar a la fraccin arcilla se ha de recurrir a la centrifugacin. Durante el presente ejercicio prctico el estudiante conocer los mtodos ms comnmente empleados en Hidrobiologa para la determinacin del contenido orgnico y de las distintas fracciones granulomtricas de los sedimentos lacustres.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
34
1. DETERMINACIN GRANULOMTRICA POR EL MTODO DEL TAMIZ. Indudablemente el mtodo ms ampliamente empleado para el anlisis de los sedimentos es a travs de una batera de tamices cuyos poros difieren en tamao y permiten separar las fracciones del sedimento atendiendo al tamao de la partcula. El lmite menor del tamiz se coloca frecuentemente a 0.062 mm o la divisin entre arena muy fina y limo de acuerdo a la escala de Wentworth (Wentworth 1922, Tabla 1). Tabla 1. Categora de tamao de las partculas del sedimento de acuerdo a Wenworth (1922). Clasificacin Wenworth Arena Muy Gruesa Arena Gruesa Arena Media Arena Fina Arena Muy Fina Limo Arcilla Tamao de la partcula (mm) 1-2 0,5 1 0,25 0,5 0,125 0,25 0,0625 0,125 0,0039 0,0625 < 0,0039 Tamao del poro del tamiz (mm) 1 0.5 0.25 0.125 0.0625 * **
(*) Se separan por el tiempo de sedimentacin. (**) Se separan por centrifugacin. Procedimiento: 1.1. Coloque una porcin mayor a 100 gramos de sedimento en una bandeja o papel de alumnio y dejelo expuesto a la intemperie hasta que este completamente seco. 1.2. Del sedimento seco, pese 100,0 gramos. Arregle una batera de tamices en el siguiente orden de abajo hacia arriba: (0.0625)(0.125)-(0.25)-(0.5)-(1). 1.3. Lleve las columnas de tamices al agitador electrico, coloque la muestra en el tamiz superior y encienda a velocidad media agitando la muestra por 15 minutos. 1.4. Apague el equipo y pese cada fraccion en una balanza analtica. 1.5. Determine el porcentaje de cada fraccin y clasifiquela de acuerdo a la categorizacin de Wenworth.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
35
2. DETERMINACIN DE LIMOS Y ARCILLAS La determinaciones de las fracciones del sedimento que pasan a travs del tamiz de 0,0625 mm pueden separarse y determinarse por medio de los mtodos del hidrmetro y de la pipeta. Durante este ejercicio practico utilizaremos el METODO DE LA PIPETA. 3. DETERMINACIN DE MATERIA ORGNICA. Existen tres procedimientos generales para estimar el contenido de matera orgnica en los sedimentos: 1) Prdida de peso por ingnicin de la muestra; 2) Determiancin del CO2 producido durante la combustin de la muestra, y 3) determinacin de Carbono Orgnico o Nitrgeno. El mtodo de la combustin is la tcnica mejor diseada para producir resultados confiables en el anlisis del contenido orgnico en los sedimentos. Procedimiento: 1. Coloque los crisoles debidamente rotulados con lpiz en una mufla a 550C durante una hora, deje enfriar en el desecador por 10 minutos. Pese el crisol vaco y anote este peso. 2. Agregue una cantidad aproximada de 20-50 grs de sedimento y coloque en el horno a 105C durante 24 a 48 horas. 3. Pese el crisol con la muestra una vez que este se ha enfriado en el desecador. Anote este peso. 4. Coloque el crisol con la muestra en una mufla a 550C por 1 hora. Deje enfriar en el desecador por 15 minutos y pese nuevamente. Anote el resultado. Calculos: Peso Seco = Peso del Crisol con la Muestra a 105 C Peso del Crisol vacio Peso Calcinado = Peso del Crisol con la Muestra a 550C Peso del Crisol vaco. Materia Orgnica (gr) = Peso Seco Peso Calcinado % Materia Orgnica = Materia Orgnica (gr) x 100 / Peso Seco (gr)
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
36
Ejercicio Prctico No. 7:
DETERMINACIN DE PIGMENTOS FOTOSINTTICOS
Introduccin: La evaluacin de la concentracin de clorofila en un volumen determinado de agua puede utilizarse como indicador de la biomasa algal en el mismo. La clorofila es soluble en solventes orgnicos tales como ter, acetona, metanol, cloroformo y piridina. Suelen utilizarse acetona o metanol para su extraccin, ya que rompen los puentes entre los pigmentos y las protenas y solubilizan las clorofilas. La determinacin puede hacerse por colorimetra, espectrofotometra, fluorometra, estimacin de magnesio, etc. Se realizar la determinacin espectrofotomtrica de las clorofilas a, b y total. Esta determinacin depende de la ley de Lambert-Beer. Se miden las absorbancias ( densidades pticas) a diferentes longitudes de onda. Deben conocerse los coeficientes de absorcin especficade los pigmentos puros a cada longitud de onda. Coeficiente de absorcin especfica = D/(d . C) Siendo: D = densidad ptica d = longitud en cm del recorrido de la luz en la celda C = concentracin de pigmentos (g/l) MARCHA DE EXTRACCIN La extraccin de la clorofila debe realizarse en oscuridad y a baja temperatura para reducir al mnimo la fotooxidacin. Se procede de la siguiente manera: 1. Preparacin de la muestra: Las muestras de agua deben ser filtradas a travs de filtros de membrana o de fibra de vidrio. Cuando se utilizan filtros de membrana se recomienda el de 0.45m, y si se emplean los de fibra de vidria es
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
37
2.
3.
4.
5.
recomendable utilizar los de 0.5-0.7m. Presin 0.3 atm. Despus de finalizar la filtracin, el filtro se remueve mientras est an hmedo e inmediatamente se procede a la extraccin de los pigmentos. Cuando la extraccin no puede ser hecha inmediatamente, los filtros deben ser doblados a la mitad con el extracto hacia la parte interna del filtro, colocados en sobres de papel absorbente, o en papel de aluminio en oscuridad y congelados inmediatamente a 20 60C. Extraccin: Aunque muchos compuestos cloroflicos y carotenoides pueden ser extrados con solventes orgnicos, en algunas algas la extraccin no se completa al menos que se produzca la ruptura celular. Para ello el filtro debe ser colocado en un mortero de vidrio-vidrio y se aaden 3 a 4 ml de una solucin al 90% de acetona alcalina (o metanol). Macere la muestra por 45 segundos y decante la solucin en un tubo de centrfuga graduado. Aada 3 ml ms de la solucin de acetona y macere por 15 segundos ms. Aada esta solucin de lavado al mismo tubo de centrfuga anterior y registre el volumen total. Tape el tubo y mantngalo refrigerado y en la oscuridad hasta que haya finalizado con todos los filtros. Centrifugue en una centrfuga clnica (3000 a 4000 rpm, aprox 1000g) por 5 minutos. Remueva cuidadosamente el sobrenadante procurando no remover los residuos sedimentados. Utilice una pipeta Pasteur de punta curva. Coloque el lquido en una cubeta del espectrofotmetro. Mida el coeficiente de extincin del extracto de pigmentos a 750 nm (turbidez del blanco), 665, 664, 663, 647, 630 y 480 nm. La absorcin de 750nm es sustrada de los otros valores para corregir en contra de turbidez y compuestos coloreados. La calibracin al 100% de transmitancia debe hacerse con la solucin de acetona al 90%. Aada 0.1 ml de HCl 0.1N por ml de extracto directamente a la celda, tape y agite vigorosamente. Dejelo reposar por 5 minutos. Vuelva a determinar los coeficientes de extincin a 750, 665 y 663 nm.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
38
6.
Lave la celda copiosamente con la solucin de acetona alcalina y seque por agitacin la celda antes de usarla en otra muestra.
Clculos: Mtodo Monocromtico (Lorenzen, 1967) Chl a (g/l o mg/m3) = (k) (F) (E665o E665a) (v)
(V) (Z)
Donde: E665o = absorbancia turbidez-corregida a 665nm antes de la acidificacin = A665o A750o, A es el valor de absorbancia. E665a= absorbancia turbidez-corregida despus de la acidificacin= A665a- A750a K= coeficiente de absorcin de la clorofila a, = 11,0 F= factor para igualar la reduccin en absorbancia a concentracin inicial de clorofila, 1.7:0.7, o = 2.43. R: cociente mximo de E665o : E665a en la ausencia de feopigmentos, = 1.7 v = volumen del extracto en ml V = volumen del agua filtrada en litros Z = longitud de la celda en cm
Feopigmentos = (k) (F) (E665o-E665o) (v)
(V) (Z)
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
39
Ejercicio Prctico No. 8:
Determinacin de Biomasa y Abundancia Bacteriana en Aguas Naturales
Introduccin : Las transformaciones bioqumicas de materia orgnica disuelta (MOD) y particulada (MOP) realizada por hongos y bacterias son fundamentales para el ciclaje de nutrientes y flujo energtico dentro de los ecosistemas acuticos. Las tasas (velocidades) del crecimiento bacteriano y su productividad son pobremente conocidos en los ecosistemas acuticos. Gran parte de la ausencia de progreso ha resultado de la lenta aplicacin de metodologas de laboratorio a comunidades de bacterias con una gran heterogeneidad. Recientemente se han desarrollado un gran nmero de mtodos que permiten la determinacin del crecimiento y productividad de comunidades de bacterias in situ. La evaluacin de la composicin de especies y el nmero relativo de bacterias heterotrficas por enumeracin directa o por plaqueo sobre medios de cultivos pueden darnos una informacin til acerca del potencial heterotrfico de la comunidad microbiana pero aportan poco cuando queremos conocer la velocidad de los procesos in situ. Todos los cultivos en placas son altamente selectivos y ninguno da un conteo viable total. El conteo directo ha sido facilitado con mtodos de teido de las bacterias con colorantes fluorescentes, filtracin en filtros negros de policarbonatos y examinacin con microscopa de epifluorescencia. El conteo directo es considerado como el mtodo ms confiable para la evaluacin de la dinmica de la comunidad. Las estimaciones de la biomasa a partir del nmero de clulas y de las dimensiones celulares promedio mejoran considerablemente las estimaciones de la dinmica de la comunidad, particularmente las medidas de la productividad bacteriana. Las poblaciones, el tamao celular, el DNA, y la distribucin de la biomasa de bacterias pelgicas pueden ser obtenidas por la intensidad de la fluorescencia producida las clulas teidas con colorantes especfico para cidos nucleicos. La adhesin del colorante
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
40
a las clulas puede producir fluorescencia cuando es excitado con luz de una longitud de onda apropiada. Como resultado las clulas pueden ser diferenciadas de otras partculas a los lmites ms bajos de deteccin del microscopio ptico. Diferentes colorantes fluorescentes estn disponibles. El anaranjado de acridina se adhiere al ADN y ARN de las clulas vivas. Cuando es excitado con luz (436 o 490 nm), el complejo de ADN fluoresce en color verde y el ARN en color rojo. Desafortunadamente, otras partculas no vivas pueden llegar a ser teidas y fluorescen. En aguas que contienen mucho material en suspensin es aconsejable utilizar otro colorante. Por ejemplo, DAPI (46-diamino-2-fenilindol) es especfico para el ADN de las clulas, cuando es excitado a 365 nm , el complejo ADN-DAPI flueresce en color azul, mientras que el DAPI asociado a un material distinto al DNA fluoresce en un amarillo plido. Procedimiento: 1. Obtenga una muestra de agua con una botella de Van Dorn limpia. Preserve la muestra con una solucin de glutaraldehido al 5%. Registre el volumen inicial y final para determinar el factor de dilucin. Mantenga las muestras en hielo y en la oscuridad, Prepare la unidad de filtracin millipore y coloque un filtro de gran porosidad. Monte el filtro negro de 0,2 m sobre el otro filtro. Todos los filtros deben ser humedecidos con agua destilada. Filtre un volumen apropiado de muestra (0,3 a 3 ml para aguas productivas; 5 ml para aguas oligotrficas) con una intensidad baja del vaco (<0.3 atm). Libere el vaco inmediatamente cuando la filtracin est completa. Lave brevemente las paredes del embudo con agua destilada estril (filtrada en 0,2m). Aada 2,0 ml del colorante de anaranjado de acridina al 0.01% (2 ml del stock mas 18 ml de agua filtrada) al filtro dentro del embudo y expngalo por 2 min. Despus de la tincin, drene el colorante a travs del filtro con una fuerza de vaci baja y lave con 2 a 3 ml de agua destilada filtrada estril. Remueva el filtro Nucleopore, seque por 30 segundos sobre un filtro de acetato celulosa y colquelo plano
2.
3.
4.
5.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
41
6.
7.
8.
sobre una gota de aceite de inmersin no fluoresecente en un portaobjetos limpio. Deje caer una gota de aceite de inmersin en el centro del filtro. Cubra con un cubre objetos. Despus de un breve perodo, presione suavemente para expeler el exceso de aceite. Mantenga la preparacin en la oscuridad hasta su examinacin. Con un microscopio compuesto de epifluorescencia observe la muestra en un cuarto semi oscuro. Use aceite de inmersin a 1250X. Cuente las clulas bacterianas. Cuente de 10 a 15 campos por lmina preparada hasta contar por lo menos 300 clulas por cada muestra. Calcule las densidades bacterianas
Bacteria/ml = (factor de conversin de la membrana x N)
D
Donde N= numero promedio de bacterias por campo (nmero total de bacterias contadas/numero total de campos examinados) D= factor de dilucin. Factor de conversin de la membrana = area de filtracin/area del campo contado
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
42
Ejercicio Prctico No. 9
Caracterizacin del Habitat Lacustre: Determinacin de Parmetros Fsicos, Qumicos y Biolgicos
1. Introduccin Durante este ejercicio prctico se establecern varias estaciones de muestreo en un sector comprendido entre la Baha El Tablazo y la Baha de Urub (Desembocadura del Ro Limn). La idea fundamental es la de aplicar diferentes mtodos para registrar algunos parmetros fsicos, qumicos y biolgicos, que son relevantes en la caracterizacin del habitat lacustre. El sistema del Lago de Maracaibo es un estuario parcialmente mezclado, constituido por cuatro zonas, que si bien tienen sus caractersticas propias, de complejidad diversa, son hidrulica y ecolgicamente interdependientes: El Lago de Maracaibo propiamente dicho, con un espejo de agua de 12.400 km 2, el Estrecho de Maracaibo (480 km2), la Baha El Tablazo (640 km2) y el Golfo de Venezuela (12.800 km2). Particularmente, la Baha El Tablazo tiene una forma trapezoidal y dimensiones medias de 27 km en direccin EO y 24 km en direccin N-S, y una profundidad media de 3 m con un 25% de su area con profundidades menores a 1,5 m La cuenca es una amplia fosa de hundimiento ocupada en la actualidad por el Lago y extensas planicies aluviales y delimitadas por un marco montaoso de altura y caractersticas fisiogrficas variables, abarcando por el Sur y Sureste los flancos de la Cordillera de Los Andes, por el Oeste y Noroeste los de la Sierra de Perij y por el Este las estribaciones de la Serrana de Coro.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
43
2. Objetivos Al finalizar la prctica el estudiante estar en capacidad de: a. Elaborar un diseo de muestreo ajustado a los requerimientos de los objetivos propuestos. b. Identificar las caractersticas relevantes del habitat estudiado. c. Utilizar los equipos apropiados para la toma de muestras de agua, sedimento y biota d. Analizar las muestras con metodologas especificas a fin de determinar los siguientes parmetros fsicos, qumicos: profundidad de Secchi, pH, Oxgeno Disuelto, Conductividad, Alcalinidad, Dureza, profundidad, salinidad, granulometra y contenido orgnico de los sedimentos. e. Discutir el estado del ecosistema lacustre en base a las caractersticas fsicas, qumicas y biolgicas. Estaciones de Muestreo El rea de estudio comprende el sector entre la Baha El Tablazo y la Baha de Urub (Ro Limn). En esta rea se ubicarn cuatro estaciones de muestreo las cuales intentan incluir la mayora de las caractersticas presentes en este macrohabitat.
4. Procedimiento:
4.1. Preparacin del Equipo: Los estudiantes deben asistir al laboratorio por lo menos con un da de antelacin a la prctica con la finalidad de preparar y empacar los diferentes equipos y materiales que se emplearn en el desarrollo de las prtica. A tal fn el estudiante debe elaborar una lista de chequeo, de manera de asegurar la inclusin de todos los equipos y materiales. Las soluciones a emplear deber ser cuidadosamente revisadas y chequear que son suficientes para el nmero de determinaciones a realizar. Asimismo, soluciones buffer y electrolitos deben ser chequeados. Una vez que todo el material est completo, ser guardado en cajas de cartn o similar, asegurando muy bien el material de vidrio. El da de la salida de campo el material ser transportado desde el laboratorio al vehculo,
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
44
asegurndose que todo el material ha sido transportado. Es responsabilidad de los estudiantes que todo el equipo y material est debidamente empacado y transportado al vehculo. 4.2. Captacin de Muestras: a. AGUA: La Botella de Van Dorn ser utilizada para la captacin de las muestras de agua a diferentes profundidades. El procedimiento de uso de la Botella ha sido discutido en clase. Estas muestras de agua sern destinadas a la determinacin de gran parte de los anlisis qumicos en el laboratorio. Por esta razn de cada profundidad se llenarn 2 envases plsticos de 500 ml debidamente rotulados con la siguiente informacin: fecha y hora de muestreo, lugar, estacin, profundidad. Estas muestras sern almacenadas en fro para su posterior uso. De igual manera, se llenarn 2 botellas de vidrio para la determinacin del Oxgeno Disuelto. Estas muestras de oxgeno sern fijadas en el campo utilizando MnSO4 y KI-KOH. Por ltimo, se determinar in situ el pH, temperatura, conductividad, Solidos Totales Disueltos y la salinidad con los equipos porttiles. b. SEDIMENTO: Para la captacin de muestras del sedimento se emplear la draga de Eckman, la cual ser armada desde la embarcacin y activada desde la superficie a travs del mensajero. La muestra ser subida a la lancha y vaciada en bolsas plsticas fuertes de por lo menos 5L de capacidad. Se agregar una pequea cantidad de formol al 10% y sern almacenadas en fro hasta su posterior uso.Cada muestra debe ser rotulada con la siguiente informacin: Lugar, Fecha, hora, Estacin. c. BIOTA: Utilizando las redes de zooplancton, se tomarn dos muestras de toda la columna de agua, dejando caer la red hasta el fondo y luego recogindola a una velocidad constante. La red ser cuidadosamente lavada con agua y la muestra al final de la red ser recogida en un envase plstico al cual se le aadir Lugol para su preservacin. d. OTROS: Se evaluar la transparencia del agua utilizando el disco de Secchi. Se registrar la profundidad de Sechhi . Adicionalmente se tomar un registro de la profundidad mxima de la estacin.
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
45
NOTAS IMPORTANTES: - El estudiante debe llevar un cuaderno de campo a fin de registrar toda la informacin levantada in situ. Se recomienda elaborar una tabla indicando la estacin y los parmetros a determinar. Asimismo, debe anotar cualquier observacin que parezca importante a fin de obtener toda la informacin adecuada para caracterizar el habitat. - Todo el equipo utilizado en el campo debe ser cuidadosamente lavado con agua dulce a fin de evitar su deterioro. - Si no est seguro de cmo funciona un equipo, pregunte primero!!! - Utilice ropa apropiada para el trabajo de campo. - Tenga MUCHO CUIDADO con los diferentes reactivos utilizados, son altamente corrosivos. - Como norma de seguridad el bote estar equipado con chalecos salvavidas. Si no sabe nadar utilicelos durante todo el viaje. - La prctica no finaliza despues de la salida de campo. El Oxgeno Disuelto debe ser determinado una vez que regresemos al laboratorio. Asmismo el equipo, una vez lavado, debe ser devuelto a su lugar de origen.
1. Equipos Y Materiales: Disco de Secchi Draga de Eckman Botella de Van Dorn Cuerdas marcadas Mensajeros Baldes Cava Plstica Pizetas con agua destilada Filtros con agua potable Red de Plancton Envases plasticos de 500 ml (20) Bolsas Plsticas para Bentos (10) Equipo Porttil (pHmetro, Conductimetro, TDS, etc) Pilas de 9V Hielo
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
46
Tamices de 500 m Chalecos Salvavidas Reactivos para Oxgeno: MnSO4 y KI-KOH Cuaderno de Campo Solucion de Lugol Viales para el plancton Cuaderno de Campo Jeringas plasticas de 3 cc (4)
Prof. JOS ELI RINCN RAMREZ
Mtodos Hidrobiolgicos -Manual de Trabajos Prcticos
47
BIBLIOGRAFA
American Public Health Association et al. 1998. Standard Methods for the Examination of Water, Sewage, and Wastewater. 20th Edition. American Public Health Association, Washington, D.C. 1185 pp. Brower, J.; Zar, J. & von Ende, C. 1989. Field and Laboratory Methods for General Ecology. Wm.C. Brown Publishers. Iowa. 237 pp. Cabello, D.; Soriano, P.; Segnini, S. & Daz, A. 1996. Ecologa Animal: gua de trabajos prcticos. Universidad de Los Andes. Consejo de Publicaciones. Departamento de Biologa de la Facultad de Ciencias.134 pp. Gee, J.H.R. 1986, Freshwater Studies. Practical Ecology Series. George Allen & Unwin, London. 86 pp. Golterman, H.L, R.S. Clymo, & M.A.M. Ohnstand. 1978. Methods for Physical & Chemical Analysis of Fresh Waters. IBP Handbook N8. Blackwell Scientific Publication, London. Pp.213. Hamilton, L.F. & Simpson, S.G. 1971. Clculos de Qumica Analtica. McGraw-Hill, Mxico. 328 pp. Lind, O. T. 1985. Handbook of common methods in Limnology. 2nd Edition. Kendall/Hunt Publishing Company. Iowa. Pp 199. Wetzel, R.G. & Likens, G. E. 2000. Limnological Analyses. 3rd Edition. Springer-Verlag, New York. Pp 429. Wetzel, R.G. 2000.Limnology: Lake and River Ecosystems. Third edition. Academic Press. California. 1006 pp
Prof. JOS ELI RINCN RAMREZ
You might also like
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadFrom EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadNo ratings yet
- Manual Metodos Hidrobiologicos PDFDocument47 pagesManual Metodos Hidrobiologicos PDFElva EstefaneroNo ratings yet
- Análisis físico y químico de la calidad del aguaFrom EverandAnálisis físico y químico de la calidad del aguaRating: 5 out of 5 stars5/5 (1)
- Laboratorios BioquímicaDocument12 pagesLaboratorios BioquímicaOANo ratings yet
- Guia de Practicas Bioquimica PDFDocument110 pagesGuia de Practicas Bioquimica PDFElizabeth Roxana Canchari LazoNo ratings yet
- Guia de Practicas Laboratorio de Calidad Del AguaDocument111 pagesGuia de Practicas Laboratorio de Calidad Del AguaKaRina RomeroNo ratings yet
- Monica Mendoza Pre2Document8 pagesMonica Mendoza Pre2monica mendozaNo ratings yet
- Informe de Laboratorio - Bio Quimica 2Document17 pagesInforme de Laboratorio - Bio Quimica 2EBER ELOY CONTRERAS DE LA CRUZ100% (1)
- PRACTICA 2-Agua y SolucionesDocument2 pagesPRACTICA 2-Agua y SolucionesBreylin PachecoNo ratings yet
- Guía # 4 - Soluciones y Equilibrio QuímicoDocument6 pagesGuía # 4 - Soluciones y Equilibrio QuímicojorgeNo ratings yet
- DISOLUCIONESDocument5 pagesDISOLUCIONESweberNo ratings yet
- Practicas 6 7 Contam AmbDocument9 pagesPracticas 6 7 Contam Ambmihail calcina taiñaNo ratings yet
- Manual de Practicas de Laboratorio Integral II 2017Document9 pagesManual de Practicas de Laboratorio Integral II 2017Jesús Monroy GuadarramaNo ratings yet
- Manual de Practicas de Laboratorio Integral II 2017Document9 pagesManual de Practicas de Laboratorio Integral II 2017Jesús Monroy GuadarramaNo ratings yet
- UshhhhhhhhhhhhhhhhhhhhhhhDocument11 pagesUshhhhhhhhhhhhhhhhhhhhhhhAndres Camilo Velez HerreraNo ratings yet
- Unidad de Aprendizaje Ii El Lenguaje de Los Compuestos QuimicosDocument5 pagesUnidad de Aprendizaje Ii El Lenguaje de Los Compuestos QuimicosjaimedanielmontejoaranaNo ratings yet
- Acidos y BasesDocument8 pagesAcidos y BasesyhuillcamNo ratings yet
- Informe de Practica N 2Document19 pagesInforme de Practica N 2Jessica Milagros Ayuque SantiagoNo ratings yet
- Lab #4Document8 pagesLab #4Nerry LevyNo ratings yet
- Densidad H2soDocument5 pagesDensidad H2soEber Juan Chira CanchosNo ratings yet
- TRABAJO FINAL QuimiDocument11 pagesTRABAJO FINAL QuimiLisbeth CalvayNo ratings yet
- Practicas de Bioquímica 2009Document38 pagesPracticas de Bioquímica 2009george_mtm28No ratings yet
- LaboratorioDocument27 pagesLaboratorioJhonathan Cutipa QuispeNo ratings yet
- LaboratorioDocument26 pagesLaboratorioPatriciaNo ratings yet
- Experiencia de LaboratorioDocument13 pagesExperiencia de LaboratorioThania Yitzel ArrochaNo ratings yet
- Diseño de Prácticas de Laboratorio y de Práctico de ProblemasDocument12 pagesDiseño de Prácticas de Laboratorio y de Práctico de ProblemasMica TorésNo ratings yet
- Informe de Practica 10Document6 pagesInforme de Practica 10Israel David LuperaNo ratings yet
- Informe Hito 5Document8 pagesInforme Hito 5sevastian veizagaNo ratings yet
- PREPARACION DE SOLUCIONES (Bueno) PDFDocument45 pagesPREPARACION DE SOLUCIONES (Bueno) PDFvaleria giraldoNo ratings yet
- INFORME BIOQUIMICA Soluciones AcuosasDocument5 pagesINFORME BIOQUIMICA Soluciones AcuosasMajo BenavidesNo ratings yet
- INFORMEBIOQUIMICADocument5 pagesINFORMEBIOQUIMICAMajo BenavidesNo ratings yet
- Lab 8. Preparación de Soluciones y TitulaciónDocument4 pagesLab 8. Preparación de Soluciones y Titulaciónjuliana beltranNo ratings yet
- Informe de Quimica 07 PSDocument18 pagesInforme de Quimica 07 PSrosemary010528No ratings yet
- Qan U2 Ea SelmDocument6 pagesQan U2 Ea SelmSergio Martinez100% (1)
- 9° QUÍMICA-TallerAc1 - RevCoordÁrea-AcDocument4 pages9° QUÍMICA-TallerAc1 - RevCoordÁrea-AcgustavoNo ratings yet
- Matriz Aguas ResidualesDocument9 pagesMatriz Aguas Residualesflabia vidaurreNo ratings yet
- Guia Formativa, Laboratorista Quimico. CECyTEH. Gobierno de HidalgoDocument51 pagesGuia Formativa, Laboratorista Quimico. CECyTEH. Gobierno de HidalgoNan Mejia Tlaka100% (4)
- Preinforme Laboratorio de QuimicaDocument16 pagesPreinforme Laboratorio de QuimicaFrancisco Ramirez VanegasNo ratings yet
- Informe de Laboratorio Preparación deDocument9 pagesInforme de Laboratorio Preparación deJESSICA SABI GOMESNo ratings yet
- Práctica 3Document15 pagesPráctica 3Ari UCNo ratings yet
- Informe de La Determinacion de DBO5Document15 pagesInforme de La Determinacion de DBO5Lizy Ardiles Amado0% (1)
- P11 - Equilibrio Iónico y PHDocument4 pagesP11 - Equilibrio Iónico y PHAngie Celeny GarzonNo ratings yet
- Guía Práctica 4 - Virtual - Soluciones - Diluciones y PHDocument8 pagesGuía Práctica 4 - Virtual - Soluciones - Diluciones y PHJames BenavidesNo ratings yet
- tp2 AGUApHSOLUCIONES ENF 2022Document4 pagestp2 AGUApHSOLUCIONES ENF 2022Yovana GutierrezNo ratings yet
- Universidad Autónoma Tomas FríasDocument13 pagesUniversidad Autónoma Tomas FríasArmando Ticona100% (1)
- Actividad Formativa Seccion 55 Laboratorio de HigieneDocument3 pagesActividad Formativa Seccion 55 Laboratorio de HigieneBarbara BrevisNo ratings yet
- Informe de Practica de Quimica InorganicaDocument30 pagesInforme de Practica de Quimica InorganicaLili Cerquera QuinayaNo ratings yet
- Práctica 1 BI-244Document17 pagesPráctica 1 BI-244CN Kenyu AlexNo ratings yet
- Quimica InformeDocument4 pagesQuimica InformePäu JiménezNo ratings yet
- Tratamiento Físico QuímicoDocument13 pagesTratamiento Físico QuímicoElmer Chilon MinchanNo ratings yet
- Quimica 8Document7 pagesQuimica 8Alvaro BautistaNo ratings yet
- Manual de Química para Ingenieros Civiles 2018Document46 pagesManual de Química para Ingenieros Civiles 2018Elizabet Hernández ÁlvarezNo ratings yet
- PL 03 - Soluciones (Guia Unmsm Laboratorio Quimica)Document2 pagesPL 03 - Soluciones (Guia Unmsm Laboratorio Quimica)CARLOS ENRIQUE TARAZONA VALVERDENo ratings yet
- Guia Analisis AmbientalDocument294 pagesGuia Analisis AmbientalBrando Martinez HernandezNo ratings yet
- Taller Lodos 2Document38 pagesTaller Lodos 2JANNY MICHELT MESA LUGONo ratings yet
- Blas Furiati - Reporte de Practica 7Document6 pagesBlas Furiati - Reporte de Practica 7Blas FuriatiNo ratings yet
- Trabajo de Fisicoquimica Ambiental PDFDocument11 pagesTrabajo de Fisicoquimica Ambiental PDFJavierD1995No ratings yet
- Lab 3 PH y AmortiguadoresDocument3 pagesLab 3 PH y AmortiguadoresDiego Giraldo BoteroNo ratings yet
- Manual de Practicas de Quimica OrganicaDocument69 pagesManual de Practicas de Quimica OrganicaShandira Itzel Idiaquez RiosNo ratings yet
- Buenas Practicas ExploracionDocument24 pagesBuenas Practicas ExploracionJabileth PortilloNo ratings yet
- UreaDocument41 pagesUreaFernanda MartinezNo ratings yet
- Capacidad ExportadoraDocument5 pagesCapacidad ExportadoraRichard SantosNo ratings yet
- Modelo 1 ParcialDocument2 pagesModelo 1 Parcialnatalia2004100% (1)
- Blusa y Sus ModificacionesDocument36 pagesBlusa y Sus ModificacionesIntershenyNo ratings yet
- Taller de Psicologia Del Color: Juliana Areiza Cano 10°3Document56 pagesTaller de Psicologia Del Color: Juliana Areiza Cano 10°3Wilder RenteríaNo ratings yet
- Sistemas de Salud de ArgentinaDocument29 pagesSistemas de Salud de Argentinastella maris100% (1)
- Satipatthana SuttaDocument18 pagesSatipatthana SuttaAna Maria Rodriguez RodriguezNo ratings yet
- Cuestionario de Tecnología Del ConcretoDocument7 pagesCuestionario de Tecnología Del ConcretoJose Luis Ricardo Adriam RomeroNo ratings yet
- Revista Quimica Teorica y PracticaDocument84 pagesRevista Quimica Teorica y PracticaCarlosNo ratings yet
- Etica Profesional 1 CodigosDocument4 pagesEtica Profesional 1 CodigosGuadu MendozaNo ratings yet
- Dermatitis SeborreicaDocument24 pagesDermatitis SeborreicaRafael Cruz MNo ratings yet
- Lipesa 3003 HDSDocument6 pagesLipesa 3003 HDSJose David Perez ArangoNo ratings yet
- 7B Martes 13 de Oct de 2020Document1 page7B Martes 13 de Oct de 2020Henry LinNo ratings yet
- Tipos de MineriaDocument8 pagesTipos de MineriaGIANELLA MOLINA RIOSNo ratings yet
- Código: MIS-4-1-3-FR07 VERSIÓN 02Document17 pagesCódigo: MIS-4-1-3-FR07 VERSIÓN 02ALICIA MARÍA GÁMEZ CAUSILNo ratings yet
- Aparato Respiratorio (Word Triptico)Document2 pagesAparato Respiratorio (Word Triptico)Diego ChimoyNo ratings yet
- Capitulo IiDocument13 pagesCapitulo IiCarolin LunaNo ratings yet
- Ecologia de PoblacionesDocument28 pagesEcologia de PoblacionesCamilo :DNo ratings yet
- 4 Problemas SolucionesDocument4 pages4 Problemas Solucionesshelviton0% (1)
- Problema de Aplicación de Ecuación 2Document8 pagesProblema de Aplicación de Ecuación 2Wilman RenteriaNo ratings yet
- ADITIVOSDocument8 pagesADITIVOSVladimir Sisalema DelgadoNo ratings yet
- Matriz - Riesgos Sofia CañizalesDocument13 pagesMatriz - Riesgos Sofia Cañizalesmilan7981No ratings yet
- Biocombustibles de Tercera Generación A Partir de MicroalgasDocument13 pagesBiocombustibles de Tercera Generación A Partir de MicroalgasGIANNY GUILLERMO CORTES RUBIONo ratings yet
- Curso Practico de Trabajos en AlturaDocument69 pagesCurso Practico de Trabajos en Alturacarlitos_12587100% (1)
- Flujo Grama Accidente CasinoDocument2 pagesFlujo Grama Accidente CasinoAngelo MolinaNo ratings yet
- QUIMICA Final EJE IIDocument28 pagesQUIMICA Final EJE IIJesús Martínez MejíaNo ratings yet
- Cuestionario Factores de ResilienciaDocument5 pagesCuestionario Factores de ResilienciaJERSON EMILIO CARRASCAL RINCONNo ratings yet
- Responsabilidad OftalmologoDocument393 pagesResponsabilidad OftalmologoalbertpoNo ratings yet
- Tarea1.3 EduuDocument35 pagesTarea1.3 EduuEduardo D Uc UicabNo ratings yet