Professional Documents
Culture Documents
Informe Acido Acetico Yesid
Uploaded by
SnaiderCespedesSuarez0 ratings0% found this document useful (0 votes)
18 views5 pagesCopyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
18 views5 pagesInforme Acido Acetico Yesid
Uploaded by
SnaiderCespedesSuarezCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 5
Analisis a Realizar a el proyecto
Realizado por: Laura Arias
Anderson Murcia
Camilo Pea
Snaider Gallego
Camila Arias
1. Anlisis de la materia prima
2. CARBOHIDRATOS DE LAS UVAS PASAS
3.
4. A continuacin, se muestran una serie de tablas con la cantidad de carbohidratos
de las uvas pasas, uno de los alimentos pertenecientes a la categora de las frutas
desecadas:
5. La siguiente tabla muestra una lista de la cantidad de hidratos de carbono simples
de las uvas pasas:
Nutriente Cantidad Nutriente Cantidad
Azcar 69,30 g. Lactosa 0 g.
Fructosa 34,80 g. Maltosa 0 g.
Galactosa 0 g. Oligosacridos 0 g.
Glucosa 34,50 g. Sacarosa 0,00 g.
6. En la tabla siguiente, se muestra una lista de la cantidad de cidos orgnicos de
las uvas pasas:
Nutriente Cantidad Nutriente Cantidad
cido actico 0 g. cido oxlico 0 g.
cido ctrico 0,10 g. cido tartrico 0 g.
cido lctico 0 g. cidos orgnicos disponibles 0 g.
cido mlico 1,46 g.
7. A continuacin, se muestra la lista de fitosteroles de las uvas pasas:
Nutriente Cantidad Nutriente Cantidad
Avenaesterol d5 0 mg. Estigmasterol 0 mg.
Avenaesterol d7 0 mg. Estigmasterol d7 0 mg.
Beta sitosterol 0 mg. Fitosterol 0 mg.
Brasicaesterol 0 mg. Otros fitosteroles 0 mg.
Campesterol 0 mg.
8. La tabla siguiente contiene los hidratos de carbono no disponibles de las uvas
pasas:
Nutriente Cantidad Nutriente Cantidad
Almidn 0 g. Lignina 0 g.
Almidn 0 g. Polisacridos no celulsicos 0,20 g.
resistente insolubles
Celulosa 0,80 g.
Polisacridos no celulsicos
solubles
1 g.
9. La cantidad de estos nutrientes corresponde a 100 gramos de uvas pasas.
2. anlisis de la fermentacin
Rendimiento: Es la relacin entre el alcohol producido y el azcar puesto a disposicin de la
levadura, tericamente por 100 Kg de melaza se obtienen 33 litros de alcohol.
A partir de las reacciones:
C6H12O6 2C2H5OH + CO2 + ENERGA 0
C11H22O11 4C2H5OH + 4CO2
se calcula el alcohol terico producido si toda la glucosa y sacarosa presente en el mosto se
transforman en etanol. El rendimiento se puede expresar como:
R = (alcohol real/alcohol terico)*1000
PH: Este es un factor importante en la fermentacin, debido a su importancia en el control de la
contaminacin bacterial como tambin al efecto en el crecimiento de las levaduras, en la
velocidad de fermentacin y en la formacin de alcohol. Durante la fermentacin la levadura toma
el nitrgeno de los aminocidos orgnicos, perdiendo su carcter anftero y pasando a cidos, lo
cual origina una disminucin del pH del medio. Cuanto ms bajo el pH del medio, tanto menor el
peligro de infeccin, pero si se trabaja con pH muy bajos la fermentacin es muy lenta, ya que la
levadura no se desarrolla de la forma conveniente. Segn estudios se hall que el pH ms
favorable para el crecimiento de la saccharomyces cerevisiae se encuentra entre 4.4 - 5.0, con un
pH de 4.5 para su crecimiento ptimo.
Concentracin del sustrato: Suele ser satisfactoria una concentracin de azcar del 10 al 18%, el
valor ms corriente es del 12%. Cuando se trabaja con concentraciones de azcar muy altas, del
orden de 22%, se observa una deficiencia respiratoria en la levadura y un descenso de la velocidad
de fermentacin; por el contrario, al trabajar con concentraciones muy bajas, el proceso resulta
antieconmico ya que requiere un mayor volumen para la fermentacin. Por esto se utiliza como
sustrato la melaza, que tiene de 10 - 15% de azcar.
3. anlisis del producto terminado
Valoracin de un vinagre
Objetivo
Determinar la concentracin de cido actico en un vinagre comercial.
Teora
La valoracin de un cido con una base es un proceso que por lo general comprende dos
partes: estandarizacin de la base con un cido patrn y valoracin de la solucin de
inters con la base ya estandarizada.
La base debe ser estandarizada porque reacciona fcilmente con el CO
2
del aire o con
componentes cidos que pueden estar presentes en el recipiente donde se almacena. Si el
recipiente est hecho de polietileno o de polipropileno, el CO
2
se difunde con facilidad a
travs de las paredes del envase y reacciona con la base:
CO
2
+ NaOH ---> NaHCO
3
El cido que se utiliza para la estandarizacin es generalmente un slido de alta pureza y
estabilidad. En este experimento se usar ftalato cido de potasio como patrn primario.
La reaccin de neutralizacin con la base es:
KHC
8
H
4
O
4
+ NaOH ---> KNaC
8
H
4
O
4
+ H
2
O
n
b
= n
a
= (m
a
/ M
a
) = (m
a
/ 204.1) (19.1)
El punto de equivalencia de la reaccin se determina por valoracin colorimtrica utilizando
un indicador, siendo el ms apropiado para este caso la fenolftalena. La solucin de
ftalato, disuelto en el erlenmeyer, es inicialmente incolora y luego vira a un color rosa
permanente con la adicin de la base.
Cb = (n
b
/ V
b
) (19.2)
El procedimiento a seguir para la valoracin del vinagre es idntico al de estandarizacin
de la base.
n CH
3
COOH = V
b
x C
b
(19.3)
Con ayuda de la ecuacin 20.3 se puede determinar el porcentaje de cido actico en el
vinagre:
Porcentaje CH
3
COOH = (19.4)
Materiales y equipo
Ftalato cido de potasio, NaOH, vinagre, fenolftalena
Bureta
Erlenmeyer
Beaker
Embudo
Procedimiento
Se preparan 100 mL de solucin de NaOH aproximadamente 0.20 M. Enseguida se toma
una bureta, se lava con agua desionizada y se purga con la solucin anteriormente
preparada. La bureta se llena con esta solucin
Valoracin de un vinagre
Pesar dos muestras de ftalato cido de potasio cuyo peso est en el rango de 0.45 a 0.55
g. Transferir cada muestra a un erlenmeyer y aadir 25.00 mL de agua destilada con el fn
de disolverlas. Adicionar dos gotas de fenolftalena a cada solucin.
Valorar cada una de las soluciones de ftalato con el NaOH hasta obtener un color rosa
permanente.
Despus de descartar las dos soluciones ya valoradas, se lavan los erlenmeyers con
pequeas porciones de agua destilada y se aaden 5.00 mL del vinagre a cada uno. Luego
se adicionan 25.00 mL de agua destilada y dos gotas de indicador.
La valoracin de las muestras de vinagre se hace con el NaOH hasta obtener un color rosa
permanente.
Datos y resultados
Datos de la valoracin de un vinagre
Experimento Sustancia masa /volumen V NaOH (mL) Concentracin
1
a
ftalato ______ g C
NaOH
= M
1
b
ftalato ______ g C
NaOH
= M
2
a
Vinagre _____ mL ______ g/mL
2
b
Vinagre _____ mL ______ g/mL
You might also like
- % SacarosaDocument3 pages% SacarosaSnaiderCespedesSuarezNo ratings yet
- Técnicas de MuestreoDocument509 pagesTécnicas de MuestreoLeitox6987% (23)
- Cromatografia en Capa FinaDocument6 pagesCromatografia en Capa FinaSnaiderCespedesSuarezNo ratings yet
- Cuantificacion Turbidimetrica de SulfatosDocument7 pagesCuantificacion Turbidimetrica de SulfatosSnaiderCespedesSuarezNo ratings yet
- NTC2177 Buretas Tiempo de 30 SDocument6 pagesNTC2177 Buretas Tiempo de 30 SFërnando Rodrîguëz HerreräNo ratings yet
- Técnicas de MuestreoDocument509 pagesTécnicas de MuestreoLeitox6987% (23)
- Marcha analítica cationesDocument5 pagesMarcha analítica cationesariza44595No ratings yet
- NTC271Document10 pagesNTC271SnaiderCespedesSuarezNo ratings yet
- 2200Document10 pages2200Wendy TorresNo ratings yet
- NTC271Document10 pagesNTC271SnaiderCespedesSuarezNo ratings yet
- NTC 2052 Pipetas Aforadas (De Un Solo Trazo)Document10 pagesNTC 2052 Pipetas Aforadas (De Un Solo Trazo)David MoyanoNo ratings yet
- Delmar-Protocolo 15 12 2017Document21 pagesDelmar-Protocolo 15 12 2017Delmar Ernesto Lopez QuirozNo ratings yet
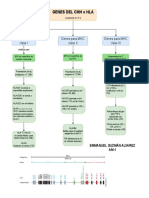
- Genes de HLA o MHCDocument1 pageGenes de HLA o MHCEmmanuel GNo ratings yet
- Atb DR VaqueDocument3 pagesAtb DR VaqueSamuel Vaque RamírezNo ratings yet
- Ejes y PlanosDocument14 pagesEjes y PlanosbrauliolgNo ratings yet
- Higiene Ambiental IIDocument40 pagesHigiene Ambiental IIdarial10No ratings yet
- Eras GeológicasDocument3 pagesEras GeológicasMARIA JOSE RIVERA CASTRILLONNo ratings yet
- TrabajoDocument5 pagesTrabajojose armandoNo ratings yet
- Exposición. Práctica #6. Glutatión y Su Rol OxidativoDocument27 pagesExposición. Práctica #6. Glutatión y Su Rol OxidativoStefani RSNo ratings yet
- Unidad 3 Tema 3.2.6 SclerosporalesDocument3 pagesUnidad 3 Tema 3.2.6 SclerosporalesLuizNo ratings yet
- Relaciones Afectivas: Aprendiendo a AmarDocument13 pagesRelaciones Afectivas: Aprendiendo a AmarJulian FloresNo ratings yet
- Investigación y Ciencia 347 - Agosto 2005 PDFDocument99 pagesInvestigación y Ciencia 347 - Agosto 2005 PDFDichter Dichter D100% (3)
- Tarea 14-Ejemplos de SilogismosDocument5 pagesTarea 14-Ejemplos de SilogismosC CASTILLONo ratings yet
- Fichas Técnicas ActualizadasDocument16 pagesFichas Técnicas ActualizadasJhonatan Paredes100% (1)
- Fermentacion Acética - IndustrialDocument28 pagesFermentacion Acética - Industrialhidalmis meriño britoNo ratings yet
- PIlates TerapéuticoDocument105 pagesPIlates TerapéuticoMariana GeraliNo ratings yet
- Resumo Columna VertebralDocument7 pagesResumo Columna VertebralRachel HuberNo ratings yet
- Revista Natura Ciclo 15 PDFDocument138 pagesRevista Natura Ciclo 15 PDFYuri GzlsNo ratings yet
- Historia y Ramas de La Medicina ForenseDocument25 pagesHistoria y Ramas de La Medicina ForenseJosue100% (1)
- 9 Articulaciones. PGMDocument33 pages9 Articulaciones. PGMshelsie100% (1)
- 401 Alteraciones EquilibrioDocument7 pages401 Alteraciones EquilibrioLisset AdasmeNo ratings yet
- Ciclo de Nitrogeno y AzufreDocument2 pagesCiclo de Nitrogeno y AzufreALEX CRISTOPHER CJUNO QUISPENo ratings yet
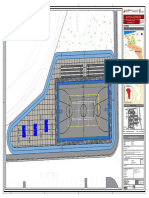
- 01 Urbanismo Antonio Ricaute - CANCHA Y PISTA DE TROTEDocument1 page01 Urbanismo Antonio Ricaute - CANCHA Y PISTA DE TROTEELIANANo ratings yet
- Examen SustitutorioDocument4 pagesExamen SustitutorioGulliano Gussepi Silva PazNo ratings yet
- Encuesta para Medir Estrés LaboralDocument8 pagesEncuesta para Medir Estrés LaboralPerla Duran100% (1)
- Consolidado Texto Modulo IVDocument936 pagesConsolidado Texto Modulo IVANGELO MOISES ABAD MACIASNo ratings yet
- EcologíaDocument2 pagesEcologíaEliza ZavaletaNo ratings yet
- Datura StramoniumDocument25 pagesDatura StramoniumAna PerezNo ratings yet
- Manual de Intervención en Crisis en Situaciones de Desastre PDFDocument38 pagesManual de Intervención en Crisis en Situaciones de Desastre PDFDr. José Antonio Ayerdis ZamoraNo ratings yet
- Traumatismo CraneoencefálicoDocument52 pagesTraumatismo CraneoencefálicoCesar BarriosNo ratings yet
- El Timo y Sus GeneralidadesDocument5 pagesEl Timo y Sus GeneralidadesGiane VacaNo ratings yet