Professional Documents
Culture Documents
Objetivos de Quimica
Uploaded by
XXXFHERXXX0 ratings0% found this document useful (0 votes)
11 views3 pagesOriginal Title
OBJETIVOS DE QUIMICA.docx
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
11 views3 pagesObjetivos de Quimica
Uploaded by
XXXFHERXXXCopyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 3
INTRODUCCION
El trabajo que a continuacin se le presentara con tiene informacin
relacionada respecto a con la Experiencia de Melde, Ondas estacionarias-
Movimiento armonico forzado, con el propsito fundamental de desarrollar
habilidades que permitan realizar obsevaciones de experimentos sencillos y de
las condiciones bajo las cuales se realizan.
En este quinto laboratorio de fsica estudiaremos la el comportamiento del
armnico forzado (en este caso por medio de las cuerda).Tambien Con la
ayuda de la experiencia de Melde podremos experimetar la variacin de
frecuencia a tensin constante. Luego Veremos la variacin de tensin y
frecuencia constante y procederemos a determinar las longitudes de onda, todo
esto gracias a un generador de ondas.
Tambien trabajaremos con el programaPasco Capstone para ver la resonancia
de un resorte.
OBJETIVOS
Determinar experimentalmente la relacin entre la tensin de la cuerda y
el nmero de segmentos de la onda estacionaria.
Tambien se determinara experimentalmente la relacin entre la
frecuencia de oscilacin de la cuerda y el numero de segmentos de la
onda estacionaria.
Calcular la densidad lineal de la cuerda utilizada.
Determinar la relacin entre la frecuencia de oscilacin de la cuerda y la
longitud de onda.
Investigar el movimiento de un sistema masa resorte que oscila prximo
a su frecuencia natural.
La corrosin electroqumica es un proceso espontneo que denotasiempre la
existencia de una zona andica (laque sufre la corrosin), una zonacatdica y
un electrolito, y esimprescindible la existencia deestos tres elementos,
adems deuna buena unin elctrica entrenodos y ctodos, para
que estetipo de corrosin pueda tener lugar.La corrosin ms
frecuentesiempre es de naturalezaelectroqumica y resulta de
laformacin sobre la superficiemetlica de multitud de
zonasandicas y catdicas; el electrolitoes, en caso de no estar
sumergidoo enterrado el metal, el agua condensada de la
atmsfera, para lo que la humedadrelativa deber ser del 70%.El
proceso de disolucin de un metal en un cido es igualmente un
procesoelectroqumico. La infinidad de burbujas que aparecen sobre la
superficie metlicarevela la existencia de infinitos ctodos, mientras
que en los nodos se vadisolviendo el metal. A simple vista es imposible
distinguir entre una zona andica yuna catdica, dada la naturaleza
microscpica de las mismas (micropilasgalvnicas). Al cambiar
continuamente de posicin las zonas andicas y catdicas,llega un
momento en que el metal se disuelve totalmente.
Ya que la corrosin de los metales en ambientes hmedos es de naturaleza
electroqumica, una aproximacin lgica para intentar parar la
corrosin sera mediante mtodos electroqumicos. Los mtodos
electroqumicos para la proteccincontra la corrosin requieren de un
cambio en el potencial del metal para prevenir oal menos disminuir su
disolucin.
CELDAS ELECTROLTICAS:
La celda electroltica transforma una corriente elctrica en una
reaccin qumica de oxidacin-reduccin que no tiene lugar de modo
espontneo. En muchas de estas reacciones se descompone una
sustancia qumica por lo que dicho proceso recibe el nombre de
electrolisis. Tambin reciben los nombres de
celda electroltica o cuba electroltica
. A diferencia de la celda voltaica, en la clula electroltica, los dos
electrodos no necesitan estar separados, por lo que hay un slo recipiente
en el que tienen lugar las dos semirreacciones.
CELDAS GALVNICAS:
La energa liberada por una reaccin redox espontnea puede usarse para
realizar trabajo elctrico. Esta tarea se cumple por medio de una
celda voltaica(o galvnica), un dispositivo en el que la transferencia de
electrones tiene lugar a lo largo de un camino externo, y no directamente
entre los reactivos. Se lleva a cabo una reaccin espontnea de este tipo
cuando se coloca una tira de zinc en contacto con una disolucin que contiene
Cu2_. A medida que la reaccin avanza, el color azul de los iones Cu2_(ac )
se desvanece, y se deposita cobre metlico sobre el zinc. Al mismo
tiempo, el zinc comienza a disolverse.
Zn(s) + Cu2+(ac) Zn2+(ac) + Cu(s)
You might also like
- ESLINGASDocument5 pagesESLINGASXXXFHERXXX100% (1)
- Pin TurasDocument54 pagesPin TurasRodrigo MuñozNo ratings yet
- 251945727-Elaboracion-de-Sidra Bio PDFDocument30 pages251945727-Elaboracion-de-Sidra Bio PDFSabrina Gutierrez GarciaNo ratings yet
- Pernos Soldadura 01 ASTM A325 A490 AISC - FCPDocument73 pagesPernos Soldadura 01 ASTM A325 A490 AISC - FCPluisocsaincaNo ratings yet
- Clasificación de Material de Laboratorio Por Su Uso y EquipamientoDocument42 pagesClasificación de Material de Laboratorio Por Su Uso y EquipamientoLolo West0% (1)
- Sesion #17 - Procesos Unitarios 17 - Polimerizacion & FermentacionDocument72 pagesSesion #17 - Procesos Unitarios 17 - Polimerizacion & FermentacionManuel Garcia Pantigozo100% (5)
- Informe Bromatologia ReyesDocument38 pagesInforme Bromatologia ReyesMirella Reyes Yalli100% (1)
- 8 Compromisos PAT 2015 CIRCADocument6 pages8 Compromisos PAT 2015 CIRCAXXXFHERXXXNo ratings yet
- Informe de Turbina PeltonDocument24 pagesInforme de Turbina PeltonSolorzano Chuquimantari Joubert100% (12)
- Seccion de FlotacionDocument9 pagesSeccion de FlotacionXXXFHERXXXNo ratings yet
- LeonDocument5 pagesLeonXXXFHERXXXNo ratings yet
- LAB 03-2019-1 Luis SancaDocument12 pagesLAB 03-2019-1 Luis SancaXXXFHERXXXNo ratings yet
- Impacto Ambiental Del Uso de Sustancias RefrigerantesDocument11 pagesImpacto Ambiental Del Uso de Sustancias RefrigerantesXXXFHERXXXNo ratings yet
- Refrigeracion en La Industria FarmaceuticaDocument9 pagesRefrigeracion en La Industria FarmaceuticaXXXFHERXXXNo ratings yet
- SESION 11 - Ejercicios de Cinematica de MecanismosDocument9 pagesSESION 11 - Ejercicios de Cinematica de MecanismosXXXFHERXXXNo ratings yet
- T12 Tareas de PrealineamientoDocument6 pagesT12 Tareas de PrealineamientoXXXFHERXXXNo ratings yet
- Lab 2 RefirgeracionDocument9 pagesLab 2 RefirgeracionXXXFHERXXXNo ratings yet
- Refrigeracion en La Industria Farmaceutica y PetroquimicaDocument10 pagesRefrigeracion en La Industria Farmaceutica y PetroquimicaXXXFHERXXXNo ratings yet
- Estratégica Del MantenimientoDocument13 pagesEstratégica Del MantenimientoXXXFHERXXXNo ratings yet
- Informe Lab. 6Document16 pagesInforme Lab. 6XXXFHERXXXNo ratings yet
- Refrigeracion en La Industria Farmaceutica y PetroquimicaDocument10 pagesRefrigeracion en La Industria Farmaceutica y PetroquimicaXXXFHERXXXNo ratings yet
- Laboratorio 2 Estructuras MetalicasDocument4 pagesLaboratorio 2 Estructuras MetalicasXXXFHERXXXNo ratings yet
- Modelos AtómicosDocument2 pagesModelos Atómicosprofeafrancoh100% (2)
- Taller Carbohidratos HAYDE MAURICIODocument14 pagesTaller Carbohidratos HAYDE MAURICIOHeidi MauNo ratings yet
- Química Ambiental - Alcalindad Del AguaDocument5 pagesQuímica Ambiental - Alcalindad Del AguaJonathan ManriqueNo ratings yet
- Cinetica y Equilibrio 1Document2 pagesCinetica y Equilibrio 1Anamaria LozadacampoNo ratings yet
- Ciclo Del Agua-2Document8 pagesCiclo Del Agua-2Lyly CkNo ratings yet
- Globo de Nitrogeno - (Document14 pagesGlobo de Nitrogeno - (Lisseth AstudilloNo ratings yet
- Frutos SecosDocument4 pagesFrutos SecosGema ToapantaNo ratings yet
- Migracion de PoliofelinasDocument14 pagesMigracion de PoliofelinasManuel Emigdio Doria ViloriaNo ratings yet
- Ensayos de Actitud y Interlaboratorios ONACDocument16 pagesEnsayos de Actitud y Interlaboratorios ONACHarold MondragonNo ratings yet
- Investigacion Previa - Estilación Por Arrastre de VaporDocument6 pagesInvestigacion Previa - Estilación Por Arrastre de VaporJose Daniel Correa RangelNo ratings yet
- Ejercicios Espectroscopia Ir-1Document5 pagesEjercicios Espectroscopia Ir-1Neftaly Sarahi RodriguezNo ratings yet
- DOMOS SALINOS DEL SURESTE DE MEXICO Orig PDFDocument27 pagesDOMOS SALINOS DEL SURESTE DE MEXICO Orig PDFLuis M. Callejas YescasNo ratings yet
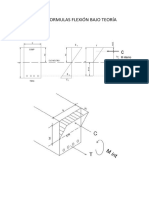
- Deducción Formulas Flexion Teoría ElásticaDocument6 pagesDeducción Formulas Flexion Teoría ElásticaAlejandro San MartinNo ratings yet
- El Cloruro de ViniloDocument2 pagesEl Cloruro de ViniloNatalia GonzalezNo ratings yet
- GUÍAS DE LABORATORIO BIO 110 Modalidad Virtual 2.0Document59 pagesGUÍAS DE LABORATORIO BIO 110 Modalidad Virtual 2.0Adrian PalaciosNo ratings yet
- Biologia TallerDocument4 pagesBiologia TallerAndy PerezNo ratings yet
- 02 RECONOCIMIENTO DE ELEMENTOS DE LA MATERIA ORGÁNICA (1) - Convertido........Document17 pages02 RECONOCIMIENTO DE ELEMENTOS DE LA MATERIA ORGÁNICA (1) - Convertido........Yerson Yair Pacheco GuerreroNo ratings yet
- Bitácora de Práctica 4.4. Obtención de DNA PlasmídicoDocument3 pagesBitácora de Práctica 4.4. Obtención de DNA PlasmídicoOz HdzNo ratings yet
- Algoritmo-10 6 (8732)Document6 pagesAlgoritmo-10 6 (8732)Itzel SaucedaNo ratings yet
- Tereftalato de PolietilenoDocument3 pagesTereftalato de PolietilenoArturo GarciaNo ratings yet
- Elaboración de Un Jabón de Barra Con Extractos de Semilla de Girasol.Document26 pagesElaboración de Un Jabón de Barra Con Extractos de Semilla de Girasol.César A. F. VillarNo ratings yet
- 1 DqoDocument7 pages1 DqoErick Guillermo Quispe RiveraNo ratings yet
- TubingDocument5 pagesTubingAntonio LantiguaNo ratings yet
- Práctica 2 Lab de MaterialesDocument5 pagesPráctica 2 Lab de MaterialesJair DelgadoNo ratings yet