Professional Documents
Culture Documents
Laboratorio Termo Icimsssss
Uploaded by
Juan José Montoya San MartínOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Laboratorio Termo Icimsssss
Uploaded by
Juan José Montoya San MartínCopyright:
Available Formats
Universidad de La Frontera
Facultad de Ingeniera y Ciencias
Departamento de Ingeniera Mecnica
Laboratorio N2
Aplicaciones de la 1era Ley de la Termodinmica
Nombre de los Estudiantes : Mara Victoria Irigoin
Ignacio Ros
Carlos Tern
Andrs Ortega
Oscar Llanquitruf
Fabin LLanquitru
David Bustos
Nicols Anselmo
Juan Jos Montoya
Ricardo Palma
Simn Seplveda
Cristbal Bravo
Mauricio Cifuentes
Matas Zabala
Diego Sanhueza
Jean Pierre Schuffenegger
Juan Contreras
Nombre de la Asignatura : Termodinmica Aplicada
Carrera : Ingeniera Civil Industrial m. Mecnica
Fecha de entrega : 03 de Octubre de 2014
2
Objetivo:
Realizar un balance de energa en un sistema cerrado cclico con la finalidad de demostrar la
validez del principio de conservacin de la energa.
Diagrama Presin- Entalpa del proceso:
3
Tabla de datos:
El flujo msico es permanente y tiene el valor de 2,4 lb/min = 0,04 lb/sec.
Estados
Presin
(psi)
Temperatura
(F)
Altura
(ft)
Volumen
(ft
3
/lb)
Densidad
(lb/ft
3
)
Entalpia
(BTU/lb)
1 158,7 146 0,098425 0,286191 3,494169 94,14
2 158,7 104 2,2802 0,012783 78,228897 32,043
3 62,7 50 2,2802 0,011742 85,164367 32,043
4 62,7 76 0,75459 0,695984 1,436814 86,492
Calculo del rea:
Datos:
Dimetro exterior (De): 9,4 mm = 0.3700
Espesor (e): 0,016
El dimetro interior (Di) ser igual al dimetro
exterior menos dos veces el espesor, como se
aprecia en la figura.
Di = De-2e = 0,338 = 0,028 ft
El rea entonces ser:
Clculo de energas:
Para hacer el balance energtico, se necesitan los valores de las energas cinticas y potencial. Las
frmulas para calcular estas energas y las velocidades son:
En la siguiente tabla se muestran los valores de los resultados.
Estado Velocidad (ft/sec) e
c
(BTU/lb) e
p
(BTU/lb)
1 18,3750 0,00674283 0,00012589
2 0,08207 1,3448*10
-5
0,00291644
3 0,7539 1,1347*10
-3
0,00291644
4 44,6859 0,03987757 0,00096514
4
Para calcular el balance energtico del sistema, es necesario calcular los balances de los
subsistemas y as evaluar la actividad energtica del sistema total.
Balance subsistema 1-2
)
Balance energtico parcial:
5
Balance subsistema 3-4
)
Balance energtico parcial:
6
Balance subsistema 4-1
)
Balance energtico parcial:
)
)
Balance energtico del sistema total
E
TOTAL DEL SISTEMA
=0
Se cumple la primera ley de la termodinmica, la cual seala que la energa no se crea ni se
destruye solo se transforma.
7
Conclusiones
Una de las principales cosas que podemos determinar de este laboratorio, es que la energa se
conserva. Esto debido a que los flujos de energa de salida son iguales a los flujos de energa de
entrada, por lo que se cumple la ley de conservacin de la energa para un sistema cclico cerrado.
En el tramo 4-1 no existe transferencia de calor, esto porque la energa se manifiesta nicamente
en forma de trabajo, dado que el compresor realiza un proceso de compresin adiabtico.
Comparando los tramos 1-2 y 3-4, vemos que en el primero ocurre la salida de calor, mientras que
en el segundo ocurre la entrada de calor. Si bien el calor de salida supera al de entrada, el trabajo
que se ejerce en el compresor se encarga de equilibrar la situacin, concluyendo as que el trabajo
corresponde a la diferencia entre el calor de salida con el de entrada.
El proceso 2 3 muestra que la entalpa y la altura del inicio y final del proceso es constante, no as
su temperatura y presin (reducida en la correspondiente vlvula). Esto porque es la nica parte
del sistema en la cual no existe variaciones de calor ni trabajo, solo existe disminucin de presin y
temperatura, que da como resultado un aumento en la densidad.
Los niveles ms altos de entalpa se presentan cuando la altura es menor (tramo 4-1).
You might also like
- Informe Laboratorio 1Document12 pagesInforme Laboratorio 1Juan José Montoya San MartínNo ratings yet
- Reglamento de Trabajo de Titulo FicaDocument31 pagesReglamento de Trabajo de Titulo FicaAlanTigheChavezNo ratings yet
- PlanificacionDocument1 pagePlanificacionJuan José Montoya San MartínNo ratings yet
- FemDocument2 pagesFemJuan José Montoya San MartínNo ratings yet
- PlanificacionDocument1 pagePlanificacionJuan José Montoya San MartínNo ratings yet
- Fem Montoya Pinto Sepúlveda IcimDocument19 pagesFem Montoya Pinto Sepúlveda IcimJuan José Montoya San MartínNo ratings yet
- Canciones ViacrucisDocument1 pageCanciones ViacrucisJuan José Montoya San MartínNo ratings yet
- Máquinas HidráulicasDocument1 pageMáquinas HidráulicasJuan José Montoya San MartínNo ratings yet
- Avance 1Document11 pagesAvance 1Juan José Montoya San MartínNo ratings yet
- Misa A La ChilenaDocument3 pagesMisa A La ChilenaJuan José Montoya San MartínNo ratings yet
- 15 - Preentacion PPT Turbina Francis - Clase 16.9.2013Document34 pages15 - Preentacion PPT Turbina Francis - Clase 16.9.2013Victor HernándezNo ratings yet
- Laboratorio PERT IODocument3 pagesLaboratorio PERT IOJuan José Montoya San MartínNo ratings yet
- Avance 1Document11 pagesAvance 1Juan José Montoya San MartínNo ratings yet
- Nta Sra CarmenDocument92 pagesNta Sra CarmenJuan José Montoya San MartínNo ratings yet
- 4-Procesos de PoissonDocument79 pages4-Procesos de PoissonJuan José Montoya San MartínNo ratings yet
- Horario 3 Año MartinDocument5 pagesHorario 3 Año MartinJuan José Montoya San MartínNo ratings yet
- Art 04Document6 pagesArt 04Eduardo Urrutia MonarNo ratings yet
- Tarea Nº2Document2 pagesTarea Nº2Juan José Montoya San MartínNo ratings yet
- Entrada MisaDocument2 pagesEntrada MisaJuan José Montoya San MartínNo ratings yet
- PertDocument2 pagesPertJuan José Montoya San MartínNo ratings yet
- PertDocument4 pagesPertJuan José Montoya San MartínNo ratings yet
- Tema 5.-Termodinamica y EquilibrioDocument130 pagesTema 5.-Termodinamica y EquilibrioJuan José Montoya San MartínNo ratings yet
- Donaciones EjeDocument1 pageDonaciones EjeJuan José Montoya San MartínNo ratings yet
- Clase Quimica 1Document5 pagesClase Quimica 1Juan José Montoya San MartínNo ratings yet
- Cristo Ha Resucitado para Interceder Por NosotrosDocument1 pageCristo Ha Resucitado para Interceder Por NosotrosJuan José Montoya San MartínNo ratings yet
- Resumen 1p Org&CeDocument7 pagesResumen 1p Org&CeJuan José Montoya San MartínNo ratings yet
- Ejercicios Profe 1p 2p 3pDocument28 pagesEjercicios Profe 1p 2p 3pJuan José Montoya San MartínNo ratings yet
- Calificaciones 2014 S1Document2 pagesCalificaciones 2014 S1Juan José Montoya San MartínNo ratings yet
- Experiencia N°08Document5 pagesExperiencia N°08JOAQUIN ALESSANDRO CABRERA CHAMORRONo ratings yet
- Mesa NiveladoraDocument6 pagesMesa NiveladoraReinel OrjuelaNo ratings yet
- RESUMEN UNIDAD 4 Sistemas y Maquinas de FluidosDocument7 pagesRESUMEN UNIDAD 4 Sistemas y Maquinas de FluidosArmando CGNo ratings yet
- Unidad 2-Tercera ParteDocument47 pagesUnidad 2-Tercera ParteLC JayNo ratings yet
- Conductividad Termica VariableDocument11 pagesConductividad Termica VariablehumbertoNo ratings yet
- Porta 3 Procesos 3Document28 pagesPorta 3 Procesos 3Ari Rojas RamirezNo ratings yet
- DiseñoII Unidad4-1Document46 pagesDiseñoII Unidad4-1anderson ardilaNo ratings yet
- Tarea Unidad 1 - Estructuras HidraulicasDocument40 pagesTarea Unidad 1 - Estructuras HidraulicasEdison Silvio Santillan MartinNo ratings yet
- PresentacionDocument52 pagesPresentacionRobert HdzNo ratings yet
- ProgramasAsignaturas Titulacion 5232 AsigUMA 101775Document3 pagesProgramasAsignaturas Titulacion 5232 AsigUMA 101775Energya CorporacionNo ratings yet
- Introducción A Los Intercambiadores de CalorDocument7 pagesIntroducción A Los Intercambiadores de CalorRonald FrankieNo ratings yet
- Examen Parcial 2Document1 pageExamen Parcial 2LesthadNo ratings yet
- Los Arietes Hidráulicos PDFDocument7 pagesLos Arietes Hidráulicos PDFLuis Miguel Orrego MonsalveNo ratings yet
- 3 3 HidrogeologiaDocument164 pages3 3 HidrogeologiaNestor NovoaNo ratings yet
- Copia de Unidad 2 - Fase 3 - Trabajo Colaborativo EstudiantesDocument25 pagesCopia de Unidad 2 - Fase 3 - Trabajo Colaborativo Estudiantesyulitza muñozNo ratings yet
- 6 SifonesDocument11 pages6 Sifonesandy pulache puescasNo ratings yet
- Medidores de Flujo Y.GDocument10 pagesMedidores de Flujo Y.GAndres AcevedoNo ratings yet
- CanaletasDocument1 pageCanaletasLlanelid Fernández LópezNo ratings yet
- Cilindros Inclinados PepaDocument8 pagesCilindros Inclinados PepaDennys Fernando GuaspachaNo ratings yet
- Radio Critico de AislamientoDocument4 pagesRadio Critico de AislamientoDark FuryNo ratings yet
- Flujo en Tuberias Capitulo 8Document117 pagesFlujo en Tuberias Capitulo 8Javier Vinicio Yupangui GuanucheNo ratings yet
- TRABAJO Fenomenos TransporteDocument12 pagesTRABAJO Fenomenos TransporteLuis Alberto Rondon GutierrezNo ratings yet
- Artículo Agitación y MezcladoDocument6 pagesArtículo Agitación y Mezcladoalexandra guzmanNo ratings yet
- Filtros para ServiciosDocument15 pagesFiltros para ServiciosGustavo De Haro GonzálezNo ratings yet
- Stap Dn65-100 Es MainDocument8 pagesStap Dn65-100 Es MainOPER123No ratings yet
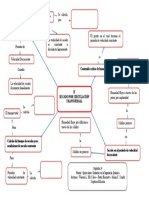
- Secado Por Circulación TransversalDocument1 pageSecado Por Circulación Transversaljose ruizNo ratings yet
- Ejercicios de Hidráulica IiDocument6 pagesEjercicios de Hidráulica IiJENNIFER MORALESNo ratings yet
- MC Soplador ReactorDocument6 pagesMC Soplador ReactorortegaroberNo ratings yet
- Azud Watertech GW Du SP Ed1Document5 pagesAzud Watertech GW Du SP Ed1Alexis LosadaNo ratings yet
- Ejercicios Con ReaccionDocument3 pagesEjercicios Con ReaccionMatias CozzoNo ratings yet