Professional Documents
Culture Documents
3 Quim Inorg Compostos de Coordenação Parte 31
Uploaded by
Mayra FonsecaOriginal Description:
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
3 Quim Inorg Compostos de Coordenação Parte 31
Uploaded by
Mayra FonsecaCopyright:
Available Formats
18/01/2014
Conceitos
Universidade Federal dos Vales do Jequitinhonha e Mucuri
Instituto de Cincia e Tecnologia
COMPLEXOS: as espcies coordenadas apresentam
carga
Diamantina - MG
ADUTOS: a espcie coordenada apresenta carga nula
SAIS COMPLEXOS: Carga nula, so compostos de
um ction e um niom.
Profa. Dra. Flaviana Tavares Vieira
COR
-A cor de um complexo depende: do metal e de
seu estado de oxidao.
-O [Cu(H2O)6]2+ azul claro pode ser convertido
em azul escuro com a adio de NH3(aq):
[Cu(NH3)6]2+
-Geralmente necessita-se de um orbital d
parcialmente preenchido para que um
complexo seja colorido.
-ons metlicos d0 normalmente so incolores.
Excees: MnO4- e CrO42-.
-Compostos coloridos absorvem luz visvel.
COR
Para determinar o espectro de absoro de um
complexo:
um estreito feixe de luz passado por um
prisma (que separa a luz em comprimentos de
onda diferentes),
COR
A cor percebida a soma das luzes no absorvidas
pelo complexo.
A quantidade de luz absorvida versus o
comprimento de onda um espectro de absoro
para um complexo.
COR
-A luz monocromtica (1 comprimento de
onda) passada atravs da amostra,
A luz no absorvida detectada.
o prisma girado para que diferentes
comprimentos de onda de luz sejam produzidos
como uma funo de tempo.
18/01/2014
COR
COR
O grfico de absoro versus comprimento de
onda o espectro de absoro.
Ex.: o espectro de absoro para o [Ti(H2O)6]3+
tem uma absoro mxima em 510 nm (verde e
amarelo).
Logo, o complexo transmite toda
a luz, exceto a verde e a amarela.
Portanto o complexo violeta.
COR
*Disco de Newton
complementares.
mostrando
as
cores
Ex.: O trans-[Co(NH3)4Cl2]+ absorve luz na
regio do vermelho do espectro visvel (a
absoro mais intensa em 680 nm. Qual a cor
do complexo?
COR
Para que o complexo tenha cor, ele deve
absorver luz visvel.
A luz consiste em radiao eletromagntica
com comprimento de onda variando entre
aproximadamente 400 a 750 nm.
A energia dessa radiao eletromagntica
inversamente proporcional ao seu comprimento
de onda.
E = h. = h(c/)
Um composto absorver radiao visvel
quando aquela radiao possuir a energia
necessria para mover um eltron de seu estado
de energia mais baixo (fundamental) para um
estado excitado.
Assim, as energias especficas de radiao que
uma substncia absorve determina as cores que
ela exibe.
MAGNETISMO
COR
Espectro Visvel de Luz
11
Qualquer material submetido a um campo
magntico interage com este de alguma
maneira, com uma intensidade que depende
das suas propriedades magnticas, podendo ser
atrado (PARAMAGNTICO) ou repelido
(DIAMAGNTICO).
Como parmetro para definio dessas
propriedades, normalmente
se
usa a
suscetibilidade magntica, que reflete a
mundana de peso de uma amostra quando
submetida a um campo magntico.
18/01/2014
MAGNETISMO
Medida da Susceptibilidade Magntica
Balana de Gouy
-Os experimentos para essas definies podem
ser feitos usando-se uma balana de Gouy.
Medidas de Momento Magntico
-A susceptibilidade magntica foi uma das primeiras propriedades
empregadas amplamente na caracterizao de compostos de
coordenao.
Amostra Diamagntica
(repelida pelo campo)
Amostra Paramagntica
(atrada pelo campo)
13
MAGNETISMO
-Muitos complexos de metais de transio so
paramagnticos (eltrons desemparelhados).
Existem algumas observaes interessantes.
Considere um on metlico d6:
[Co(NH3)6]3+ no tem nenhum eltron
desemparelhado, mas o [CoF6]3- tem 4
eltrons desemparelhado por on.
Precisamos desenvolver uma teoria de ligao
para esclarecer tanto a cor como o magnetismo
em complexos de metais de transio.
Ligaes nos Compostos
de Coordenao
16
Ligaes nos Compostos de
Coordenao
-Os fundamentos bsicos das ligaes qumicas
responsveis pela formao dos compostos de
coordenao so similares aos que asseguram as ligaes
nos outros tipos de compostos.
-Existem alguns aspectos que tornam necessria uma
discusso particularizada sobre as interaes entre as
espcies qumicas constituintes dos compostos de
coordenao.
-Atualmente as ligaes nos compostos de coordenao
so explicadas pelas:
Teoria do orbital molecular (TOM)
Teoria da ligao de valncia (TLV)
Teoria do campo cristalino (TCC)
Teoria do Orbital Molecular
18
18/01/2014
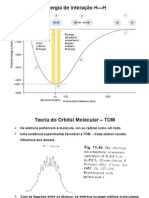
Teoria do Orbital Molecular -TOM
-Quando 2 tomos se aproximam at uma distncia de
equilbrio entre as foras atrativas e repulsivas
estabelecendo uma ligao, os eltrons desses tomos
passam a ocupar orbitais moleculares, que, em muitos
aspectos, assemelham-se aos orbitais atmicos.
-Da mesma forma que os orbitais atmicos (s, p, d, f) so
caracterizados por um conjunto de nmeros qunticos, os
orbitais moleculares (, , ) tambm o so.
-De forma similar, a distribuio eletrnica nos orbitais
moleculares tambm se faz de acordo com a Regra de
Hund e o Princpio de Excluso de Pauli.
19
Paramagntico: O2 tem eltrons
desemparelhados.
Diamagntico: N2 no tem eltrons
desemparelhados.
-Regra de Hund: eltrons numa mesma subcamada tendem a
permanecer desemparelhados (em orbitais separados), com spins
paralelos. Portanto, haver uma menor repulso intereletrnica.
-Princpio da Excluso de Pauli: afirma que 2 partculas idnticas
no podem ocupar o mesmo estado quntico simultaneamente.
Para eletrons de 1 mesmo tomo, ele implica que 2 eltrons no
podem ter os mesmos 4 nmeros qunticos.
Exemplo: se os nmeros qunticos n, l, e ml so iguais nos 2
eltrons, estes devero necessariamente ter os nmeros ms
diferentes e portanto os 2 eltrons tm spins opostos.
*Dessa forma, os orbitais so preenchidos eltron eltron (nunca
adicionando 2 eltrons por vez e com mesmo spin no orbital). Se
mais de 1 orbital em uma subcamada estiver disponvel,
adiciona-se eltrons com spins paralelos aos diferentes orbitais
daquela subcamada at complet-la, antes de emparelhar 2
eltrons em um dos orbitais.
20
Ordem de Ligao
O.L.= (nmero de eltrons em OMs ligantes
nmero de eltrons em OMs antiligantes)
O.L. = 0
As propriedades paramagnticas do oxignio se evidenciam
quando oxignio lquido colocado entre os plos de um
magneto. O lquido prende-se ao maneto em vez de fluir.
Teoria da Ligao de Valncia no pode explicar isso porque:
Uma alta ordem de ligao indica alta energia
de ligao e baixo comprimento de ligao.
-Estrutura de Lewis do O2:
Todos os eltrons esto emparelhados, dessa forma o O2
diamagntico.
Diagrama de Orbitais Moleculares para o H2:
(1s)2
Diagrama de Configurao Eletrnica para o Be2
2 eltrons em um orbital ligante
resultando em uma molcula
estvel
Ordem de ligao: (no de e- ligantes no de e- antiligantes) / 2
O.L.= (2-0) / 2 = 1
18/01/2014
Molculas Diatmicas Homonucleares do
Segundo Perodo da Tabela Peridica
Li2
O.L. = (2 -2) = 0
No h ligao
Ns precisamos usar orbitais 2p para formar os OMs pois os
tomos de boro tem eltrons 2p.
Diagrama de Configurao Eletrnica para o Li2
TOM: Diagrama de Orbitais Moleculares
O.L. = ( 4 2 ) = 1
Ligao simples
O orbital (1s*) cancela o orbital
(1s)
28
TOM: Diagrama de Orbitais Moleculares
Exerccio: Preencha os orbitais moleculares para
molculas diatmicas dos elementos do segundo perodo
Exerccio: Preveja a existncia de He2 e He2+.
Molculas e ons Diatmicos
da Primeira Linha da Tabela peridica
29
18/01/2014
Preenchimento dos orbitais moleculares e dados fsicos
para molculas diatmicas homonucleares dos elementos
do segundo perodo.
O2
31
32
Preenchimento dos orbitais moleculares para molcula
heteronuclear (HCl).
33
Nveis de energia relativas para os orbitais moleculares
para molculas homonucleares
34
Orbitais Moleculares em Alguns
Compostos Octadricos
35
18/01/2014
Diagrama de Orbital Molecular Para o
[Co(NH3)6]3+
Diagrama de Orbital Molecular para o
[CoF6]3-
Teoria da Ligao de Valncia - TLV
O Modelo de Ligao da Sobreposio de Orbitais
Teoria da Ligao pela Valncia
39
Teoria da Ligao de Valncia (TLV)
-Interao entre orbitais de valncia das espcies
consideradas
-Inicialmente era usada para explicar a existncia de
molculas simples
Variao da energia potencial durante a formao da ligao H-H a partir de tomos de hidrognios isolados
-Sobreposio de orbitais: aumenta a probabilidade de
encontrar os eltrons de ligao no espao entre os dois
ncleos.
-A idia de que as ligaes so formadas pela
sobreposio de orbitais atmicos a base para a
teoria de ligao de valncia.
-Linus Pauling usou para complexos
-A ligao covalente que se origina da sobreposio de
2 orbitais, um de cada um dos 2 tomos como no H2,
chamada de ligao sigma ().
-Interao metal ligante atravs de interao cido base de Lewis.
-A densidade eletrnica de uma ligao maior em
torno do eixo da ligao.
18/01/2014
Teoria da Ligao pela Valncia
-De acordo com este modelo, o
em um complexo forma
covalente coordenada com
sendo os 2 eltrons do par
ligao doados pelo ligante.
tomo central
uma ligao
cada ligante,
envolvido na
-Para tal, o tomo central utiliza um conjunto
apropriado de orbitais hbridos formados
pela combinao de alguns de seus orbitais
(n-1)d, ns, e alguns de seus np.
Ligao Qumica nos Complexos
-A 1 descrio com razovel sucesso sobre a
ligao nos ons complexos foi estabelecida
pela ligao de valncia ou formao de
orbitais hbridos.
43
Interferncias Construtivas e Destrutivas
44
Formao de Ligao Covalente
de Funes de Ondas
Sobreposio dos orbitais 1s do hidrognio
para formar a ligao sigma em H-H
1s + 2py
Sem ligao
Ligao
Sem ligao
Ligao
Ligao
Sobreposio dos orbitais 1s do hidrognio e 2p
do fluor para formar a ligao sigma em H-F
Sobreposio dos orbitais 2p de 2 tomos de
fluor para formar a ligao sigma F-F
48
18/01/2014
49
Pontos principais da abordagem da TLV:
-Os orbitais sobrepem-se para formar uma ligao
entre 2 tomos;
50
Hibridizao dos Orbitais Atmicos
Teoria VESPR:
-2 eltrons, de spins opostos, podem ser acomodados
nos orbitais sobrepostos, em geral, 1 eltron
fornecido por cada 1 dos tomos ligados;
-Devido a sobreposio dos orbitais, os eltrons de
ligao tm maior probabilidade de ser encontrados
em uma regio do espao influenciada por ambos os
ncleos.
Os orbitais 2p em um tomo.
Estrutura de
Lewis
Modelo
molecular
Geometria dos pares
de eltrons
Configurao da camada de valncia do carbono no estado fundamental
Hibridizao
Os orbitais atmicos podem se mesclar ou
hibridizar para formar os orbitais hbridos.
Quando 2 orbitais atmicos combinam-se, 2
novos orbitais so produzidos nesse tomo.
Os orbitais 2px, 2py e 2pz encontram-se ao longo dos eixos x, y e z, a 90o
entre si.
18/01/2014
Conjunto de orbitais hbridos que surgem da
mistura de orbitais atmicos s, p e d:
-O nmero de orbitais hbridos requeridos por um tomo em uma
molcula ou on determinado pela geometria dos pares de
eltrons em torno desse tomo. Um orbital hbrido necessrio
para cada par de eltrons no tomo central;
-Se o orbital s da camada de valncia no tomo central em uma
molcula ou on for mesclado com um orbital p da camada de
valncia nesse mesmo tomo, 2 orbitais hbridos so criados. Eles
so separados por 180o e o conjunto de 2 orbitais chamado sp;
- s + 2 p = 3 orbitais hbridos so criados: sp2 ( = 120o);
- s + 3 p = sp3 (=109,5o, o ngulo tetradrico);
Combinando Orbitais Atmicos para formar Orbitais
Hbridos do tomo Central
-Na formao da ligao qumica, a combinao
linear de 2 ou mais orbitais atmicos em um tomo
produz orbitais atmicos hbridos.
REGRA: O nmero de orbitais atmicos que so
combinados igual ao nmero de orbitais hbridos
resultantes.
-Todos os orbitais hbridos so degenerados (iguais
em energia)
-2 d + sp3 = sp3d (trigonal) ou sp3d2 (octadrica)
Arranjo dos Orbitais Hbridos
Orbitais
hbridos
sp
sp2
sp3
sp3d
Sp3d2
Orbitais atmicos
utilizados
Nmero de
orbitais hbridos
Geometria dos
pares de eltrons
2
3
4
5
6
Linear
Trigonal planar
Tetradrica
Bipiramidal
trigonal
Octadrica
s+p
s+p+p
s+p+p+p
s+p+p+p+d
s+p+p+p+d+d
Figura
Geomtrica
2 pares
de
eltrons
sp
BeCl2
3 pares de
eltrons
sp2
BF3
4 pares de
eltrons
sp3
CH4
Teoria da Ligao de Valncia para o Metano, CH4
Figura Geomtrica
5 pares de
eltrons sp3d
PF5
Hibridizao
Arranjo dos Orbitais Hbridos
6 pares de
eltrons
sp3d2
SF6
4 orbitais sobrepostos sp3
10
18/01/2014
As ligaes na molcula de metano
Orbital no tomo de C
livre
Orbitais hibridizados no tomo de C
no metano
4 orbitais hbridos sp3
Cada ligao no metano resulta da sobreposio do
orbital 1s do H e do orbital sp3 do C.
Orbitais sp3
do C
4 ligaes
Orbital 1s
do H
64
Formao de 4 orbitais
semi-preenchidos.
65
66
11
18/01/2014
Orbitais Hbridos de Molculas e ons
Orbitais Hbridos de Molculas e ons
com Geometria Trigonal Planar dos Pares de Eltrons
com Geometria Linear dos Pares de Eltrons
Ligaes duplas: modelo de ligao para o etileno,
C2H4
Estrutura de
Lewis e as
ligaes no
etileno
Ligaes C-H: formadas
pela
sobreposio
dos
orbitais hbridos sp2 do C
com orbitais 1 s do H. A
ligao entre os tomos de
C e H surge da sobreposio
de orbitais sp2.
A ligao C-C
formada
pela
sobreposio
dos
orbitais
2p
no
hibridizados de cada
tomo. Observe a
ausencia de densidade
eletrnica ao longo do
eixo da ligao C-C.
Hibridao sp
Ligaes triplas: modelo de ligao para o acetileno, CH2O.
Orbitais hbridos do Be
*Cada ligao no BeH2 resulta da
sobreposio de 1 orbital 1s do H e
do orbital hbrido sp do Be.
12
18/01/2014
Exemplos com Eltrons Livres
Estrutura de Lewis
Pares de eltrons livres: 1
Geometria:
Geometria: trigonal
bipiramidal
Gangorra
Forma de T
Linear
Pares de eltrons livres ocupam primeiro o plano trigonal
posio equatorial para minimizar a repulso de 90o.
Formao de Alguns ons Complexos
Estrutura de Lewis
-6 pares de
eltrons em torno
do tomo de S:
exceo regra
do octeto.
Todos os ngulos = 90o.
Geometria: octadrica
76
Ligao Metal -Ligante
-Todos os ligantes tm pares livres que so
doados ao on metlico.
-A ligao entre o metal e o ligante uma
ligao de 2 eltrons, mas ambos vm do
ligante e nenhum vem do metal.
-A ligao metal-ligante altera as propriedades
fsicas do metal:
Ag+(aq) + e- Ag(s), E = +0,799 V
[Ag(CN)2]-(aq)+ e- Ag(s)+2CN-(aq),E=-0,031 V
-A maior parte dos ons metlicos existe em
gua como [M(H2O)6]n+.
-Carga no on complexo = carga no metal +
cargas nos ligantes.
-tomo doador: o tomo ligado diretamente ao
metal.
Nmero de coordenao (NC): o nmero de
ligantes ligados ao metal.
Os NC mais comuns so 4 e 6.
13
18/01/2014
Cargas, nmeros de coordenao e
geometrias
-Alguns ons metlicos tm NC constante
(Ex.: Cr3+ e Co3+ tm NC=6).
-O tamanho do ligante afeta o nmero de coordenao
(Ex: o [FeF6]3- se forma mas somente o [FeCl4]- estvel).
-A quantidade de carga transferida do ligante para o metal
afeta o NC (Ex: [Ni(NH3)6]2+ se forma, mas somente o
[Ni(CN)4]2- estvel).
Complexos tetracoordenados so tetradricos ou
quadrticos planos (normalmente encontrados para ons
metlicos d8).
Complexos hexacoordenados so octadricos.
Nmero Atmico Efetivo (NAE)
Quanto mais diretamente o ligante ataca o
orbital do metal, maior a energia do
orbital d.
-Os complexos adquirem estabilidade quando o NAE
iguala-se ao nmero atmico de um gs nobre
Complexos que obedecem a regra do NAE
Complexos
Espcies
Nmero
de
eltrons
NAE
Gs
nobre
Co3+
24
12
36
Kr
6 CN[Ag(NH3)4]+
Ag+
4 NH3
46
8
54
Xe
[PtCl6]2-
Pt+4
6 Cl-
74
12
86
Rn
[Co(CN)6
]3-
Molcula do [CoF6]3Co3+
Complexos que no obedecem ao NAE
Complexos
Espcies
Nmero
de
eltrons
NAE
[Cr(NH3)6]3+
Cr3+
6 NH3
21
12
33
[Ni(NH3)6]2+
Ni2+
6 NH3
26
12
38
[CoCl4]2-
Co2+
4 Cl-
25
8
33
Molcula do [NiCl4]2Ni2+
14
18/01/2014
Falha da TLV:
-As estruturas de Lewis falham na descrio
correta da ligao em um caso extremamente
visvel, a molculas de O2.
-A molcula de O2 paramagntica, o que
requer a presena de eltrons desemparelhados.
-A estrutura de Lewis teria todos os eltrons
emparelhados. A abordagem da TOM mostra
que essa molcula possui 2 eltrons
desemparelhados.
Verificando o Aprendizado
1. D a geometria molecular, a geometria eletrnica e a
hibiridizao do tomo central.
-Nesse estado ele paramagntico e fica preso
aos plos de um im.
Verificando o Aprendizado
1. D a geometria molecular, a geometria eletrnica e a
hibiridizao do tomo central.
a. SiF62-
a. SiF62-
b. SeF4
b. SeF4
c. ICl2
Oxignio lquido: o gs oxignio condensa-se em
um lquido a -183oC.
c. ICl2-
d. XeF4
d. XeF4
Respostas:
a. Geometria Molecular e Eletrnica: octadrica, hibridizao sp3d2
b. Gometria eletrnica: bipiramidal trigonal; Geometria molecular: gangorra;
Hibridizao: sp3d2
c. Gometria eletrnica: bipiramidal trigonal; Geometria molecular: linear;
Hibridizao: sp3d
d. Gometria eletrnica: octadrica; Geometria molecular: quadrada plana;
Hibridizao: sp3d2
Teoria do Campo Cristalino - TCC
-Vrias propriedades magnticas e das cores
dos complexos de metais de transio esto
relacionadas presena de eltrons d nos
orbitais do metal.
-Uma teoria satisfatria para a ligao
qumica nos compostos de coordenao
deve permitir explicar: a cor, as
propriedades magnticas, a estereoqumica
e a fora de ligao.
Teoria do Campo Cristalino
89
90
15
18/01/2014
Teoria do Campo Cristalino - TCC
-Objetivos iniciais: o estudo de algumas
propriedades de ons metlicos de cristais
inico que contm eltrons d do nvel de
valncia.
91
-A TCC procura explicar a ligao qumica
nos complexos apenas em termos de
foras eletrostticas, as quais so duas:
-Atrao entre o on metlico com carga
positiva e o ligante de carga negativa ou
polar;
-Repulso entre os pares isolados dos
ligantes e os eltrons que ocupam as
orbitais d do metal.
93
Teoria do Campo Cristalino - TCC
A TCC descreve a ligao em complexos de
metais de transio.
A formao de 1 complexo uma reao cidobase de Lewis.
Ambos os eltrons na ligao vm do ligante e
so doados para 1 orbital vazio hibridizado no
metal.
A carga doada do ligante para o metal.
Hiptese da TCC: a interao entre o ligante e
o metal eletrosttica.
-Embora na ausncia de uma perturbao
externa, os orbitais d possuam a mesma
energia, num complexo octadrico, o tomo
central est rodeado por 6 pares isolados de
eltrons pertencentes aos ligantes.
-Logo, os 5 orbitais d so todos repelidos pelos
eltrons dos ligantes.
-A intensidade desta repulso depende, no
entanto, da orientao do orbital d que est a
se considerar.
94
-Ambos os eltrons na ligao vm do ligante e so
doados para um orbital vazio hibridizado no metal.
-Hiptese da TCC: a interao entre o ligante e o metal
eletrosttica.
-Quanto mais diretamente o ligante ataca o orbital do
metal, maior a energia do orbital d.
-A ligao que resulta fortemente polar, de certo carter
covalente.
-Mas, como feito no modelo TCC, em geral suficiente
supor que a interao inteiramente eletrosttica
95
96
16
18/01/2014
Orientaes dos Orbitais d em um
Campo Cristalino Octadrico
Conjunto de Orbitais d
97
-Observa-se na figura anterior que os lobos esto
orientados em direo aos vrtices do octaedro na
direo definida pelos eixos x e y e z, por isso
possuem maior energia em relao a dxy, dxz e dyz.
-Estas interaes fazem com que os 5 orbitais d num
complexo octadrico sofram um desdobramento
em 2 nveis de energia.
99
-O on metlico complexo tem uma energia
menor do que o metal e os ligantes separados.
-Entretanto, existem algumas repulses liganteeltron d que ocorrem, uma vez que o metal
tem orbitais d parcialmente preenchidos.
Em 1 campo octadrico, a degenerecncia dos
5 orbitais d suspensa.
Em 1 campo octadrico, os 5 orbitais d no
tm a mesma energia: 3 orbitais degenerados
tm mais energia do que 2 orbitais
degenerados.
98
-Chama-se energia de desdobramento do
campo cristalino () a diferena de energias
entre esses 2 conjuntos de orbitais d.
-O valor de () depende do metal e da
natureza dos ligantes e tem um efeito direto
sobre a cor e sobre as propriedades
magnticas dos complexos.
-Conjuntos t2g: dxy, dxz, dyz
eg: dz2, dx2-y2
100
Supomos um arranjo octadrico de cargas
negativas colocadas em torno do on metlico
(que positivo).
Os orbitais dx2-y2 e dz2 localizam-se nos
mesmos eixos das cargas negativas.
Conseqentemente, h uma grande e
desfavorvel interao entre ligante (-) e
esses orbitais.
Esses orbitais formam o par degenerado de
nveis de energia de alta energia.
Os orbitais dxy, dyz, e dxz dividem as cargas
negativas em duas partes iguais.
17
18/01/2014
Conseqentemente, h uma repulso menor
entre ligante e metal para esses orbitais.
Esses orbitais formam o conjunto de nveis
degenerados de energia mais baixa.
A diferena de energia a energia de
desdobramento do campo cristalino .
O Ti3+ um on metlico d1.
Conseqentemente, o eltron est em um
orbital de baixa energia.
Para o Ti3+, a diferena entre os nveis de
energia, da ordem do comprimento de
onda da luz visvel.
medida que o complexo [Ti(H2O)6]3+
absorve luz visvel, o eltron promovido
a um nvel de energia mais alto.
Uma vez que h apenas um eltron, existe
apenas uma linha de absoro possvel
para essa molcula.
A cor de um complexo depende da ordem
de grandeza de que, por sua vez,
depende do metal e dos tipos de ligantes.
-O on metlico do complexo tem uma energia menor do que
o metal e os ligantes separados.
-Entretanto, existem algumas repulses ligante-eltron d que
ocorrem, uma vez que o metal tem orbitais d parcialmente
preenchidos.
-Eltrons nos dois orbitais d(dz2 e dx2-y2) apontam
diretamente ao longo do eixo cartesiano e diretamente para
os ligantes, estes so normalmente de simetria eg
(duplamente degenerado).
-Em compostos octadricos, esses eltrons (eg) so
repelidos mais fortemente pela carga negativa nos ligantes
que os eltrons nos outros 3 orbitais d (dxy,dyz,dxzsimetria
t2g (triplamentedegenerado)).
T2g LUMO
eg HOMO
105
106
Complexos Octadricos
107
108
18
18/01/2014
Desdobramento dos Orbitais d pelo Campo Cristalino
num Complexo Octadrico
Diagrama de nveis de energia: campo octadrico
A distncia em energia entre eles chamada , o campo cristalino desdobra-se
em energia.
109
110
Teoria do Campo Cristalino - TCC
- A estabilidade do complexo deve-se a interao metalligante, que de natureza eletrosttica
- Os ligantes so cargas pontuais negativas
112
113
114
19
18/01/2014
115
Srie Espectroqumica
116
Srie Espectroqumica: uma lista de ligantes
em ordem crescente de : Cl- < F- < H2O <
NH3 < en < NO2- (ligado a N) < CN Ligantes de Campo Fraco localizam-se no
extremo inferior da srie espectroqumica.
Ligantes de Campo Forte localizam-se no
extremo superior da srie espectroqumica.
117
-A diferena de energia entre as orbitais d, , da
mesma ordem de grandeza de um fton de luz
visvel (E=h).
Espectro de Absoro do [Ti(H2O)6]3+
-, portanto, possvel para um complexo de metal
de transio absorver luz visvel, que excita um
eltron dos orbitais d de mais baixa energia para
os orbitais d de mais alta energia.
Exemplo: [Ti(H2O)6]3+.
119
-Processo de absoro de fton pelo on [Ti(H2O)6]3+
-Representao grfica do espectro de absoro do on [Ti(H2O)6]3+.
-A energia do fton coincide com a energia do desdobramento do campo cristalino.120
20
18/01/2014
COR nos Complexos
Medidas dos valores de 10 Dq (UV-vis)
Espectro UV-vis do [Ti(H2O)6]3+
122
Relao entre cores absorvidas e
transmitidas
Disco de Newton
123
Complexos octadricos de campo forte
e de campo fraco
125
124
Teoria do Campo Cristalino - TCC
Srie Espectroqumica
: Cl- < F- < H2O < NH3 < en < NO2- (ligado aN) <
CN-
21
18/01/2014
Complexos Octadricos de Campo Forte
127
Configuraes eletrnicas em complexos
octadricos
Ainda aplicamos a regra de Hund para os orbitais
d.
Os primeiros 3 eltrons entram em orbitais d
diferentes com seus spins paralelos.
Lembre-se: os eltrons s so perdidos antes.
Logo, o Ti3+ um on d1, o V3+ um on d2 e o Cr3+
um on d3.
Temos uma escolha para a colocao do 4o eltron:
se ele vai para um orbital de energia mais alta,
ento h um custo de energia ();
Energia de Estabilizao do Campo
Cristalino - EECC
128
Configuraes eletrnicas em complexos
octadricos
Se ele vai para 1 orbital de menor energia, h um
custo de energia diferente (chamado de energia de
emparelhamento do spin devido ao emparelhamento
de um eltron).
Os ligantes de campo fraco tendem a favorecer a
adio de eltrons a orbitais de energia mais alta
(complexos de spin alto) porque < energia de
emparelhamento.
Os ligantes de campo forte tendem a favorecer a
adio de eltrons a orbitais de energia mais baixa
(complexos de spin baixo) porque > energia de
emparelhamento.
Energia de Estabilizao de Campo
cristalino em compostos Octadricos
Espcies
EECC = Dq + P
P energia de emparelhamento (repulso entre eltrons e
trabalho para inverter spin)
Dq > P spin baixo
Dq < P spin alto
Ligantes de campo fraco spin alto
Ligantes de campo forte
spin baixo
Campo Fraco
Campo forte
Configurao
EECC
Configurao
EECC
d0
Sc3+
T2g0 eg0
0 Dq
T2g0 eg0
0 Dq
d1
Ti3+
T2g1 eg0
-4 Dq
T2g1 eg0
-4 Dq
d2
V3+
T2g2 eg0
-8 Dq
T2g2 eg 0
-8 Dq
d3
Cr3+
T2g3 eg0
-12 Dq
T2g3 eg0
-12 Dq
d4
Mn3+
T2g3 eg1
-6 Dq
T2g4 eg0
-16 Dq
d5
Fe3+
T2g3 eg2
0 Dq
T2g5 eg0
-20Dq
d6
Co3+
T2g4 eg2
-4 Dq
T2g6 eg0
-24Dq
d7
Rh2+
T2g5 eg 2
-8 Dq
T2g6 eg1
-18Dq
d8
Ni2+
T2g6 eg2
-12 Dq
T2g6 eg2
-12Dq
d9
Cu2+
T2g6 eg 3
-6 Dq
T2g6 eg3
-6Dq
d10
Zn2+
T2g6 eg4
0 Dq
T2g6 eg4
0Dq
22
18/01/2014
Configurao eletrnica
para situao de campo forte
Evidncias da Validade da TCC
Composto
Hred em KJ/mol
Configurao (spin alto)
CaCl2
2258
d0 t2g0, eg0
0 Dq
ScCl2
2380
d1 t2g1, eg0
-4 Dq
TiCl2
2501
d2 t2g2, eg0
-8 Dq
VCl2
2579
d3 t2g3, eg0
-12 Dq
-6 Dq
EECC
CrCl2
2586
d4
MnCl2
2537
d5 t2g3, eg2
0 Dq
FeCl2
2531
d6 t2g4, eg2
-4 Dq
CoCl2
2691
d7 t2g5, eg2
-8 Dq
NiCl2
2772
d8 t2g6, eg2
-12 Dq
t2g3,
eg1
CuCl2
2811
d9 t2g6, eg3
-6 Dq
ZnCl2
2734
d10 t2g6, eg4
0 Dq
134
Complexos Octadricos de Campo Fraco
Configurao eletrnica
para situao de campo fraco
135
136
Campo Tetradrico
Complexos Tetradricos
137
138
23
18/01/2014
Configurao eletrnica dos complexos d
Fatores que afetam
a magnitude de 10 Dq
139
140
Efeito do Nmero de Ligantes e Geometria
Efeito da Carga do Metal
141
142
Propriedades Magnticas
Efeito da Natureza do Metal
143
144
24
18/01/2014
Ocorrncia de Complexos Tetradricos
Efeito do campo cristalino em
compostos tetradricos
Ligantes de campo fraco com EECC pouco importante
- Os ligantes se localizam entre os orbitais t2g do metal
(vrtices do cubo)
- Os valores de 10 Dq so sempre menores do que as
energias de emparelhamentos (P)
- Compostos tetradricos so sempre de spin alto
Metal com baixo estado de oxidao
10 Dq(td) = 4/9 (10Dq(oh))
Ligantes volumosos (efeito estrico)
Quando no h EECC (d0, d5 ou d10)
Fatores que afetam o Valor de 10 Dq
Efeito da carga do on central
Efeito da simetria do campo cristalino
Efeito da natureza do ligante
I-<Br-<SCN-<Cl-<NO3-<F-<OH-<Ox2<H2O<NCS<CH3CN<NH3<en<dipy<phen<NO2-<CN-<CO
Nmero quntico principal do orbital d de valncia
Complexos Tetradricos e
Quadrticos Planos
A maior parte dos ons metlicos d8
formam complexos quadrticos planos.
a maioria dos complexos de spin baixo
(i.e. diamagntico).
Ex.: Pd2+, Pt2+, Ir+ e Au3+.
Complexos Tetradricos e
Quadrticos Planos
Complexos quadrticos planos podem ser
pensados como a seguir: comece com um
complexo octadrico e remova 2 ligantes ao longo
do eixo z.
Como conseqncia, os 4 ligantes no plano so
puxados para dentro do metal.
Em relao ao campo octadrico, o orbital
enormemente reduzido em energia, os orbitais dyz,
e dxz reduzem-se em energia, os orbitais dxy,
elevam-se em energia.
Complexos
Tetradricos e
Quadrticos Planos
-A maioria dos ons metlicos d8
complexo quadrtico plano.
-A maioria dos complexos de
spin baixo (ex:
diamagntico).
Ex.: Pd2+, Pt2+, Ir+, e Au3+.
25
18/01/2014
Compostos de Simetria Tetragonal e
Efeito Jahn-Teller
Efeito do Campo Cristalino em
Compostos Quadrado Planares
Casos extremos de distores tetragonais
Formados por ons d8 e ligantes fortes ou ons d4 com ligantes fracos
Orbitais dx2-y2 so repelidos por 4 ligantes, dz2 apenas por 2
ligantes
Configuraes Eletrnicas do
Efeito Jahn-Teller
Configurao d
Efeito Jahn-Teller
d0
No existe
Condio de existncia
Nenhuma
d1
Existe
Com qualquer ligante
d2
Existe
Com qualquer ligante
d3
No existe
Nenhuma
d4
Existe
Com qualquer ligante
d5
Existe
Spin baixo
d6
Existe
Spin alto
d7
Existe
Com qualquer ligante
d8
No existe
Nenhuma
d9
Existe
Com qualquer ligante
d10
No existe
Nenhuma
154
Referncias Bibliogrficas
-Farias, R.F.
Qumica de coordenao:
fundamentos e atualidades. Campinas, SP:
Editora tomo, 2005.
-Barros, H.L.C. Qumica inorgnica:
introduo. Belo Horizonte: 1992.
uma
-Shriver, D.F.; Atkins, P.W. Qumica inorgnica. 3
ed. Porto Alegre: 2003.
155
26
You might also like
- ZeólitasDocument4 pagesZeólitasMayra FonsecaNo ratings yet
- Tratamento Aeróbio Com Lodo AtivadoDocument6 pagesTratamento Aeróbio Com Lodo AtivadoMayra FonsecaNo ratings yet
- Aeração e Tratamento de Efluentes Com Aeradores - Tratamento Por Ar DifusoDocument6 pagesAeração e Tratamento de Efluentes Com Aeradores - Tratamento Por Ar DifusoMayra FonsecaNo ratings yet
- Síntese de Plástico InorgânicoDocument4 pagesSíntese de Plástico InorgânicoMayra Fonseca100% (1)
- Síntese de Adutos Entre CobreDocument7 pagesSíntese de Adutos Entre CobreMayra FonsecaNo ratings yet
- Síntese de Compostos Cobre-GlicinaDocument19 pagesSíntese de Compostos Cobre-GlicinaJASobrinho_2No ratings yet
- Aula 5 Quím BDocument36 pagesAula 5 Quím BGuilhermeNo ratings yet
- SimuladoDocument82 pagesSimuladosantos kNo ratings yet
- Curso 12168 Aula 14 v1Document61 pagesCurso 12168 Aula 14 v1Gerson GersonNo ratings yet
- Espectrometria MolecularDocument31 pagesEspectrometria MolecularPaula_Castilho100% (1)
- Acido-Base Teoria de Pearson 1 PDFDocument35 pagesAcido-Base Teoria de Pearson 1 PDFEdnoelma BarbosaNo ratings yet
- TOM PARTES 1, 2 e 3Document8 pagesTOM PARTES 1, 2 e 3Amanda JustinianoNo ratings yet
- CESPE - Perito Criminal Federal 2004 - Resolução ComentadaDocument42 pagesCESPE - Perito Criminal Federal 2004 - Resolução ComentadaRobson Timoteo DamascenoNo ratings yet
- Preparação Teste 2 - 10º - 19 - 20Document19 pagesPreparação Teste 2 - 10º - 19 - 20SuuurmNo ratings yet
- Teoria Do Orbital Molecular TOMDocument21 pagesTeoria Do Orbital Molecular TOMAna Laura ValerianoNo ratings yet
- Tabela Periódica - PropriedadesDocument29 pagesTabela Periódica - PropriedadesArchibaldo NetoNo ratings yet
- ROTAQIB2009Document121 pagesROTAQIB2009Marcos Eletricidade RefrigeraçãoNo ratings yet
- Lista de Exercícios 1Document2 pagesLista de Exercícios 1Leonardo ZammarNo ratings yet
- Química Orgânica CompletoDocument72 pagesQuímica Orgânica Completolohanne bernardesNo ratings yet
- Teoria Do Orbital Molecular: Orbitais Nas MoléculasDocument32 pagesTeoria Do Orbital Molecular: Orbitais Nas MoléculasMahira AdnaNo ratings yet
- Exerc Lig EngDocument1 pageExerc Lig EngCarlos Eduardo BarrosNo ratings yet
- TLV e TomDocument36 pagesTLV e TomAmanda PavãoNo ratings yet
- Catalise em Compostos de CoordenaçãoDocument42 pagesCatalise em Compostos de Coordenaçãonetochemistry0% (1)
- Teoria Do Campo Ligante PDFDocument22 pagesTeoria Do Campo Ligante PDFLuila MavendorfNo ratings yet
- Teoria Do Orbital MolecularDocument28 pagesTeoria Do Orbital MolecularHauster M. CamposNo ratings yet
- Análise Conformacional PDFDocument21 pagesAnálise Conformacional PDFHenrique MenesesNo ratings yet
- Lista de Exercícios - P1Document7 pagesLista de Exercícios - P1malhenasmNo ratings yet
- Ensaio Visual e Dimension Amen To de Solda n2 PROMIMPDocument150 pagesEnsaio Visual e Dimension Amen To de Solda n2 PROMIMPOsvaldoPerez100% (8)
- QuestligquimicaDocument2 pagesQuestligquimicaKilça Tanaka BotelhoNo ratings yet
- Aula 4 - Ligações QuímicaDocument98 pagesAula 4 - Ligações QuímicaAbner AlmeidaNo ratings yet
- Ligações Covalentes - TomDocument64 pagesLigações Covalentes - TomMarcus Vinicius100% (1)
- Estrutura AtômicaDocument122 pagesEstrutura AtômicaAndre Luiz do NascimentoNo ratings yet
- Lista 3Document4 pagesLista 3Douglas Alexandre0% (1)
- Revista CienciasDocument259 pagesRevista CienciasgleydsonferreiraNo ratings yet
- Química Inorgânica Não Tão Concisa - J.D. LeeDocument527 pagesQuímica Inorgânica Não Tão Concisa - J.D. LeeAloísio Santos100% (3)