Professional Documents
Culture Documents
Guía de Prácticas Quimica Organica II
Uploaded by
Joselyn KarinaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Guía de Prácticas Quimica Organica II
Uploaded by
Joselyn KarinaCopyright:
Available Formats
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
PRACTICA N 1: SUSTITUCION AROMATICA ELECTROFILICA
1.1
PREPARACION DEL NITROBENCENO.
Reaccin General:
NO2
+
HNO3
H2SO4
60 C
H2O
La preparacin del nitrobenceno debe ser llevada con
cuidado a fin de evitar una nitracin adicional, es decir
la formacin de m-dinitrobenceno. Colocar 35 ml de cido
ntrico concentrado en un recipiente de 500 ml y aadir
lentamente
40
ml
de
cido
sulfrico
concentrado,
manteniendo la mezcla fra durante la adicin colocando el
frasco en un bao de agua helada. Colocar un termmetro en
la mezcla nitratante y luego aadir lentamente 29 ml de
benceno. El benceno debe ser aadido poco a poco, digamos
de tres en tres ml y agitar el contenido del frasco muy
bien despus de cada adicin: la temperatura de la mezcla
no debe exceder los 50 C y debe ser mantenida bajo control
si es necesario enfriando con agua fra la mezcla. Cuando
todo el benceno se halla aadido, colocar un condensador de
reflujo al frasco y calentar en bao mara, el que debe ser
mantenido a 60 C, por un lapso de 45 minutos. Durante el
perodo de calentamiento, el frasco de reaccin debe de
agitarse de vez en cuando (mucho mejor si es constante!) a
fin de quebrar las dos fases que se estn formando.
Despus del calentamiento de 45 minutos, colocar el
contenido del frasco en un gran exceso de agua fra (unos
300 ml) en el cual el nitrobenceno, siendo ms pesado que
el agua, se hunde en el fondo. Agitar la mezcla
vigorosamente a fin de remover tanto cido como sea posible
del nitrobenceno. Decante tanto como sea posible, la capa
acuosa
sobrenadante
y
luego
el
lquido
residual
transferirlo a una pera de decantacin. Libere la capa
inferior de nitrobenceno, eliminando la capa superior y
retornar el nitrobenceno a la pera de separacin y agitar
vigorosamente con un volumen igual de agua helada. Deje que
el nitrobenceno se separe nuevamente y liberar la capa de
nitrobenceno. Repetir estos lavados, usando solucin de
Carbonato de Sodio, hasta que cesen los vapores de dixido
de carbono. Luego transferir el nitrobenceno a un
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
erlenmeyer pequeo y aadir un poco de cloruro de calcio
granular. Dejar en reposo hasta que el lquido quede
bastante claro (usualmente se puede esperar unos 20
minutos). Filtrar por gravedad el nitrobenceno utilizando
un papel filtro a un recipiente, a fin de someterlo a
destilacin para su purificacin final. El nitrobenceno
destila entre 207 a 211 C (a 760 mmHg). Determinar el
rendimiento.
El nitrobenceno es un lquido amarillo plido tiene un olor
caracterstico de almendras. El nitrobenceno es la base
para la preparacin de anilina, que es el compuesto base
para la preparacin de colorantes artificiales.
1.2 PREPARACION DEL ACIDO PICRICO: 2, 4, 6-trinitrofenol
Reaccin general:
OH
OH
+
HNO3
H2SO4
O2 N
NO2
+
H2O
NO2
Pesar 8 g. de fenol en un recipiente de fondo plano (por
ej. un erlenmeyer) y aadir 10 ml de cido sulfrico
concentrado y agitar la mezcla, la misma que se pone
caliente. Ahora calentar el recipiente en un bao de agua
mara por espacio de unos 30 minutos a fin de completar la
formacin del cido fenol sulfnico y finalmente enfriar la
mezcla en un bao de agua helada. Luego colocar el
recipiente en una campana de extraccin (o en su defecto en
un lugar bastante ventilado) y mientras que el cido fenol
sulfnico est todava de consistencia viscosa y como un
jarabe, aadir inmediatamente sin demora 30 ml de cido
ntrico concentrado rpidamente y mezclar los lquidos
completamente por agitacin por unos cuantos segundos.
Luego dejar que la mezcla repose sin movimiento. Usualmente
en el lapso de un minuto, una reaccin vigorosa (pero
inofensiva) empieza y se comienzan a eliminar vapores
rojizos. Cuando esta etapa finalice, calentar en un bao de
agua hirviendo por 1.5 horas, con ocasional agitacin.
Durante este perodo, el aceite pesado el cual est
presente al comienzo, llega a convertirse en una masa de
cristales. Cuando se halla completado el calentamiento,
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
aadir 100 ml de agua fra, mezclar bien y enfriar
completamente en un bao de agua helada. Filtrar los
cristales usando vaco, lavar completamente con agua a fin
de eliminar todos los residuos inorgnicos y dejar que
drene con el vaco. Recristalizar utilizando una mezcla de
1 volumen de etanol y 2 volmenes de agua. El cido pcrico
que se obtiene son hojuelas de color amarillo. Su punto de
fusin es de 122 C. Determinar el rendimiento.
1.3 PREPARACION DE BECILTIOURONIO
Reaccin general:
Cl
S
+ H2N
NH2
NH2
C S
H2
+
NH2
Cl
Tiorea, a diferencia de urea, reacciona fcilmente debido
a su forma tautomrica, en presencia de agentes qumicos
adecuados, particularmente haluros de alquilo; de all que
se halla escogido cloruro de bencilo para que reaccione con
tiorea en solucin etanlica para dar cloruro de SBenciltiorea, una sal que se estabiliza por resonancia.
Estas
sales
sometidas
a
hidrlisis
cida
dan
los
correspondientes tioles. Ej. C6H5CH2SH, el cual puede ser
fcilmente preparado. Adicionalmente, la sal (II) es
ampliamente empleada para identificar cidos carboxlicos y
otros cidos como sales cristalinas de benciltiouronium.
Simultneamente, aadir cloruro de bencilo (8.3 g, 8.0 ml)
y tiorea pulverizada a 10 ml de etanol al 95% en un
recipiente de 100 ml que tiene un condensador de reflujo.
Calentar la mezcla en un bao de agua con ocasional
agitacin hasta que ocurra reaccin y finalice la
efervescencia; luego calentar la mezcla bajo reflujo por
unos 30 minutos. Luego enfriar la solucin en un bao aguahielo y filtrar el depsito cristalino de cloruro de
benciltiouronium usando vaco, lavarlo con acetato de etilo
helado y secar en un desecador. El punto de fusin es de
170-174 C. El producto es lo suficientemente puro para
usarlo como reactivo. Es muy soluble en agua helada y
etanol, pero puede ser recristalizado usando una mezcla
acetato de etilo-etanol.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
1.4 Espectro IR de algunas sustancias relacionadas a la
prctica.
Nitrobenceno
Fenol
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
Acido Pcrico
Benceno
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
1.5 Cuestionario
1. Llevar a cabo el mecanismo de reaccin de la
preparacin del nitrobenceno.
2. Como se lleva acabo la determinacin del rendimiento
en una reaccin qumica.
3. Llevar a cabo el mecanismo de reaccin de la
formacin del cido pcrico.
4. Porqu el 2,4,6-trinitrofenol tiene caractersticas
cidas y se le denomina cido pcrico? (Sugerencia:
Explique esto tomando en cuenta el pKa del cido
pcrico y el fenol)
5. Hacer un comentario evaluativo y crtico de los
espectros IR mostrados en esta prctica. (Sugerencia
establezca similitudes, diferencias y encuentre la
posicin de cada grupo funcional)
6. Haga un breve resumen del uso del nitrobenceno.
7. Haga un breve resumen del cido pcrico.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
PRACTICA N 2: ESPECTROSCOPIA INFRARROJA
2.1
INTRODUCCION
Los Espectros infrarrojos de los compuestos orgnicos
son por lo general demasiado complejos para utilizarlos de
una forma tan completa como puede hacerse con un espectro
de RMN. Fundamentalmente el uso de la espectroscopia
infrarroja es la identificacin de grupos funcionales, ya
que cada grupo tiene una absorcin caracterstica a
determinada frecuencia. La relacin de frecuencias, o de
las llamadas tablas de interpretacin IR, han sido hechas
en la base de numerosos experimentos y se ha podido
apreciar su similitud cuando existen grupos funcionales
similares.
En esencia, todos los compuestos orgnicos presentarn
algunos picos de absorcin en el infrarrojo entre 2800 y
3000 cm-1, ya que esta es la regin aparecen las
frecuencias caractersticas de los grupos CH de las cadenas
alifticas.
Luego las frecuencias de tensin O-H de los alcoholes (o
de los fenoles) conducen a bandas de absorcin anchas en la
regin de 3200 a 3600 cm-1; estos es fundamentalmente a la
presencia
de
puentes
de
hidrgenos
de
los
grupos
hidroxilos. Cuando el hidroxilo est formando parte de un
grupo carboxilo (-COOH), en el espectro IR debe de aparecer
una banda adicional de CO, tpico de las tensiones
carbonlicas y que se da a 1710 cm-1 aproximadamente.
2.2
PROBLEMAS Y EJERCICIOS.
1. Un
compuesto
usado
como
aditivo
en
la
gasolina
(antidetonante)
fue
analizado
por
un
mtodo
de
combustin. Una muestra del compuesto que pes 9.394 mg
rindi 31.154 mg. De CO2 y 7.977 mg. de agua en la
combustin.
i.
Calcular el porcentaje de composicin del compuesto.
ii. Determinar su frmula mnima o emprica.
2. La combustin de una muestra desconocida pes 8.23 mg. y
dio 9.62 mg. de CO2 y 3.94 mg de agua. Otra muestra pes
5.32 mg y dio 13.49 mg de AgCl en el anlisis de
halgenos. Determinar la composicin en porcentaje y la
frmula emprica de este compuesto orgnico.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
3. Un compuesto slido, extrado de la corteza de Abeto fue
analizado para determinar su composicin en porcentaje.
Una muestra (11.32 mg) fue incinerada en un aparato de
combustin. El dixido de carbono (24.87 mg) y el agua
(5.82 mg) fueron recolectados y pesados. De estos
resultados:
i.
Calcular el porcentaje de la composicin del slido.
ii. Determinar su frmula emprica.
iii. De un anlisis por espectrometra de masas, se
encontr que el peso molecular fue de 420 g/mol.
Indicar su frmula molecular.
4. Una sustancia tiene la frmula molecular de C4H9N. Hay
alguna posibilidad que este material contenga un triple
enlace?
5. En compuestos de estructura similar, cul de cada uno
de los siguientes pares de fragmentos estructurales
orgnicos
originara
una
absorcin
infrarroja
ms
intensa? por qu?
i.
C=O C=C
ii. C=C-Cl C=C-H
iii. O-H N-H
6. Diga
cmo
podran
distinguirse
cada
uno
de
los
siguientes pares de compuestos en base a sus espectros
infrarrojo.
i.
CH3CH2CH2N(CH3)2 y CH3CH2CH2NH2.
ii. CH3CH2CH2CO2H y CH3CH2CO2CH3
iii. CH3CH2COCH3 y CH3CH2CO2CH3.
7. Se est oxidando ciclohexanol a ciclohexanona Cmo
puede indicarle la espectroscopia IR que la reaccin se
ha completado?
8. Qu datos aportados por las espectroscopias
podran utilizarse para distinguir entre:
i.
O
OH
de
IR
ii. etanol y etanodiol.
iii. etanol y cloroetanol
iv. cido actico y acetona
v.
N CH3
N H
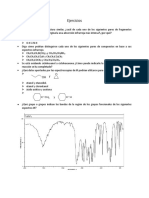
9. Qu grupo o grupos indican las bandas de la regin de
los grupos funcionales de los siguientes espectros IR?
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
______________________________________________________________________
i.
ii.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
10
______________________________________________________________________
iii.
iv.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
11
______________________________________________________________________
v.
vi.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
12
______________________________________________________________________
vii.
viii.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
13
______________________________________________________________________
ix.
x.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
14
______________________________________________________________________
xi.
xii.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
15
______________________________________________________________________
10. Proponga una estructura para cada uno de los
siguientes compuestos a partir de sus espectros
infrarrojos
i. C6H5Cl
ii. C4H8O2
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
16
______________________________________________________________________
iii. C4H8O2
iv. C2H4O2
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
17
______________________________________________________________________
v. C8H7N
vi. C7H6O
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
18
______________________________________________________________________
PRACTICA N 3: ESPECTROSCOPIA DE RESONANCIA MAGNETICA
NUCLEAR PROTONICA (1H)
3.1
INTRODUCCION (TEORIA)
Se sabe que una carga elctrica en movimiento crea un
campo magntico. Si los ncleos atmicos giran, como poseen
carga, tambin crearn un campo magntico. Muchos istopos
tienen lo que parece ser un espn mecnico, al cual se
asigna un momento angular de espn. Todos los sistemas
microfsicos estn cuantizados, y lo que nos importa aqu
es el nmero de espn. Dicho nmero es el momento angular
mximo observable para un ncleo dado. Para la presente
discusin, basta decir que ciertos ncleos muestran dicha
propiedad. Por ejemplo 1H, 13C, 15N, 19F y 31P entre otros
elementos tienen un espn de . Entre los elementos ms
frecuentes con espn de 1 se encuentra el 2H (deuterio, un
istopo del hidrgeno) y el 14N. Otros ncleos activos de
RMN son el litio, boro, cloro y uno de los istopos del
oxgeno. Los ncleos que carecen de espn ms frecuentes
son el 12C, 16O y el 32S.
Todo istopo con un espn distinto de cero se
caracterizar por un momento magntico nuclear, que se
presenta mediante el smbolo . Este puede imaginarse como
un
imn de barra de intensidad . Evidentemente, si el
ncleo (imn) se coloca en un campo magntico, se producir
una interaccin. Como si fuese un imn, el ncleo se ver
atrado o repelido por el campo magntico. Puesto que en un
sistema de espn
slo existen dos posibilidades, slo
sern factibles dos orientaciones en el campo magntico,
designadas por mas (+) o menos (-). As, queda claro que el
mtodo de RMN requiere tanto de un campo magntico como de
una fuente externa de energa.
Esta es una diferencia con las tcnicas de IR o
espectroscopia Ultravioleta, que precisan exclusivamente de
la muestra y de una radiacin incidente.
El resultado de algunos clculos sencillos (que deben
ser vistos para estudios ms avanzados) muestra que la
energa de una transicin desde un estado menos a uno ms
(es decir de - a +) es igual a Hoh/2. Puesto que E =
h, la anterior expresin ser equivalente a ho.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
19
______________________________________________________________________
E =
Ho h
2
= h o
donde:
= constante giromagntica, caracterstica del ncleo.
Ho = intensidad del campo magntico aplicado.
H = constante de Planck.
Operando, puede verse que 2o = Ho. Esta es la
denominada condicin de resonancia. Aunque no es importante
memorizar esta ecuacin, recurdese que si no existe campo
magntico, es decir, si Ho = 0, no hay diferencia de
energa entre los niveles, la ecuacin completa se anula,
no se observar el fenmeno de la resonancia.
La relacin entre la separacin energtica y el campo
magntico puede ilustrarse mediante la siguiente figura.
Conceptualmente lo que sucede en un experimento de RMN
es relativamente sencillo de explicar. En ausencia de un
campo magntico, los espines nucleares se hallan dispuestos
al azar o de manera desordenada, en todas las posibles
direcciones. Cuando se aplica un campo magntico, dichos
espines tienden a orientarse en la misma direccin que el
campo aplicado (estado de menor energa) o bien opuestos al
mismo (de mayor energa). A medida que la molcula
encuentre
una
radiacin
incidente,
se
producir
la
absorcin de energa y uno de los espines se invertir, es
decir, un ncleo en el estado de energa inferior cambiar
su orientacin y pasar al estado de energa superior. La
absorcin de esta energa es lo que detecta el aparato de
RMN.
Puesto que la energa no puede absorberse de forma
indefinida, debe de existir algn mecanismo por el que
aquellos espines en el estado de energa puedan perder
energa. Esta prdida de energa o relajacin, no puede
tener lugar por fluorescencia o fosforecencia, como ocurre
en la espectroscopia Ultravioleta e Infrarroja. Los ncleos
excitados liberan energa a travs de un mecanismo
denominado relajacin espn-red. Esto en efecto son
conceptos mas avanzados y el lector puede dirigirse a
referencias concernientes a RMN avanzada.
3.1.1
El Desplazamiento qumico
De acuerdo a lo mencionado anteriormente, se podra
concluir que todos los protones absorben a la misma
frecuencia, o tienen idntica condicin de resonancia.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
20
______________________________________________________________________
Afortunadamente, las posiciones de absorcin reales
varan ligeramente segn sea el entorno electrnico de cada
protn. Los electrones circulantes crean un campo magntico
local opuesto al campo magntico aplicado. La densidad
electrnica alrededor de un ncleo de hidrgeno (o de
cualquier otro ncleo) depender, en primera aproximacin,
del efecto inductivo de los restantes grupos unidos al
tomo que soporta dicho hidrgeno. Esto significa que los
factores locales de entorno cambiarn la posicin de
resonancia; en consecuencia, no todos los protones se
observarn a la misma combinacin de campo y frecuencia.
Estos
factores
qumicos
dan
lugar
al
denominado
desplazamiento qumico.
3.2
EJERCICIOS
1. Prediga los patrones de desdoblamiento esperados para
cada una de las siguientes molculas:
a) CHBr2CH3
b) CH3OCH2CH2Br
c) ClCH2CH2CH2Cl
d) CH3CH2OCOCH(CH3)2
2. Trace estructuras para compuestos que satisfagan
siguientes descripciones:
a) C2H6O; un singulete.
b) C3H7Cl;un doblete y un septuplete.
c) C4H8Cl2O; dos tripletes.
d) C4H8O2; un singulete, un triplete y un cuadruplete.
las
3. El siguiente espectro de RMN corresponde a un compuesto
de frmula C4H8O2 y es un ster. Sugerir una estructura
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
21
______________________________________________________________________
4. El grupo funcional en este compuesto (C3H7NO2) es un
grupo
nitro.
Debajo
del
espectro
estn
los
desplazamientos de cada familia de seales. Cul es su
estructura?
Assign.
A
B
C
Shift(ppm)
4.361
2.033
1.029
5. Dar una estructura, o estructuras, consistente con cada
uno de los siguientes conjuntos de datos de RMN
a)
C3H3Cl5: t, 4.52 (1H); d, 6.07 (2H).
b)
C4H9Br: d, 1.04 (6H); m 1.95 (1H); d, 3.33 (2H)
c)
C3H5Cl3: s, 2.20, (3H); s, 4.02 (2H)
d)
C10H14: s, 1.30 , (9H); s, 7.28 (5H)
e)
C10H14: d, 0.88
(6H), m, 1.86 (1H); d, 2.45
(2H); s, 7.12 (5H)
f)
C9H10: quint, 2.04 , (2H); t, 2.91 (4H); s, 7.17 ,
(4H).
g)
C10H13Cl: s, 1.57 (6H); s, 3.07 , (2H); s, 7.27 ,
(5H).
6. Sugerir estructuras para los siguientes datos de RMN:
a)
C4H8O2: 1.2 (t, 3H); 2.3 (cuart, 2H); 3.6 (s,
3H).
b)
C9H10O: 1.2 (t, 3H); 3.0 (cuart, 2H) y 7.4 a 8.0
(multiplete, 5H).
c)
C10H14: 1.3 (s, 9H) y 7.2 (multiplete, 5H).
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
22
______________________________________________________________________
d)
e)
f)
g)
h)
i)
j)
k)
l)
m)
n)
o)
p)
q)
r)
s)
t)
u)
v)
w)
x)
y)
z)
C10H12O2: 2.0 (s, 3H); 2.9 (t, 2H); 4.3 (t, 2H) y
7.3 (s, 5H).
C8H7N: 3.7 (s, 2H) y 7.2 (s, 5H).
C4H6Cl2O2: 1.4 (t, 3H); 4.3
(cuart, 2H) y 5.9
(s, 1H).
C7H14O: 0.9 (t, 6H); 1.6 (sexteto, 4H) y 2.4 (t,
4H).
C5H10O2: 1.2 (d, 6H); 2.0
(s, 3H) y 5.0
(septeto, 1H).
C6H12O2: 1.5 (s, 9H); y 2.0 (s, 3H).
C9H10O2: 2.1 (s, 3H); 5.1 (s, 2H) y 7.3 (s, 5H).
C10H12O2: 1.2 (t, 3H); 3.5 (s, 2H); 4.1 (cuart,
2H) y 7.3 (s, 5H).
C10H12O2: 1.5 (d, 3H); 2.1 (s, 3H); 5.9 (cuart,
1H) y 7.3 (s, 5H).
C10H12O: 1.0 (t, 3H); 2.3 (cuart, 2H); 3.6 (s,
2H) y 7.2 (s, 5H).
C2H4Br2: 2.5 (d, 3H) y 5.9 (cuart, 1H).
C3H6Br2: 2.4 (quint, 2H) y 3.5 (t, 4H).
C8H9Br: 2.0 (d, 3H); 5.0 (cuart, 1H) y 7.3
(multiplete, 5H).
C14H14: 2.9 (s, 4H) y 7.2 (s, 10H).
C11H17N: 1.0 (t, 6H); 2.5 (cuart, 4H); 3.6 (s,
2H) y 7.3 (s, 5H).
C3H5ClO2: 1.7 (d, 3H); 4.5 (cuart, 1H) y 12.2 (s,
1H).
C3H5ClO2: 2.8 (t, 2H); 3.8 (t, 2H) y 12.2 (s,
1H).
C10H14: 1.2 (d, 6H); 2.3 (s, 3H); 2.9 (septet,
1H) y 7.0 (s, 4H).
C7H12O4: 1.3 (t, 6H); 3.4 (s, 2H) y 4.2 (cuart,
4H).
C9H8O: 3.4 (s, 4H) y 7.2 (s, 4H).
C9H10: 2.0 (quint, 2H); 2.9 (t, 4H) y 7.2 (s,
4H).
C3H4O2: 3.6 (t, 2H) y 4.3 (t, 2H).
C5H9BrO2: 1.2 (t, 3H); 2.9 (t, 2H); 3.5 (t, 2H) y
4.0 (cuart, 2H).
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
23
______________________________________________________________________
PRACTICA N 4: ALCOHOLES
4.1
GENERALIDADES.
Son
compuestos
de
frmula
general
R-OH,
cuya
caracterstica, como se aprecia, es la presencia del grupo
oxhidrilo unido a un tomo de carbono aliftico. Esta
ltima apreciacin es importante, ya que si el grupo
oxhidrilo est unido a un tomo de carbono aromtico, el
resultado es la presencia de otra familia de compuestos
denominados fenoles. Los fenoles, a pesar de tener como
grupo funcional caracterstico el OH, no son alcoholes.
H
H
OH
H C OH
H
H
C
C
C
C
H C OH
H
C
H
C
C
C
H
Fenol
Metanol
Alcohol Benzlic
Los alcoholes pueden ser:
a) Primarios: Cuando el grupo oxhidrilo se encuentra unido
a un carbono primario.
b) Secundario: Cuando el grupo oxhidrilo se encuentra unido
a un carbono secundario.
c) Terciario: Cuando el grupo oxhidrilo se encuentra unido
a un carbono terciario.
H
R C OH
H
1
H
R C OH
R'
2
R''
R C OH
R'
3
Los alcoholes, dependiendo de cuantos grupos OH posean
podrn ser monoles, dioles, trioles, etc. si tienen uno,
dos, tres, etc. grupos OH respectivamente.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
24
______________________________________________________________________
4.2
REACCIONES.
CH3CH2CH2CH2OH
monol
CH2 OH
CH OH
H2C CH2
OH
OH
CH2 OH
triol
diol
4.2.1
Ensayo
de
identificacin
dicromato de potasio.
con
solucin
de
Tomar 1 ml de solucin de dicromato de potasio al 10% y
diluir con 1 ml de agua destilada, agregar 2-3 gotas de
cido sulfrico concentrado y 0.5 a 1 ml de muestra
(etanol, metanol). Calentar suavemente en bao mara.
Anotar los resulltados.
4.2.2
Ensayo con solucin de Permanganato de potasio.
Colocar 1 ml de muestra problema (etanol) en un tubo de
ensayo, luego adicionar una gota de solucin de hidrxido
de sodio y unas gotas de solucin de permanaganato de
potasio al 0.1%. Colocar en bao mara por unos minutos,
observar y anotar los resultados.
4.2.3
Test de los esteres
Tomar 1 ml de alcohol etlico y 1 ml de cido actico y 0.5
ml de cido sulfrico concentrado; calentar suavemente en
bao mara por un minuto. Detectar el olor a frutas o un
aroma fragancioso, tpico de la formacin de steres.
Repetir este test usando pentan-1-ol (alcohol amlico) en
vez de etanol. Observar y anotar los resultados.
4.2.4
Test de Iodoformo
Tomar dos tubos de ensayo, en uno colocar 1 ml de etanol y
en el otro 1 ml de propan-2-ol (alcohol isoproplico);
agregar a cada uno de ellos 1 ml de solucin de hidrxido
de sodio al 10%, luego aadir una solucin de ioduro de
potasio al 10% y unos cristales de yodo metlico. Agitar
simultneamente los dos tubos hasta la formacin de un
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
25
______________________________________________________________________
precipitado amarillo de iodoformo. Anotar cual de los dos
alcoholes reacciona con mayor rapidez.
4.3
Otras reacciones
4.3.1
Diferenciacin
de
alcoholes
secundarios y terciarios.
Este ensayo se realiza con el reactivo de
concentrado y cloruro de zinc anhidro)
R O
H
i.
ii.
ZnCl2
R
- [HOZnCl2
Cl -
Lucas
(HCl
RCl
ROH + ZnCl2
primarios,
Reactivo: Disolver 16 g. de cloruro de zinc anhidro en
10 ml de cido clorhdrico concentrado, enfriando para
evitar una prdida de cloruro de hidrgeno.
Procedimiento: Aadir tres o cuatro gotas de alcohol
a 2 ml del reactivo en un pequeo tubo de ensayo.
Agitar vigorosamente el tubo, y dejar reposar la
mezcla a temperatura ambiente. Los alcoholes primarios
inferiores al hexlico se disolvern; los superiores
al hexlico no se disolvern apreciablemente y la fase
acuosa permanecer clara; despus de 2 a 5 minutos los
alcoholes secundarios reaccionarn para producir una
solucin opalescente de cloruro de alquilo insoluble.
Con los alcoholes terciarios, allicos y benclicos,
hay una separcin casi inmediata de dos fases debido a
la formacin de un cloruro de alquilo insoluble. Si
queda alguna duda acerca de si el alcohol es
secundario o terciario puede repetirse el ensayo
empleando esta vez cido clorhdrico concentrado. Con
este reactivo los alcoholes terciarios reaccionan
inmediatamente para formar el cloruro de alquilo
insoluble, mientras que los secundarios no reaccionan.
Un segundo mtodo para distinguir entre alcoholes
primarios y secundarios o terciarios se basa en que los
terciarios son inertes frente a la oxidacin con cido
crmico:
3H C OH + 2CrO3 + 6H+
3+
C O + 2Cr
+ 6 H 2O
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
26
______________________________________________________________________
i.
ii.
4.3.2
Reactivo: Disolver 1 g. de xido crmico en 1 ml de
cido sulfrico concentrado y diluirlo cuidadosamente
con 3 ml de agua.
Procedimiento: Disolver 20 mg o una gota de alcohol en
1 ml de acetona de una pureza de grado reactivo y
aadir 1 gota del reactivo. Sacudir la mezcla. Los
alcoholes primarios y secundarios reaccionan en unos
10 segundos para dar una suspensin opaca de color
azul verdoso. Los alcoholes terciarios no reaccionan
con el reactivo. Otras sustancias fcilmente oxidables
tales como aldehdos, fenoles y enoles tambin
reaccionan con este reactivo.
Diferenciacin de monoles y polioles.
Accin sobre las sales de cobre: En dos tubos de ensayo
colocar 1 ml se solucin de sulfato de cobre, adicionar a
uno de los tubos 0.5 ml de un monol y al otro 0.5 ml de un
poliol, luego aadir a cada uno de ellos 1 ml de solucin
de hidrxido de sodio. Calentar suavemente y anotar los
resultados para cada uno de los tubos.
4.5
Reduccin de Benzofenona con Borohidruro
NaBH4: Preparacin del difenilmetanol.
O
HO
de
sodio
NaBH4
EtOH, H2O
Procedimiento.
Disolver la benzofenona (2 mmmol) en 5 ml de etanol en un
pequeo erlenmeyer y agitar la solucin con agitador
magntico. En un tubo de ensayo disolver el NaBH4 (2.2
mmol)en 1.5 ml de agua helada y esta solucin aadir gota a
gota a la solucin etanlica de benzofenona a temperatura
ambiental. Despus de que todo el borohidruro de sodio ha
sido aadido, continuar la agitacin por 40 minutos
adicionales. Luego, lentamente coloque la mezcla en un
beaker que contiene 10 ml de agua helada y 1 ml de HCl
concentrado. Despus de unos minutos, recolectar el
precipitado por filtracin al vaco y lavarlo con pequeas
porciones de agua. Secar el producto y recristalizarlo
usando ter de petrleo.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
27
______________________________________________________________________
Preguntas
1. Llevar a cabo las reacciones que se han hecho en el
laboratorio
2. Proponer cuales son las caractersticas ms importantes
del espectro infrarrojo de los alcoholes.
3. Como diferenciar un alcohol primario, de uno secundario
y de uno terciario a travs de pruebas qumicas.
Explicar la respuesta con reacciones qumicas.
4. Usando la espectroscopa infrarroja como se podra
diferenciar un alcohol primario de uno secundario y de
uno terciario. Ver los ejemplos
5. Explicar los espectros de RMN protnica para el metanol,
etanol y el Propan-1-ol.
6. Discutir el mecanismo de reduccin cuando se usa NaBH4
en solucin etanlica.
7. Sugiera otro esquema de sntesis para la preparacin del
difenilmetanol.
8. Cules seran las caractersticas ms saltantes de los
espectros
infrarrojo
de
la
benzofenona
y
del
difenilmetanol?
Espectros Infrarrojos
Metanol
CH3OH
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
28
______________________________________________________________________
Etanol
C2H5OH
1-Propanol
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
29
______________________________________________________________________
2-Propanol
ter-Butanol
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
30
______________________________________________________________________
Benzofenona
difenilmetanol
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
31
______________________________________________________________________
Metanol
Parameter
D(A)
D(B)
ppm
Hz
4.19
3.410
Etanol
Assign.
A
B
C
3.687
2.61
1.226
Shift(ppm)
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
32
______________________________________________________________________
1-Propanol
Assign.
Shift(ppm)
A
B
C
D
J(A,C)=6.6HZ.
2-Propanol
Assign.
A
B
C
Shift(ppm)
4.008
2.16
1.200
3.582
2.26
1.57
0.94
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
33
______________________________________________________________________
PRACTICA N5: ALDEHIDOS Y CETONAS
5.1 GENERALIDADES: Reacciones del grupo carbonilo
El grupo carbonilo es el grupo funcional caracterizado
por contener carbono y oxgeno unidos por un doble enlace.
La electronegatividad del carbono y del oxgeno est bien
marcada: en la escala de Pauling es de 2.5 y 4.5,
respectivamente. Debido a que esta diferencia es bastante
grande es que el grupo carbonilo se encuentra bastante
polarizado. El extremo carbonado de este dipolo es menos
electronegativo y en consecuencia es un cido Lewis.
Entonces el oxgeno es ms electronegativo, por lo tanto al
grupo carbonilo se le representa de forma dipolar de la
siguiente manera:
O
La polaridad del grupo carbonilo influencia las
propiedades de solubilidad de las molculas que lo
contienen. Si las dos restantes valencias del tomo de
carbono se hallan ocupadas por grupos alquilo de tamao
mediano o grande, el compuesto carbonlico ser soluble en
disolventes hidrocarbonados. No es nada extrao que un
compuesto orgnico sea soluble en diferentes solventes
orgnicos. La propiedad ms interesante es que debido a la
polaridad del grupo carbonilo (es decir a su dipolo), su
extremo negativo puede formar enlaces puente hidrgeno con
el agua y con los disolventes protnicos del tipo
alcoholes, como se indica seguidamente:
H3C
R(H)
C O
H O
H3C
Si los grupos alquilo no son muy grandes, la molcula
que contiene el carbonilo puede ser tambin soluble en
agua. En general, esto es as para los aldehdos y cetonas
de bajo peso molecular. Como cabe esperar, el butano es
virtualmente inmiscible en el agua. En cambio la acetona
que tiene el mismo peso molecular (58), es completamente
miscible con el agua. A medida que los grupos alquilo o
arilo se hacen mayores, la porcin orgnica de la
molcula comienza a dominar las propiedades de la
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
34
______________________________________________________________________
solubilidad de la misma. Por ejemplo la di-n-hexil cetona
es insoluble en agua y miscible con el n-hexano.
5.1.1 Olor
Las propiedades de solubilidad de los aldehdos, cetonas
y otros carbonlicos vienen determinadas sea por el grupo
carbonilo o bien por los restos hidrocarbonados ligados al
mismo. En los casos intermedios, hay una ligera solubilidad
en los dos tipos de solventes, pero en cada extremo la
solubilidad est dominada por una u otra porcin de la
molcula. Por otro lado, el olor de un compuesto es siempre
consecuencia de su estructura global. Es una creencia
general
que
los
receptores
olfativos
tienen
formas
definidas. Algunas molculas que poseen grupos funcionales
y una reactividad bastante distintas pueden tener un olor
parecido, debido a que su forma es similar. Aunque es
difcil oler un grupo metilo sobre la posicin 7 del
dodecano o un etilo unido a un esteroide, se pueden hacer
algunas generalizaciones sencillas y aprenderse algunos
aromas frecuentes. Esta es una propiedad que caracteriza a
muchos aldehidos y cetonas. Dos ejemplos comunes son el
anisaldehdo, compuesto incoloro pero de olor a anisado
caracterstico, y el benzaldehdo, que huele a almendras
amargas. Otra molcula, cuyo olor probablemente se recuerde
cuando se hizo la determinacin del peso molecular, es el
alcanfor.(Fig. 5.1)
CHO
CHO
O
OCH3
Anisaldehido
Benzaldehido
Alcanfor
Fig. 5.1: Algunos aldehidos y cetonas
de carcter fragancioso
El alcanfor es una cetona terpnica cuya
forma
molecular
es
aproximadamente
esfrica.
Su
olor,
en
realidad, es el patrn para las molculas esfricas. Se
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
35
______________________________________________________________________
dice que muchas de tales molculas tienen olor canforceo y
huelen de forma similar a las bolas antipolillas.
Dos aldehdos cuyos nombres indican su olor son el
cinamaldehdo y la vainillina (Fig. 5.2). Aunque el olor de
canela es dbil en el cinamaldehido, puede distinguirse
claramente. La vainillina (4-hidroxi-3-metoxibenzaldehdo),
a pesar de ser un slido tiene un olor intenso.
CH CH CHO
CHO
HO
CH3O
Fig. 5.2: Cinamaldehido y vainillina
5.2 Preparacin de -Benzaldoximas (Fig. 5.3)
H
CHO
+
C NOH
NH2OH
Fig. 5.3: Preparacin de una Benzaldoxima
Procedimiento: En un Erlenmeyer de 250ml, mezclar una
solucin de 14 g de NaOH en 40 ml de agua y 21 g de
benzaldehido. Aadir 15 g de clorhidrato de hidroxilamina
en pequeas porciones y agitar la mezcla continuamente
(mucho mejor si se emplea un agitador magntico). Se puede
desarrollar algo de calor y el benzaldehido eventualmente
desaparece. Una vez que la mezcla se enfra, se separa una
masa cristalina de derivado sdico de la oxima. Aadir
suficiente agua hasta que se forme una solucin clara y
aadir dixido de carbono a saturacin. Se separa una
emulsin de la oxima y extraer la oxima con ter, secar el
extracto sobre sulfato de magnesio o sulfato de sodio,
filtrar y remover el ter usando el rotavapor. Purificar el
derivado por destilacin al vaco, 124C/12 mmHg. Este
producto solidifica gradualmente en enfriamiento con hielo.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
36
______________________________________________________________________
5.3 Preparacin de Acetoxima (Fig. 5.4)
O
CH3
N
CH3
+ NH2OH
CH3
OH
CH3
Fig. 5.4: Preparacin de la acetoxima
Procedimiento: Preparar una solucin de 12.5 g de
clorhidrato de hidroxilamina en 20 ml de agua contenidos en
un erlenmeyer de 100 ml. Disolver 7 g de NaOH en polvo en
20 ml de agua, enfriar la reaccin en un bao agua-hielo, y
luego
aadirlo
a
la
solucin
de
clorhidrato
de
hidroxilamina. Colocar un termmetro en la solucin y
enfriar el frasco en un bao agua-hielo hasta que la
temperatura este enter 5 y 10C. Ahora aadir 12 ml de
acetona (mida exactamente con bureta o pipeta) y agitar la
mezcla. Durante la adicin la temperatura se incrementar,
pero que no lo hag por encima de 15. La acetoxima comienza
a cristalizar cuando se ha aadido la mitad de la acetona.
Cuando se haya aadido la totalidad de la acetona, deje que
la mezcla repose en un bao agua-hielo por 15 minutos y
luego filtrar el derivado al vaco.
5.4 Preparacin de Derivados
Preparacin de Dinitrofenilhidrazonas
NO2
R1
H2 NNH
NO2
NO2
R1
C O
R2
C NNH
NO2
R2
Aadir etanol (5 ml) a 2,4-dinitrofenilhidrazina (0.25
g.) en un beaker y aadir cido sulfrico concentrado (0.50
ml) cuidadosamente. Disolver el compuesto carbonlico
desconocido en un pequeo volumen de etanol y aadir esta
disolucin al sobrenadante claro de la solucin de
dinitrofenilhidrazina. Calentar la mezcla si no hay
separacin inmediata de un precipitado y dejar reposar por
espacio de unos diez minutos. Si no ocurre separacin
aadir agua gota a gota hasta que ocurra la precipitacin.
Filtrar el slido.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
37
______________________________________________________________________
5.5 Diferenciacin de aldehidos y cetonas
Ensayo de Tollens
Reactivos: Solucin A. Disolver 3 g. de AgNO3 en 30 ml de
agua. Solucin B. Hidrxido de sodio al 10%. Cuando se
requiere utilizar el reactivo, mezclar en un tubo de ensayo
limpio 1 ml de solucin A con 1 ml de la solucin B y
aadir a gotas una solucin diluda de amonaco justo hasta
que se diuelva el xido de plata.
Adase unas cuantas gotas de una solucin diluida del
compuesto a 2 o 3 ml de la solucin reactivo preparado. En
un ensayo positivo, la plata se deposita en forma de espejo
de plata en las paredes del recipiente ya sea en fro o
despus de calentar en un bao de agua caliente.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
38
______________________________________________________________________
PRACTICA N 6: ACIDOS CARBOXILICOS
6.1 Introduccin
Los cidos carboxlicos son slidos cristalinos a excepcin
del cido frmico, actico (p.f. 18 C, cuando es glacial)
y
el lctico (p.f.18 C y de carcter viscoso, como
jarabe). El cido frmico (p.e. 100 C) y el actico (p.e.
118 C) son los nicos miembros que son fcilmente
voltiles. El cido lctico puede ser destilado pero solo
bajo presin reducida. El cido frmico y el actico tienen
olores pungentes bastantes caractersticos. Mientras que el
cido cinmico tiene un olor o fragancia agradable pues el
y sus derivados son componentes de la canela.
Los cidos alifticos son todos solubles en agua fra
mientras que los cidos aromticos son muy ligeramente
solubles en agua, pero fcilmente solubles en agua
hirviendo,
El
cido
ftlico,
teniendo
dos
grupos
carboxilos, es ms soluble que los otros cidos aromticos
en agua helada.
6.2 Reacciones generales
Los
cidos
carboxlicos
tienen
caractersticas, como por ejemplo:
a.
b.
c.
d.
e.
una
serie
de
Son solubles en solucin de NaOH
Son solubles en solucin de Na2CO3 y liberan CO2.
Si los cidos o sus sales se calientan con cal sodada,
el grupo carboxilo se elimina y se producen productos
voltiles.
Con alcoholes y en presencia de cido sulfrico
producen steres, los que tienen olores o fragancias
muy caractersticas.
Las sales neutras de muchos cidos tratados con cloruro
frrico dan diferentes coloraciones y precipitados.
6.3 Reacciones
a.
Solubilidad en NaOH: Colocar 0.1 g de un determinado
cido, aadir agua destilada y observar. Los que no han
solubilizado de manera apreciable, aadir solucin de
NaOH al 10% y observar el comportamiento. Observar que
los fenoles disuelven en NaOH originando fenxidos.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
39
______________________________________________________________________
b.
Solubilidad en solucin de carbonato de sodio: Ntese
que los fenoles cuando se solubilizan en solucin de
NaOH tambin se disolvern en solucin de Na2CO3, pero
sin la evolucin de CO2, es decir sin la formacin del
derivado sdico. Esta es una reaccin muy til para
distinguir entre un cido carboxlico y la mayora de
los fenoles.
Nota: Algunos fenoles sustitudos, en especial los
nitrofenoles, son los suficientemente cidos como para
liberar CO2 a prtir de Na2CO3. Los nitrofenoles, sin
embargo, todos ellos dan soluciones amarillas o rojas
con Na2CO3.
c.
Calentamiento con cal sodada. Por ejemplo, puede
utilizar cido saliclico, que cuando se calienta con
cal sodada se libera fenol, el cual puede ser detectado
por el olor o por la coloracin verdosa que da con
solucin de cloruro frrico.
d.
Formacin de steres: calentar a bao mara 1 ml de
etanol con 0.5 ml de un cido carboxlico y aadir unas
pocas gotas de H2SO4. Enfriar y a fin de resaltar el
olor aadir agua y percibir el olor. Este test es
particularmente til para identificar cido actico y
cido saliclico.
e.
Reaccin con cloruro frrico. Para el xito de esta
reaccin es importante que la solucin este neutra. Un
exceso de cido usualmente inhibe la produccin de
color o precipitado, y un exceso de lcali da un
precipitado marrn-rojizo de cloruro frrico. Una
solucin neutra se hace de la siguiente manera: Colocar
0.5 g del cido en un tubo de ensayo y aadir solucin
de amonaco hasta que est ligeramente alcalino al
papel tornasol. Calentar en bao mara, hasta que se
haya eliminado por completo el olor a amonio. A esta
solucin fra aadir solucin de cloruro frrico.
6.4 Cloruro frrico acuoso:
La solucin de cloruro frrico contiene algunas veces
un gran exceso de HCl el mismo que podra interferir
con las diferentes reacciones. Si es muy marcadamente
acdico aadir solucin diluida de NaOH gota a gota a
la solucin de cloruro frrico hasta que un pequeo
precipitado de hidrxido frrico aparezca. Filtrar y
usar la solucin filtrada clarificada. Esta solucin
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
40
______________________________________________________________________
es dbilmente cida pero no interfiere con los
ensayos, mostrados a continuacin:
a.
El formato o acetato dan una solucin rojo profunda la
misma que cambia, cuando se somete a ebullicin, a la
formacin de un precipitado pardo rojizo de la sal
bsica frrica.
b.
El succinato, benzoato y ftalato dan una coloracin
marrn que son las sales frricas bsicas.
c.
Una
coloracin
salicilato.
d.
Disolver unos pocos cristales de fenol en agua y aadir
la solucin de cloruro frrico: se debe producir una
coloracin violeta.
e.
Con cido oxlico da una coloracin amarilla plido.
violeta
indica
la
presencia
de
6.5 Cuestionario
1.
Representar las reacciones que se han llevado a cabo
con frmulas qumicas y fundamentar su eleccin.
2.
Haga una breve resea (ubicacin, fuentes y usos) de
los llamados cidos omega.
3.
Ubicar por lo menos tres espectros de RMN de cualquier
cido
carboxlico
y
explicar
los
patrones
de
desdoblamiento.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
41
______________________________________________________________________
PRACTICA N 7: DERIVADOS DE ACIDOS CARBOXILICOS
7.1 SNTESIS DE ASPIRINA (Acido acetilsaliclico)
ANTECEDENTES
La aspirina (cido acetilsaliclico), es un antipirtico y
analgsico, muy empleado en medicina. Aqu se estudiar la
accin de tres catalizadores en la acetilacin del
oxhidrilo del cido saliclico.
REACCIONES
COOH
OH
COOH
(CH3CO)2O/H+
O C CH3
PARTE EXPERIMENTAL
Distribuya por partes iguales 3 g de cido salicilico en
tres tubos de ensayo de 13 X 100 mm. Aada a cada tubo 2 mi
de anhdrido actico: Al primer tubo adale 0.2 g de
acetato de sodio anhidro, anote la hora, agite con un
termmetro, y registre el tiempo transcurrido hasta que la
temperatura aument 4 C y aproximadamente la cantidad de
slido
se
ha
disuelto.
Despus,
contine
agitando
ocasionalmente con una varilla de vidrio, i mientras inicia
la siguiente acetilacin. Limpie el termmetro, colquclo
dentro del segundo tubo, aada 5 gotitas (use un
microgotero) de piridina, agite, observe que tiempo
transcurre hasta que aumente 4 C la temperatura, anote
tambin qu cantidad de slido queda en ese tubo. Aada 5
gotitas de cido sulfrico al tercer tubo, agite con el
termmetro y observe el tiempo que tarda la temperatura en
aumentar 4 C. Tabule los resultados, ordenando los
catalizadores de acuerdo con su actividad.
Caliente los tres tubos en bao mara durante 5 a 10
minutos, hasta que se disuelva todo el slido y se complete
la reaccin, despus vierta todas las soluciones en un
erlenmeyer de 125 ml conteniendo 50 ml de agua y lave los
tubos con agua. Sacuda para acelerar la hidrlisis del
exceso de anhdrido actico, y luego enfre en bao de
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
42
______________________________________________________________________
hielo, raspe el matraz y recoja el slido cristalino, en un
embudo Buchner y con succin, lvelo con agua y squele.
Determine el punto de fusin y el rendimiento.
Ensaye la solubilidad de una muestra en agua caliente y
observe las peculiares caractersticas de la solucin
acuosa al enfriarse y cuando se raspan las paredes del tubo
con una varilla de vidrio.
7.2 Procedimiento alterno
Mezclar 10 ml de anhdrido actico y 10 ml de cido actico
en un beaker. Aadir esta mezcla a 6 g. de cido saliclico
que estn en un recipiente adecuado y colocar un
condensador
de
reflujo.
Calentar
la
reaccin
por
aproximadamente 40 minutos y luego colocar la solucin
caliente en 100 ml de agua helada la que est contenida en
un beaker y agitar vigorosamente y se observar que los
cristales de cido acetilsaliclico se separarn. Filtrar
los cristales o material crudo en un embudo buchner con
vaco, lavar los cristales con agua helada, drenar bien y
secar los cristales o slido en una estufa a 100 C.
Determinar el rendimiento. Para obtener una buena pureza,
recristalizar utilizando cido actico.
7.3 Sntesis de Acetanilida
FUNDAMENTO
Las aminas primarias y secundarias
reaccionan con los
anhdridos de cidos o haluros de acilo formando amidas.
Algunas se preparan por deshidratacin de las sales correspondientes. A menudo se usa la acilacin de grupos amino
para proteger el grupo amino.
REACCIONES.
O
NH2
NHC CH3
NH3
O2CCH3
calor
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
43
______________________________________________________________________
TECNICA
En un beaker de 500 ml tomar 10 ml de anilina, 9 ml de HCl
concentrado a lo que se aade aproximadamente 250 ml de
agua. Agitar bien a fin de disolver completamente la
anilina y se deber obtener un producto caso incoloro si la
anilina utilizada a estado en un elevado estado de pureza.
En todo caso se recomienda usar carbn activado por lo que
se debe de aadir unos 2 g de carbn activado, mezclar
bien, hervir por unos 2 minutos y luego filtrar por
gravedad. Se deber obtener una solucin incolora. Mientras
tanto preparar una solucin de 16.5 g de acetal de sodio en
50 ml de agua.
A la solucin incolora aadir 13 ml de anhdrido actico
con agitacin hasta que se obtenga una solucin homognea.
Luego de manera inmediata colocar esta solucin en la
solucin de acetato de sodio contenida en un beaker.
Colocar esto en un bao de agua helada y agitar la mezcla
vigorosamente hasta que se separen completamente los
cristales de acetanilida. Filtrar al vaco, drenar bien y
secar en una estufa. Se puede recristalizar utilizando una
mezcla alcohol agua.
Procedimiento alterno
Aadir 20 ml de una mezcla de volmenes iguales de
anhdrido actico y cido actico a 10 ml de anilina
contenida en un erlenmeyer. Colocar un condensador de
reflujo y calentar la mezcla por unos 10 a 15 minutos. Lueo
colocar el lquido caliente en 200 ml de agua helada,
agitar constantemente durante la adicin y se observar
como cristaliza la acetanilda. Filtrar al vaco, drenar
bien y lavar varias veces con agua. Secar y el producto se
puede purificar una mezcla de cido actico y agua.
Determinar el rendimiento.
Cuestionario.
1. Llevar acabo los mecanismos de reaccin para las
reacciones que se han llevado acabo.
2. Comente y analice los espectros de RMN del cido
acetilsaliclico y la acetanilida.
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
44
______________________________________________________________________
Acido Acetilsaliclico
Assign.
A
B
C
D
E
F
Shift(ppm)
11.
8.125
7.624
7.356
7.142
2.352
Facultad de Farmacia y Bioqumica, UCSM
Prcticas de Qumica Orgnica II, 2014
JD Crdenas Garca
45
______________________________________________________________________
Assign.
A
B
C
D
E
Shift(ppm)
7.79
7.49
7.30
7.10
2.138
You might also like
- LQII Practica 4 Sintesis AcetanilidaDocument5 pagesLQII Practica 4 Sintesis AcetanilidaKonugy BiotaanaNo ratings yet
- Informe de Eliminacion E1 Sintesis de Ciclohexeno Por Medio de La Desidratacion Del CicloexanolDocument5 pagesInforme de Eliminacion E1 Sintesis de Ciclohexeno Por Medio de La Desidratacion Del CicloexanolAndres CuadradoNo ratings yet
- Síntesis de Ácido PícricoDocument5 pagesSíntesis de Ácido PícricoAmparo Mejia Ruiz78% (9)
- Reporte 2: Síntesis de DifenilmetanolDocument11 pagesReporte 2: Síntesis de DifenilmetanolFrank AngelNo ratings yet
- Obtención de NitrobencenoDocument4 pagesObtención de NitrobencenoBerenice GómezNo ratings yet
- BENCILO PrevioDocument5 pagesBENCILO PrevioDaniel Bautista100% (1)
- Tarea 9 Recristalización 21Document11 pagesTarea 9 Recristalización 21ALEJANDRA LUCERO MEJ�A CRUZ100% (1)
- Laboratorio 1. Sustitución Electrofílica AromáticaDocument1 pageLaboratorio 1. Sustitución Electrofílica AromáticaLina Mariana Prieto AmadoNo ratings yet
- Aislamiento de Cafeina A Partir de Hojas de TéDocument6 pagesAislamiento de Cafeina A Partir de Hojas de TéMANUELA RAMIREZ SEPULVEDANo ratings yet
- Preparación de Dibenzalacetona A Partir de Benzaldehído y AcetonaDocument11 pagesPreparación de Dibenzalacetona A Partir de Benzaldehído y AcetonaArturo Velasco100% (1)
- Informe III. Síntesis de La AspirinaDocument9 pagesInforme III. Síntesis de La AspirinasolanoleNo ratings yet
- Ejercicios IRDocument10 pagesEjercicios IRAngel RamosNo ratings yet
- Punto de Ebullición Destilación Simple y A Presión ReducidaDocument6 pagesPunto de Ebullición Destilación Simple y A Presión ReducidaAlma DanielaNo ratings yet
- Reporte Benzoína Bencilo Acido BencilicoDocument3 pagesReporte Benzoína Bencilo Acido BencilicoAlan0% (1)
- Estandarización de Ácido Clorhídrico e Hidróxido de SodioDocument3 pagesEstandarización de Ácido Clorhídrico e Hidróxido de SodioEduar FernandezNo ratings yet
- BenzoinaDocument16 pagesBenzoinaDiego MoralesNo ratings yet
- Cristalizacion Con Carbon Activado y en Par de DisolventesDocument7 pagesCristalizacion Con Carbon Activado y en Par de Disolventes.:("*"BLacK BuLLeT"*"):.69% (16)
- Informe 1 - Benzocaina - RetrosintesisDocument10 pagesInforme 1 - Benzocaina - RetrosintesisCamilo SerranoNo ratings yet
- Síntesis de para NitroanilinaDocument2 pagesSíntesis de para NitroanilinaCristobal Cruz Cabrera100% (1)
- Acido Picrico ReporteDocument3 pagesAcido Picrico ReportePaul ValdezNo ratings yet
- Bromuro de N ButiloDocument6 pagesBromuro de N ButiloDaliaNo ratings yet
- Previo BenciloDocument6 pagesPrevio BenciloHeber Daniel Andrade Rivera100% (1)
- B NerolinaDocument3 pagesB NerolinarubenNo ratings yet
- Practica No 5 Sintesis de Cloruro de TerbutiloDocument7 pagesPractica No 5 Sintesis de Cloruro de TerbutiloanonymuusNo ratings yet
- Acido Picrico Obtencion CataDocument3 pagesAcido Picrico Obtencion CataCatalino de la MNo ratings yet
- Práctica 8 Acoplamiento de Sales de DiazonioDocument8 pagesPráctica 8 Acoplamiento de Sales de DiazonioErnesto ZavalaNo ratings yet
- Practica 5Document12 pagesPractica 5Elizabeth ChavanaNo ratings yet
- Practica #7 Reacción de Grignard Preparación de TrifenilcarbinolDocument4 pagesPractica #7 Reacción de Grignard Preparación de TrifenilcarbinolJulioNo ratings yet
- Fluoresceina y Fenolftaleina FESCDocument6 pagesFluoresceina y Fenolftaleina FESCBrenda KarenNo ratings yet
- Práctica 6. Predicciòn de La Espontaniedad de Las Reacciones RedoxDocument3 pagesPráctica 6. Predicciòn de La Espontaniedad de Las Reacciones RedoxIrving GarciaNo ratings yet
- 9.-Sustitución Electrofílica Aromática Obtención de M-Dinitrobenceno PDFDocument8 pages9.-Sustitución Electrofílica Aromática Obtención de M-Dinitrobenceno PDFRAY JETHZANo ratings yet
- Sintesis de AlquinoDocument12 pagesSintesis de AlquinoPamela AyalaNo ratings yet
- Reporte P-Nitroanilina 1.1Document12 pagesReporte P-Nitroanilina 1.1Jesus Belmont VazquezNo ratings yet
- PDF Apendice 1 Practica 1toxicologia CompressDocument4 pagesPDF Apendice 1 Practica 1toxicologia CompressCarlos Romo MartinezNo ratings yet
- Previo 1Document5 pagesPrevio 1Daniel ChavarriaNo ratings yet
- Practica No8 Reflejos en El Humano.-.Document14 pagesPractica No8 Reflejos en El Humano.-.Leion UchihaNo ratings yet
- Cuestionarios Química Orgánica.Document42 pagesCuestionarios Química Orgánica.Banks100% (2)
- Reporte #5 Ac. PícricoDocument3 pagesReporte #5 Ac. PícricoAna Karen Rodríguez ReyesNo ratings yet
- Inf 03 Destilación - V2Document7 pagesInf 03 Destilación - V2Camila Fernanda Leon HurtadoNo ratings yet
- Diagrama de Flujo Difenil CarbinolDocument2 pagesDiagrama de Flujo Difenil CarbinolAnnBukowskiNo ratings yet
- Practica 2 Identificación de Aldehídos y CetonasDocument5 pagesPractica 2 Identificación de Aldehídos y CetonasMario Edwin Martinez CoronaNo ratings yet
- Cuestionario 5Document2 pagesCuestionario 5Morteoiq8No ratings yet
- Reporte Bromuro de N-ButiloDocument4 pagesReporte Bromuro de N-ButiloEduardo Hernández HuertaNo ratings yet
- Destilacion Por ArrastreDocument7 pagesDestilacion Por ArrastreCarmen BeristainNo ratings yet
- PracticA 6 ALQUINOSDocument10 pagesPracticA 6 ALQUINOSGuadalupe Flores FuentesNo ratings yet
- Informe N°5 FicicoquimicaDocument5 pagesInforme N°5 FicicoquimicaKelly MolinaNo ratings yet
- Práctica No. 6 Nitración Del FenolDocument5 pagesPráctica No. 6 Nitración Del FenolChristian Torres ChávezNo ratings yet
- Practica 8. Transposicion Bencilica-E8Document20 pagesPractica 8. Transposicion Bencilica-E8Alexandra Marlene100% (1)
- Sesiã N 11 - UIII - Coeficiente de RepartoDocument24 pagesSesiã N 11 - UIII - Coeficiente de RepartoMiyaray LecarosNo ratings yet
- Obtencion de Cloruro de Terbutilo PDFDocument4 pagesObtencion de Cloruro de Terbutilo PDFJavier GallegoNo ratings yet
- Sintesis NerolinaDocument6 pagesSintesis NerolinaBruce WayneNo ratings yet
- Informe 6 Extracción L-L.Document20 pagesInforme 6 Extracción L-L.Maria Del CarmenNo ratings yet
- Informe 7 Extracción Ácido - BaseDocument16 pagesInforme 7 Extracción Ácido - BasePakinn ShadoowNo ratings yet
- EXTRACCIÓN Simple, Multiple y SelectivaDocument6 pagesEXTRACCIÓN Simple, Multiple y Selectiva.:("*"BLacK BuLLeT"*"):.100% (8)
- Guía de Laboratorio Practica 1 y 2Document15 pagesGuía de Laboratorio Practica 1 y 2pacopacoNo ratings yet
- Practica 2 CristalizaciónDocument7 pagesPractica 2 CristalizaciónKarla Marcela Tang VelaNo ratings yet
- Informe 8 Lipidos y JabonesDocument15 pagesInforme 8 Lipidos y JabonesAnyela Eliezer40% (5)
- Protocolo 1 SFMP (A)Document17 pagesProtocolo 1 SFMP (A)Carlos DominguezNo ratings yet
- Determinacion de CristalizacionDocument9 pagesDeterminacion de CristalizacionCristian Orozco ChavezNo ratings yet
- Guia Lab OrgII - 2013 (Sintesis)Document58 pagesGuia Lab OrgII - 2013 (Sintesis)juanxmanuelNo ratings yet
- 3.2.2CuentosFabulas Retahilas para Terapias Ludicas UNICEFDocument138 pages3.2.2CuentosFabulas Retahilas para Terapias Ludicas UNICEFMarta GutiNo ratings yet
- Cuadernillo 20 Días EditableDocument102 pagesCuadernillo 20 Días EditableSarita Pink100% (5)
- Mapa de InvestigaciónDocument1 pageMapa de InvestigaciónJoselyn KarinaNo ratings yet
- Banderín Que Os Ha Nacido HoyDocument37 pagesBanderín Que Os Ha Nacido HoyJoselyn KarinaNo ratings yet
- Ficha de Problemas de MultiplicaciónDocument3 pagesFicha de Problemas de MultiplicaciónJoselyn KarinaNo ratings yet
- Ideas y Plan de Negocios PDFDocument148 pagesIdeas y Plan de Negocios PDFjessy1831100% (1)
- Un Cuento Al Dia Antologia PDFDocument144 pagesUn Cuento Al Dia Antologia PDFSilvia Santibañez GomezNo ratings yet
- Caractersiticas Biologicas de Los Seres VivosDocument16 pagesCaractersiticas Biologicas de Los Seres VivosJoselyn KarinaNo ratings yet
- Tejido Nervioso y Enfermedades AsociadasDocument16 pagesTejido Nervioso y Enfermedades AsociadasJoselyn KarinaNo ratings yet
- El Lago AsesinoDocument1 pageEl Lago AsesinoJoselyn KarinaNo ratings yet
- Problemas de Momento de Una Fuerza para Tercer Grado de SecundariaDocument4 pagesProblemas de Momento de Una Fuerza para Tercer Grado de SecundariaJoselyn KarinaNo ratings yet
- Infografia Emprendimiento Marca CanchitaDocument1 pageInfografia Emprendimiento Marca CanchitaJoselyn Karina100% (1)
- Ficha de Practica ÓxidosDocument1 pageFicha de Practica ÓxidosJoselyn KarinaNo ratings yet
- Investigacion CañihuaDocument2 pagesInvestigacion CañihuaJoselyn KarinaNo ratings yet
- 23-2016 - EPIA-Martinez Rivas - EVALUACIÓN DE LA VISCOSIDAD Y EL COLOR DEL YOGURT BA 2016 PDFDocument102 pages23-2016 - EPIA-Martinez Rivas - EVALUACIÓN DE LA VISCOSIDAD Y EL COLOR DEL YOGURT BA 2016 PDFJoselyn KarinaNo ratings yet
- Nomenclatura Inorgánica y Estado de Oxidación para Segundo Grado de SecundariaDocument4 pagesNomenclatura Inorgánica y Estado de Oxidación para Segundo Grado de SecundariaJoselyn Karina100% (1)
- Ejercicios Movimiento MecanicoDocument21 pagesEjercicios Movimiento MecanicoJoselyn KarinaNo ratings yet
- Entrenamiento de Un Panel de Evaluacion Sensorial para El Departamento de Nutricion de La Facultad de Medicina de La Universidad de ChileDocument107 pagesEntrenamiento de Un Panel de Evaluacion Sensorial para El Departamento de Nutricion de La Facultad de Medicina de La Universidad de ChileHI LA RioNo ratings yet
- IweufchDocument9 pagesIweufchJudajoNo ratings yet
- Componentes Químicos Del MarDocument21 pagesComponentes Químicos Del MarJoselyn KarinaNo ratings yet
- Movimiento Rectilíneo Uniforme IiDocument15 pagesMovimiento Rectilíneo Uniforme IiJoselyn KarinaNo ratings yet
- Tabla Periodica Valencias ElementosDocument1 pageTabla Periodica Valencias ElementosElena Fernández SanzNo ratings yet
- Dialnet CirculacionFetal 6573030Document12 pagesDialnet CirculacionFetal 6573030Armando PaulNo ratings yet
- Dialnet NeonatologiaEquina 6001479Document7 pagesDialnet NeonatologiaEquina 6001479Isamar Lizcano100% (1)
- El AguaDocument25 pagesEl AguaJoselyn Karina0% (1)
- Covid 19 PresentaciónDocument52 pagesCovid 19 PresentaciónJoselyn Karina100% (5)
- B7e465255 Archivo Guia Estudio PDFDocument208 pagesB7e465255 Archivo Guia Estudio PDFedgarNo ratings yet
- Isla de La BasuraDocument30 pagesIsla de La BasuraMaria AngelicaNo ratings yet
- Ballena JorobadaDocument5 pagesBallena JorobadaJoselyn KarinaNo ratings yet
- TT SaenzBajañaDocument132 pagesTT SaenzBajañaYunior Andrés Castillo SilverioNo ratings yet
- Inecuaciones XDocument3 pagesInecuaciones XRamiro DominguezNo ratings yet
- Banco de Postulantes JI S 2021-2022Document5 pagesBanco de Postulantes JI S 2021-2022Daniel TipanNo ratings yet
- Planteamiento Del ProblemaDocument6 pagesPlanteamiento Del ProblemaDavid PardoNo ratings yet
- Sílabo Cátedra Integrado V Ciclo.Document32 pagesSílabo Cátedra Integrado V Ciclo.FREDY CERDANo ratings yet
- Libro 2 U1 Clasificación de Funciones RealesDocument18 pagesLibro 2 U1 Clasificación de Funciones RealesG&K FreshiesNo ratings yet
- Época IncaicaDocument7 pagesÉpoca IncaicaAngel Ccopa JuncoNo ratings yet
- Sistemas y Metodos de Regeneracion de Productos AlimenticiosDocument29 pagesSistemas y Metodos de Regeneracion de Productos AlimenticiosLeon N GabyNo ratings yet
- Paul Washer Libro Escato - 15Document13 pagesPaul Washer Libro Escato - 15Franklin Moreira100% (2)
- Sistema de Inventario de Varios PeríodosDocument23 pagesSistema de Inventario de Varios PeríodosJulieth Merino50% (2)
- Calidad Del Aire - Art.304Document2 pagesCalidad Del Aire - Art.304Luce Dávila FernandezNo ratings yet
- Curvas en V Del Generador SincronoDocument7 pagesCurvas en V Del Generador SincronoAngel Fuller100% (1)
- Tema 4Document11 pagesTema 4JOSE MOLINANo ratings yet
- 3-0-25 0710 SP 9124Document92 pages3-0-25 0710 SP 9124Jonny Ulchur MuelasNo ratings yet
- Pud 6to Unidad3 MatematicaDocument26 pagesPud 6to Unidad3 MatematicaElva DominguezNo ratings yet
- 12 PlantasDocument3 pages12 PlantasOrror Vacui100% (5)
- Monitoreo y Control Automático de Equipos IPDocument5 pagesMonitoreo y Control Automático de Equipos IPAnthony SahuanayNo ratings yet
- 01 Infotech 7 - Explorando Internet - Muestra 1Document25 pages01 Infotech 7 - Explorando Internet - Muestra 1BlankoIINo ratings yet
- Hardy CrossDocument2 pagesHardy CrossDanilo Brayan Perez CarhuamacaNo ratings yet
- LINFEDEMADocument72 pagesLINFEDEMARichard A. MejíasNo ratings yet
- Especificacion Particulares Base, Base Negra y CarpetaDocument4 pagesEspecificacion Particulares Base, Base Negra y CarpetaLorenaNo ratings yet
- 572 602LDocument49 pages572 602LIng José Carrillo VillazónNo ratings yet
- Diccionario Garifuna Martinez-2000Document60 pagesDiccionario Garifuna Martinez-2000Ellie BurkeNo ratings yet
- Auditoriaaaa Operativa Segundo Corte123Document153 pagesAuditoriaaaa Operativa Segundo Corte123anon_777889910No ratings yet
- Comunicación Serial y Paralela 1Document6 pagesComunicación Serial y Paralela 1Victor Manuel PNo ratings yet
- El PatinajeDocument2 pagesEl Patinajeerik lauraNo ratings yet
- LinfedemaDocument46 pagesLinfedemaOSCAR CARDONA PANTOJANo ratings yet
- Manejo de Toxicidades Específicas de Medicamentos OncológicosDocument135 pagesManejo de Toxicidades Específicas de Medicamentos OncológicosAmanqui Alex DerlyNo ratings yet
- Nal-2021 09 4 PonderacionesDocument20 pagesNal-2021 09 4 Ponderacionesalex rene cardonaNo ratings yet
- Semana 15 - PDF - Formato de Sílabo para El Plan de CapacitaciónDocument3 pagesSemana 15 - PDF - Formato de Sílabo para El Plan de CapacitaciónFrank SubileteNo ratings yet