Professional Documents
Culture Documents
Enzimas
Uploaded by
julietttta0 ratings0% found this document useful (0 votes)
149 views6 pagesenzimas biologia
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this Documentenzimas biologia
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
149 views6 pagesEnzimas
Uploaded by
juliettttaenzimas biologia
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 6
Enzimas
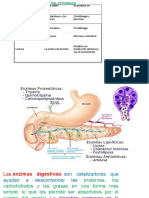
Los enzimas son los catalizadores de las reacciones en los sistemas
biolgicos: los enzimas, las protenas ms extraordinarias y de mayor
especializacin. Los enzimas tienen un gran poder cataltico, a menudo muy
superior al de los catalizadores sintticos o inorgnicos. Poseen un elevado
grado
de
especificidad
respecto
a
sus
sustratos,
aceleran
espectacularmente las reacciones qumicas especficas y funcionan en
soluciones acuosas en condiciones muy suaves de temperatura y pH. Hay
pocos catalizadores no biolgicos que tengan todas estas propiedades.
Los enzimas estn en el centro de todos los procesos bioqumicos. Actuando
en secuencias organizadas catalizan cientos de reacciones consecutivas en
las que se degradan molculas de nutrientes, se conserva y transforma la
energa qumica y se fabrican las macromolculas biolgicas a partir de
precursores sencillos.
La mayora de enzimas son protenas
Con la excepcin de un pequeo grupo de molculas de RNA cataltico,
todos los enzimas son protenas. Su actividad cataltica depende de la
integridad de su conformacin proteica nativa. Si se desnaturaliza o disocia
un enzima en sus subunidades, se suele perder la actividad cataltica. Si se
descompone una enzima en sus aminocidos constituyentes, siempre se
destruye su actividad cataltica. As, las estructuras primaria, secundaria,
terciaria y cuaternaria de las protenas enzimticas son esenciales para su
actividad cataltica.
Algunos enzimas no requieren para su actividad ms grupos qumicos que
sus residuos aminocidos. Otros requieren un componente qumico adicional
llamado cofactor. El cofactor puede ser uno o varios iones inorgnicos o una
molcula orgnica o metaloorgnica compleja denominada coenzima.
Algunos enzimas requieren tanto un coenzima como uno o ms iones
metlicos para su actividad. Un coenzima o ion metlico unido
covalentemente o de manera muy fuerte a la protena enzimtica se
denomina grupo prosttico. Un enzima completo catalticamente activo
junto con su coenzima y/o iones metlicos se denomina holoenzima. La
parte proteica de tal enzima se denomina apoenzima o apoprotena. La
mayora de ellos son derivados de las vitaminas. Finalmente, algunos
enzimas son modificados covalentemente por fosforilacin, glucosilacin y
otros procesos. Gran parte de estas alteraciones intervienen en la
regulacin de la actividad enzimtica.
Los enzimas se clasifican segn las reacciones que catalizan
Muchos enzimas se han bautizado aadiendo el sufijo asa al nombre de su
sustrato o a una palabra o frase que describe su actividad. Otros enzimas
recibieron nombres muy generales, antes de que se conociera cul era su
reaccin especfica. Otros recibieron el nombre en virtud de su origen o el
modo como se obtuvieron. A veces el mismo enzima tiene dos o ms
nombres, o dos enzimas diferentes tienen el mismo nombre. Debido a tales
ambigedades y al nmero constantemente creciente de enzimas
descubiertos, se ha adoptado por acuerdo internacional un sistema de
nomenclatura y clasificacin de los enzimas. Este sistema distribuye los
enzimas en seis clases principales, cada una de ellas con diferentes
subclases, segn el tipo de reaccin catalizada. A cada enzima se le asigna
un nmero clasificatorio de cuatro apartados y un nombre sistemtico que
identifica la accin catalizada.
La vida depende de la existencia de catalizadores poderosos y especficos:
los enzimas. Prcticamente todas las reacciones bioqumicas son catalizadas
por un enzima.
Con la excepcin de unas pocas molculas de RNA cataltico, todos los
enzimas conocidos son protenas. Muchos necesitan coenzimas no proteicos
para desempear su accin cataltica.
Las enzimas se clasifican de acuerdo con el tipo de reaccin que catalizan.
Todos los enzimas tienen nmeros y nombres formales del sistema E. C. y la
mayora tienen tambin nombres sencillos.
Cmo funcionan los enzimas?
La catlisis enzimtica de las reacciones es esencial para los sistemas vivos.
En condiciones biolgicas, las reacciones no catalizadas tienden a ser
lentas. La mayora de molculas biolgicas son muy estables al pH neutro,
la temperatura sueva y el ambiente acuoso presente en el interior de las
clulas. Adems, muchas reacciones bioqumicas comunes implican
procesos qumicos que son desfavorables o poco probables en el ambiente
celular, tales como la formacin transitoria de intermediarios cargados
inestables o la colisin de dos o ms molculas con la orientacin precisa
requerida para la reaccin. Las reacciones necesarias para digerir los
alimentos, enviar seales nerviosas o contraer el msculo no se dan a una
velocidad til sin catlisis.
Un enzima soluciona estos problemas al proporcionar un ambiente
especfico dentro del cual una reaccin determinada puede transcurrir a
mayor velocidad. El rasgo distintivo de una reaccin catalizada
enzimticamente es que tiene lugar dentro de los confines de una bolsa del
enzima denominada sitio activo. La molcula fijada el sitio activo y sobre la
que acta el enzima se denomina sustrato. La superficie del sitio activo del
enzima est revestida con residuos aa cuyos grupos sustituyentes se unen
al sustrato y catalizan la transformacin qumica. A menudo, el sitio activo
cubre al sustrato y lo secuestra completamente de la solucin. El complejo
enzima-sustrato es de importancia central en la accin de los enzimas.
Los enzimas alteran las velocidades de reaccin pero no los
equilibrios
Se puede escribir una reaccin enzimtica sencilla como:
Donde E, S y P representan el enzima, el sustrato y el producto,
respectivamente. ES y EP son complejos transitorios del enzima con el
sustrato y con el producto, respectivamente.
La funcin de un catalizador es aumentar la velocidad de una reaccin. Los
catalizadores no modifican los equilibrios de reaccin. Cualquier reaccin,
por ejemplo S P, se puede describir mediante un diagrama de la
coordenada de reaccin, una descripcin de los cambios energticos
durante la reaccin. En el diagrama de la coordenada, se representa la
energa libre del sistema frente al progreso de la reaccin (coordenada de la
reaccin). El punto de partida tanto para la reaccin hacia la derecha como
hacia la izquierda se denomina estado basal, que es la contribucin a la
energa libre del sistema de una molcula promedio (S o P) bajo un conjunto
de condiciones dadas. Para describir las variaciones de energa libre de las
reacciones, los qumicos definen un conjunto estndar de condiciones y
expresan la variacin de la energa libre de este sistema reaccionante como
AG, la variacin de energa libre estndar. Dado que en los sistemas
bioqumicos participa normalmente el H+ en concentraciones muy lejanas de
1M, los bioqumicos definen la variacin de la energa libre estndar
bioqumica, AG, como la variacin de la energa libre estndar a pH 7,0
El equilibrio entre S y P refleja la diferencia en energa libre de sus estados
basales. En el ejemplo que se muestra en la grfica, la energa libre del
estado basal de P es inferior a la de S, por lo que la AG de la reaccin es
negativa y el equilibrio favorece a P. La posicin y la direccin de este
equilibrio no se ven afectadas por ningn catalizador.
Un equilibrio favorable no indica que la conversin S P sea rpida. La
velocidad de la reaccin es dependiente de un parmetro totalmente
diferente. Existe una barrera energtica entre S y P que representa la
energa requerida para el alineamiento de los grupos reactivos, la formacin
de cargas inestables transitorias, los reordenamientos de enlaces y otras
transformaciones que se requieren para que la reaccin tenga lugar en
cualquiera de las dos direcciones. Esto viene representado por la colina
energtica de las graficas. Para que haya reaccin las molculas han de
superar esta barrera, por lo que se deben llevar a un nivel energtico
superior. En la cumbre de la colina energtica existe un pinto en el que la
cada hacia el estado P o S es igualmente probable. Es lo que se denomina
estado de transicin. El estado de transicin no es una especie qumica con
estabilidad significativa, por lo que no se ha de confundir con un
intermediario de reaccin. Es, simplemente, un momento molecular fugaz.
La diferencia entre los niveles de energa del estado basal y del estado de
transicin se denomina energa de activacin AG . La velocidad de una
reaccin refleja esta energa de activacin: a una energa de activacin ms
elevada corresponde una reaccin ms lenta. Es posible disminuir la energa
de activacin aadiendo un catalizador. La catlisis aumenta las velocidades
de reaccin disminuyendo las energas de activacin. En la grafica vemos el
diagrama de la coordenada de reaccin donde se comparan las reacciones,
catalizada por enzima y sin catalizar.
Los enzimas no constituyen una excepcin a la regla de que los
catalizadores no modifican el equilibrio de reaccin. Su nica misin es
acelerar la interconversin de S y P No se gasta enzima en el proceso el
punto de equilibrio no queda afectado. No obstante, la reaccin alcanza el
equilibrio de una manera mucho ms rpida cuando se halla presente el
enzima adecuado ya que se incrementa la velocidad de la reaccin.
Cualquier reaccin puede consistir en varias etapas que suponen la
formacin y desintegracin de especies qumicas transitorias denominadas
intermediarios de reaccin. Un intermediario de reaccin es cualquier
especie producida en el transcurso de la reaccin que tenga un tiempo de
vida qumico finito. Cuando la reaccin S P est catalizada por un enzima,
los complejos ES y EP pueden ser considerados intermediarios a pesar de
que S y P sean especies qumicas estables. Cuando en una reaccin existen
varios pasos, la velocidad global viene determinada por el paso (o pasos)
cuya energa de activacin es la ms elevada, este paso se denomina
limitante de velocidad. En un caso sencillo, el paso limitante de velocidad es
el punto de energa ms elevado en el diagrama de interconversin de S y P.
Las velocidades de reaccin y los equilibrios tienen definiciones
termodinmicas precisas
Los equilibrios de reaccin estn asociados inextricablemente a la variacin
de energa libre estndar de la reaccin, mientras que las velocidades de
reaccin estn asociadas a la energa de activacin.
Un equilibrio tal como S P viene descrito por una constante de equilibrio,
Keq, o K:
De la termodinmica, puede describirse la relacin entre K eq y AG
mediante la expresin:
La velocidad de una reaccin cualquiera viene determinada por la
concentracin de reactivo (o reactivos) y por una constante de velocidad.
Unos pocos principios explican el poder cataltico y la especificidad
de los enzimas
Los enzimas son catalizadores extraordinarios. Los aumentos de velocidad
conseguidos por los enzimas son de 5 a 17 rdenes de magnitud. Los
enzimas son tambin muy especficos, discriminando fcilmente entre
sustratos con estructuras muy similares.
Las interacciones dbiles ente enzima y sustrato son ptimas en el
estado de transicin
Estudios sobre la especificidad enzimtica llevados a cabo por Fischer le
condujeron a proponer en 1894, que los enzimas eran estructuralmente
complementarios a sus sustratos, de forma que se acoplaban del mismo
modo que una llave y una cerradura. No obstante, la hiptesis de la llave y
la cerradura puede ser engaosa cuando se aplica a la catlisis enzimtica.
Un enzima totalmente complementario a su sustrato sera un enzima muy
deficiente, como podemos demostrar.
Consideremos una reaccin imaginaria, la rotura de una vara metlica
magntica. La reaccin no catalizada se muestra en la primera figura.
Examinaremos ahora dos enzimas imaginarios que pudieran catalizar esta
reaccin. Disearemos en primer lugar un enzima perfectamente
complementario al sustrato. Para que se d la reaccin, la vara debe
alcanzar el estado de transicin de la reaccin, pero se fija de una forma tan
fuerte al sitio activo que no puede doblarse, ya que la curvatura de la vara
eliminara algunas de las interacciones magnticas entre la vara y el
enzima. Un enzima as impide la reaccin ya que estabiliza el sustrato. En
un diagrama de la coordenada de la reaccin, este tipo de complejo ES
correspondera a un pozo energtico del que le sera muy difcil salir al
sustrato. Tal enzima no sera til.
La nocin moderna de la catlisis enzimtica dice: para que un enzima
catalice una reaccin ha de ser completamente complementario al estado
de transicin de la reaccin. Ello significa que las interacciones ptimas
entre sustrato y enzima solo pueden tener lugar en el estado de transicin.
La figura demuestra de qu modo puede actuar un enzima de este tipo. La
vara de metal se fija a la enzima, pero solo se usan unas cuantas
interacciones para formar el complejo ES. El sustrato ligado aun ha de
experimentar el aumento de energa libre necesario para alcanzar el estado
de transicin.
Los enzimas reales funcionan segn un principio anlogo. En el complejo ES
se forman algunas interacciones dbiles, pero el complemento total de las
interacciones dbiles posibles entre sustrato y enzima solo se forma cuando
el sustrato alcanza el estado de transicin. La energa libre liberada por la
formacin de esas interacciones equilibra parcialmente la energa requerida
para llegar a la cima de la colina energtica. La suma de la energa de
activacin desfavorable AG y la energa de fijacin AG B favorable da como
resultado una energa de activacin menor. El estado de transicin tampoco
es una especie estable en el enzima, sino que representa un punto breve en
el tiempo que pasa un sustrato en la cima de la colina energtica. Sin
embargo, la reaccin catalizada por el enzima es mucho ms rpida que el
proceso sin catalizar, porque la colina es mucho ms baja.
Los enzimas utilizan la energa de fijacin para proporcionar
especificidad de reaccin y catlisis
La especificidad se refiere a la capacidad de un enzima de discriminar entre
un sustrato y una molcula competitiva.
El propio enzima puede sufrir un cambio conformacional cuando se fija el
sustrato, el cual tambin se encuentra inducido por mltiples interacciones
dbiles con el sustrato. Esta situacin se conoce como encaje inducido,
mecanismo postulado por Daniel Koshland en 1958. El encaje inducido
puede servir para disponer grupos especficos funcionales del enzima en la
orientacin adecuada para catalizar la reaccin. El cambio conformacional
tambin permite la formacin de interacciones dbiles adicionales en el
estado de transicin.
Grupos catalticos especficos contribuyen a la catlisis
En la mayora de los enzimas, la energa de fijacin usada para formar el
complejo ES es tan solo una de las diversas contribuciones al mecanismo
cataltico general. Una vez unido el sustrato al enzima, grupos funcionales
catalticos situados adecuadamente colaboran en la rotura o formacin de
enlaces mediante una variedad de mecanismos.
Catlisis cido-base general
Muchas reacciones bioqumicas suponen la formacin de intermediarios
cargados inestables que tienden a descomponerse rpidamente en sus
especies reactivas constituyentes no pudiendo, de este modo, reaccionar. Lo
intermediarios cargados a menudo se pueden estabilizar transfiriendo
protones a o desde el sustrato o intermediario para formar una especie que
se descompone en productos ms fcilmente que en reactivos.
Varias cadenas laterales de aa pueden actuar de modo similar como
dadores y aceptores de protones en el sitio activo del enzima. Estos grupos
se suelen posicionar de forma precisa en el sitio activo de un enzima para
permitir la transferencia de protones, generando incrementos de velocidad
del orden de 102 a 105. Este tipo de catlisis tiene lugar en la mayora e
enzimas.
Catlisis covalente
En la catlisis covalente se forma un enlace covalente transitorio entre el
enzima y el sustrato. Esto altera la ruta de la reaccin y solo se produce
catlisis si la nueva ruta tiene una energa de activacin inferior a la de la
ruta no catalizada. Diversas cadenas laterales de aa, as como los grupos
funcionales de algunos cofactores enzimticos, sirven como nuclefilos en
algunos enzimas para la formacin de enlaces covalentes con los sustratos.
Catlisis por iones metlicos
You might also like
- Practica 3. Reaccion ColorimetricasDocument12 pagesPractica 3. Reaccion ColorimetricasLaydiPNo ratings yet
- Guía Trabajos Prácticos de BIOQUÍMICA 2021Document22 pagesGuía Trabajos Prácticos de BIOQUÍMICA 2021Emy CativaNo ratings yet
- Genomas de Orgánulos Procariotas y EucariotasDocument14 pagesGenomas de Orgánulos Procariotas y EucariotasjuliettttaNo ratings yet
- Ecología MicrobianaDocument9 pagesEcología MicrobianajuliettttaNo ratings yet
- Uniones CelularesDocument22 pagesUniones Celularesjulietttta100% (1)
- Tarea FOL07Document2 pagesTarea FOL07julietttta25% (4)
- Glúcidos y Su GlucobiologíaDocument3 pagesGlúcidos y Su GlucobiologíajuliettttaNo ratings yet
- Metabolismo CelularDocument17 pagesMetabolismo CelularjuliettttaNo ratings yet
- Bloque II Biología Selectividad AndalucíaDocument24 pagesBloque II Biología Selectividad Andalucíajulietttta100% (1)
- Estructura Externa Del Cromosoma EucarióticoDocument9 pagesEstructura Externa Del Cromosoma Eucarióticojulietttta50% (2)
- Operon LacDocument2 pagesOperon LacErick Luria PerezNo ratings yet
- Primer Examen Parcial Unidad IDocument2 pagesPrimer Examen Parcial Unidad Ia_preyNo ratings yet
- Free Test Qali 2o ParteDocument9 pagesFree Test Qali 2o ParteJavier Ortega MimbreroNo ratings yet
- Trabajo Colaborativo 3Document9 pagesTrabajo Colaborativo 3MtrWilliamNo ratings yet
- MembranaDocument35 pagesMembranaDaniela TelloNo ratings yet
- GLUCOLISISDocument35 pagesGLUCOLISISBelem ValenciaNo ratings yet
- Informe y Preinforme - N°3 Desnaturalización de ProteínasDocument25 pagesInforme y Preinforme - N°3 Desnaturalización de ProteínasDamaris Anabela Mogollón PortilloNo ratings yet
- Ejercicios ReplicacionDocument5 pagesEjercicios ReplicacionJimena Alvarado0% (1)
- Biomoléculas OrgánicasDocument9 pagesBiomoléculas OrgánicasDavid ReynosoNo ratings yet
- Plan Analítico Bioquimica de Alimentos 2019-2010 CiiDocument9 pagesPlan Analítico Bioquimica de Alimentos 2019-2010 CiidavidNo ratings yet
- Cuestionario Practica No.1 Seccion 1 5qm2Document43 pagesCuestionario Practica No.1 Seccion 1 5qm2IvanNo ratings yet
- Metabolismo Energético Del EritrocitoDocument5 pagesMetabolismo Energético Del EritrocitoZeTh Spektor100% (1)
- T6-Aa y ProtDocument64 pagesT6-Aa y ProtIgnacio MachadoNo ratings yet
- Bnu U3 A2Document7 pagesBnu U3 A2Marifer sanchezNo ratings yet
- Procesamiento y Presentación de AntígenosDocument16 pagesProcesamiento y Presentación de AntígenosHugoRafaelGarciaMirandaNo ratings yet
- Amplificación Aleatoria de ADN PolimórficoDocument2 pagesAmplificación Aleatoria de ADN PolimórficoNARUHODONo ratings yet
- Convenio SCHNEIDER ELECTRICDocument6 pagesConvenio SCHNEIDER ELECTRICShirley Jaimes ChungaNo ratings yet
- Esquema de Las VitaminasDocument2 pagesEsquema de Las VitaminasSuscet MenaNo ratings yet
- TERPENOSDocument42 pagesTERPENOSapi-372036491% (11)
- Purificación de La Enzima Lactato DeshidrogenasaDocument5 pagesPurificación de La Enzima Lactato DeshidrogenasaMiriam AlcaideNo ratings yet
- Diagrama de Flujo PCRDocument4 pagesDiagrama de Flujo PCRMartha Duran50% (2)
- Métodos InmunológicosDocument19 pagesMétodos Inmunológicosmariipiii100% (3)
- Introducción de VitaminasDocument10 pagesIntroducción de VitaminasAngearelis SarmientoNo ratings yet
- EscorbutoDocument4 pagesEscorbutoTonyNo ratings yet
- 6ta Práctica Dig - Intestino Delga.y GruesoDocument10 pages6ta Práctica Dig - Intestino Delga.y GruesoJonathanAparcoEslavaNo ratings yet
- Molécula ARNtDocument3 pagesMolécula ARNtLuiggiRonaldMaciasBNo ratings yet
- Informen - 8Document12 pagesInformen - 8Juan OrellanaNo ratings yet
- Estructura Del ADNDocument23 pagesEstructura Del ADNArianna ValdezNo ratings yet