Professional Documents
Culture Documents
PRÁCTICA No.3 FISICOQUIMICA AMBIENTAL
Uploaded by
IsaTovarOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
PRÁCTICA No.3 FISICOQUIMICA AMBIENTAL
Uploaded by
IsaTovarCopyright:
Available Formats
PRCTICA #3
CINTICA QUMICA
PRODUCCIN DE CO2 A PARTIR DE
CARBONATOS
1. INTRODUCCION
Velocidad de Reaccin
El objetivo de la Cintica Qumica consiste en explorar las leyes que rigen el
cambio de la composicin de un sistema en el tiempo y su relacin con las
variables que definen su estado, en particular, con la presin, la temperatura y la
composicin. La velocidad de reaccin de un sistema reactivo:
a A + b B + ... d D + e E + ...
formulada en trminos de concentraciones molares, se define como:
v = 1 a d[A] dt = 1 b d[B] dt = ... = 1 d d[D] dt = 1 e d[E] dt de dt
donde e es el grado de avance de la reaccin en trminos de la concentracin:
e V
En trminos de nmeros de moles o de presiones parciales, la expresin es
similar, reemplazando las concentraciones por estas propiedades.
Velocidad de reaccin y temperatura: ecuacin de Arrhenius
Para las reacciones elementales, la dependencia de la constante de velocidad con
la temperatura viene recogida de manera bastante razonable por la Ley de
Arrhenius:
k = A eEa/(R T)
donde A es el llamado factor preexponencial y Ea es la energa de activacin del
proceso. En la formulacin original de la ley, tanto A como Ea se toman como
constantes independientes de T y caractersticas del proceso.
2. OBJETIVOS
2.1 Verificar la cintica de la reaccin en funcin de la temperatura. Efectuar
una Reaccin Acido-base con desprendimiento de gas.
3. MATERIAL.
a) Balanza granataria.
b) Vidrios de reloj.
c) 4 globos grandes.
d) 4 matraces Erlenmeyer de 125 ml.
e) Embudo de talle corto.
f) Parrilla de calentamiento.
g) Recipiente para bao de hielo.
h) Termmetro.
5. REACTIVOS.
a) Carbonato de Sodio. Na2CO3
b) Acido Clorhdrico. HCl
c) Hielo. H2O
6. PROCEDIMIENTO.
Pesar 4 muestras, de 2 g cada una de Na2CO3, y colocarlas en 4 globos grandes
distintos, mediante la ayuda del embudo.
Colocar 10 ml de HCl 3M en cada uno de 4 matraces Erlenmeyer de 125 ml.
(Etiquetar los matraces del 1 al 4).
Enfriar al matraz 1 a 0 C, y al 2 a 15 C en el bao de hielo; llevar el 3 a 30 C y
calentar el 4 a 60 C en la parrilla usando bao mara.
Cuando todos los matraces estn a la temperatura especificada, colocar los
globos (conteniendo la sal) en la boca de cada matraz y, a un mismo instante,
vaciar el contenido de los mismos a los matraces.
Observar y anotar conclusiones.
REACCIONES.
2 H+ (aq) + CO3(aq) CO2 (g) + H2O (l)
COMENTARIOS Y SUGERENCIAS.
1. Se sugiere precisin en cuanto a temperaturas y cantidades especificadas para
el experimento, pues la cintica vara con estos factores.
2. De la misma forma, sera interesante realizar un experimento, variando las
concentraciones de HCl utilizado (3 M, 4 M, 5M, etc.) a la misma temperatura y ver
los efectos cualitativos y cuantitativos de la concentracin en las velocidades de
reaccin.
3. Asegurarse de que los globos estn perfectamente atados a los matraces;
adems de que sean lo suficientemente grandes para soportar la presin y la
cantidad del gas liberado.
7. ACTIVIDADES Y PREGUNTAS.
7.1 Que grfica representa la dependencia de la constante de velocidad con
respecto a la temperatura, explicar dicha grfica?
7.2 Que ocurre con la velocidad de reaccin al variar la concentracin y la
temperatura?
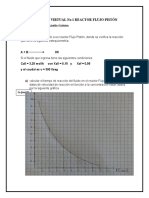
7.3 Cual es el valor de la energa de activacin para una reaccin si la
constante de velocidad se duplica cuando la temperatura aumenta de 15 a
25 C? Sabemos que k2 (298 K) = 2 x k1 (288 K).
7.4 Cmo podra disearse un estudio cuantitativo de este experimento
mediante el uso de la Ecuacin de Arrhenius en cintica qumica?
7.5 De forma grfica analizar lo ocurrido al variar la temperatura y la
concentracin durante la prctica, explicar lo observado en el experimento.
Comprobar si se cumple o no lo expresado en la ecuacin de Arrhenius.
10. RECUPERACIN, DESACTIVACIN Y/O ALMACENAMIENTO TEMPORAL
DE LOS RESIDUOS QUMICOS
10.1 ALMACENAMIENTO TEMPORAL
Los residuos generados durante la practica deben almacenarse en el recipiente
para cidos y bases.
11. BIBLIOGRAFA
11.1 GLASTONE,S. Tratado de qumica fsica. Editorial Aguilar S.A
11.2 LEVINE,I. Fisicoqumica, Volumen 1, Quinta Edicin, McGrawHill/Interamericana de Espaa, S.A.U., Madrid, 2004.
11.3 ATKINS,P.W. Fisicoqumica, Tercera Edicin, Addison Wesley.
Iberoamericana, Wilmington, Delaware, E.U.A. 1991
12. AUTORES.
Paola Arango Romero
Departamento de Ingeniera Ambiental
Universidad Autnoma del Cauca
You might also like
- Ejercicios Resueltos Reactor Tanque Agitado Continuo (RTAC)Document5 pagesEjercicios Resueltos Reactor Tanque Agitado Continuo (RTAC)LUYELIS RODRÍGUEZNo ratings yet
- TRABAJO FINAL ASERHI F.A.I.CDocument40 pagesTRABAJO FINAL ASERHI F.A.I.CIsaTovar100% (1)
- Programa de Control de PlagasDocument5 pagesPrograma de Control de PlagasIsaTovarNo ratings yet
- Actividades Unidad 3Document40 pagesActividades Unidad 3IsaTovarNo ratings yet
- Cinética Química Producción de Co2 A Partir de CarbonatosDocument5 pagesCinética Química Producción de Co2 A Partir de CarbonatosIsaTovarNo ratings yet
- HidrocraqueoDocument13 pagesHidrocraqueoAlvaroManriqueAliagaNo ratings yet
- Laboratorio de Perdisulfato Arriba PerúDocument5 pagesLaboratorio de Perdisulfato Arriba Perújhony deyvi carmona casimiroNo ratings yet
- Trabajo Practico Cinética QuímicaDocument3 pagesTrabajo Practico Cinética QuímicaGerman JuarezNo ratings yet
- PolimerizacionDocument1 pagePolimerizacionTihara LorenzoNo ratings yet
- Balances de Materia Con Reacción QuímicaDocument27 pagesBalances de Materia Con Reacción QuímicaJoel Salomón Pareja RomeroNo ratings yet
- RedoxDocument6 pagesRedoxYonnySainzNo ratings yet
- Capitulo 4 - Equilibrio QuimicoDocument34 pagesCapitulo 4 - Equilibrio QuimicoMaria Paula BuitragoNo ratings yet
- Bioquimica 37 Enzimología y Bioenergética Jessica OrozcoDocument3 pagesBioquimica 37 Enzimología y Bioenergética Jessica OrozcoJessica OrozcoNo ratings yet
- Activada de La Enzima Catalasa en Diversos TejidosDocument4 pagesActivada de La Enzima Catalasa en Diversos TejidosMilena Paulette Valarezo AlvarezNo ratings yet
- Efectos de La TemperaturaDocument11 pagesEfectos de La TemperaturaSinaí VictoriaNo ratings yet
- Actividad 4 QuimicaDocument5 pagesActividad 4 QuimicaOskarina PerezNo ratings yet
- Quimica EjerciciosDocument6 pagesQuimica EjerciciosAlanx YepezNo ratings yet
- Catalisis Apunte 1Document25 pagesCatalisis Apunte 1Julieta MengarelliNo ratings yet
- PRÁCTICO VIRTUAL No 1 REACTOR FLUJO PISTÓNDocument6 pagesPRÁCTICO VIRTUAL No 1 REACTOR FLUJO PISTÓNEnzo Muñoz EstradaNo ratings yet
- Determinación Del Orden de Reacción de La Nitrosación de La DimetilureaDocument4 pagesDeterminación Del Orden de Reacción de La Nitrosación de La DimetilureaJessyk MaciasNo ratings yet
- Arch Doc5295327Document6 pagesArch Doc5295327LORENA AGUIRRE LONDONONo ratings yet
- Marco Teorico y ObjetivosDocument3 pagesMarco Teorico y ObjetivosDarla Monserar Santin VidalNo ratings yet
- Velocidad de ReacciónDocument30 pagesVelocidad de ReacciónRicardo Bermeo MolinaNo ratings yet
- EstequiometriaDocument26 pagesEstequiometriaJeff NavarroNo ratings yet
- Capítulo 11 Reacciones de AlcoholesDocument28 pagesCapítulo 11 Reacciones de AlcoholesMariaNo ratings yet
- P13 - BioquimicaDocument4 pagesP13 - BioquimicaAna RojasNo ratings yet
- EncimasDocument30 pagesEncimasRichy Q-CcNo ratings yet
- Condensación de ClaisenDocument5 pagesCondensación de ClaisenAlberto Antonio Alvarez AlvaradoNo ratings yet
- Balance de Materia Con Reacción Quimica Sem 7Document35 pagesBalance de Materia Con Reacción Quimica Sem 7Hernán Cambillo CabezasNo ratings yet
- Introducción A La Catalisis - ST PDFDocument33 pagesIntroducción A La Catalisis - ST PDFbrillidNo ratings yet
- PDF Ecuacion de ArrheniusDocument88 pagesPDF Ecuacion de ArrheniusANGELA BRISETH ESPINOZA CAJASNo ratings yet
- 3 Unidad. Balance EcuacionesDocument3 pages3 Unidad. Balance EcuacionesGuillermo Carrera SolarNo ratings yet
- Informe de Fisico Quimica Cinetica Figmm UniDocument24 pagesInforme de Fisico Quimica Cinetica Figmm UniLuis Angel Paz SalazarNo ratings yet
- 11 RendimientosDocument7 pages11 RendimientosLalix Lee50% (2)