Professional Documents
Culture Documents
Color de La Llama
Uploaded by
NåThý InOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Color de La Llama
Uploaded by
NåThý InCopyright:
Available Formats
ENSAYO A LA LLAMA
Fundamento terico
El anlisis espectroscpico indica que cuando se descompone la luz que
emite un slido incandescente, mediante un prisma, se obtiene un espectro
continuo en la que estn representados todos los colores de la luz visible en
forma de bandas, es decir, el violeta sumergido en l, este a su vez en el
verde y as sucesivamente, mientras que la luz que emite loa gases o
vapores incandescente al ser sometidos a un prisma este emite un espectro
discontinuo, constituido por lneas aisladas que son caractersticas para el
elemento, hecho que permite identificarlo.
La explicacin de estas lneas caractersticas se puede explicar acudiendo a
uno de los principios de Niels Bohr. Al excitar a un tomo mediante energa
calorfica, sus electrones de nivel interior ascienden a un nivel, inmediato
superior.
Como el estado excitado es fugaz, los electrones desplazados vuelven
nuevamente a sus niveles originales, a la vez emiten la misma cantidad de
energa absorbida en forma de onda luminosa. Los espectros de muchos
tomos en el anlisis cuantitativo corriente se descubren con el
espectroscopio ordinario y con la llama del mechero Bunsen. Los espectros
obtenidos son muy simples y fciles de distinguir; de ah el gran inters que
ofrece el estudio de las lneas espectrales.
OBJETIVOS
Reconocer en la muestra problemas la presencia de algunos metales
alcalinos o alcalinotrreos por medio de sus coloraciones caractersticas a la
llama.
MATERIALES
Muestra de problemas (sales cloruro)
Un tubo de ensayo con tapn de jebe conteniendo HCI concentrado
Una gradilla con tubo de ensayo
Un mechero Bunsen
Varilla de vidrio con alambre de Nicron
PROCEDIMIENTO EXPERIMENTALES
1. Quitamos la impureza del alambre de nicron sumergiendo el alambre
en el tubo de ensayo que contiene en HCl concentrada y llevamos a
la zona de mayor temperatura de la llama del mechero Bunsen y si la
llama colorea es que existen impurezas. Repetimos la operacin hasta
que no se produzca coloracin alguna.
2. Una vez limpia el alambre de nicron sumergimos en el tubo de ensayo
en el cual se encuentra la muestra problema a que vamos a analizar.
Luego acercamos la varilla al mechero Bunsen y calentndolo hasta
que aparezca la coloracin. Anotamos sus resultados.
Cloruro de cobre CuCl2
color: azul-verde intenso
Cloruro de sodio NaCl
Cloruro de litio LiCl
Cloruro de estroncio SrCl
color: amarillo intenso
color: amarillo
color: rojo intenso
Cloruro de bario BaCl2
color : verde claro
Cloruro de potasio KCl
color:violeta
Cloruro de calcio CaCl2
color: rojo- anaranjado
3. Repetimos los pasos anteriores para cada una de las soluciones
problemas que encontramos en nuestra mesa de trabajo.
CUESTIONARIO:
1. Cmo explicas la coloracin de las llamas en presencia de las
sales utilizadas?
Origen de los colores:
El color es un fenmeno fsico de la luz o de la visin, asociado con las
diferentes longitudes de onda en la zona visible del espectro
electromagntico. La percepcin del color es un proceso neurofisiolgico
muy complejo.
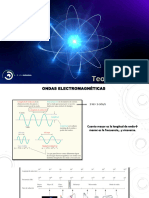
La luz visible est formada por vibraciones electromagnticas cuyas
longitudes de onda van de unos 350 a unos 750 nanmetros
(milmillonsimas de metro). La luz con longitud de onda de 750 nanmetros
se percibe como roja, y la luz con la longitud de onda de 350 nanmetros se
percibe como violeta. Las luces de longitudes de onda intermedias se
perciben como azul, verde, amarilla o anaranjada.
Todos los objetos tienen la propiedad de absorber y reflejar o emitir ciertas
radiaciones electromagnticas. La mayora de los colores que
experimentamos normalmente son mezclas de longitudes de onda y reflejan
o emiten las dems; estas longitudes de onda reflejadas o emitidas son las
que producen sensacin de color.
Los distintos colores de luz tienen en comn el ser radiaciones
electromagnticas que se desplazan con la misma velocidad,
aproximadamente, 300.000 kilmetros por segundo (velocidad de la luz). Se
diferencian en su frecuencia y longitud de onda:
Frecuencia = Velocidad de la Luz/Longitud de onda, o lo que es lo mismo
v=c/
Dos rayos de luz con la misma longitud de onda () tienen la misma
frecuencia y el mismo color.
Origen de los colores en la llama del mechero
Los tomos y los iones estn constituidos en su interior, por una parte
central muy densa, cargada positivamente, denominada ncleo y por
partculas negativas llamadas electrones, los cuales rodean al ncleo a
distancias relativamente grandes. De acuerdo a la teora cuntica, estos
electrones ocupan un cierto nmero de niveles de energa discreta. Resulta
evidente, por lo tanto, creer que la transicin de un electrn de un nivel a
otro debe venir acompaada por la emisin o absorcin de una cantidad de
energa discreta, cuya magnitud depender de la energa de cada uno de los
niveles entre los cuales ocurre la transicin y, consecuentemente, de la
carga nuclear y del nmero de electrones involucrados. Si en un tomo poli
electrnico, un electrn salta de un nivel de energa E1 a un nivel de energa
E2, la energa de la transicin electrnica, E, es igual a E2 E1. Si E2
representa un nivel de energa inferior a E1, entonces, la transicin viene
acompaada por la emisin de una cantidad E de energa (en forma de
luz), la cual est relacionada con la longitud de onda de luz emitida por la
ecuacin:
E = (hc)/
donde :
h = Constante de Planck
c = Velocidad de la Luz
= Longitud de Onda de la Luz Emitida
E = hv
En otras palabras, la energa de una transicin electrnica es inversamente
proporcional a la longitud de onda de la luz emitida o absorbida y
directamente proporcional a la frecuencia de radiacin. Un espectro atmico
est compuesto por una o ms longitudes de onda. Debido a que los
elementos tienen diferente carga nuclear, diferente tamao y diferente
nmero de electrones, es razonable concluir que cada elemento est
caracterizado por un espectro atmico, el cual es diferente al de cualquier
otro elemento.
El espectro a la llama de los compuestos de los metales alcalinos es un
espectro atmico de emisin y se representan como lneas espectrales
discretas.
ENSAYOS A LA LLAMA
Los vapores de ciertos elementos imparten un color caracterstico a la
llama. Esta propiedad es usada en la identificacin de varios elementos
metlicos como sodio, calcio, etc.. La coloracin en la llama es causada por
un cambio en los niveles de energa de algunos electrones de los tomos de
los elementos. Para un elemento particular la coloracin de la llama es
siempre la misma, independientemente de si el elemento se encuentra en
estado libre o combinado con otros.
2. Qu es un cuanto?
Es el comportamiento fundamental de la materia a escala molecular. Una
aplicacin de la qumica cuntica es el estudio del comportamiento
de tomos y molculas, en cuanto a sus
propiedades pticas, elctricas, magnticas y mecnicas, y tambin
su reactividad qumica, sus propiedades, pero tambin se estudian
materiales, tanto slidos extendidos como superficies.
-Tabla del cuanto
Nmeros
cunticos
principal
(n)
Significado fsico
Energa total del electrn (nivel energtico en
que se encuentra el electrn)
Distancia del electrn al ncleo.
Valores
permitidos
1, 2, 3....
Subnivel energtico en donde est el electrn,
dentro del nivel determinado por n.
secundario
o azimutal
(l)
Forma del orbital:
l = 0: orbital s (esfrico)
l = 1: orbital p (bilobulado)
(un orbital p en la direccin de cada eje
coordenado: px, py, pz)
0, 1, 2, ..., n-1
l = 2: orbital d
magntico
(m)
Orientacin del orbital cuando se aplica un
campo magntico externo.
-l, ..., 0, ..., + l
espn (s)
Sentido de giro del electrn en torno a su
propio eje.
1/2
As, cada conjunto de cuatro nmeros cunticos caracteriza a un electrn:
ndetermina el nivel energtico
l determina el subnivel energtico
m determina el orbital concreto dentro de ese subnivel
sdetermina el electrn concreto dentro de los que pueden alojarse en
cada orbital
(puede haber dos electrones en cada orbital).
Esto se refleja en el Principio de exclusin de Pauli (1925): en un tomo no
puede haber dos electrones que tengan los cuatro nmeros cunticos
iguales, al menos se tendrn que diferenciar en uno de
3. Completa el cuadro:
SAL UTILIZADA
ELEMENTO
COLOR DE LA LLAMA
Cloruro de cobre CuCl2
cobre
Azul-verde intenso
Cloruro de sodio NaCl
sodio
Amarillo intenso
Cloruro de litio LiCl
litio
rojo
Cloruro de estroncio
SrCl2
estroncio
Rojo intenso
Cloruro de bario BaCl2
bario
Verde claro
Cloruro de potasio KCl
potasio
Violeta
Cloruro de calcio CaCl2
calcio
Rojo-anaranjado
You might also like
- Manual Guia Completo Quimica Analitica GeneralDocument24 pagesManual Guia Completo Quimica Analitica GeneralNatalia Arias EspinozaNo ratings yet
- 1 LaboratorioDocument15 pages1 LaboratorioJunior YupanquiNo ratings yet
- Practica 3 EFECTO FOTOELECTRICO Y RAYOS CATODICOSDocument7 pagesPractica 3 EFECTO FOTOELECTRICO Y RAYOS CATODICOSCruz Aulis AldoNo ratings yet
- Modelo Atómico ActualDocument77 pagesModelo Atómico ActualNeyibe Neried Gutierrez HerradaNo ratings yet
- Cap. 6. Estructura Electrónica Átomos. Química I. UTNDocument78 pagesCap. 6. Estructura Electrónica Átomos. Química I. UTNJavierNo ratings yet
- ESPECTROS y COLORES DE LAS LLAMAS 2012Document5 pagesESPECTROS y COLORES DE LAS LLAMAS 2012Juan MuscarelliNo ratings yet
- Modelo atómico actual y números cuánticosDocument4 pagesModelo atómico actual y números cuánticosSamuel SuarezNo ratings yet
- Dualidad Onda-Partículas, U3.Document17 pagesDualidad Onda-Partículas, U3.RAUL SEBASTIAN NEAVEZ DEL BOSQUENo ratings yet
- Ensayos A La LlamaDocument9 pagesEnsayos A La LlamaMisael diaz diazNo ratings yet
- Análisis Químicos Por Vía SecaDocument5 pagesAnálisis Químicos Por Vía SecaGabriel Banegas MercadoNo ratings yet
- s3 Reportedelaboratorio Colorimetriaalallama Grupo5 SosaDocument11 pagess3 Reportedelaboratorio Colorimetriaalallama Grupo5 SosaBrayan Jonathan Sosa SernaqueNo ratings yet
- Espectro luz ondas frecuenciasDocument3 pagesEspectro luz ondas frecuenciasAmy Michelle Chavez100% (1)
- Modelos atómicos y números cuánticosDocument63 pagesModelos atómicos y números cuánticosMartin SeljakNo ratings yet
- 3-Teoría Cuántica-VfinalDocument48 pages3-Teoría Cuántica-VfinaljuanixgenoNo ratings yet
- Teoría Cuántica y La Estructura Electrónica de Los ÁtomosDocument14 pagesTeoría Cuántica y La Estructura Electrónica de Los ÁtomosNayrobi AcostaNo ratings yet
- Clases QM1121 Unidad 4Document23 pagesClases QM1121 Unidad 4jubitzaNo ratings yet
- El EspectroDocument11 pagesEl EspectroArely GómezNo ratings yet
- Configuracion Electronica y Espectro de Los ElementosDocument9 pagesConfiguracion Electronica y Espectro de Los ElementosAlan Machaca ArocutipaNo ratings yet
- Mecanica CuanticaDocument13 pagesMecanica CuanticaYoSoyChinoNo ratings yet
- Colorimetría A La LlamaDocument10 pagesColorimetría A La LlamaRichard Nunez PinedoNo ratings yet
- Física Cuántica Principio Icertidumbre 1Document33 pagesFísica Cuántica Principio Icertidumbre 1Dick RodriguezNo ratings yet
- Qué Es El Espectro de EmisiónDocument2 pagesQué Es El Espectro de EmisióngaregraunNo ratings yet
- EspectrofotometríaDocument25 pagesEspectrofotometríaARELY GARC�A PONCENo ratings yet
- Tema 4. Quimica I - 2018Document28 pagesTema 4. Quimica I - 2018Alex TorresNo ratings yet
- Resumen Estructura Atómica y Tabla PeriódicaDocument10 pagesResumen Estructura Atómica y Tabla PeriódicaAndrea MolinaNo ratings yet
- Resumen EstructuraDocument2 pagesResumen EstructurateresacamposcalvoNo ratings yet
- Tarea de Quimica Unidad 1 GRUPO 13Document32 pagesTarea de Quimica Unidad 1 GRUPO 13Jean Piero Mauricio HURTADO DIAZNo ratings yet
- QUIMICADocument15 pagesQUIMICAJhonatan Reyes InfantesNo ratings yet
- Quimica (Temas 5-6)Document9 pagesQuimica (Temas 5-6)mgc00191No ratings yet
- Modelo Mecano CuanticoDocument46 pagesModelo Mecano CuanticoVíctor Cárcamo Echeverría100% (2)
- Transiciones ElectrónicasDocument6 pagesTransiciones ElectrónicasMartha Ayala Samillán67% (3)
- Química Inorgánica: Estructura AtómicaDocument40 pagesQuímica Inorgánica: Estructura AtómicaPilar MendozaNo ratings yet
- Fisica Atomica Presentacion FisicaDocument10 pagesFisica Atomica Presentacion FisicaJose Luis Bolivar CristoforiNo ratings yet
- Cap. 6. Estructura Electrónica ÁtomosDocument54 pagesCap. 6. Estructura Electrónica ÁtomosMarcia JaraNo ratings yet
- Base Experimental de La Teoría CuanticaDocument5 pagesBase Experimental de La Teoría CuanticaBrenda Liz Ramos100% (1)
- Apuntes Quimica Unidad 1 Electromecanica-MecatronicaDocument19 pagesApuntes Quimica Unidad 1 Electromecanica-MecatronicaKaren Alexandra Ruíz SánchezNo ratings yet
- Química General T7-14Document49 pagesQuímica General T7-14Ilian GilNo ratings yet
- Módulo V - Estructura Electrónica y Propiedades Periódicas 2019Document27 pagesMódulo V - Estructura Electrónica y Propiedades Periódicas 2019LeonelTrapaniNo ratings yet
- Espectros ÓpticosDocument18 pagesEspectros Ópticosmau365100% (1)
- Espectro de AbsorciónDocument9 pagesEspectro de Absorción.:("*"BLacK BuLLeT"*"):.90% (20)
- Base Experimental de La Teoría CuanticaDocument6 pagesBase Experimental de La Teoría CuanticaKarina OsorioNo ratings yet
- Apuntes de Estructura Atómica. Tercera ParteDocument17 pagesApuntes de Estructura Atómica. Tercera ParteBrandon PaichoNo ratings yet
- Espectros atómicos y radiación electromagnéticaDocument11 pagesEspectros atómicos y radiación electromagnéticaRubenNo ratings yet
- La Naturaleza Ondulatoria de La LuzDocument15 pagesLa Naturaleza Ondulatoria de La LuzJuan RamírezNo ratings yet
- EspectrometriaDocument61 pagesEspectrometriaDavid Rivas Macas100% (1)
- 3 Teoría CuánticaDocument29 pages3 Teoría CuánticaANTONIA JIMENEZ SANTIAGONo ratings yet
- Teoría cuántica y el modelo atómicoDocument29 pagesTeoría cuántica y el modelo atómicoDiana VillegasNo ratings yet
- Apunte QuimicaDocument62 pagesApunte QuimicacokemaxmaxNo ratings yet
- Espectros atómicos y niveles de energíaDocument30 pagesEspectros atómicos y niveles de energíaOrianaPalacioNo ratings yet
- Teoría cuántica de Max Planck y modelo atómico de BohrDocument4 pagesTeoría cuántica de Max Planck y modelo atómico de BohrDaniel CruzhNo ratings yet
- Test de Color A La LlamaDocument5 pagesTest de Color A La LlamaFreddy MoralesNo ratings yet
- Clase 8. Teorización - Naturaleza de La LuzDocument4 pagesClase 8. Teorización - Naturaleza de La Luzjhoan ortegaNo ratings yet
- Semana 2 - Teoria Cuantica y Estructura Electronica de Los Atomos 1 PDFDocument88 pagesSemana 2 - Teoria Cuantica y Estructura Electronica de Los Atomos 1 PDFJeremy SteinNo ratings yet
- Quim T6 TeoriaDocument51 pagesQuim T6 TeoriaRamiroNo ratings yet
- Informe Lab 1 QuimicaDocument22 pagesInforme Lab 1 Quimicajoel noriegaNo ratings yet
- EspectofotometríaDocument8 pagesEspectofotometríaWilliam_Oliva100% (1)
- Hectorjosecirovelasquez 2006 PDFDocument88 pagesHectorjosecirovelasquez 2006 PDFolindaNo ratings yet
- EspectrofotometriaDocument15 pagesEspectrofotometriaellinoir1892% (12)
- Caratula UnjbgDocument1 pageCaratula Unjbgale137No ratings yet
- Rases Motivadoras de La VidaDocument15 pagesRases Motivadoras de La VidaNåThý InNo ratings yet
- Adolescentes Hasta Los 40toDocument2 pagesAdolescentes Hasta Los 40toNåThý InNo ratings yet
- LacteosDocument3 pagesLacteosNåThý InNo ratings yet
- Informe Nº09 TacnaDocument2 pagesInforme Nº09 TacnaNåThý InNo ratings yet
- 3er Informe de LaboratorioDocument63 pages3er Informe de LaboratorioNåThý InNo ratings yet
- Objetivo: Procedimiento Lavado Y Desinfeccion de Vajilla, Cuberteria Y UtensiliosDocument1 pageObjetivo: Procedimiento Lavado Y Desinfeccion de Vajilla, Cuberteria Y UtensiliosNåThý InNo ratings yet
- Caratula UnjbgDocument1 pageCaratula Unjbgale137No ratings yet
- CARTA para Colegio de IngenierosDocument2 pagesCARTA para Colegio de IngenierosNåThý InNo ratings yet
- Nancy Hidalgo PeruDocument34 pagesNancy Hidalgo PeruNåThý InNo ratings yet
- Alimentostransgenicos 100812200901 Phpapp01Document5 pagesAlimentostransgenicos 100812200901 Phpapp01Dannia Gomez SaavedraNo ratings yet
- Nancy Hidalgo PeruDocument34 pagesNancy Hidalgo PeruNåThý InNo ratings yet
- El Boson de HiggsDocument1 pageEl Boson de HiggsNåThý InNo ratings yet
- 5TO AÑO - RAZ - MAT - GUIA Nº2 - Planteo de Ecuaciones IIDocument7 pages5TO AÑO - RAZ - MAT - GUIA Nº2 - Planteo de Ecuaciones IILeonardoctavioNo ratings yet
- Perú, crisol de razas: mestizos, amerindios y blancosDocument2 pagesPerú, crisol de razas: mestizos, amerindios y blancosNåThý InNo ratings yet
- Mestizos y Criollos en El Perc3ba Colonial Nc2ba 72Document44 pagesMestizos y Criollos en El Perc3ba Colonial Nc2ba 72NåThý InNo ratings yet
- 5TO AÑO - RAZ - MAT - GUIA Nº3 - EdadesDocument7 pages5TO AÑO - RAZ - MAT - GUIA Nº3 - EdadesLeonardoctavioNo ratings yet
- 5TO AÑO - RAZ - MAT - GUIA Nº3 - EdadesDocument7 pages5TO AÑO - RAZ - MAT - GUIA Nº3 - EdadesLeonardoctavioNo ratings yet
- Adquisición de bujes para transformadoresDocument11 pagesAdquisición de bujes para transformadoresjoan75No ratings yet
- Manual Cojines HolmatroDocument7 pagesManual Cojines HolmatroIván PérezNo ratings yet
- Ensayo PSU Biología 2018Document44 pagesEnsayo PSU Biología 2018Bernardita Gabriela Arqueros ArnelloNo ratings yet
- Efecto fotoeléctrico y sus aplicacionesDocument3 pagesEfecto fotoeléctrico y sus aplicacionesAlejandra EspinosaNo ratings yet
- Fundicion de MetalesDocument22 pagesFundicion de MetalesINGEMECMENDEZNo ratings yet
- Ondas estacionarias en tubosDocument4 pagesOndas estacionarias en tubosyefferon0% (1)
- FORMALDEHÍDODocument8 pagesFORMALDEHÍDOEduardo SalinasNo ratings yet
- Bomba LinconlDocument11 pagesBomba Linconlolaff jardinez morenoNo ratings yet
- Funcionamiento de Maquinas Electricas Rotativas2Document27 pagesFuncionamiento de Maquinas Electricas Rotativas2671224No ratings yet
- Iniciación a Arduino: Guía Completa para PrincipiantesDocument10 pagesIniciación a Arduino: Guía Completa para Principiantessonia veigaNo ratings yet
- Clave de Respuestas Trimestral Sexto Grado Bloque3 2018-2019Document18 pagesClave de Respuestas Trimestral Sexto Grado Bloque3 2018-2019Rrb Resber100% (1)
- Mecanica de Materiales 2ed Gere TimoshenkoDocument835 pagesMecanica de Materiales 2ed Gere TimoshenkoMateo Sandoval100% (5)
- Catalogo Champion BujiasDocument40 pagesCatalogo Champion BujiasRichard79% (19)
- Proceso de HalogenaciónDocument12 pagesProceso de HalogenaciónZoe D'LarreguiNo ratings yet
- Manual Opus Ole 2 0Document71 pagesManual Opus Ole 2 0navimonteNo ratings yet
- Horno Hoffman - Tesis BogotaDocument111 pagesHorno Hoffman - Tesis BogotaguillocivilNo ratings yet
- Taller 1Document5 pagesTaller 1RONI MAURICIO JAYA CAMACHONo ratings yet
- EGT: Medición de la temperatura de los gases de escape en motores de turbinaDocument4 pagesEGT: Medición de la temperatura de los gases de escape en motores de turbinaSuker RodríguezNo ratings yet
- PreguntasDocument5 pagesPreguntasFernando LeyvaNo ratings yet
- Osciladores de Onda Senoidal-1Document20 pagesOsciladores de Onda Senoidal-1Haideliz GarcíaNo ratings yet
- Uso del óxido de cerio dopado con praseodimio en SOFCDocument5 pagesUso del óxido de cerio dopado con praseodimio en SOFCManuelGarcíaNo ratings yet
- Filtrado APIDocument2 pagesFiltrado APICristhian Ayma100% (1)
- Dinámica. Teoría y Problemas ResueltosDocument6 pagesDinámica. Teoría y Problemas ResueltosjmarfilaNo ratings yet
- Instalación de Equipos de Aire AcondicionadoDocument2 pagesInstalación de Equipos de Aire AcondicionadoHugo Romero100% (1)
- Elec1. Bases de La ElectrotecniaDocument20 pagesElec1. Bases de La ElectrotecniaJoseElHerreroNo ratings yet
- Historia de La Mineralogía y La CristalografíaDocument11 pagesHistoria de La Mineralogía y La CristalografíaEdrsonGabrielPerezNo ratings yet
- Minería Jesús de NazaretDocument172 pagesMinería Jesús de NazaretMax Yuri Champi HermozaNo ratings yet
- DX3 Manual Del Usuario-1Document270 pagesDX3 Manual Del Usuario-1Marco Antonio Leon Chavez82% (11)
- Prestige APS45HJ Manual de UsuarioDocument16 pagesPrestige APS45HJ Manual de Usuarioautoperi2010100% (5)
- PracticaDocument11 pagesPracticaEmmanuel PugaNo ratings yet