Professional Documents
Culture Documents
QI-10F-55 (TP - Ácidos y Bases) EA - C1
Uploaded by
David Alva AlbaOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
QI-10F-55 (TP - Ácidos y Bases) EA - C1
Uploaded by
David Alva AlbaCopyright:
Available Formats
ACADEMIA PRE UNIVERSITARIA KEPLER
QUMICA
RAZ. MATEMTICO
CIDOS Y BASES
KOH( ac )
K (OH)
Base
monohidroxilica
1. GENERALIDADES DE LOS CIDOS Y BASES
H 2 O H OH
cidos
1. Presentan sabor agrio
2. Cambian de color a los pigmentos orgnicos
3. Reaccionan con metales activos liberando
Sus tancia
anfotera
Es aquella que puede
comportarse como
cido o base
hidrgeno: Zn HCl ZnCl 2 H 2
4. Reaccionan con carbonatos y bicarbonatos
liberando CO 2
CaCO 3 HCl CaCl 2 H 2 O CO 2
NaHCO 3 HCl NaCl H 2 O CO 2
5. Sus
soluciones
acuosas
conducen
la
electricidad
6. Su accin es neutralizada por las bases
7. Al medir experimentalmente con un pHimetro
arroja: pH < 7
Segn Bronsted Lowry:
Bases
1. Presentan sabor amargo
2. Cambian de color a los pigmentos orgnicos
3. Al tacto se sienten resbalosas o jabonosas
4. No dan reaccin con los carbonatos y
bicarbonatos
5. Sus
soluciones
acuosas
conducen
la
electricidad
6. Su accin es neutralizada por los cidos
7. Al medir experimentalmente con un pHimetro
arroja: pH > 7
2. TEORAS CIDOS BASES
Fueron 3 los hombres
caractersticas:
Teora
Svante
Arrhenius
(1884)
Bronsted
y Lowry
(1923)
Gilbert
Newton
Lewis
(1932)
que
dieron
hidrgeno H
Sustancia que en
una
reaccin
qumica dona 1
protn
Sustancia que en
una
reaccin
qumica acepta 1
par
de
e
(electrofilico)
OH
Sustancia que en una
reaccin
qumica
acepta 1 protn
Sustancia que en una
reaccin qumica dona
1
par
de
e
(nucleoflico)
Segn Arrhenius:
-
H 2 SO 4( ac ) SO 2
4 2
H
2 protones
cido diprtico
Base cido cido Base
conjugada
conjugado
Para conjugarlo:
NH 3
NH
4 ;
H2O
HCN H2O CN H3O
cido Base Base cido
conjugado conjugado
Por conjugado: HCN y CN ; H 2 O y H3O
Observacin:
- Toda reaccin Bronsted Lowry es reversible y
el conjugado siempre tiene carcter y fuerza
diferente al reactante respectivo.
- Sustancia anfiprtica: Es aquella que se
comporta como cido o base de Bronsted
Lowry segn las circunstancias.
- Todo cido de Arrhenius es un cido de
Bronsted - Lowry
Ejemplo:
Anfiprtic
o
Av. Daniel Carrin N 585 Urb Albrecht Trujillo
Telfono: 293705
cido
Conjugado
Base
Conjugado
WWW.academiakepler.com
QI-10F-55
OH
dichas
cido
Base
En solucin acuosa En solucin acuosa
libera
iones, libera iones hidrxilo
NH3 H2O NH4 OH
ACADEMIA PRE UNIVERSITARIA KEPLER
QUMICA
H 2O
H 3O
OH
NH 3
NH
4
NH
2
HSO
4
H 2 SO 4
SO 2
4
HPO 2
4
H 2PO
4
PO 3
4
RAZ. MATEMTICO
4. DETERMINACIN
ACIDEZ
I IA VIIA VA IA
Sustancias con
enlace doble
O=C=O
Iones
1 ;
Fe 3 ; Ag
Cd 2 ; H1
HClO 4 ,
fuerte:
HBr,
HCl,
Bases fuertes: bases alcalinas, NaOH, KOH,
Todas las sales inorgnicas u orgnicas, son
Ba OH 2 , etc.
electrolitos:
KNO 3 , Fe 2 SO 4 3 , etc
KClO 4 ,
NaCl,
Observacin: Los electrolitos fuertes no
presentan reacciones reversibles o en todo
caso, su Keq es muy grande.
2. Electrolito Dbil: Es toda sustancia que en el
agua se disocia lentamente y en un porcentaje
menor del 100%
Ejemplo:
Base
NH 3 ;
H2O
cidos
CH3COOH ,
dbiles:
HCN,
H 2 O , etc
CH 2 CH 2
Cl1 ;
OH1
Bases dbiles:
etc
Algunas
Al(OH) 3 , C 2H 5OH ,
bases
alcalinas
trreas
Mg(OH) 2 , Ca(OH) 2
Observacin:
Los
electrolitos
dbiles
presentan reaccin reversible y equilibrio
qumico.
- cidos dbiles: Keq Ki = Ka
- Bases dbiles: Keq Ki = Kb
Ejemplo:
H O
I I
CH3COOH H C C O H
I
H
H1
Cuando el enlace H 1 A 1 es ms polar,
es ms fcil que la molcula HA tienda a
romperse produciendo mas H1 . Un alto
grado de polaridad es caracterstica de los
cidos fuertes
Av. Daniel Carrin N 585 Urb Albrecht Trujillo
Telfono: 293705
Hl,
excelentes
3. DETERMINACIN CUALITATIVA DE ACIDEZ
La fuerza de los cidos depende de algunos
factores como las propiedades del disolvente, la
temperatura y la estructura molecular del cido.
Cuando comparamos la fuerza entre dos cidos en
un mismo solvente y a la misma temperatura
entonces la variable a analizar se enfoca a la
estructura de los cidos:
Para un cido HA su fuerza se mide por su
tendencia a ionizarse: HA H1 X 1
Y los factores a analizar son la fuerza de enlace y
la polaridad del enlace
- Cuando el enlace H A es ms fuerte, es ms
difcil que la molcula HA se rompa y el cido
ser ms dbil porque se producen pocos
-
cido
H 2 SO 4 ,
Observacin:
- Toda base de Bronsted Lowry es tanbin una
base de Lewis
- Caractersticas de algunos cidos y bases Lewis
BF3 ; H 3BO 3
LA
1. Electrolito Fuerte: Es aquella sustancia que
se disocia en sus iones con gran rapidez y en un
100% (totalmente) son excelentes conductores
del calor y la electricidad.
Ejemplo:
B F3 N H3 BF3 NH3
Sustancias con
enlace simple
DE
ELECTROLITO
Sustancia que al contacto con el agua puede
disociarse en iones hacindola conductora de la
corriente elctrica con regular o alta eficiencia, son
de 2 clases:
Segn Lewis:
cido
CUANTITATIVA
CH 3COOH ( ac )
CH 3COO H
K E.Q K i K a 1,75 10 5
DETERMINACIN CUANTITATIVA DE ACIDEZ Y
BASICIDAD
A) Auto ionizacin del Agua
WWW.academiakepler.com
QI-10F-55
ACADEMIA PRE UNIVERSITARIA KEPLER
QUMICA
RAZ. MATEMTICO
A condiciones estndar a 25C 1 atm, se cumple:
H2O
1 mol/L
1 mol/L
+
OH
1 mol/L } Balance
0
} Inicial
: 1 mol/L
:
0
10 7 mol / L
10 7 mol / L
Escala de pH
pH
10 7 mol / L
:
} Avance en el
Solucin
cida
[H
1+
-1
] > [OH ]
pH < 7
laboratorio
1 10
10
mol / L
10
mol / L
mol / L } Equilibrio inico
Solucin
neutra
[H1+] = [OH-1 ]
Solucin
bsica
[H
pH = 7
Observacin:
KE.Q.
OH
K w KE.Q. H2O H
H2O
OH
Kw 1014
1.
Por lo tanto en la condicin del equilibrio
inico evaluamos el producto inico del agua
(Kw)
Slo a 25C Kw 10 14
10,6: Leche de magnesia
11,4: Limpiador domstico
con amonico
14
Del anlisis: H
10pH 10pOH
OH
En toda solucin neutra:
H OH
107 pH pOH 7
3.
En toda solucin cida:
H OH
pH pOH
4.
En toda solucin bsica:
H OH
pH pOH
Es aquel factor numrico que indica el grado
de concentracin de iones H de una
solucin
pH Log
C.
7:
Agua destilada
7,2: Saliva al comer
7,36: Sangre
7,4: Lgrimas
7,8: Huevos frescos
2.
B. POTENCIAL DE IONES HIDRGENO (pH)
-
6
6,6: Saliva despus
de comer
107 107 10(pHpOH)
pH pOH 14
Kw OH1 H3O 1 1014
B
a
s
i
c
i
d
a
d
Jugo gstrico
Jugo de limn
Jugo de naranja
Agua expuesta
aire
Conclusiones:
Observacin:
A 25C se determin experimentalmente:
OH1 H3O 1 107M
1+
-1
] < [OH ]
pH > 7
A
c
i
d
e
z
0
1:
2,4:
3,5:
5,5:
1
10pH
Log H H
H
POTENCIAL DE IONES OXHIDRILOS (pOH)
-
Indica
relativamente
la
concentracin
de
iones (OH) que posee una solucin
pOH Log
1
10pOH
Log OH OH
OH
D. ESCALA DEL pH:
Av. Daniel Carrin N 585 Urb Albrecht Trujillo
Telfono: 293705
WWW.academiakepler.com
QI-10F-55
ACADEMIA PRE UNIVERSITARIA KEPLER
QUMICA
RAZ. MATEMTICO
PRCTICA DE CLASE
C) El in
01. Indique verdadero (V) o falso (F) sobre los cidos y
bases.
I. Los cidos atacan al polvo de hornear,
NaHCO3 y la caliza, CaCO3 , produciendo
CO2 y vapor de agua.
II. Las bases presentan consistencia jabonosa al
tacto.
III. Los cidos reaccionan con un metal activo,
desplazando su hidrgeno que sale en forma
monoatmica.
A) VFV
D) FVF
B) VVF
E) VFF
E)
(F)
los
H2O HSO4 H3O
IV.
NH3 H2O NH4 OH
SO4
B) 1
C) 2
E) 4
A)
NaHCO3 H2O H2CO3 NaOH
B)
HI HCN I
C)
HCl NO3 Cl HNO3
D)
Al OH 2
H2 0 Al(OH)3 H
E)
HCN KOH H2O KCN
H2CN
-
El
H3PO4 y
el
H2CO3 son
especies
cidas.
II.
En (a) un par conjugado es CO3
/HCO3
.
H2PO4 acta como cido en (a) y
como base en (b).
III. El
A) Los compuestos HCl y HCOOH son cidos
monoprticos.
B) Los compuestos KOH y Ca(OH)2 son bases.
C) Solo se aplica en soluciones acuosas.
D) El amoniaco NH3 no es una base de Arrhenius.
se
A) VFV
D) VVV
B) FFV
E) VVF
Cr
6H2O Cr(H2O)6
III. Todo cido de Lewis tambin es cido de
Brnsted-Lowry.
05. Para la siguiente reaccin cido-base de Brnsted y
Lowry:
C2H5NH2 H2O C2H5NH3 OH estab
lezca la proposicin correcta.
A) El agua es un receptor del protn
B) La etilarnina, C2H5NH2 , acta como cido
C) FVF
09. Respecto a las siguientes proposiciones indique
cules son correctas.
I. El in cianuro CN y el amoniaco son bases de
Lewis.
II. Una reaccin cido-base de Lewis es:
Av. Daniel Carrin N 585 Urb Albrecht Trujillo
Telfono: 293705
III.
I.
04. Marque lo incorrecto con respecto a la teora de
Arrhenius.
produce iones hidronio H3O
H2O CN HCN OH
(b) H2PO-4 H2CO3 H3PO4 ........
C) VVV
II.
(a) H2PO-4 CO3
......... HCO3
Los cidos descomponen los carbonates
metlicos con desprendimiento de dixido de
carbono.
II. Las disoluciones acuosas de las bases son
jabonosas al tacto y conducen la corriente
elctrica.
III. Modifican el color de los indicadores como el
papel de tornasol y la fenolftaleina.
E) Cuando se disocia un cido en agua, /
08. Se tienen las siguientes reacciones de protlisis:
I.
B) FVV
E) FVF
CH3COO H2O CH3COOH OH
07. De acuerdo a la teora de Brnsted-_Lowry, cul de
los equilibrios no involucra una reaccin cido-base?
D) Solo es vlida cuando las sustancias estn
disueltas en agua.
E) Un cido es catalogado como monoprtico,
diprtico, triprtico, etc., dependiendo de la
cantidad de hidrgeno en su frmula.
A) VVF
D) VFV
pares
I.
A) 0
D) 3
C) NaOH, KOH y Ca(OH)2 son bases.
03. Determine
verdadero
(V)
o
falso
respecto
a
las
caractersticas
de
cidos y bases.
C2H5NH2 son
el
06. En cuntas reacciones el agua acta como una
base?
02. Sobre la teora de Arrhenius, indique la proposicin
incorrecta.
B) El H2SO4 y el H2CO3 son cidos diprticos.
H2O y
El
conjugados.
C) VVV
A) Los cidos en solucin acuosa aumentan la
concentracin del ion H+.
C2H5NH3 es el cido conjugado
de la etilarnina.
D) El in hidrxido OH" es la base conjugada del in
A) solo I
D) solo I y II
B) solo II
E) I,II y III
C) solo III
10. Al reaccionar CuSO4 con NH3 se forma un in
azul oscuro cuya estructura qumica es:
WWW.academiakepler.com
QI-10F-55
ACADEMIA PRE UNIVERSITARIA KEPLER
QUMICA
RAZ. MATEMTICO
16. Se tiene una solucin de H2SO4 , 0,02 M, calcule
su pH a 25 C?
Dato: log2 0,3
A) 1,4
D) 12,6
B) 2,3
E) 3,0
C) 0,4
17. Se tiene 0,37g de Ca(OH)2 en 0,5 L de solucin.
Calcule el pH de la solucin. Log 2 =0,3
Marque la proposicin incorrecta.
A) El in Cu2 es un cido.
A) 2,7
D) 1,7
B) El NH3 acta como base.
B) 12,3
E) 11,3
C) Hay cuatro enlaces covalentes coordinados.
C) 10,8
D)
NH3 acta como cido de Lewis.
18. Una solucin de 100 mL de Ca OH 2 0,12N se
E)
El in es un aducto.
diluye agregando 150 mL do agua
Indique las proposiciones verdaderas:
I. La molaridad final es 0,024 M
II. Su in es menor de 7.
III. .La Solucin enrojece al papel de tornasol azul.
11. Segn la teora de Lewis, cul de las especies tiene
carcter bsico?
C) Ag
A) SO2
B) HCl
D) K 2O
E) BF3
A) I y II
D) II y III
12. A partir de las siguientes reacciones, establezca el
orden de fuerza de acidez.
I.
II.
III.
HX HZ H2X
HY HX H2X
HZ HY H2Z
A) 10
D) 3,0
H2O
N.
A) 1
D) 12
aumenta con el
aumento de la temperatura.
II. A 25 C se cumple que K= 1014 .
III. El agua se considera un electrlito muy dbil.
A) solo I
D) I y II
B) slo II
E) I, II y III
A) 9,2
D) 5,4
El valor de K W nos indica la proporcin en la
cual el aguase ioniza.
II. A nivel submicroscpico, en el agua.
III. A cualquier temperatura, la concentracin de los
I.
iones H3O y OH son iguales en el agua.
B) II y III
E) I, III
A) 0,26 x 10
14
D) 0,33 x 10
B) 10
C) 7
B) 2,3
E) 3,7
C) 10,3
22. Determine la concentracin de HCN que presenta un
pH de 4,5.
Ka = 5 x 10 10
Log3 =0,5
A) 3 M
D) 1,5 M
B) 2 M
E) 1,8 M
C) 2,5 M
23. Cuantas de la siguientes sales al disolverse en agua
enrojecen el papel del tornasol?
C) II
KNO3; NH4Cl; KCl; ZnBr
2
15. Cul es la concentracin de OH es una solucin
de HCl 3M a 25 C?
8
B) 2
E) 13
21. Un cido monoprtico 0,01 M se disocia en 2% a 25
C. Cul es su pOH?
Log2=0,3
C) solo III
14. Cuntas proposiciones son correctas?
A) I y II
D) III
C) 23
de cido HNO3 0,15 M a 20 mL de base KOH 0,25
13. Indique las proposiciones correctas.
La ionizacin del
B) 17
E) 4,0
20. Calcule el pH de la solucin obtenida de aadir 30 mL
A) HX< HY< HZ B) HZ< HX< HY C) HY< HZ< HX
D) HZ < HY < HX E) HX< HZ< HY
I.
C) I, II y III
19. Cul es el pH de una solucin preparada al mezclar
100 mL de HCl 0,005 M con 400 mL de NaCI 0,02 M?
B) II y III
E) solo II
14
C) 3,33 x 10
E) 0,33 x 1016
A) 0
D) 1
B) 4
C) 3
E) 2
24. Si introducimos un pedazo de papel tornasol en cada
una de las siguientes soluciones, cul de ellas se
tornar de color azl?
I. NH4Br
II. KNO2 ac
III. Na2SO4 ac IV. Cl ac
Av. Daniel Carrin N 585 Urb Albrecht Trujillo
Telfono: 293705
WWW.academiakepler.com
QI-10F-55
ACADEMIA PRE UNIVERSITARIA KEPLER
QUMICA
A) solo IV
D) III y IV
B) I y II
E) solo I
RAZ. MATEMTICO
PREGUNTAS DE EXAMEN DE ADMISIN
C) solo II
CEPUNT 2010 I: 3er Sum. B (Abr. Ago. 2009)
25. En la siguiente reaccin:
CH3COOH H2O
CH3COO H3O
Los cidos
de Brnsted Lowry son:
H O H O+
A) 2 / 3
H O CH COO
B) 2 / 3
CH3COOH CH3COO
C)
/
CH3COOH H3O+
D)
/
CH3COO H3O+
E)
/
CEPUNT 2009 II: 3er Sum. A (Oct. Feb. 2009)
26. Segn el concepto cido base, versin Brnsted
Lowry, en la reaccin:
CH3NH2 H2O
CH3NH3 OH
El par cido base conjugada, estara conformado
por:
A) Los reactantes
CH3NH2
C)
y OH
HO
E) 2 y OH
B) Los productos
HO
CH3NH3
D) 2 y
CEPUNT 2009 II: 3er Sum. B (Oct. Feb. 2009)
27. Son especies qumicas que tienen carcter bsico,
segn la teora cido base de G. N. Lewis:
1. Los aniones
2. NH3 3. C2H5NH2
4. UO22+
5. S2
SON CIERTAS:
A) 1, 2, 3 y 5 B) Slo 2, 3 y 5C) Slo 1 y 5
D) Slo 2 y 3 E) 4
UNT 2009 II A:
28. Una solucin de detergente tiene un pOH = 2,4;
entonces la concentracin molar del in hidronio
es:
( log4 0,6 )
A) 5,0 x103
B) 1,2 x1011
D) 2,5 x10 10
E) 2,5 x10 12
C) 4,8 x106
UNT 2009 II B:
29. Un estudiante prepar una solucin 0,1 M de
cido frmico ( HCOOH ) y determin su pH, siendo
este igual a 2,4. La Ka para el cido frmico es:
Dato: log4 0,6
A) 4,20 x106
D) 1,67 x10
B) 6,00 x104
E) 1,67 x10
C) 1,67 x104
CEPUNT 2009 I: 3er Sum. B (Abr. Ago. 2008)
30. El pH de una solucin de amonaco ( NH3 ) 0,5M
que esta disociado en un 0,2%; es:
A) 13
D) 7
Av. Daniel Carrin N 585 Urb Albrecht Trujillo
Telfono: 293705
B) 11
E) 3
C) 9
WWW.academiakepler.com
QI-10F-55
ACADEMIA PRE UNIVERSITARIA KEPLER
QUMICA
Av. Daniel Carrin N 585 Urb Albrecht Trujillo
Telfono: 293705
RAZ. MATEMTICO
WWW.academiakepler.com
QI-10F-55
You might also like
- Todas Las Cosas Que Escribí Cuando NingDocument95 pagesTodas Las Cosas Que Escribí Cuando Ningandrea avila perezNo ratings yet
- Tipos de Magia GoldenDocument14 pagesTipos de Magia GoldenBlanca arbona alcover100% (1)
- Raíces griegas y latinasDocument44 pagesRaíces griegas y latinasDavid Alva AlbaNo ratings yet
- Polinomios EspecialesDocument4 pagesPolinomios EspecialesDavid Alva AlbaNo ratings yet
- Palmerin de Inglaterra 1a ParteDocument184 pagesPalmerin de Inglaterra 1a ParteFabián Coelho100% (1)
- Banco de Preguntas de FilosofiaDocument116 pagesBanco de Preguntas de FilosofiaDavid Alva Alba100% (1)
- I Bimestre Tema 1 SucesionesDocument6 pagesI Bimestre Tema 1 SucesionesDavid Alva AlbaNo ratings yet
- GeoPoliVolDocument6 pagesGeoPoliVolDavid Alva AlbaNo ratings yet
- I Bimestre Tema 2 Distribuciones Graficas y NumericasDocument4 pagesI Bimestre Tema 2 Distribuciones Graficas y NumericasDavid Alva AlbaNo ratings yet
- Principio de SuperposicionDocument15 pagesPrincipio de SuperposicionXimena Pajuelo Sacramento100% (1)
- Sistemas de NumeracionDocument3 pagesSistemas de NumeracionDavid Alva AlbaNo ratings yet
- Operaciones Fundamentales - PrácticaDocument3 pagesOperaciones Fundamentales - PrácticaDavid Alva AlbaNo ratings yet
- Operaciones Fundamentales - TeoríaDocument3 pagesOperaciones Fundamentales - TeoríaDavid Alva AlbaNo ratings yet
- Aritmetica 2010 - 3 - #02 - Divisibilidad y MultiplicidadDocument1 pageAritmetica 2010 - 3 - #02 - Divisibilidad y MultiplicidadDavid Alva AlbaNo ratings yet
- Estatica - PracticaDocument2 pagesEstatica - PracticaDavid Alva AlbaNo ratings yet
- AprendisajeDocument2 pagesAprendisajeDavid Alva AlbaNo ratings yet
- Vectores - PracticaDocument5 pagesVectores - PracticaDavid Alva AlbaNo ratings yet
- Modulo Humanidades Español Ciclo IV Grado NovenoDocument48 pagesModulo Humanidades Español Ciclo IV Grado NovenoLaurita Guerrero Franco100% (4)
- Cocientes Notables - Binomio de Newton - PracticaDocument3 pagesCocientes Notables - Binomio de Newton - PracticaDavid Alva AlbaNo ratings yet
- Lengua JeDocument15 pagesLengua JeDavid Alva AlbaNo ratings yet
- Módulo Lenguaje PDFDocument135 pagesMódulo Lenguaje PDFDavid Alva AlbaNo ratings yet
- Para El Blog MateDocument13 pagesPara El Blog MateCjprNo ratings yet
- AR-10A-04 (P - Divisbilidad)Document2 pagesAR-10A-04 (P - Divisbilidad)David Alva AlbaNo ratings yet
- Abril - Julio 2014 11° Áreas de Figuras Planas y CurvasDocument6 pagesAbril - Julio 2014 11° Áreas de Figuras Planas y CurvasDavid Alva AlbaNo ratings yet
- Ar-10l-12 (Compendio Iv - Sem 17 - 22) BG - L1-L2Document18 pagesAr-10l-12 (Compendio Iv - Sem 17 - 22) BG - L1-L2David Alva AlbaNo ratings yet
- Ar-10m-03 (Compendio I) - RG - c5-l5Document23 pagesAr-10m-03 (Compendio I) - RG - c5-l5David Alva AlbaNo ratings yet
- Ar-10j-08 (Compendio Iii - Sem 11 - Sem 16) BG - C3-C4-L3-L4Document24 pagesAr-10j-08 (Compendio Iii - Sem 11 - Sem 16) BG - C3-C4-L3-L4David Alva AlbaNo ratings yet
- Admision Unmsm 2015Document4 pagesAdmision Unmsm 2015David Alva AlbaNo ratings yet
- Abril - Julio 2014 3° Congruencia de TriángulosDocument4 pagesAbril - Julio 2014 3° Congruencia de TriángulosDavid Alva AlbaNo ratings yet
- AR-10Y-05 (TP - COMPENDIO II) RG - IntermedioDocument24 pagesAR-10Y-05 (TP - COMPENDIO II) RG - IntermedioDavid Alva AlbaNo ratings yet
- AR-10A-04 (P - Divisbilidad)Document2 pagesAR-10A-04 (P - Divisbilidad)David Alva AlbaNo ratings yet
- I Bimestre Tema 2 Planteo de EcuacionesDocument4 pagesI Bimestre Tema 2 Planteo de EcuacionesDavid Alva AlbaNo ratings yet
- Abril - Julio 2014 1° ÁngulosDocument3 pagesAbril - Julio 2014 1° ÁngulosDavid Alva AlbaNo ratings yet
- Practica de Raz. Verbal PDFDocument16 pagesPractica de Raz. Verbal PDFDavid Alva AlbaNo ratings yet
- 10c Cultivo de Conchas de AbanicoDocument20 pages10c Cultivo de Conchas de AbanicoraswerNo ratings yet
- Adivinanzas - para Niños Con Respuestas. 12 - 10 - 10Document3 pagesAdivinanzas - para Niños Con Respuestas. 12 - 10 - 10LIPANURUNo ratings yet
- 2Document4 pages2Antoine CheroNo ratings yet
- Informe Promocion Anticipada 2020Document105 pagesInforme Promocion Anticipada 2020Nardelly olayaNo ratings yet
- Cáncer de Páncreas y CarcinomaDocument29 pagesCáncer de Páncreas y CarcinomaJuan ArgentNo ratings yet
- Rne Grupo 14Document6 pagesRne Grupo 14VALERY RENGIFONo ratings yet
- GSA: El Riesgo Oculto en Los (Re) Encuentros. Barbara GonyoDocument11 pagesGSA: El Riesgo Oculto en Los (Re) Encuentros. Barbara GonyoGavi CanoNo ratings yet
- Un Discurso Sobre Las Ciencias Ensayo (Autoguardado)Document12 pagesUn Discurso Sobre Las Ciencias Ensayo (Autoguardado)alejandro hernandezNo ratings yet
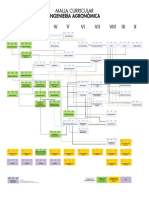
- Malla Curricular Ing Agronómica UNALDocument1 pageMalla Curricular Ing Agronómica UNALkmigeNo ratings yet
- Cap 23 GeometriaDocument6 pagesCap 23 Geometriaerwin_carryNo ratings yet
- PDFDocument234 pagesPDFRamiro ObandoNo ratings yet
- Diseño BARBER SHOP DONDE ALEXDocument1 pageDiseño BARBER SHOP DONDE ALEXKj Gh GomezNo ratings yet
- EmocionesDocument6 pagesEmocionesAlex AlexNo ratings yet
- 08 Principios de Diseño Urbano Espacio Vital y AmbienteDocument27 pages08 Principios de Diseño Urbano Espacio Vital y AmbienteSergio CitalanNo ratings yet
- Fragmentos de Memoria. Profesores y luchas de la UTDocument374 pagesFragmentos de Memoria. Profesores y luchas de la UTdaniel garcíaNo ratings yet
- Bobinas en MineríaDocument5 pagesBobinas en MineríaDarwin Torres RojasNo ratings yet
- Pact. Preoperatorio Esquema LlaveDocument3 pagesPact. Preoperatorio Esquema LlaveLizeth Johanny Huaypar RamosNo ratings yet
- Historia Clínica MédicaDocument6 pagesHistoria Clínica MédicaRigoberto TorresNo ratings yet
- Lengua Castellana - Tipos de TextosDocument15 pagesLengua Castellana - Tipos de TextosYovanna MejiasNo ratings yet
- Ic303 T7 Techint Reporte - FinalDocument7 pagesIc303 T7 Techint Reporte - FinalDaniel CutimboNo ratings yet
- Actividad Escrita 5 Aplicaciones de Ecuacion LinealDocument4 pagesActividad Escrita 5 Aplicaciones de Ecuacion LinealJHon MarkNo ratings yet
- Historia y detalles del municipio de San Pedro SacatepéquezDocument59 pagesHistoria y detalles del municipio de San Pedro SacatepéquezMilton AlfaroNo ratings yet
- Trastorno Cognitivo Leve (Alzheimer)Document11 pagesTrastorno Cognitivo Leve (Alzheimer)José Ramón Rodríguez BajoNo ratings yet
- Trastornos psiquiátricos y psicofarmacologíaDocument5 pagesTrastornos psiquiátricos y psicofarmacologíaYony FCqNo ratings yet
- Segmentación de La Población ObjetivaDocument3 pagesSegmentación de La Población ObjetivaDANIELA BOCANGEL SALASNo ratings yet
- Análisis Espacial de BarcinoDocument5 pagesAnálisis Espacial de BarcinoFABRICIO GABRIEL SEMINARIO RAMIREZNo ratings yet