Professional Documents
Culture Documents
Propiedades de Los Comp Organicos
Uploaded by
David Andrés Quezada EspinosaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Propiedades de Los Comp Organicos
Uploaded by
David Andrés Quezada EspinosaCopyright:
Available Formats
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Propiedades de los alcoholes
Los alcoholes son compuestos que presentan en
la cadena carbonada uno o ms grupos hidroxi u
oxidrilo (-OH).
Propiedades Fsicas:
Las propiedades fsicas de un alcohol se basan
principalmente en su estructura. El alcohol
esta compuesto por un alcano y agua.
Contiene un grupo hidrofbico (sin afinidad
por el agua) del tipo de un alcano, y un grupo
hidroxilo que es hidrfilo (con afinidad por el
agua), similar al agua. De estas dos unidades
estructurales, el grupo OH da a los alcoholes
sus propiedades fsicas caractersticas, y el
alquilo es el que las modifica, dependiendo de
su tamao y forma.
El grupo OH es muy polar y, lo que es ms
importante, es capaz de establecer puentes de
hidrgeno: con sus molculas compaeras o con
otras molculas neutras.
Solubilidad:
Puentes de hidrgeno: La formacin de puentes de hidrgeno permite la asociacin entre las
molculas de alcohol. Los puentes de hidrgeno se forman cuando los oxgenos unidos al
hidrgeno en los alcoholes forman uniones entre sus molculas y las del agua. Esto explica la
solubilidad del metanol, etanol, 1-propanol, 2-propanol y 2 metil-2-propanol.
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
alcohol-alcohol
alcohol-agua
A partir de 4 carbonos en la cadena de un alcohol, su solubilidad disminuye rpidamente en
agua, porque el grupo hidroxilo (OH), polar, constituye una parte relativamente pequea en
comparacin con la porcin hidrocarburo. A partir del hexanol son solubles solamente en
solventes orgnicos.
1 propanol
Hexanol
Existen alcoholes de cuatro tomos de
carbono que son solubles en agua, debido a la
disposicin espacial de la molcula. Se trata
de molculas simtricas.
2-metil-2-propanol
Existen alcoholes con mltiples molculas de
OH (polihidroxilados) que poseen mayor
superficie para formar puentes de hidrgeno, lo
que permiten que sean bastante solubles en
agua.
1,2,3 propanotriol
(glicerina)
Punto de Ebullicin: Los puntos de ebullicin
de los alcoholes tambin son influenciados
por la polaridad del compuesto y la cantidad
de puentes de hidrgeno. Los grupos OH
presentes en un alcohol hacen que su punto de
ebullicin sea ms alto que el de los
hidrocarburos de su mismo peso molecular.
En los alcoholes el punto de ebullicin
aumenta con la cantidad de tomos de carbono
y disminuye con el aumento de las
ramificaciones.
El punto de fusin aumenta a medida que
aumenta la cantidad de carbonos.
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Densidad: La densidad de los alcoholes aumenta con el nmero de carbonos y sus
ramificaciones. Es as que los alcoholes alifticos son menos densos que el agua mientras que
los alcoholes aromticos y los alcoholes con mltiples molculas de OH,
denominadospolioles, son ms densos.
(Constantes Fsicas de algunos alcoholes)
Nombre
Punto de fusinC Punto de ebullicin C
Densidad
Metanol
-97,5
64,5
0,793
1-propanol
-126
97,8
0,804
2-propanol
-86
82,3
1-butanol
-90
117
0,810
2-butanol
-114
99,5
0,806
2-metil-1-propanol
-108
107,3
0,802
2-metil-2-propanol
25,5
82,8
0,789
1-pentanol
-78,5
138
0,817
Ciclohexanol
24
161,5
0,962
Propiedades Qumicas:
0,789
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Los alcoholes pueden comportarse como cidos o bases, esto gracias al efecto inductivo, que
no es ms que el efecto que ejerce la molcula de OH como sustituyente sobre los carbonos
adyacentes. Gracias a este efecto se establece un dipolo.
La estructura del alcohol est relacionada con su acidez. Los alcoholes, segn su estructura
pueden clasificarse como metanol, el cual presenta un slo carbono, alcoholes primarios,
secundarios y terciarios que presentan dos o ms molculas de carbono.
Alcohol Terciario
2-metil-2-propanol
Alcohol Secundario
2-butanol
Alcohol Primario
1-butanol
Metanol
Metanol > alcohol primario > alcohol secundario > alcohol terciario(>: mayor
acidez)
Debido a que en el metanol y en los alcoholes primarios el hidrgeno est menos firmemente
unido al oxgeno, la salida de los protones de la molcula es ms fcil por lo que la acidez ser
mayor en el metanol y el alcohol primario.
Deshidratacin: la deshidratacin de los
alcoholes se considera una reaccin de
eliminacin, donde el alcohol pierde su grupo
OH para dar origen a un alqueno. Aqu se pone
de manifiesto el carcter bsico de los
alcoholes. La reaccin ocurre en presencia de
cido sulfrico (H2SO4) en presencia de calor.
La deshidratacin es posible ya que el alcohol
acepta un protn del cido, para formar el
alcohol protonado o in alquil hidronio.
El alcohol protonado pierde una molcula de
agua y forma un in alquil-carbonio:
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
El in alquil-carbonio pierde un protn lo que
regenera la molcula de cido sulfrico y se
establece el doble enlace de la molcula a la
cual est dando origen el alcohol.
El calentamiento de un alcohol en presencia de cido sulfrico a temperaturas inferiores a las
necesarias para obtener alquenos producir otros compuestos como teres y steres.
Obtencin de alcoholes: al igual que a partir de los alcoholes se pueden obtener otros
compuestos, los alcoholes pueden ser obtenidos a partir de hidratacin o hidroboracin
oxidacin de alquenos, o mediante hidrlisis de halogenuros de alquilo. Para la obtencin de
alcoholes por hidratacin de alquenos se utiliza el cido sulfrico y el calor.
La hidroboracin: (adicin de borano R3B) de
alqueno en presencia de perxido de hidrgeno
(H2O2) en medio alcalino da origen a un
alcohol.
La hidrlisis: de halogenuros de alquilo o
aralquilo se produce en presencia de agua y
hidrxidos fuertes que reaccionan para formar
alcoholes.
En la industria la produccin de alcoholes se realiza a travs de diversas reacciones como las
ya mencionadas, sin embargo se busca que stas sean rentables para proporcionar la mxima
cantidad de producto al menor costo. Entre las tcnicas utilizadas por la industria para la
produccin de alcoholes se encuentra la fermentacin donde la produccin de cido butrico a
partir de compuestos azucarados por accin de bacterias como el Clostridium butycum dan
origen al butanol e isopropanol. Para la produccin de alcoholes superiores en la industria la
fermentacin permite la produccin de alcoholes isoamlico, isobutlico y n-proplico a partir
de aminocidos. Es as como la industria utiliza los procesos metablicos de ciertas bacterias
para producir alcoholes.
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Propiedades de los Aldehdos y
Cetonas
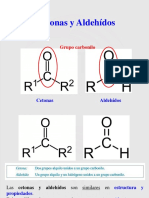
Los aldehdos y las cetonas: son compuestos
caracterizados por la presencia del grupo
carbonilo (C=O). Los aldehdos presentan el
grupo carbonilo en posicin terminal mientras
que las cetonas lo presentan en posicin
intermedia. El primer miembro de la familia
qumica de los aldehdos es el metanal o
formaldehdo (aldehdo frmico), mientras que
el primer miembro de la familia de las cetonas es
la propanona o acetona (dimetil acetona)
Propanona
Metanal
Las cetonas aromticas reciben el nombre de
felonas.
Metil-fenil-cetona
Propiedades Fsicas:
La presencia del grupo carbonilo convierte a
los aldehdos y cetonas en compuestos
polares. Los compuestos de hasta cuatro
tomos de carbono, forman puente de
hidrgeno con el agua, lo cual los hace
completamente solubles en agua. Igualmente
son solubles en solventes orgnicos.
Punto de Ebullicin: los puntos de ebullicin de los aldehdos y cetonas son mayores que el de
los alcanos del mismo peso molecular, pero menores que el de los alcoholes y cidos
carboxlicos comparables. Esto se debe a la formacin de dipolos y a la ausencia de formacin
de puentes de hidrgeno intramoleculares en stos compuestos.
(Constantes fsicas de algunas aldehidos y cetonas)
Nombre
Pto. de fusin(C) Pto. de ebullicin(C)
Solubilidad (gr/100 gr
de H2O)
Metanal
-92
-21
Muy soluble
Etanal
-122
20
Soluble al infinito
Propanal
-81
49
16
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Benzaldehdo
-26
178
0,3
Propanona
-94
56
Soluble al infinito
Butanona
-86
80
26
2-pentanona
-78
102
6,3
3 pentanona
-41
101
Acetofenona
21
202
Insoluble
Propiedades Qumicas:
Los aldehdos y cetonas se comportan como cidos debido a la presencia del grupo carbonilo,
esto hace que presenten reacciones tpicas de adicin nucleoflica.
Reacciones de adicin nucleoflica: Estas reacciones se producen frente al (reactivo de
Grignard), para dar origen a un oxihaluro de alquil-magnesio que al ser tratado con agua da
origen a un alcohol. El metanal forma alcoholes primarios y los dems aldehdos forman
alcoholes secundarios.
La reaccin de adicin nucleoflica en las
cetonas dan origen a alcoholes terciarios.
Otras reacciones de adicin nucleoflica pueden producirse con el cido cianhdrico, el sulfito
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
cido de sodio, la hidroxilamina, hidracina, semicarbacida, fenilhidracina y con el 2,4
dinitrofenilhidracina, para dar origen a diferentes compuestos qumicos.
Los aldehdos y cetonas tambin pueden dar
origen a otros compuestos
mediantereacciones de sustitucin
halogenada, al reaccionar con los halgenos
sustituyen uno o varios hidrgenos del
carbono unido al carbonilo.Este mtodo
permite obtener la monobromoactona que es
un poderoso gas lacrimgeno.
Reacciones de condensacin aldlica: En esta
reaccin se produce la unin de dos aldehdos o
dos cetonas en presencia de una solucin de
NaOH formando un polmero, denominado
aldol.
Reacciones de oxidacin: Los aldehdos se
oxidan con facilidad frente a oxidantes
dbiles produciendo cidos. Mientras que las
cetonas slo se oxidan ante oxidantes muy
enrgicos que puedan romper sus cadenas
carbonadas. Es as que las reacciones de
oxidacin permiten diferenciar los aldehdos
de las cetonas en el Laboratorio.
Sntesis y obtencin de aldehdos y cetonas
alifticas:
Los aldehdos y cetonas pueden ser obtenidos
mediante la oxidacin de alcoholes.
La hidratacin de alquinos en presencia de
cido sulfrico en solucin acuosa y sulfato
mercrico permite obtener aldehdos y
cetonas.
Sntesis de Aldehdos Aromticos:
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Los aldehdos aromticos presentan un anillo
aromtico unido al grupo carbonilo. El
representante
de este grupo de compuestos es el benzaldehido.
La obtencin del benzaldehido puede ser
mediante oxidacin del tolueno, del cloruro de
bencilo o por hidrlisis del cloruro de
bencilideno.
Benzaldehido
Sntesis de cetonas aromticas
Las cetonas aromticas (fenonas) presentan uno o dos anillos aromticos unidos al grupo
carbonilo.
Metal-fenil-cetona
difenil-cetona
La mayora de las cetonas aromticas se
preparan por acilacin de Friedel-Crafts,
donde el benceno reacciona con los cloruros
de cido en presencia de cloruro de aluminio.
As el grupo acilo entra al anillo para
producir las fenonas.
Uso de los aldehdos y cetonas:
Aldehdos:
El metanal o aldehdo frmico es el aldehdo con
mayor uso en la industria, se utiliza
fundamentalmente para la obtencin de resinas
fenlicas y en la elaboracin de explosivos
(pentaeritrol y el tetranitrato de pentaeritrol,
TNPE) as como en la elaboracin de resinas
alqudicas y poliuretano expandido.
Tambin se utiliza en la elaboracin de uno de
los llamados plsticos tcnicos que se utilizan
fundamentalmente en la sustitucin de piezas
metlicas en automviles y maquinaria, as como
para cubiertas resistentes a los choques en la
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
manufactura de aparatos elctricos. Estos
plsticos reciben el nombre de POM
(polioximetileno)
Cetonas:
La cetona que mayor aplicacin industrial
tiene es la acetona (propanona) la cual se
utiliza como disolvente para lacas y resinas,
aunque su mayor consumo es en la
produccin del plexigls, emplendose
tambin en la elaboracin de resinas epoxi y
poliuretanos. Otras cetonas industriales son
la metil etil cetona (MEK, siglas el ingls) y
la ciclohexanona que adems de utilizarse
como disolvente se utiliza en gran medida
para la obtencin de la caprolactama, que es
un monmero en la fabricacin del Nylon 6 y
tambin por oxidacin del cido adpico que
se emplea para fabricar el Nylon 66.
Muchos aldehdos y cetonas forman parte de los aromas naturales de flores y frutas, por lo cual
se emplean en la perfumera para la elaboracin de aromas como es el caso del benzaldehdo
(olor de almendras amargas), el aldehdo ansico (esencia de ans), la vainillina, el piperonal
(esencia de sasafrs), el aldehdo cinmico (esencia de canela). De origen animal existe la
muscona y la civetona que son utilizados como fijadores porque evitan la evaporacin de los
aromas adems de potenciarlos por lo cual se utilizan en la industria de la perfumera.
aldehido ansico
muscona
civetona
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Propiedades de las Aminas
Las aminas son compuestos orgnicos
derivados del amoniaco (NH3), y son producto
de la sustitucin de los hidrgenos que
componen al amoniaco por grupos alquilo o
arilo.
Las aminas se clasifican de acuerdo al nmero
de sustituyentes unidos al nitrgeno en aminas
primarias, aminas secundarias y terciarias.
Amina primaria
Amina primaria
aromtica
Amina secundaria
Propiedades Fsicas:
Las aminas son compuestos incoloros que se oxidan con facilidad lo que permite que se
encuentren como compuestos coloreados. Los primeros miembros de esta serie son gases con
olor similar al amonaco. A medida que aumenta el nmero de tomos de carbono en la
molcula, el olor se hace similar al del pescado. Las aminas aromticas son muy txicas se
absorben a travs de la piel.
Amina secundaria
aromtica
Solubilidad: Las aminas primarias y
secundarias son compuestos polares, capaces
de formar puentes de hidrgeno entre s y con
el agua, esto las hace solubles en ella. La
solubilidad disminuye en las molculas con
ms de 6 tomos de carbono y en las que
Amina terciaria
aromtica
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
poseen el anillo aromtico.
Punto de Ebullicin: El punto de ebullicin de las aminas es ms alto que el de los
compuestos apolares que presentan el mismo peso molecular de las aminas. El nitrgeno es
menos electronegativo que el oxgeno, esto hace que los puentes de hidrgeno entre las aminas
se den en menor grado que en los alcoholes. Esto hace que el punto de ebullicin de las aminas
sea ms bajo que el de los alcoholes del mismo peso molecular.
(Constantes fsicas de algunas Aminas)
Pto. de fusin(C)
Pto. de
ebullicin(C)
Solubilidad (gr/100 gr
de H2O)
Metil-amina
-92
-7,5
Muy soluble
Dimetil-amina
-96
7,5
Muy soluble
Trimetil-amina
-117
91
Fenil-amina
-6
184
3,7
Difenil-amina
53
302
Insoluble
Metilfenil-amina
-57
196
Muy poco soluble
Nombre
Propiedades Qumicas:
Las aminas se comportan como bases. Cuando
una amina se disuelve en agua, acepta un
protn formando un in alquil-amonio.
Sntesis de aminas: Las aminas se obtienen tratando derivados halogenados o alcoholes con
amoniaco.
Produccin de aminas a partir de derivados
halogenados
Las aminas inferiores se preparan
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
comercialmente haciendo pasar amoniaco y
vapores de alcohol en presencia de xido de
thorio o de aluminio caliente.
La reduccin de diversos compuestos como nitroderivados, nitrilos, aldehdos o cetonas
tambin tiene entre sus productos finales las aminas.
Reacciones para reconocer aminas en el
laboratorio.
Para diferenciar las aminas entre s en el
laboratorio se hacen reaccionar con una
solucin de nitrito de sodio y cido
clorhdrico, esto da origen a cido nitroso
inestable. Cada tipo de amina tendr un
comportamiento diferente frente al cido
nitroso, dependiendo adems de la temperatura
a la cual se lleve a cabo la reaccin.
En cuanto a las aminas primarias: las aminas
alifticas (link con Nomenclatura Orgnica
cuarta etapa) reaccionan con el cido nitroso
para dar un alcohol con desprendimiento de
nitrgeno y agua.
Las aminas aromticas al reaccionar con cido nitroso a temperatura elevada en presencia de
cido sulfrico diluido se comportan como las aminas alifticas, pero si la reaccin ocurre a
0C se produce una sal de diazonio soluble en agua.
Las aminas secundarias tanto alifticas como aromticas al reaccionar con el cido nitroso
generan N-nitrosaminas oleosas e insolubles en agua, llamadas tambin compuestos N-
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
nitrosos.
En cuanto a las aminas terciarias tanto alifticas como aromticas al reaccionar con el cido
nitroso generan derivados N-nitrosados y productos complejos respectivamente que son
motivo de estudio.
Aminas. Dnde se encuentran?
Las aminas se encuentran formando parte de la
naturaleza, en los aminocidos que conforman
las protenas que son un componente esencial
del organismo de los seres vivos. Al
degradarse las protenas se descomponen en
distintas aminas, como cadaverina y putrescina
entre otras. Las cuales emiten olor
desagradable. Es por ello que cuando la carne
de aves, pescado y res no es preservada
mediante refrigeracin, los microorganismos
que se encuentran en ella degradan las
protenas en aminas y se produce un olor
desagradable.
Las aminas son parte de los alcaloides que son
compuestos complejos que se encuentran en las
plantas. Algunos de ellos son la morfina y la
nicotina. Algunas aminas son biolgicamente
importantes como la adrenalina y la
noradrenalina.
Las aminas secundarias que se encuentran en
las carnes y los pescados o en el humo del
tabaco.
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Estas aminas pueden reaccionar con los nitritos
presentes en conservantes empleados en la
alimentacin y en plantas, procedentes del uso
de fertilizantes, originando N-nitrosoaminas
secundarias, que son carcingenas.
Propiedades de las Aminas
Las aminas son compuestos orgnicos
derivados del amoniaco (NH3), y son producto
de la sustitucin de los hidrgenos que
componen al amoniaco por grupos alquilo o
arilo.
Las aminas se clasifican de acuerdo al nmero
de sustituyentes unidos al nitrgeno en aminas
primarias, aminas secundarias y terciarias.
Amina primaria
Amina primaria
aromtica
Amina secundaria
Propiedades Fsicas:
Las aminas son compuestos incoloros que se oxidan con facilidad lo que permite que se
encuentren como compuestos coloreados. Los primeros miembros de esta serie son gases con
olor similar al amonaco. A medida que aumenta el nmero de tomos de carbono en la
molcula, el olor se hace similar al del pescado. Las aminas aromticas son muy txicas se
absorben a travs de la piel.
Amina secundaria
aromtica
Amina terciaria
aromtica
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Solubilidad: Las aminas primarias y
secundarias son compuestos polares, capaces
de formar puentes de hidrgeno entre s y con
el agua, esto las hace solubles en ella. La
solubilidad disminuye en las molculas con
ms de 6 tomos de carbono y en las que
poseen el anillo aromtico.
Punto de Ebullicin: El punto de ebullicin de las aminas es ms alto que el de los
compuestos apolares que presentan el mismo peso molecular de las aminas. El nitrgeno es
menos electronegativo que el oxgeno, esto hace que los puentes de hidrgeno entre las aminas
se den en menor grado que en los alcoholes. Esto hace que el punto de ebullicin de las aminas
sea ms bajo que el de los alcoholes del mismo peso molecular.
(Constantes fsicas de algunas Aminas)
Pto. de fusin(C)
Pto. de
ebullicin(C)
Solubilidad (gr/100 gr
de H2O)
Metil-amina
-92
-7,5
Muy soluble
Dimetil-amina
-96
7,5
Muy soluble
Trimetil-amina
-117
91
Fenil-amina
-6
184
3,7
Difenil-amina
53
302
Insoluble
Metilfenil-amina
-57
196
Muy poco soluble
Nombre
Propiedades Qumicas:
Las aminas se comportan como bases. Cuando
una amina se disuelve en agua, acepta un
protn formando un in alquil-amonio.
Sntesis de aminas: Las aminas se obtienen tratando derivados halogenados o alcoholes con
amoniaco.
Produccin de aminas a partir de derivados
halogenados
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Las aminas inferiores se preparan
comercialmente haciendo pasar amoniaco y
vapores de alcohol en presencia de xido de
thorio o de aluminio caliente.
La reduccin de diversos compuestos como nitroderivados, nitrilos, aldehdos o cetonas
tambin tiene entre sus productos finales las aminas.
Reacciones para reconocer aminas en el
laboratorio.
Para diferenciar las aminas entre s en el
laboratorio se hacen reaccionar con una
solucin de nitrito de sodio y cido
clorhdrico, esto da origen a cido nitroso
inestable. Cada tipo de amina tendr un
comportamiento diferente frente al cido
nitroso, dependiendo adems de la temperatura
a la cual se lleve a cabo la reaccin.
En cuanto a las aminas primarias: las aminas
alifticas (link con Nomenclatura Orgnica
cuarta etapa) reaccionan con el cido nitroso
para dar un alcohol con desprendimiento de
nitrgeno y agua.
Las aminas aromticas al reaccionar con cido nitroso a temperatura elevada en presencia de
cido sulfrico diluido se comportan como las aminas alifticas, pero si la reaccin ocurre a
0C se produce una sal de diazonio soluble en agua.
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Las aminas secundarias tanto alifticas como aromticas al reaccionar con el cido nitroso
generan N-nitrosaminas oleosas e insolubles en agua, llamadas tambin compuestos Nnitrosos.
En cuanto a las aminas terciarias tanto alifticas como aromticas al reaccionar con el cido
nitroso generan derivados N-nitrosados y productos complejos respectivamente que son
motivo de estudio.
Aminas. Dnde se encuentran?
Las aminas se encuentran formando parte de la
naturaleza, en los aminocidos que conforman
las protenas que son un componente esencial
del organismo de los seres vivos. Al
degradarse las protenas se descomponen en
distintas aminas, como cadaverina y putrescina
entre otras. Las cuales emiten olor
desagradable. Es por ello que cuando la carne
de aves, pescado y res no es preservada
mediante refrigeracin, los microorganismos
que se encuentran en ella degradan las
protenas en aminas y se produce un olor
desagradable.
PROPIEDADES DE LOS COMPUESTOS ORGNICOS
Las aminas son parte de los alcaloides que son
compuestos complejos que se encuentran en las
plantas. Algunos de ellos son la morfina y la
nicotina. Algunas aminas son biolgicamente
importantes como la adrenalina y la
noradrenalina.
Las aminas secundarias que se encuentran en
las carnes y los pescados o en el humo del
tabaco.
Estas aminas pueden reaccionar con los nitritos
presentes en conservantes empleados en la
alimentacin y en plantas, procedentes del uso
de fertilizantes, originando N-nitrosoaminas
secundarias, que son carcingenas.
You might also like
- Pandeo y PegasDocument3 pagesPandeo y PegasDavid Andrés Quezada EspinosaNo ratings yet
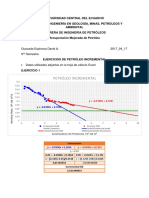
- Quezada David Incremental Oil-Screening EORDocument9 pagesQuezada David Incremental Oil-Screening EORDavid Andrés Quezada EspinosaNo ratings yet
- Antropocentrismo y BiocentrismoDocument6 pagesAntropocentrismo y BiocentrismoDavid Andrés Quezada EspinosaNo ratings yet
- Zero Routine Flaring by 2030Document2 pagesZero Routine Flaring by 2030David Andrés Quezada EspinosaNo ratings yet
- Sucker Rod LiftDocument16 pagesSucker Rod LiftDavid Andrés Quezada EspinosaNo ratings yet
- FÓRMULASDocument22 pagesFÓRMULASDavid Andrés Quezada EspinosaNo ratings yet
- ToolfaceDocument6 pagesToolfaceDavid Andrés Quezada EspinosaNo ratings yet
- Cover LetterDocument12 pagesCover LetterDavid Andrés Quezada EspinosaNo ratings yet
- Modelo EstructuralDocument10 pagesModelo EstructuralDavid Andrés Quezada EspinosaNo ratings yet
- Placa BombaDocument2 pagesPlaca BombaDavid Andrés Quezada EspinosaNo ratings yet
- Industria 4.0Document14 pagesIndustria 4.0David Andrés Quezada Espinosa100% (1)
- Industria 4.0Document2 pagesIndustria 4.0David Andrés Quezada EspinosaNo ratings yet
- EcotoxicologíaDocument6 pagesEcotoxicologíaDavid Andrés Quezada EspinosaNo ratings yet
- Pruebas de PresiónDocument2 pagesPruebas de PresiónDavid Andrés Quezada EspinosaNo ratings yet
- Reglamento Ambiental para Las Operaciones Hidrocarburíferas en El EcuadorDocument2 pagesReglamento Ambiental para Las Operaciones Hidrocarburíferas en El EcuadorDavid Andrés Quezada EspinosaNo ratings yet
- Operaciones de PescaDocument6 pagesOperaciones de PescaDavid Andrés Quezada EspinosaNo ratings yet
- Ajuste ControladoresDocument1 pageAjuste ControladoresDavid Andrés Quezada EspinosaNo ratings yet
- Tablas FluidosDocument178 pagesTablas FluidosDavid Andrés Quezada EspinosaNo ratings yet
- Multi PortDocument3 pagesMulti PortDavid Andrés Quezada EspinosaNo ratings yet
- Digital OilfieldDocument2 pagesDigital OilfieldDavid Andrés Quezada EspinosaNo ratings yet
- Cero AbsolutoDocument1 pageCero AbsolutoDavid Andrés Quezada EspinosaNo ratings yet
- SaeDocument4 pagesSaeDavid Andrés Quezada EspinosaNo ratings yet
- Ajuste ControladoresDocument1 pageAjuste ControladoresDavid Andrés Quezada EspinosaNo ratings yet
- Gráfica AccionesDocument2 pagesGráfica AccionesDavid Andrés Quezada EspinosaNo ratings yet
- Operaciones de PescaDocument6 pagesOperaciones de PescaDavid Andrés Quezada EspinosaNo ratings yet
- Iso IecDocument2 pagesIso IecDavid Andrés Quezada EspinosaNo ratings yet
- Operaciones de PescaDocument6 pagesOperaciones de PescaDavid Andrés Quezada EspinosaNo ratings yet
- Operaciones de PescaDocument6 pagesOperaciones de PescaDavid Andrés Quezada EspinosaNo ratings yet
- Gráficas FQDocument3 pagesGráficas FQDavid Andrés Quezada EspinosaNo ratings yet
- Quimica 2 Lab 5Document19 pagesQuimica 2 Lab 5Kasandra CallupeNo ratings yet
- Practica 1 Condensación AldolicaDocument12 pagesPractica 1 Condensación AldolicaAlfonsoNo ratings yet
- Cetonas: propiedadesDocument3 pagesCetonas: propiedadesdaniela alvarezNo ratings yet
- PC2 1°semestre Quimica LT 4°medio DiferenciadoDocument6 pagesPC2 1°semestre Quimica LT 4°medio Diferenciadocibercat-1No ratings yet
- Aldehidos y CetonasDocument12 pagesAldehidos y CetonasDaniel OrdoñezNo ratings yet
- Química OrgánicaDocument58 pagesQuímica OrgánicaGus EspNo ratings yet
- Resumen de Las AminasDocument3 pagesResumen de Las AminaszethNo ratings yet
- Algunas Pruebas de Aldehidos y CetonasDocument7 pagesAlgunas Pruebas de Aldehidos y CetonasJuan Jose Luna RamosNo ratings yet
- Aldehidos y CetonasDocument4 pagesAldehidos y CetonasAngelly PeñaNo ratings yet
- Facultad de Ciencias: Título de La Práctica de LaboratorioDocument7 pagesFacultad de Ciencias: Título de La Práctica de LaboratorioLaura Valentina Coral OcampoNo ratings yet
- Preguntasicfesdequmica PDFDocument79 pagesPreguntasicfesdequmica PDFKaren JulietaNo ratings yet
- Tarea 4 Quimica Organica Cilia BalantaDocument18 pagesTarea 4 Quimica Organica Cilia Balantajohn ortegaNo ratings yet
- Pruebas de identificación de aldehídos y cetonasDocument9 pagesPruebas de identificación de aldehídos y cetonasAdriana Melanie Bereches100% (1)
- Guia Quimica OrganicaDocument20 pagesGuia Quimica OrganicaSheylla M RamosNo ratings yet
- Evaluacion Tercer Periodo 10 y 11 2015Document15 pagesEvaluacion Tercer Periodo 10 y 11 2015Adriana EspinalNo ratings yet
- Quimica 4-2Document28 pagesQuimica 4-2Anonymous lNum6zyXGNo ratings yet
- Ácidos CarboxilicosDocument17 pagesÁcidos CarboxilicosKharín YaamNo ratings yet
- Práctica 6. Aldehídos y Cetonas PDFDocument6 pagesPráctica 6. Aldehídos y Cetonas PDFjuan camiloNo ratings yet
- Alcoholes: concepto, clasificación y nomenclaturaDocument5 pagesAlcoholes: concepto, clasificación y nomenclaturaGabriel TorresNo ratings yet
- Quita EsmalteDocument4 pagesQuita EsmalteLuis Rocha100% (1)
- Reacciones químicas de aldehídos y cetonasDocument2 pagesReacciones químicas de aldehídos y cetonasYonhy William Condori TiconaNo ratings yet
- Práctica #13 Alcoholes, Aldehidos y CetonasDocument45 pagesPráctica #13 Alcoholes, Aldehidos y CetonasElyajah Fernandez GonzalesNo ratings yet
- 2 Cetonas y Aldehidos - ResumenDocument23 pages2 Cetonas y Aldehidos - ResumenDaniela LSNo ratings yet
- Problemas CarbanionesDocument11 pagesProblemas CarbanionesStephanie MckenzieNo ratings yet
- 2) Guía de Ejercicios Aldehidos y CetonasDocument2 pages2) Guía de Ejercicios Aldehidos y CetonasFederico Andres OcampoNo ratings yet
- Grupos funcionales, isomería y nomenclatura orgánicaDocument99 pagesGrupos funcionales, isomería y nomenclatura orgánicaFernanda MoralesNo ratings yet
- Preinforme Práctica de Laboratorio de Química OrgánicaDocument26 pagesPreinforme Práctica de Laboratorio de Química OrgánicamariaNo ratings yet
- Síntesis de Ácido Cinámico A Partir de Ácido SuccinicoDocument6 pagesSíntesis de Ácido Cinámico A Partir de Ácido SuccinicoHerman Ruiz CalderinNo ratings yet
- Alcohol EsDocument14 pagesAlcohol Escristian lizarazoNo ratings yet
- Importancia cetonas industriaDocument2 pagesImportancia cetonas industriaAndres HernandezNo ratings yet