Professional Documents
Culture Documents
Absorcion
Uploaded by
Jonnthan SalasOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Absorcion
Uploaded by
Jonnthan SalasCopyright:
Available Formats
DETERMINACIN DE COBRE EN UNA MUESTRA PROBLEMA A PARTIR DE UNA SOLUCIN MADRE DE 1000PPM
DE COBRE
GIAN FRANCO OLIVIERI U. SECCIN 03
SUMARIO.
Para la determinacin de Cobre en una muestra problema mediante un anlisis de E.A.A, se hizo
necesario la realizacin de una curva de calibracin mediante la preparacin de 4 patrones partiendo de una
solucin madre de 1000ppm cobre, las concentraciones de estos patrones fueron de 1, 2, 4 y 5 ppm
sucesivamente, dado que en ese intervalo de concentraciones se garantiza la linealidad de la ley de Beer, una vez
medidas las absorbancias y construida la curva de calibracin, se obtuvo la siguiente ecuacin para dicha curva:
A 0,0007 0,0211C
Los datos presentan una correlacin lineal de 0,9978 aunque se observa que estos no se ajustan del todo
a una lnea recta como lo predice le ley de Beer, debido a errores generados por las desviaciones de esta ley.
Posteriormente se analiz la muestra problema luego de una dilucin, dando como resultado una
absorbancia de 0,049, con este valor y haciendo uso de la ecuacin de la curva se obtuvo el valor de la
concentracin de cobre en la muestra problema diluida, finalmente aplicando un factor de dilucin se obtiene la
concentracin real de Cobre en la muestra la cual es de
C cr = 9,1564 0,2079 ppm.
INTRODUCCIN
de ser absorbida y la potencia del mismo haz despus
La absorcin atmica es un mtodo de
determinacin
cuantitativa
de pasar por la muestra y ser absorbida parte de ella.
utilizado
Dicho fenmeno de absorcin atmica en llama
generalmente a la determinacin de elementos
obedece a la ley de Lambert-Beer la cual ser nuestro
metlicos.
Se dice que es un mtodo
punto de apoyo para realizar un anlisis cuantitativo del
cuantitativo ya que se deben usar fuentes
cobre en la muestra problema, junto con un conjunto de
separadas que emitan radiacin caracterstica
tcnicas analticas de espectroscopia de absorcin
del elemento que se va a determinar.
atmica.
La siguiente practica tiene como
objetivo la Determinacin de Cobre en una
Espectrofotometra de absorcin atmica en llama:
Se basa
en la absorcin
de radiacin
Muestra Problema a partir de una solucin
electromagntica por partculas atmicas presentes en
madre de 1000 ppm de Cobre, para ello nos
una llama. El proceso de absorcin se debe a que cada
apoyremos en el hecho de que los tomos en su
elemento tiene un nmero especfico de electrones
estado base o fundamental pueden absorber
asociados con su ncleo, llamado estado base a la
radiacin electromagntica a una frecuencia
configuracin orbital ms estable de un tomo.
dada, para luego establecer una relacin entre la
Ley de Lambert-Beer:
potencia del haz de la fuente de emisin antes
La concentracin de un analito es directamente
muy cerca del analito, de tal manera que su resolucin
proporcional a su absorbancia.
por el monocromador resulta imposible.
A = -log(P/Po) = .b.c (1)
Procesos que ocurren en la llama:
Otra causa de las interferencias es debida a la
presencia de productos de la combustin molecular que
poseen bandas de absorcin anchas o productos en
forma de partculas que dispersan la radiacin. Ambos
1.
2.
Nebulizacin: transforma la disolucin de
disminuyen la intensidad del haz transmitido y dan
la muestra en un aerosol constituido por
lugar a errores analticos positivos. Estas bandas de
diminutas gticas de lquido.
absorcin se conocen como Background o radiacin de
Desolvatacin: en esta etapa el disolvente
fondo y esto se corrige midiendo la absorbancia de un
se evapora para producir un aerosol
blanco.
molecular finamente dividido.
3.
Interferencias Qumicas:
Fusin: proceso mediante el cual el aerosol
se funde.
4.
5.
Se producen como consecuencia de diversos
Vaporizacin: conduce a la formacin de un
procesos qumicos que ocurren durante la atomizacin
gas.
por los siguientes factores:
Atomizacin: ocurre la disociacin de la
1.
disminuyen la velocidad de atomizacin. Como
molcula en un gas atmico.
6.
consecuencia se obtienen resultados bajos. Esta
Excitacin: por medio de la cual se pasan
interferencia se puede eliminar o atenuar usando
los tomos constituyentes del gas formado
temperaturas ms elevadas, o empleando agentes
en la etapa anterior a su nivel de energa
liberadores, que son cationes que reaccionan
ms alto, el cual va acompaado de una
preferentemente con la interferencia e impiden su
radiacin atmica.
7.
Formacin de compuestos de baja volatilidad, que
interaccin con el analito.
Ionizacin: mediante el cual el tomo
2.
Equilibrios de disociacin.
excitado forma iones y a su vez este
3.
Ionizacin en la llama.
proceso va acompaado de una radiacin
inica.
Una de las maneras de impedir la interferencia
qumica por concepto de ionizacin en la llama, se debe
a la adicin de un supresor inico, que proporciona una
Interferencias en E.A.A. llama:
Pueden ser de dos tipos: espectrales y
qumicas.
Interferencias espectrales:
Se producen cuando la absorcin de una
especie que interfiere se sobrepone o aparece
concentracin relativamente alta de electrones a la
llama; como consecuencia se evita la ionizacin del
analito.
Instrumental utilizado en E.A.A. llama:
Las partes principales de un espectrofotmetro
de absorcin atmica en llama son:
1.
La fuente de radiacin, la cual emite el
espectro del elemento de inters, en nuestro
Instrumentos:
o
Espectrofotmetro de Absorcin
caso la lmpara de ctodo hueco, la cual
Atmica, marca: Perkin Elmer
consiste en un nodo de tungsteno y un
Modelo 3100, combustible:
ctodo cilndrico, sellado en un tubo de
Acetileno, Oxidante: Aire
vidrio lleno de un gas inerte como el Ar, a
una presin de 1-5 torr. El ctodo esta
Lampara de Ctodo Hueco marca:
Photrom Lamps
constituido con el metal cuyo espectro se
desea obtener.
2.
Celda de la muestra, siendo la misma la
llama.
3.
Monocromador,
el
cual
dispersa
emitida de la fuente y separa la lnea
suministrada por el tcnico de laboratorio, la
fin.
el
cual
es
un
Muestra Problema:
La muestra empleada en el anlisis, fue
espectral particular que se emplea para este
Detector,
misma
tubo
fotoelctrico, es decir una indicacin de
El
espectrofotmetro
utilizado
en
Cu
en
concentracin
METODOLOGA
corriente elctrica.
Registrador.
contena
desconocida.
fotomultiplicador que se basa en el efecto
5.
Solucin de Cu: concentracin: 1000
ppm, suministrada en el laboratorio.
las
distintas longitudes de onda de la luz que es
4.
Reactivos:
De una solucin madre de 1000 ppm de Cu
tomar 10 ml y diluirlos a 100 ml con agua
la
destilada.
prctica es uno de doble haz
La radiacin procedente de la lmpara de
Tomar de esa solucin alcuotas de 1, 2, 4 y 5
ctodo hueco se divide mecnicamente en
ml, y diluir cada una a 100 ml utilizando agua
dos haces, uno de los cuales pasa a travs
destilada.
de la llama y el otro fuera de ella. Un
Preparar el blanco (matriz de correccin)
espejo semiplateado, reconduce ambos
Calibrar el espectrofotmetro con el blanco
haces, por un mismo camino hacindolos
pasar
alternativamente
travs
monocromador y de all al detector
del
dos veces antes de comenzar a medir.
Una vez calibrado el equipo y ajustados los
parmetros correspondientes al elemento a
analizar, se mide la absorbancia tanto del
PARTE EXPERIEMENTAL
blanco como de cada una de las soluciones
patrn,
registrando
correspondientes.
RESULTADOS EXPERIMENTALES
los
valores
TABLA 1: Datos de absorcin de soluciones patrones de Cu para la construccin de la curva de calibracin.
CONCENTRACIN (PPM)
1,00 0,012
2,00 0,013
4,00 0,047
5,00 0,060
?
ABS
0,0202
0,045
0,086
0,105
0,049
SD
0,0005
0,0012
0,0020
0,0016
0,0012
TABLA 2: Concentracin de Cu en la Muestra Problema
CONCENTRACIN DE COBRE EN LA MUESTRA PROBLEMA (PPM)
9,1564 0,2079
DISCUSIN DE RESULTADOS
fundamental que puedan absorber la radiacin y
proporcionalmente disminuir la concentracin obtenida.
Para
la
determinacin
de
la
concentracin de Cobre en una muestra
problema por medio de la Espectroscopia de
Absorcin Atmica en Llamas se sigue el
mtodo de la construccin de una Curva de
Calibracin Absorbancia Vs Concentracin a
partir de cuatro soluciones patrn de 1, 2, 4 y 5
Las desviaciones estndar proporcionadas por
el equipo fueron bajas por lo que se garantiza una buena
medicin de la absorbancia en los patrones, las
desviaciones se le pueden atribuir tambin a la falta de
exactitud al preparar las soluciones, ya sea por errores
humanos o de tipo instrumental, puesto que los equipos
de medicin proporcionan cierto error.
ppm respectivamente; se escoge ese intervalo de
concentraciones
ya
que
se
garantiza
la
linealidad de la ley de Beer en dicho rango.
Se obtuvo la siguiente ecuacin para la
curva de calibracin:
A 0,0007 0,0211C
Los datos presentan una correlacin
lineal muy buena de 0,9978 aunque se observa
Posteriormente se analiz la muestra problema
luego de una dilucin, dando como resultado una
absorbancia de 0,049, con este valor y haciendo uso de
la ecuacin de la curva se obtuvo el valor de la
concentracin de cobre en la muestra problema diluida,
finalmente aplicando un factor de dilucin se obtiene la
concentracin real de Cobre en la muestra la cual es de
que estos datos no se ajustan del todo a una
lnea recta como lo predice le ley de Beer,
C cr = 9,1564 0,2079 ppm.
debido a errores generados por las desviaciones
de esta ley.
Una posible causa de error es posible
que se vean influidos los valores de absorbancia
por interferencias por ionizacin es decir que
ocurre en parte ionizacin del analito y por lo
tanto existen menos tomos en su estado
Debido a que no se cuenta con un valor de
concentracin real de la muestra problema no es posible
comparar el valor obtenido con un valor terico.
CONCLUSIONES
lo predice le ley de Beer, debido a errores
generados por las ligeras desviaciones de esta ley.
Por medio de la espectroscopia atmica se
pudo determinar cuantitativamente y en
forma sencilla, la concentracin de Cobre
en una muestra problema por lo cual se
puede decir que la espectroscopia atmica
La concentracin de Cobre en la muestra problema
determinada por el mtodo absorcin atmica en
llama es de 9,1564 0,2079 ppm.
es un mtodo efectivo para determinar
BIBLIOGRAFA
cuantitativamente dicho elemento.
La
curva de calibracin presenta la
HARRIS,
Daniel. Anlisis Qumico Cuantitativo.
Grupo Editorial Iberoamrica, 1.992.
siguiente ecuacin:
A 0,0007 0,0211C
Los datos presentan una correlacin lineal
de 0,9978 aunque se observa que estos no
se ajustan del todo a una lnea recta como
HOBART H WILLARD. Mtodos Instrumentales de
Anlisis Cuarta edicin. Editorial Continental.
SKOOG, WEST. Anlisis Instrumental. Cuarta Edicin
Mc Graw Hill. 1994
ANEXOS
Clculos Tpicos:
Concentracin de los Patrones:
C p1
Csm .V1.V3
(1000 ppm).(10ml ).(1ml )
1 ppm
C p1
(100ml ).(100ml )
V2 .V4
De manera anloga se procede con los dems patrones.
Concentracin de la Muestra Problema Diluida:
De la Grfica de Absorcin Vs. Concentracin de los patrones se obtiene la siguiente ecuacin para la
curva de calibracin:
A = 0,0007 + 0,0211*C
Cuya correlacin es de 0,9978, la cual no se ajusta del todo a una lnea recta, por lo que se presentan
desviaciones a la Ley de Beer.
Para un valor de absorbancia en la muestra problema de 0,049, y de la ecuacin anterior, se tiene que la
concentracin de Cobre en la muestra problema diluida es la siguiente:
C cr = 2,2891 ppm
Para hallar la concentracin real de cobre en la muestra problema se multiplica por el factor de dilucin:
Cc r 2,2891 pm.
100ml
9,1564 ppm
25ml
Clculo de error mximo de cada solucin patrn:
C pi
donde:
C sm .V1 .V3 C sm V1 .V3 C sm .V1 .V3 C sm .V1 .V3 .V2 C sm .V1 .V3 .V4
V2 .V4
V2 .V4
V2 .V4
V22 .V4
V2 .V42
Cpi = Error por dilucin en cada solucin patrn (ppm).
Csm = Error Concentracin de Solucin Madre, se puede tomar como1 ppm.
V1= Tolerancia de la pipeta usada en la 1ra Alcuota (ml).
V2= Tolerancia Matraz usado para enrasar la 1ra Dilucin (ml).
V3= Tolerancia de la pipeta usada en la 2da Alcuota (ml).
V4= Tolerancia Matraz usado para enrasar la 2da Dilucin (ml)
C p1
(1 ppm).(10ml ).(1ml ) (1000 ppm).(0,023ml ).(1ml ) (1000 ppm).(10ml ).(0,007 ml )
(100ml ) 2
(100ml ) 2
(100 ml ) 2
(1000 ppm).(10ml ).(1ml ).(0,08ml ) (1000 ppm).(10ml ).(1ml ).(0,08ml )
(100ml ) 3
(100ml ) 3
0,0119 ppm
anloga se procede con los dems patrones.
Error en la determinacin de la concentracin de la muestra problema diluida:
x= y/m
donde:
y = Error al medir la Absorbancia (incertidumbre del espectrofotmetro, igual a 0.001).
0,001
0,0474
0,0211
De manera
La concentracin de la muestra problema diluida, est dada por:
C mpd 2,2891 0,0474 ppm
Error en la concentracin de la muestra problema (real):
C mp
C mp
C mpd .V6
V5
C mpd * V6
V5
C mpd * V6 * V5
(V5 ) 2
(0,0474 ppm).(100ml ) (2,2891 ppm).(0,08ml ) (2,2891 ppm).(100m).(0,03ml )
( 25ml )
( 25ml )
(25ml ) 2
C mp 0,2079 ppm
Finalmente la Concentracin de Cobre en la Muestra Problema es: C mp 9,1564 0,2079 ppm
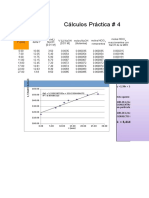
Grficos:
y = 0,0211x + 0,0007
0,12
R = 0,9987
0,1
0,08
0,06
0,04
0,02
0
0
Grfico 1. Absorbancia vs Concentracin (ppm)
You might also like
- Cálculos Práctica SaponificaciónDocument2 pagesCálculos Práctica SaponificaciónJonnthan SalasNo ratings yet
- Cuadros y Figuras Editados ResultadosDocument12 pagesCuadros y Figuras Editados ResultadosJonnthan SalasNo ratings yet
- HeurísticasDocument8 pagesHeurísticasJonnthan SalasNo ratings yet
- Proyecto OE PDFDocument3 pagesProyecto OE PDFAlbertoNo ratings yet
- Cálculos Práctica SaponificaciónDocument2 pagesCálculos Práctica SaponificaciónJonnthan SalasNo ratings yet
- Ejemplo Cancelación de SeguroDocument1 pageEjemplo Cancelación de SeguroBairon Ibarra PuertaNo ratings yet
- El ProblemaDocument2 pagesEl ProblemaJonnthan SalasNo ratings yet
- Tesis QuipuscoDocument139 pagesTesis QuipuscojoseNo ratings yet
- Acetona PDFDocument10 pagesAcetona PDFJonnthan SalasNo ratings yet
- Características Simulador Modular-Simultaneo o HibridoDocument7 pagesCaracterísticas Simulador Modular-Simultaneo o HibridoJonnthan SalasNo ratings yet
- DFDocument18 pagesDFJuddy NeiNo ratings yet
- Presión de Vapor Vs TemperaturaDocument2 pagesPresión de Vapor Vs TemperaturaJonnthan SalasNo ratings yet
- Desarrollo de Modelos Cinéticos para Bioprocesos XantanoDocument471 pagesDesarrollo de Modelos Cinéticos para Bioprocesos XantanoAndrea BocanegraNo ratings yet
- Cinetica PH para DiscusionDocument37 pagesCinetica PH para DiscusionJonnthan SalasNo ratings yet
- Butanol 1 PDFDocument170 pagesButanol 1 PDFJonnthan SalasNo ratings yet
- POTENCIOMETRIADocument6 pagesPOTENCIOMETRIAJonnthan SalasNo ratings yet
- Cooling System For Propylene PolymerizatDocument11 pagesCooling System For Propylene PolymerizatJonnthan SalasNo ratings yet
- 8 5Document31 pages8 5Jonnthan Salas100% (1)
- Pre Informe 4 VertederosDocument6 pagesPre Informe 4 VertederosJonnthan SalasNo ratings yet
- Cat. HeterogeneaDocument18 pagesCat. HeterogeneaJonnthan SalasNo ratings yet
- Catalisis PDFDocument27 pagesCatalisis PDFJaime Coronado CarmonaNo ratings yet
- Clase 1 y 2Document67 pagesClase 1 y 2Jonnthan SalasNo ratings yet
- MichelleDocument1 pageMichelleJonnthan SalasNo ratings yet
- Conv. ForzadaDocument2 pagesConv. ForzadaJonnthan SalasNo ratings yet
- Absorción Atómica en LlamaDocument13 pagesAbsorción Atómica en LlamaJonnthan SalasNo ratings yet
- AbsorcionDocument7 pagesAbsorcionJonnthan SalasNo ratings yet
- Imforme Flujos CompresiblesDocument9 pagesImforme Flujos CompresiblesJonnthan SalasNo ratings yet
- Clase 7Document23 pagesClase 7Jonnthan SalasNo ratings yet
- Aspirina IiDocument11 pagesAspirina IiJonnthan Salas100% (1)
- 230-Reglamento de Infraestructura DeportivaDocument20 pages230-Reglamento de Infraestructura DeportivaNaly CQ0% (1)
- Transferencias de ingresos y trabajo asalariadoDocument16 pagesTransferencias de ingresos y trabajo asalariadoAni BarreraNo ratings yet
- Caso Titulos Valores Mercantil Miercoles 17Document9 pagesCaso Titulos Valores Mercantil Miercoles 17MarcialEduardoUrbinaMadridNo ratings yet
- La Mama y El m19Document17 pagesLa Mama y El m19sergio parraNo ratings yet
- Etica Social Definicion PDFDocument2 pagesEtica Social Definicion PDFSusanNo ratings yet
- Minuta Señor Notario de Fe Pública.Document3 pagesMinuta Señor Notario de Fe Pública.Giovanni JémioNo ratings yet
- Diciplina de La INPDocument229 pagesDiciplina de La INPDavid Lopez100% (2)
- 81 preguntas entrevista trabajoDocument4 pages81 preguntas entrevista trabajoLeydiArellanoNo ratings yet
- Entrevista Laclau - Del PostMarxismo Al Radicalismo DemocraticoDocument21 pagesEntrevista Laclau - Del PostMarxismo Al Radicalismo Democraticogalahad_tannhauser9981100% (1)
- Junta Revolucionaria de GobiernoDocument12 pagesJunta Revolucionaria de GobiernoErick FigueraNo ratings yet
- Marco TeoricoDocument4 pagesMarco TeoricoMicHael MayWeatherNo ratings yet
- EL ROMANTICISMO Exposición LenguaDocument5 pagesEL ROMANTICISMO Exposición LenguaVale UrregoNo ratings yet
- Contrato Multicanal Banca MóvilDocument3 pagesContrato Multicanal Banca MóvilJesús Sánchez LaynezNo ratings yet
- La Historia de La QuinaDocument11 pagesLa Historia de La QuinaCamila Ortiz AlvarezNo ratings yet
- Oprimidos y opresores: la lucha por la libertadDocument3 pagesOprimidos y opresores: la lucha por la libertadWagner RodriguesNo ratings yet
- Teoría ecológica de la Escuela de ChicagoDocument4 pagesTeoría ecológica de la Escuela de ChicagoDiana Retamal Vidal100% (1)
- Atta 9 Ev 01 TerminadoDocument7 pagesAtta 9 Ev 01 TerminadoGina CortesNo ratings yet
- 15-11-2014 Apoya Atención Ciudadana Con Carta de No Antecedentes Penales A Ciudadanos. B111468Document2 pages15-11-2014 Apoya Atención Ciudadana Con Carta de No Antecedentes Penales A Ciudadanos. B111468Guillermo Padrés ElíasNo ratings yet
- Flores Hernández ArianaDocument1 pageFlores Hernández ArianaUlises GamerNo ratings yet
- Tasas Municipales y Sustento TerritorialDocument16 pagesTasas Municipales y Sustento TerritorialmicaNo ratings yet
- Resumen Primer ParcialDocument11 pagesResumen Primer ParcialMaria Pía GarciaNo ratings yet
- Imperio Romano ResumenDocument10 pagesImperio Romano ResumenMarlyn CastroNo ratings yet
- 2022 Mof Azafata-MozoDocument2 pages2022 Mof Azafata-MozoelmosNo ratings yet
- Extracto Tarjeta de Crédito: Cupón de PagoDocument2 pagesExtracto Tarjeta de Crédito: Cupón de PagoJader Sair RangelNo ratings yet
- Diagrama - Procedimiento Adquisición y Bajas de ActivosDocument3 pagesDiagrama - Procedimiento Adquisición y Bajas de ActivosLuis ChuchónNo ratings yet
- Contrato de Derechos Litigiosos y HerencialesDocument4 pagesContrato de Derechos Litigiosos y HerencialesJESUS ORLANDO GODOY SARMIENTONo ratings yet
- Revista LAURA CREATIVA Calcetines Con El Método de 4 PasosDocument31 pagesRevista LAURA CREATIVA Calcetines Con El Método de 4 PasosDorina Andrei100% (1)
- Resumen Krugman de Vuelta A La Economia de La Gran DepresionDocument17 pagesResumen Krugman de Vuelta A La Economia de La Gran DepresionArnold Holguin Galeano100% (1)
- Soncillo Un Nombre y Una HistoriaDocument105 pagesSoncillo Un Nombre y Una HistoriaSANTIAGONo ratings yet
- Andrea, Mujer Trabajadora 2023Document2 pagesAndrea, Mujer Trabajadora 2023antonio paredesNo ratings yet