Professional Documents
Culture Documents
Unidad 3
Uploaded by
arthur59270 ratings0% found this document useful (0 votes)
342 views2 pagesEste documento contiene 16 problemas relacionados con la estructura de gases. Los problemas cubren temas como la velocidad cuadrática media, la velocidad promedio, la velocidad más probable, la distribución de Maxwell de velocidades, la presión ejercida por gases y la energía cinética de moléculas a diferentes temperaturas. El documento proporciona los fundamentos para comprender conceptos clave sobre el comportamiento de gases a nivel molecular.
Original Description:
estructura de gases
Original Title
UNIDAD 3
Copyright
© © All Rights Reserved
Available Formats
PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentEste documento contiene 16 problemas relacionados con la estructura de gases. Los problemas cubren temas como la velocidad cuadrática media, la velocidad promedio, la velocidad más probable, la distribución de Maxwell de velocidades, la presión ejercida por gases y la energía cinética de moléculas a diferentes temperaturas. El documento proporciona los fundamentos para comprender conceptos clave sobre el comportamiento de gases a nivel molecular.
Copyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
342 views2 pagesUnidad 3
Uploaded by
arthur5927Este documento contiene 16 problemas relacionados con la estructura de gases. Los problemas cubren temas como la velocidad cuadrática media, la velocidad promedio, la velocidad más probable, la distribución de Maxwell de velocidades, la presión ejercida por gases y la energía cinética de moléculas a diferentes temperaturas. El documento proporciona los fundamentos para comprender conceptos clave sobre el comportamiento de gases a nivel molecular.
Copyright:
© All Rights Reserved
Available Formats
Download as PDF, TXT or read online from Scribd
You are on page 1of 2
Asignatura: Fisicoqumica
Semestre : tercero
Docente: M.Sc..Arturo Espinoza M
UNIDAD 3. ESTRUCTURA DE GASES
1. Una caja cuadrada contiene He a 25C .si los tomos chocan con las paredes en forma
perpendicular a una razn de 4x1022 veces por segundo , calcule la fuerza y la presin
ejercida sobre la pared , dado que el rea de la pared mide 100cm2 y la velocidad de
los tomos es de 600 ms-1.
2. Calcule la energa cintica promedio de traslacin de una molcula de N2 y de 1 mol
de N2 a 20C.
3. A qu temperatura deben enfriarse los tomos de He para que tengan la misma vrms
que el O2 a 25C.
4. La crms del metano es 846ms-1 .cul es la temperatura del gas.
5. Calcule el valor de la crms de las molculas de ozono en la estratosfera, donde la
temperatura es de 250 K.
6. A qu temperatura tendrn los tomos de He el mismo valor que la crms de las
molculas de N2 a 25C.resuelva este problema sin calcular el valor de crms del N2.
7. Calcular la velocidad cuadrtica media, la velocidad promedio y la velocidad ms
probable de una molcula de oxigeno molecular a 300 K y 500 K .comparar con los
valores para el hidrogeno.
8. Calcular la energa correspondiente al mximo de la curva de distribucin de
energa.
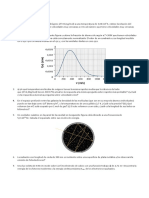
9. El siguiente figura muestra las curvas de distribucin de rapidez de maxwell de un
cierto gas ideal a dos temperatura diferentes (T1 yT2) .calcule el valor de T2.
Gestin: I/2016
Asignatura: Fisicoqumica
Semestre : tercero
Docente: M.Sc..Arturo Espinoza M
10. La cantidad ( )2 = 2 2 + 2 es el cuadrado de la desviacin de la rapidez
de una molcula de la rapidez promedio. Calcular el valor promedio de esta cantidad
empleando la distribucin de Maxwell, tomar luego la raz cuadrada del resultado para
obtener la raz de la desviacin cuadrtica media de la distribucin.
11. Las rapideces de 12 partculas (cm/s) son 0,5 1,5 1,8 1,8 1,8 1,8 2 2,5 3 3,5 y
4.Encuentre la rapidez promedio , la raz de la rapidez media cuadrtica y la rapidez
ms probable de esta partculas. Explique sus resultados.
12. En un recipiente que contiene gas, supngase que en un instante inicial cualquiera,
todas las molculas tienen la misma energa de traslacin 4x10-13 ergs. Con el
trascurso del tiempo el movimiento se hace catico y las energas se distribuyen
finalmente segn maxwell. a) calcular la temperatura final del sistema, b) Qu
fraccin de molculas se encuentra al final en el intervalo de energas 3,97x10-13 y
4,03x10-13 ergs.
13. Si 2,0 1023 tomos de argn (Ar) colisionan sobre 4,0 cm2 de pared por segundo a
un ngulo de 90 con respecto a la pared, cuando se mueven con una velocidad de 45
000 cm s1, qu presin (en atm) ejercen sobre la pared?
14. La velocidad raz cuadrtica media (vrcm) del CH4 es 846 ms1. Cul es la
temperatura del gas?
15. A cierta temperatura, la rapidez de seis molculas gaseosas en un recipiente son
2,0ms1; 2,2ms1; 2,6ms1; 2,7ms1; 3,3ms1 y 3,5ms1. Calcule la velocidad raz
cuadrtica media (crcm) y la velocidad promedio () de las molculas. Estos dos
valores promedio son cercanos uno al otro, pero el valor raz cuadrtico medio es
siempre el mayor. Por qu?
16. Calcule el valor de cmp para el C2H6 a 25 C. Cul es la razn del nmero de
molculas con velocidad de 989ms1 con respecto al nmero de molculas con
velocidad de cmp?
Gestin: I/2016
You might also like
- Guia Numero 1Document2 pagesGuia Numero 1eutectic1992No ratings yet
- TCM18Document10 pagesTCM18Manuel IgnacioNo ratings yet
- Teoria Cinetica de Los GasesDocument12 pagesTeoria Cinetica de Los GasesPame VerdezotoNo ratings yet
- Taller 1 Química Física III PDFDocument1 pageTaller 1 Química Física III PDFQueiroz PortorrealNo ratings yet
- Repartido 1Document2 pagesRepartido 1Jorge RodriguezNo ratings yet
- Teoría Cinética de GasesDocument2 pagesTeoría Cinética de GasesFernandoNo ratings yet
- Teoría Cinética de Los Gases 2023-I Parte 1Document12 pagesTeoría Cinética de Los Gases 2023-I Parte 1danielNo ratings yet
- Taller 5 Termodinamica - 2020 PDFDocument2 pagesTaller 5 Termodinamica - 2020 PDFJuan Esteban Franco Avila0% (1)
- GENERAL Tarea 2Document1 pageGENERAL Tarea 2YO MONo ratings yet
- Taller 1 CinéticaDocument7 pagesTaller 1 CinéticaBARBARA ZAMORA YUSTINo ratings yet
- Practica1 Ley de Graham OkDocument28 pagesPractica1 Ley de Graham OkHugo Cesar GNo ratings yet
- Problemas. Teoría Cinética de Los GasesDocument2 pagesProblemas. Teoría Cinética de Los GasesPablo HomovcNo ratings yet
- General Tarea 2Document1 pageGeneral Tarea 2Gabriel Andres Gomez CallaNo ratings yet
- Problemas Resueltos y Propuestos Energia Cinetica MolecularDocument3 pagesProblemas Resueltos y Propuestos Energia Cinetica MolecularMarco Antonio Pampa CondoriNo ratings yet
- Problemas Capitulo 11-Teoria Cinetica de Los GasesDocument4 pagesProblemas Capitulo 11-Teoria Cinetica de Los GasesRafael Quispe VelasquezNo ratings yet
- Problemas Tema III (Teoría Cinética de Los Gases)Document3 pagesProblemas Tema III (Teoría Cinética de Los Gases)Anonymous KCqm0c3No ratings yet
- Teoría Cinética de Los Gases EjerciciosDocument1 pageTeoría Cinética de Los Gases EjerciciosJorge Jara AvalosNo ratings yet
- Primer Taller Fisica de OndasDocument3 pagesPrimer Taller Fisica de OndasCarlos Ramos VillegasNo ratings yet
- Práctica 1 (Ley de Graham)Document5 pagesPráctica 1 (Ley de Graham)Hector CastilloNo ratings yet
- Taller - Estado Solido: para KDocument3 pagesTaller - Estado Solido: para KVarón JohanNo ratings yet
- QUÍMICADocument10 pagesQUÍMICACAROL JULIETH CHAVARRIA VALENCIANo ratings yet
- Tarea 4 TermoDocument15 pagesTarea 4 TermoAngel AcostaNo ratings yet
- Ejercicios y Problemas 1 - Propiedades de Los GasesDocument5 pagesEjercicios y Problemas 1 - Propiedades de Los GasesHeather NielsenNo ratings yet
- Conceptos de Teoría Cinético MolecularDocument16 pagesConceptos de Teoría Cinético MolecularivonneNo ratings yet
- Difusion y Mecanismos de DifusiónDocument81 pagesDifusion y Mecanismos de Difusiónalfredo1124100% (16)
- 3° Semana FQDocument4 pages3° Semana FQALFRED JHEFFERSON MENDOZA ATENCIONo ratings yet
- GEN Tarea 2Document1 pageGEN Tarea 2Daniel FeymanNo ratings yet
- Problemas Tema 1Document3 pagesProblemas Tema 1David CanoNo ratings yet
- DescarburizacionDocument8 pagesDescarburizacionsabato_No ratings yet
- Capítulo3 TEORÍA CINÉTICADocument2 pagesCapítulo3 TEORÍA CINÉTICAGalilea AcarapiNo ratings yet
- Conductividad Termica de Los Materiales y Ley de FourierDocument122 pagesConductividad Termica de Los Materiales y Ley de FourierCynthia NegreteNo ratings yet
- Problemas Resueltos Teoria Cinetico Molecular PDFDocument3 pagesProblemas Resueltos Teoria Cinetico Molecular PDFCleython Saenz CahuanaNo ratings yet
- 2 1Document3 pages2 1WALTER SUEL ARROYONo ratings yet
- Ejercicios Cinética Química Parte 02Document2 pagesEjercicios Cinética Química Parte 02ELMER CHAVEZ GONZALESNo ratings yet
- Teoria Cinentica de Los GasesDocument6 pagesTeoria Cinentica de Los GasesPatricio Eugenio Hinrichsen LippiNo ratings yet
- Problemas y Cuestiones EyMADocument21 pagesProblemas y Cuestiones EyMAInésDraaijerNo ratings yet
- Práctico 2 - 2016 - Estructura de Los GasesDocument2 pagesPráctico 2 - 2016 - Estructura de Los GasesCarlos J. F. ChoqueNo ratings yet
- Practica 1Document8 pagesPractica 1rest relaxNo ratings yet
- Taller 4 TermodinámicaDocument10 pagesTaller 4 TermodinámicaJuancho Morales50% (6)
- Informe Fisicoquimica 1Document11 pagesInforme Fisicoquimica 1PedroNo ratings yet
- Guía de Prácticos de Física II - Práctica v. 1.00 (Final)Document14 pagesGuía de Prácticos de Física II - Práctica v. 1.00 (Final)Valeria Laura Vera Escobar100% (1)
- Teorema de EquiparticiónDocument34 pagesTeorema de EquiparticiónC DiazNo ratings yet
- 1 PDFDocument10 pages1 PDFchrisNo ratings yet
- Taller 4.1 Termodinamica - 2019Document3 pagesTaller 4.1 Termodinamica - 2019Vane GomezNo ratings yet
- Cuad 1btoDocument28 pagesCuad 1btoJUANKARLOS70No ratings yet
- Exameng 19Document24 pagesExameng 19Carlos González- CobosNo ratings yet
- Deber de Velocidad y GramDocument5 pagesDeber de Velocidad y GramCris MuñozNo ratings yet
- Problemas de Velocidades MolecularesDocument2 pagesProblemas de Velocidades MolecularesyakimboNo ratings yet
- Practica #3 Lab FisicoquimicaDocument10 pagesPractica #3 Lab FisicoquimicaJUAN CARLOS CACERES BASILIONo ratings yet
- Hoja de Tarea 3 (Asignación)Document10 pagesHoja de Tarea 3 (Asignación)María Fernanda Sifontes0% (1)
- 02 Diapositiva de Modelo Cinético-Molecular Del Gas Ideal, Capacidades Caloríficas.Document20 pages02 Diapositiva de Modelo Cinético-Molecular Del Gas Ideal, Capacidades Caloríficas.EDINSON100% (1)
- CapI FisicaDocument3 pagesCapI FisicaPatricio SabettaNo ratings yet
- Manual de Prácticas de Laboratorio de Química AplicadaDocument44 pagesManual de Prácticas de Laboratorio de Química AplicadaCarlos ACNo ratings yet
- Teoria Cinetica de Los GasesDocument10 pagesTeoria Cinetica de Los GasesAldahir MarNo ratings yet
- Problemas Tema 1Document3 pagesProblemas Tema 1Carolina GonzalezNo ratings yet
- Teoria Fisica de Los GasesDocument5 pagesTeoria Fisica de Los GasesJhon RgbNo ratings yet
- Ingeniería química. Soluciones a los problemas del tomo IFrom EverandIngeniería química. Soluciones a los problemas del tomo INo ratings yet
- Tratamiento Termico2Document28 pagesTratamiento Termico2arthur5927No ratings yet
- BECERRIL ESPINOSA JOSE VENTURA Ecuaciones Diferenciales Tecnicas de Solucion y AplicacionesDocument252 pagesBECERRIL ESPINOSA JOSE VENTURA Ecuaciones Diferenciales Tecnicas de Solucion y AplicacionesMGDArmas33% (3)
- SolucionesExamenFinal 2013071625Document4 pagesSolucionesExamenFinal 2013071625arthur5927No ratings yet
- DesigualdadesDocument2 pagesDesigualdadesarthur5927No ratings yet
- Calculo II Santiago RelosDocument176 pagesCalculo II Santiago RelosHuarachi Herrera Josue100% (3)
- Tratamiento TermicoDocument26 pagesTratamiento Termicoarthur5927No ratings yet
- Industria de AlimentosDocument3 pagesIndustria de Alimentosarthur5927No ratings yet
- CalculoDocument3 pagesCalculoarthur5927No ratings yet
- Libro de Resumenes 7 Dic FinalDocument42 pagesLibro de Resumenes 7 Dic Finalarthur5927No ratings yet
- Conceptos Basicos TermodinamicaDocument23 pagesConceptos Basicos Termodinamicaarthur5927No ratings yet
- Salidaamarupp Umss 1 16 Entrenamiento 2016062108Document20 pagesSalidaamarupp Umss 1 16 Entrenamiento 2016062108arthur5927No ratings yet
- Modelado Matematico de PapalisaDocument22 pagesModelado Matematico de Papalisaarthur5927No ratings yet
- CalculoDocument3 pagesCalculoarthur5927No ratings yet
- Metodos GeofisicosDocument20 pagesMetodos Geofisicosarthur5927No ratings yet
- Presentacion Docentes 2017 (Parte I) OjoDocument40 pagesPresentacion Docentes 2017 (Parte I) Ojoarthur5927No ratings yet
- Introduccion A Transferencia de CalorDocument18 pagesIntroduccion A Transferencia de Calorarthur5927No ratings yet
- Obras Hidraulicas IIDocument311 pagesObras Hidraulicas IIMaria Cecilia Suarez Rubi100% (3)
- Matematica Aplicada III - I-2017Document13 pagesMatematica Aplicada III - I-2017arthur5927No ratings yet
- Manual Analisis de AlimentosDocument72 pagesManual Analisis de Alimentosarthur5927No ratings yet
- Formulación de Alimentos Mediante Programación Lineal y No LinealDocument4 pagesFormulación de Alimentos Mediante Programación Lineal y No Linealarthur5927100% (1)
- Guía de Manejo Ambiental para Proyectos de Perforación de Pozos de Petróleo y GasDocument217 pagesGuía de Manejo Ambiental para Proyectos de Perforación de Pozos de Petróleo y GasArmel López100% (2)
- Asignatura Biologia Mod ChakanaDocument1 pageAsignatura Biologia Mod Chakanaarthur5927No ratings yet
- Reglamento de Calidad DS 1499Document29 pagesReglamento de Calidad DS 1499arthur5927No ratings yet
- Balance de Masa 2 2015 Parte IDocument8 pagesBalance de Masa 2 2015 Parte Iarthur5927No ratings yet
- PROFOUNIBOLSOXLETDocument2 pagesPROFOUNIBOLSOXLETarthur5927No ratings yet
- CotizacionDocument4 pagesCotizacionarthur5927No ratings yet
- E Specific Chiller PCM 03Document1 pageE Specific Chiller PCM 03arthur5927No ratings yet
- Plazo Fijo LuisDocument5 pagesPlazo Fijo Luisarthur5927No ratings yet
- Laboratory Heaters Classic Apparatuses EsDocument7 pagesLaboratory Heaters Classic Apparatuses Esarthur5927No ratings yet
- Hortalizas en EscabecheDocument1 pageHortalizas en Escabechearthur5927No ratings yet
- Marco ReferencialDocument17 pagesMarco ReferencialElvis MariñoNo ratings yet
- Remoción en Masas en El PerúDocument17 pagesRemoción en Masas en El PerúEduardo AvilaNo ratings yet
- Notas Sobre El Nuevo EplanDocument160 pagesNotas Sobre El Nuevo EplanPepeNo ratings yet
- Pid Principios PDFDocument18 pagesPid Principios PDFRic OgamaNo ratings yet
- Sistema ElectoralDocument9 pagesSistema ElectoralOlatz Iglesias LeonNo ratings yet
- Gse Practice Terminado .XLSX - En.esDocument10 pagesGse Practice Terminado .XLSX - En.esGeancarlo Alexis villacorta FigueroaNo ratings yet
- Catenaria PDFDocument179 pagesCatenaria PDFJUAN PABLONo ratings yet
- (PI) UNE-EN - 13160-2 2016 - Comentarios E. Pajares PDFDocument57 pages(PI) UNE-EN - 13160-2 2016 - Comentarios E. Pajares PDFJOSE ALIRIO GARCIANo ratings yet
- Petzl - Acceso Por Cuerdas - Nivel 1Document171 pagesPetzl - Acceso Por Cuerdas - Nivel 1Joao Murrieta RattoNo ratings yet
- Tarea 18 - (U2) - Lorea Valdez Alejandra Guadalupe - 1255Document3 pagesTarea 18 - (U2) - Lorea Valdez Alejandra Guadalupe - 1255Alejandra Guadalupe Lorea ValdezNo ratings yet
- Tema 6: Sistema Operativo Windows. Operaciones Con Directorios o CarpetasDocument6 pagesTema 6: Sistema Operativo Windows. Operaciones Con Directorios o CarpetasJAVIER BORDONAU CARRASCOSANo ratings yet
- Composicion Quimica Del CementoDocument56 pagesComposicion Quimica Del Cementoomarcard92% (65)
- GUADAMUDDocument12 pagesGUADAMUDyajairavera91No ratings yet
- Practica IVDocument14 pagesPractica IVLaura MoujanNo ratings yet
- Reporte 1Document11 pagesReporte 1Luis Gabriel CadenasNo ratings yet
- Secuencia 2 Sep - WalshDocument12 pagesSecuencia 2 Sep - Walshmelany sanchezNo ratings yet
- Actividad 1 Origen de Los TerremotosDocument9 pagesActividad 1 Origen de Los TerremotosnikalmillateguiNo ratings yet
- Determinacion de Cu y Zinc en LatonDocument5 pagesDeterminacion de Cu y Zinc en LatonJesus GuillenNo ratings yet
- Sampa AlfabetoDocument14 pagesSampa AlfabetoNicolas PassarelliNo ratings yet
- Relación de Ejercicios de Electricidad 2º ESODocument5 pagesRelación de Ejercicios de Electricidad 2º ESOSantiago Morales AndresNo ratings yet
- Reglas Del Silogismo SimbólicoDocument2 pagesReglas Del Silogismo SimbólicoWellington HerediaNo ratings yet
- Taller Practico Algebra Matiricial PractticaDocument15 pagesTaller Practico Algebra Matiricial PractticaKaren Julieth DIAZ MORALESNo ratings yet
- Las Ecuaciones Diferenciales y Sus Aplicaciones en La IngenieriaDocument61 pagesLas Ecuaciones Diferenciales y Sus Aplicaciones en La IngenieriaDaniel TapiaNo ratings yet
- Modulo 5Document10 pagesModulo 5Anonymous g8BKOK6No ratings yet
- Linea de Tiempo, Evalucion de La Computadora.Document3 pagesLinea de Tiempo, Evalucion de La Computadora.Andrea EucedaNo ratings yet
- 7 QuimicaDocument16 pages7 QuimicaGustavo GaldosNo ratings yet
- 1°física - Clase 5 - (1T)Document3 pages1°física - Clase 5 - (1T)anacarolinaNo ratings yet
- Repuestos Calderas F-105Document2 pagesRepuestos Calderas F-105jose corrosionNo ratings yet
- Modelando Una Silla 3DDocument5 pagesModelando Una Silla 3DJose Jhonatan Gutierrez YangaliNo ratings yet
- Manual de Instrucciones GA30VSD PDFDocument132 pagesManual de Instrucciones GA30VSD PDFAnonymous WZXqWy2100% (1)