Professional Documents
Culture Documents
Guía Equilibrio Químico
Uploaded by
Arturo AlvarezOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Guía Equilibrio Químico
Uploaded by
Arturo AlvarezCopyright:
Available Formats
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
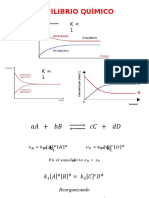
Equilibrio Qumico
RECUERDA QUE: el Equilibrio Qumico, se presenta cuando reacciones opuestas ocurren a
velocidades iguales. La velocidad a la que se forman los productos a partir de los reactivos es
igual a la velocidad a la que se forman los reactivos a partir de los productos. LAS
CONCENTARCIONES DEJAN DE CAMBIAR.
EJERCICIO 1. Escribe las expresiones de la constante de equilibrio Kc, en cada una de
las siguientes reacciones.
RECUERDA QUE: De acuerdo a la ley de accin de masas, que expresa la relacin entre las
concentraciones de los productos y los reactantes, se tiene:
+ +
(Recuerda que la ecuacin qumica debe estar balanceada)
[] []
[] []
(El subndice de c de la K, indica que se utilizan concentraciones expresadas en unidades de molaridad)
a) H2(g) + I2(g)
2 HI(g)
[]
[ ] [ ]
b) Cd+2 (ac) + 4 Br
CdBr42- (ac)
(ac)
[ ]
[+ ] [ ]
c) 2Ag(s)+ Zn2+(ac)
2 Ag+(ac)
=
+ Zn (s)
[+ ]
[+ ]
RECUERDA QUE: En reacciones heterogneas, la expresin de la constante Kc, no aparecen las
sustancias que se encuentran en estado slido y estado lquido.
Pgina 1 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
RECUERDA QUE: el valor de la constante de equilibrio solo depende de la estequiometra de la
reaccin y no de su mecanismo.
EJERCICIO 2.Para el equilibrio
2 SO3 (g)
2 SO2 (g) + O2(g)
La Kc es 4,08 .10-3 a 1000 K. Calcule el valor de Kp
En este ejercicio se pide convertir Kc (cte. de equilibrio calculada a partir de las concentraciones) a Kp, esta
relacin est dada por (cte. de equilibrio calculada a partir de las presiones de cada gas)
= ( )
n = (Moles de productos gaseoso) ( moles de reactantes gaseoso)
R= constante de los gases= 0,0821 L. atm/mol. K
T= temperatura en K
Reemplazando en la ecuacin
K p = 4,08 103 (0,082
1000K)(32)
K p = 4,08 103 (82)(1)
K p = 0,33
Para exigencias de este curso, Kc y Kp se considerarn como expresiones adimensionales.
Si K>>1 (K muy grande), significa que el equilibrio est desplazado a la derecha, por lo tanto
predominan los productos.
Si K<<1 (K muy pequea), significa que el equilibrio est desplazado a la izquierda, por lo tanto
predominan los reactivos.
EJERCICIO 3. Se determin que una disolucin acuosa de cido actico tiene las
siguientes concentraciones de equilibrio a 25C; [HC2H3O2]=1,65.10-2 M; [H+]=5,44.104
M; y [C2H3O2-]=5,44.10-4M. Calcule la constante de equilibrio Kc para la ionizacin del
cido actico a 25C. La reaccin es:
H+(ac) + C2H3O2- (ac)
HC2H3O2 (ac)
Antes de realizar algn clculo se debe balancear la ecuacin si esta no se encontrara balanceada.
En este caso, la ecuacin se encuentra balanceada.
Kc =
[H+ ] [C2 H3 O2 ]
[HC2 H3 O2 ]
Pgina 2 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
Reemplazando los datos entregados en el ejercicio se tiene:
Kc =
[5,44 104 M] [5,44 104 M]
[1,65 102 M]
K c = 1,79 105
EJERCICIO 3. A 523 K las concentraciones de PCl5, PCl3 y Cl2 en equilibrio para la
reaccin
PCl5 (g)
PCl3 (g) + Cl2 (g)
Son 0,809M, 0,190 M y 0,190M, respectivamente. Calcule a esa temperatura:
a) Las presiones parciales de las tres especies en el equilibrio.
b) La constante Kp de la reaccin.
Considerando la ecuacin de los gases ideales:
PV= nRT
P=
nRT
V
P = [ ]RT
Los [
] significan concentracin, expresada en mol/L.
Entonces reemplazando, se calcula la presin parcial para cada una de las especies que participan en esta
reaccin qumica:
a)
PPCl5 = [0,809 moles L1 ] 0,082 atm L K1 mol1 523 K
PPCl5 = 34,7 atm.
PPCl3 = [0,190 moles L1 ] 0,082 atm L K 1 mol1 523 K
PPCl3 = 8,15 atm.
PO2 = [0,190 moles L1 ] 0,082 atm L K1 mol1 523 K
PO2 = 8,15 atm.
Conociendo los valores de las presiones parciales de cada uno de los gases, se puede calcular la constante
de equilibrio en funcin de las presiones.
b)
La expresin de la constante de equilibrio Kp segn la ecuacin balanceada es
Pgina 3 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
PCl5 (g)
PCl3 (g) + Cl2 (g)
PPCl3 PCl2
PPCl5
Kp =
Reemplazando los valores de las presiones parciales:
Kp =
8,15 atm 8,15 atm
34,7 atm
K p = 1,91
La parte a) lo puedes resolver, tambin, tomando en cuenta que las concentraciones molares de cada gas,
son los moles del gas en un litro.
Para calcular la presin parcial del PCl5 con una concentracin de 0,809 M, debes comenzar diciendo que hay
0,809 moles en un litro de solucin y reemplazando en la ecuacin de los gases ideales, se tiene:
5= 0,809 0,082
523 = 34,7
EJERCICIO 3. En un recipiente de 5 litros se introducen 1,84 moles de nitrgeno y 1,02
moles de oxgeno. Se calienta el recipiente hasta 2000C establecindose el equilibrio:
N2 (g) + O2 (g)
NO (g)
En estas condiciones reacciona el 3% del nitrgeno existente. Calcule:
a) El valor de Kc a 2000C
b) La presin total en el recipiente, una vez alcanzado el equilibrio.
a)
Balanceando la ecuacin se tiene:
N2 (g) + O2 (g)
2 NO (g)
Por lo tanto la expresin de la constante de equilibrio:
Kc =
N2
Moles Iniciales
1,84
Moles que reaccionan
1,84 . (3/100) = 0,055 *
Moles formados
Moles en el equilibrio
1,84 0,055 = 1,785
[ ] en el equilibrio
1,785 mol/5L =0,357 M
*Solo reacciona el 3%
[NO]2
[N2 ] [O2 ]
O2
1,02
0,055
1,02-0,055= 0,965
0,965mol/5L=0,193M
NO
0
0
2. 0,055=0,11
0,11
0,11mol/5L=0,022
Pgina 4 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
Kc =
[0,022]2
[0,357] [0,193]
K c = 7,02 103
RECUERDA QUE: siempre en la expresin de Kc, van escritas las concentraciones molares NO los
moles.
Tambin podras haberlo resuelto, comenzando con calcular la molaridad para el N2 y el O2, y
luego calcular el 3%.
b)
Para calcular la presin total que hay en el recipiente, cuando se ha alcanzado el equilibrio se necesita
calcular el nmero total de moles en el equilibrio
Nmero total de moles en el equilibrio = 1,785 + 0,965 + 0,11 = 2,87
Ptotal =
2,87mol 0,082 atm L K 1 mol1 2273 K
5L
P = 106,9 atm
EJERCICIO 4. En una vasija que tiene una capacidad de 3 litros se hace el vaco y se
introducen 0,5 gramos de H2 y 30 gramos de I2. Se eleva la temperatura a 500 C,
establecindose el siguiente equilibrio:
I2 (g) + H2 (g)
HI(g)
El valor de Kc es 50. Calcula:
a) Moles de HI que se han formado una vez que se alcanza el equilibrio
b) Moles de I2 presentes en el equilibrio.
a)
Antes de realizar algn clculo, se debe balancear la ecuacin
I2 (g) + H2 (g)
2HI (g)
De acuerdo a los datos entregados en el problema, para poder calcular los moles de HI, se debe calcular en
primer lugar la cantidad de moles iniciales de cada especie que est reaccionando.
Calculando los moles iniciales para I2 e H2 se tiene:
n (mol) =
masa (g)
MM (
mol
Moles
Moles
Moles
Moles
30 gramos
Para I2
moles de I2 =
Para H2
moles de H2 =
Iniciales
que reaccionan
formados
en el equilibrio
254
gramos
mol
= 0,118 moles de I2
0,5 gramos
2
gramos
mol
= 0,25 moles de H2
I2
0,25
-x
H2
0,118
-x
0,25-x
0,118-x
HI
0
0
+2x
2x
Pgina 5 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
[ ] en el equilibrio(*)
(0,25-x)/3
(0,118-x)/3
2x/3
RECUERDA QUE: el nmero de X restadas, est relacionada con el coeficiente estequiomtrico de
los reactantes. (es una X porque hay un mol de I2).
Escribiendo la expresin de la constante de equilibrio
[HI]2
Kc =
[H2 ] [I2 ]
Reemplazando el valor de Kc para esta reaccin que es 50 y conociendo la concentracin en el equilibrio (*),
se tiene
[2x/3]2
50 =
[(0,25 x)/3] [(0,118 x)/3]
50 =
4x 2 /9
(0,25x)(0,118x)
9
50
(0,25 x) (0,118 x) 4x2
=
9
9
50 (0,03 0,37x + x 2 ) = 4 x 2
1,5 18,5x + 50 2 = 4 2
46 2 18,5x + 1,5 = 0
Para saber resolver, se necesita usar la ecuacin cuadrtica
x=
b b 2 4ac
2a
ax 2 + bx + c = 0
Reemplazando:
=
18,5 (18,5)2 4 46 1,5
2 46
x=
18,5 342,25 276
92
x=
18,5 8,13
92
x = 0,11 moles
x = 0,29 moles
Pgina 6 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
La solucin x=0,29 no sirve porque no tiene sentido que reaccionen ms moles de los que hay. Por lo tanto
la cantidad de moles formados de HI son
2 x = 2 0,11 = 0,22 moles de HI
a)
Los moles de I2 presentes en el equilibrio est dado por 0,118 x, por lo tanto son 0,118-0,11 = 0,008
moles.
EJERCICIO 5. En un recipiente de 1 litros y a una temperatura de 800C, se alcanza el
siguiente equilibrio:
CH4 (g) + H2O (g)
CO (g) + 3H2 (g)
a) Calcule el nmero de moles en el equilibrio para todas las especies, considerando la
siguiente tabla con datos.
b) Calcule la constante de equilibrio Kp
Moles Iniciales
Variacin n moles al
alcanzar el equilibrio
Moles en el equilibrio
CH4
2,0
H2O
0,5
-0.4
CO
H2
0,73
0,4
a) Lo primero es escribir la expresin de la constante y luego esquematizar las concentraciones en el
equilibrio a partir de los moles en equilibrio.
Kc =
[CO] [H2 ]3
[CH4 ] [H2 O]
Si reaccionan 0,4 moles de H2O y la relacin es 1:1 entre el CH4 y el H2O entonces la cantidad de moles de
CH4 que reacciona son tambin 0,4 moles.
Ahora calculando la cantidad de moles formados de H2, se tiene:
1 mol de CO
3 mol de H2
0,4 mol de CO
x mol de H2
x = 1,2 moles de H2
Moles Iniciales
Variacin n moles al
alcanzar el equilibrio
Moles en el equilibrio
CH4
2,0
-0,4
H2O
0,5
-0.4
CO
0,4
H2
0,73
1,2
0,4
Considerando que inicialmente se disponan de 0,73 moles de H2 inicialmente para conocer la cantidad de
moles de H2 en el equilibrio son: 0,73 + 1,2 = 1,93 moles de H2
Moles Iniciales
Variacin n moles al
CH4
2,0
-0,4
H2O
0,5
-0.4
CO
0,4
H2
0,73
1,2
Pgina 7 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
alcanzar el equilibrio
Moles en el equilibrio
[ ] M en el equilibrio
(2,0-0,4)=1,6
1,6/1
(0,5-0,4)=0,1
0,1/1
0,4
0,4/1
1,93
1,93/1
Ya conociendo todos los valores del nmero de moles para cada especie se calcula la constante de equilibrio
Kc usando la concentracin molar para cada una de las especies de esta reaccin qumica.
Kc =
[CO] [H2 ]3
[CH4 ] [H2 O]
[0,4mol/1L] [1,93mol/L]3
Kc =
[1,6mol/1L] [0,1mol/1L]
K c = 17,97
Esta es la constante de equilibrio considerando las concentraciones en el equilibrio, pero se pide calcular Kp,
para eso se sabe que
K P = K c (R T)n
n = (moles gaseoesos totales de producto) (moles gaseosos totales de reactantes)
n = (3 + 1) (1 + 1)
n = 2
K P = 17,97 (0,082 1073)2
K p = 1,4 105
EJERCICIO 6. En un recipiente de 10 litros, se hacen reaccionar, a 450 C, 0,75 moles
de H2 y 0,75 moles de I2, segn la ecuacin
H2 (g)
+ I2(g)
2HI(g)
Sabiendo que a esa temperatura Kc=50, calcule en el equilibrio:
a) El nmero de moles de H2, I2 y de HI.
b) La presin total en el recipiente y el valor de Kp.
Datos R= 0,082 atm.L.K-1.mol-1
a) Se debe calcular el nmero de moles de todas especies de esta reaccin qumica para eso se tiene:
Moles Iniciales
Moles que reaccionan
Moles formados
Moles en el equilibrio
[ ] en el equilibrio(*)
H2
0,75
x
0,75-x
(0,75-x)/10
I2
0,75
x
0,75-x
(0,75-x)/10
HI
0
0
2x
2x
2x/10
Pgina 8 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
Escribiendo la expresin de la constante de equilibrio para sta reaccin:
Kc =
[HI]2
[H2 ] [I2 ]
Reemplazando los valores de concentracin en el equilibrio, y el valor de la constante que es 50 se tiene:
2x 2
50 =
[ ]
10
0,75x
10
] [
0,75x
10
0,75 x
0,75 x
2x 2
50 [
] [
]=[ ]
10
10
10
0,75 x
0,75 x
5[
] [
] = 0,2x 2
1
1
5 (0,75 x) (0,75 x) = 0,2 x 2
5 (0,75 x) (0,75 x) = 0,2 x 2
5 ( 0,56 1,5x + x 2 ) = 0,2x 2
2,8 7,5x + 5x 2 = 0,2x 2
4,80x 2 7,5x + 2,8 = 0
Reemplazando en la ecuacin cuadrtica
x=
x=
b b 2 4ac
2a
7,5 7,52 (4 4,8 2,8)
2 4,8
x=
7,5 2,49
9,6
x1 = 0,94 ( no sirve)
x2 = 0.61
De los dos valores que se tiene para x, al compararlos con los valores de los moles iniciales, el x1, no sirve
pues no pueden reaccionar ms moles de los que reaccionan inicialmente.
Por lo tanto, el nmero de moles en equilibrio es:
Moles Iniciales
Moles que reaccionan
Moles formados
H2
0,75
x
-
I2
0,75
x
-
HI
0
0
2x
Pgina 9 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
Moles en el equilibrio
[ ] en el equilibrio(*)
0,75-0,61=0,14
(0,75-0,61)/10
0,75-0,61=0,14
(0,75-0,61)/10
2.0,61=1,22
2.0,61/10
Para calcular la presin total en el recipiente, es necesario calcular el nmero total de moles en el recipiente
N total de moles en el equilibrio = 0,14+0,14+1,22= 1,5 moles
Para calcular la presin total en el equilibrio se utiliza la ecuacin general de los gases donde:
P=
P=
nRT
V
1,5 moles 0,082atm L K 1 mol1 (450 + 273)K
10 L
P = 8,9 atm
El valor de Kp se calcula reemplazando en:
= ( )
K p = 50 (0,082 (450 + 273))(2(1+1))
K p = 50 (0,082 (450 + 273))(2(1+1))
K p = 50 (0,082 (450 + 273))(2(1+1))
K p = 50 (0,082 (450 + 273))(0)
K p = 50 1
K p = 50 = K c
EJERCICIO 7. En un reactor se tiene 2,1.10-3mol/L de HI puro, a una temperatura de
490C, establecindose el siguiente equilibrio:
2HI (g)
H2 (g)
Donde la constante de equilibrio
yoduro de hidrgeno (HI).
+ I2 (g),
es igual a 0,022. Determine el % de disociacin del
RECUERDA QUE: el % de disociacin de una sustancia es la relacin entre los moles que se
disocia de la sustancia y los moles iniciales multiplicado por 100.
% disociacin =
moles disociados
100
moles iniciales
Pgina 10 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
La disociacin de la molcula HI es para que se formen los productos H2 e I2, como es una reaccin de
equilibrio, no todo el reactante se disocia; esto significa que al alcanzar el equilibrio las tres sustancias (HI,
H2 e I2) coexisten.
HI
2,1. 10-3
(2,1. 10-3- 2x)
[ ] Inicial (moles/L)
[ ] en el equilibrio
(moles/L)
H2
0
x
I2
0
x
Para poder conocer el valor de x, que representa la concentracin de H2 e I2 en el equilibrio, se debe
reemplazar en la expresin de la constante de equilibrio para sta reaccin
Kc =
0,022 =
[H2 ] [I2 ]
[HI]2
xx
[(2,1 103 2x)]2
0,022 [(2,1 103 2x)]2 = x 2
0,022 (2,1 103 2x) (2,1 103 2x) = x 2
0,022 (4,41 106 8,4 103 x + 4x 2 ) = x 2
0,912x 2 + 1,85 104 x 9,07 108 = 0
Reemplazando en:
x=
x=
b b 2 4ac
2a
1,85 104 (1,85 104 )2 4 0,912 9,07 108
2 0,912
x=
1,85 104 3,42 108 + 3,54 107
1,824
x=
1,85 104 3,88 107
1,824
x=
1,85 104 6,2 104
1,824
x=
4,35 104
1,824
x = 2,3 104
Pgina 11 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
Como la disociacin de HI es 2x, quiere decir que los moles/L disociados de HI corresponden a 2 . 2,4.10-4,
esto es igual a 4.8.10-4 moles/L., por lo tanto el porcentaje de disociacin es:
% disociacin =
4,8 104
100
2,1 103
% disociacin = 23%
EJERCICIO 8. Prediga el efecto de aumentar la concentracin del reactivo subrayado
en cada una de las reacciones siguientes y para cada uno de los reactivos en el
equilibrio:
a)
CH4(g) + 2O2(g)
b)
2SO3(g)
CO2(g) + 2H2O(g)
2SO2(g) + O2(g)
RECUERDA QUE: El principio de Le Chatelier indica que: si un sistema que se encuentra en
equilibrio, se somete a una modificacin o es perturbado (cambio de presin, temperatura, o
concentracin de uno de los componentes), el sistema reaccionar desplazndose en el sentido
de compensar el cambio introducido.
a)
b)
Si en sta reaccin ocurre un aumento de la concentracin de uno de los reactantes como O2, de
acuerdo al principio de Le Chatelier, el equilibrio se desplazar hacia la derecha (de manera de
disminuir la concentracin de O2) o sea hacia los productos de manera de contrarrestar la
perturbacin producida.
En esta reaccin se produce un aumento de la concentracin de uno de los productos como O2, por
lo que el equilibrio se desplazar hacia la izquierda, o sea hacia el lado de los reactantes.
Siempre que aumentes la concentracin de un reactivo o producto el equilibrio se desplazar en sentido
contrario para compensar dicha cambio.
EJERCICIO 9. A temperaturas cercanas a 800C, el vapor que pasa por el coque (una
forma de carbono que se obtiene a partir del carbn) reacciona para formar CO 2 y H2:
C (s)
H2O (g)
CO2 (g)
H2 (g)
La mezcla de gases resultantes es un combustible industrial muy importante llamado
gas de agua.
a) A 800C la constante de equilibrio para esta reaccin es Kp=14,1. Cules son las
presiones parciales de equilibrio de H2O, CO y H2 en la mezcla de equilibrio a esta
Pgina 12 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
temperatura si comenzamos con carbono slido y 0,100 molde H2O en un recipiente
de 1,0 Litro.
b) Cul es la cantidad mnima de carbono necesaria para alcanzar el equilibrio bajo
estas condiciones?
c) Cul es la presin total de equilibrio en el recipiente?
d) Para producir la mxima cantidad de CO y H2 en el equilibrio es necesario
aumentar o disminuir la presin del sistema?.
a) Escribiendo la expresin de la constante de equilibrio Kp para esta reaccin es:
Kp =
PCO PH2
PH2O
Se debe determinar las presiones parciales de cada una de las especies de este sistema, lo primero ser
calcular la presin parcial de H2O a partir de la ecuacin general de los gases, ya que se conocen los moles
iniciales de H2O, para esto se tiene:
P=
PH2 O =
nRT
V
0,10mol 0,082 L atm K 1 mol1 (800 + 273)K
1L
PH2 O = 8,8 atm
C*
H2O
CO
H2
Presin Inicial (atm)
8,8
0
0
Presin
en el
8,8 -x
x
x
equilibrio (atm)
* No aparecen datos de presin en el equilibrio para esta sustancia, debido a que C, se encuentra en estado
slido y no aparece en la expresin de la constante de equilibrio.
Como un dato del ejercicio se entrega el valor de Kp, por lo tanto reemplazando los valores de presiones
en el equilibrio se tiene:
Kp =
PCO PH2
PH2O
14,1=
x x
8,8 x
14,1(8,8 x) = x 2
124,1 14,1x = x 2
x 2 + 14,1x 124,08 = 0
Reemplazando en la ecuacin cuadrtica:
x=
x=
b b 2 4ac
2a
14,1 (14,1)2 4(1 124,08)
21
Pgina 13 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
x=
14,1 198,81 + 496,32
2
14,1 695,13
x=
2
x=
14,1 695,13
2
x=
14,1 26,36
2
x1 = 6,13 atm.
x2 = 40,46 atm.
El valor de x2 no sirve porque es un valor negativo e indicara una presin negativa.
Despus de obtener el resultado del x, reemplazamos y obtenemos los valores de presiones parciales en el
equilibrio para cada una de las sustancias.
C*
H2O
8,8
8,8 -6,13 = 2,67
Presin Inicial (atm)
Presin
en el
equilibrio (atm)
CO
0
6,13
H2
0
6,13
b) Para poder calcular la cantidad mnima de C(s) que debe reaccionar, se debe transformar la presin
parcial del H2O en nmero de moles, utilizando la ecuacin de los gases ideales.
P=
nRT
V
n=
n=
PV
RT
6,14atm 1L
0,082 atm L K 1 mol1 (800 + 273)K
n = 0,07 mol de H2 O
Sabiendo que:
C (s)
H2O (g)
CO2 (g)
H2 (g)
Si reaccionan 0,07 moles de H2O, y la relacin estequiometrica es 1:1, entonces la cantidad mnima de
moles a reaccionar ser de 0,07 moles; Ahora transformndolo en masa de C se tiene:
n(mol) =
masa (gr)
MM(
gr
mol
gr
masa (gr) = n(mol) MM(
)
mol
Pgina 14 de 15
Programa de Acceso Inclusivo, Equidad y Permanencia
PAIEP U. de Santiago
Qumica
masa (gr) = 0,07(mol) 12(
gr
)
mol
masa (gr) = 0,84 gramos de C
c) La presin total en el equilibrio ser igual a la suma de todas las presiones parciales en el equilibrio:
Ptotal = PH2 O + PCO + PH2
Ptotal = 2,67atm + 6,14atm + 6,14atm
Ptotal = 14,95 atm
d) De acuerdo con principio de Le Chatelier, si se disminuye la presin el sistema contrarrestar ste efecto
desplazando el equilibrio hacia donde exista el mayor nmero de moles gaseosos, que en este caso es en
el lado de los productos (2 moles gaseosos), por lo tanto la presin se debe disminuir para aumentar la
cantidad de moles de CO2 y H2 que se producen.
Responsables acadmicos
Comit Editorial PAIEP.
Referencias y fuentes utilizadas
Balocchi, E.; Boyssires, L.; Martnez, M.; Melo, M.; Ribot, G.; Rodrguez, H.; Schifferli, R.; Soto, H.
(2002). "Curso de Qumica General". (7a. ed.). Chile: Universidad de Santiago de Chile, Facultad de
Qumica y Biologa
Chang, R.; College, W. (2002). Qumica. (7a. ed). Mxico: Mc Graw-Hill Interamericana Editores
S.A.
Valdebenito, A.; Barrientos, H.; Villarroel, M.; Azcar, M.I.; Ros, E.; Urbina, F.; Soto, H. (2014).
Manual de Ejercicios de Qumica General para Ingeniera. Chile: Universidad de Santiago de Chile,
Facultad de Qumica y Biologa
T. Brown, E. Lemay, B. Bursten , C.Murphy; Quimica, La Ciencia Central; 11.ed, Pearson
Educacin.
Pgina 15 de 15
You might also like
- Principio de Le ChatelierDocument8 pagesPrincipio de Le ChatelierJose Quinde ZambranoNo ratings yet
- Trabajo de Investigación 18-07-2016 García Cruzatti Ariana 4 CDocument9 pagesTrabajo de Investigación 18-07-2016 García Cruzatti Ariana 4 CAriana GarciaNo ratings yet
- Ejercicios Cinetica y Equilibrio Quimico 2020Document3 pagesEjercicios Cinetica y Equilibrio Quimico 2020Katherine Esmeralda Correa MachareNo ratings yet
- Quimica Ejercicios Resueltos Soluciones 2º Bachillerato Equilibrio QuimicoDocument35 pagesQuimica Ejercicios Resueltos Soluciones 2º Bachillerato Equilibrio QuimicoMaría Victoria Arques GalianaNo ratings yet
- Quimica Ejercicios Resueltos Soluciones 2º Bachillerato Equilibrio QuimicoDocument35 pagesQuimica Ejercicios Resueltos Soluciones 2º Bachillerato Equilibrio QuimicoEvaMarie Chavarry100% (1)
- Equilibrio QuimicoDocument12 pagesEquilibrio Quimicojoaquin gomenzoroNo ratings yet
- EJERCICIOS DE EQUILIBRIO QUIMICO Modificado VirtualDocument20 pagesEJERCICIOS DE EQUILIBRIO QUIMICO Modificado Virtualkaneki kenNo ratings yet
- Auto Evaluacion de La Unidad 2Document10 pagesAuto Evaluacion de La Unidad 2Flor TinocoNo ratings yet
- Equilibrio Químico. Soluciones Ejercicios PDFDocument27 pagesEquilibrio Químico. Soluciones Ejercicios PDFManuel HuertaNo ratings yet
- E Boletin 1 Equilibrio Quimico - SelDocument4 pagesE Boletin 1 Equilibrio Quimico - SelMabel Lazo ArevaloNo ratings yet
- Seminario Ejercicios Equilibrio QuímicoDocument18 pagesSeminario Ejercicios Equilibrio QuímicopieroNo ratings yet
- Equilibrio Quimico 202 2016Document48 pagesEquilibrio Quimico 202 2016Anthony NuñezNo ratings yet
- 0equilibrio ResueltosDocument72 pages0equilibrio ResueltosDiego Andres AltamiranoNo ratings yet
- UNIDAD IV Semana 13 - EQUILIBRIO QUIMICODocument10 pagesUNIDAD IV Semana 13 - EQUILIBRIO QUIMICOOmar Isaac Villaverde LopezNo ratings yet
- Equilibrio Químico Ejercicios Resueltos y PropuestosDocument11 pagesEquilibrio Químico Ejercicios Resueltos y PropuestosDaniel Aguilar88% (8)
- QuimicaDocument53 pagesQuimicaAXspeechware DjkNo ratings yet
- Ejercicios EVAU Equilibrio-CinéticaDocument6 pagesEjercicios EVAU Equilibrio-CinéticaElRegresoDeXD 01No ratings yet
- SEMANA N°7 Equilibrio QuímicoDocument30 pagesSEMANA N°7 Equilibrio Químicomiguel c. s.No ratings yet
- 6 Calculos EstequiometricosDocument10 pages6 Calculos EstequiometricosEfren MendozaNo ratings yet
- EjerciciosequilibrioquimicoDocument14 pagesEjerciciosequilibrioquimicoalvaro100% (2)
- Trabajo en EquipoDocument23 pagesTrabajo en EquipoJose David Escalona GarateNo ratings yet
- Equilibrios y Acido-Base Tema 10Document40 pagesEquilibrios y Acido-Base Tema 10Mónica García GrandeNo ratings yet
- UD 6 Equilibrio Químico COMPLETODocument66 pagesUD 6 Equilibrio Químico COMPLETOEmmaNo ratings yet
- Equilibrio QuimicoDocument9 pagesEquilibrio QuimicoPEDRO AARON REY CHAVEZNo ratings yet
- Equilibrio QuimicoDocument26 pagesEquilibrio Quimicogacv0925No ratings yet
- Guia No 2 - Equilibrio QuimicoDocument2 pagesGuia No 2 - Equilibrio QuimicoPatricia FRANCO VEGANo ratings yet
- Equilibrio químicoDocument10 pagesEquilibrio químicoMatias Ignacio Zarate PiñeiroNo ratings yet
- Semana #3 Equilibrio QuímicoDocument15 pagesSemana #3 Equilibrio QuímicoJosue YuNo ratings yet
- Equilibrio Quimico Teoria EjerciciosDocument34 pagesEquilibrio Quimico Teoria EjerciciosVeronica ReyesNo ratings yet
- Equilibrio Cuestiones ProblemasDocument38 pagesEquilibrio Cuestiones ProblemasGonzalo Heijo100% (1)
- Trabajo 3.equilibrio QuímicoDocument3 pagesTrabajo 3.equilibrio QuímicoDennis Joseph Chuco BlancoNo ratings yet
- Constante de EquilibrioDocument59 pagesConstante de EquilibrioJader Enrique Mario MendozaNo ratings yet
- Problemas Resueltos Tema6Document10 pagesProblemas Resueltos Tema6Alejandra Rommy Vera CabreraNo ratings yet
- Equilibrio Químico - Ejercicios 2022 Version FinalDocument4 pagesEquilibrio Químico - Ejercicios 2022 Version FinalAyelen PerezNo ratings yet
- EQUILIBRIODocument35 pagesEQUILIBRIOmiguel buriticaNo ratings yet
- Equilibrio químico reacciones disolucionesDocument2 pagesEquilibrio químico reacciones disolucionesIvan EscobarNo ratings yet
- Equilibrio Químico: Factores que lo AfectanDocument28 pagesEquilibrio Químico: Factores que lo AfectanestefanoNo ratings yet
- 1b-Constante de EquilibrioDocument8 pages1b-Constante de EquilibrioVictor Alfredo Alvarado SanchezNo ratings yet
- Problemas Equilibrio Quimico 2018-1Document12 pagesProblemas Equilibrio Quimico 2018-1Jhon Aguilar MarrerosNo ratings yet
- Apuntes Equilibrio PDFDocument28 pagesApuntes Equilibrio PDFWendy TorresNo ratings yet
- Relación de Problemas 13. Equilibrio Químico. Ejercicios de SelectividadDocument6 pagesRelación de Problemas 13. Equilibrio Químico. Ejercicios de SelectividadJosé LuisNo ratings yet
- GUIA DE EJERCICIOS Equilibrio QuimicoDocument8 pagesGUIA DE EJERCICIOS Equilibrio QuimicoDavid AvilaNo ratings yet
- SESIÓN 3 Equilibrio QuímicoDocument15 pagesSESIÓN 3 Equilibrio QuímicoA.DNo ratings yet
- tpn7 EquilibrioDocument8 pagestpn7 EquilibrioEliana TorresNo ratings yet
- Edoc - Pub - Auto Evaluacion de La Unidad 2docxDocument10 pagesEdoc - Pub - Auto Evaluacion de La Unidad 2docxBryan Sait De León ReyesNo ratings yet
- Ingeniería química. Soluciones a los problemas del tomo IFrom EverandIngeniería química. Soluciones a los problemas del tomo INo ratings yet
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSFrom EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSRating: 4.5 out of 5 stars4.5/5 (7)
- Problemas resueltos de Hidráulica de CanalesFrom EverandProblemas resueltos de Hidráulica de CanalesRating: 4.5 out of 5 stars4.5/5 (7)
- Preparar y acondicionar elementos y máquinas de la planta química. QUIE0108: Operaciones básicas en planta químicaFrom EverandPreparar y acondicionar elementos y máquinas de la planta química. QUIE0108: Operaciones básicas en planta químicaRating: 3 out of 5 stars3/5 (2)
- HidrometalurgiaDocument13 pagesHidrometalurgiajazielmonarrezNo ratings yet
- Diagramas de VariaciónDocument28 pagesDiagramas de VariaciónArturo AlvarezNo ratings yet
- Tierras raras: características y aplicaciones (REEDocument16 pagesTierras raras: características y aplicaciones (REEJhonNo ratings yet
- MineriaDocument1 pageMineriaArturo AlvarezNo ratings yet
- MineralogiaDocument3 pagesMineralogiaArturo AlvarezNo ratings yet
- VentilaciónDocument2 pagesVentilaciónArturo AlvarezNo ratings yet
- ExammDocument3 pagesExammArturo AlvarezNo ratings yet
- ExammDocument3 pagesExammArturo AlvarezNo ratings yet
- Malla Curricular 2007 Secuencia IndivdualDocument1 pageMalla Curricular 2007 Secuencia IndivdualArturo AlvarezNo ratings yet
- Tipos de LixiviaciónDocument2 pagesTipos de LixiviaciónArturo Alvarez67% (3)
- ExammDocument3 pagesExammArturo AlvarezNo ratings yet
- Optativas de GeoDocument4 pagesOptativas de GeoArturo AlvarezNo ratings yet
- MineralogiaDocument3 pagesMineralogiaArturo AlvarezNo ratings yet
- Acci GamDocument3 pagesAcci GamArturo AlvarezNo ratings yet
- DensidadDocument8 pagesDensidadArturo AlvarezNo ratings yet
- HidrometalurgiaDocument14 pagesHidrometalurgiaArturo AlvarezNo ratings yet
- Malla Curricular 2007 Secuencia IndivdualDocument1 pageMalla Curricular 2007 Secuencia IndivdualArturo AlvarezNo ratings yet
- Formacion Del MagmaDocument12 pagesFormacion Del MagmaArturo AlvarezNo ratings yet
- ConvertidoresDocument17 pagesConvertidoresArturo AlvarezNo ratings yet
- Presentación 1Document10 pagesPresentación 1Arturo AlvarezNo ratings yet
- Serie MagmÁticaDocument9 pagesSerie MagmÁticaArturo AlvarezNo ratings yet
- Serie MagmÁticaDocument9 pagesSerie MagmÁticaArturo AlvarezNo ratings yet
- Serie MagmÁticaDocument9 pagesSerie MagmÁticaArturo AlvarezNo ratings yet
- Método de NicholasDocument4 pagesMétodo de NicholasArturo AlvarezNo ratings yet
- Trabajo Aplicativo ETDocument35 pagesTrabajo Aplicativo ETLEIDY LIZBETH SAAVEDRA ROSASNo ratings yet
- RESULTADOSDocument3 pagesRESULTADOSDALSY ALEJANDRA CHINCHE MEJIANo ratings yet
- Trabajo SOM05Document3 pagesTrabajo SOM05Jose Torres ToroNo ratings yet
- Humedales Aguajales Madre de DiosDocument244 pagesHumedales Aguajales Madre de DiosYakov Mario QuinterosNo ratings yet
- Manual Espectrofotómetro Smart Spectro - LaMotte (Español)Document89 pagesManual Espectrofotómetro Smart Spectro - LaMotte (Español)Romulo Aycachi Inga100% (1)
- Cuadro ComparativoDocument4 pagesCuadro ComparativoMariana PardoNo ratings yet
- Luisa Capetillo: la mujer socialistaDocument18 pagesLuisa Capetillo: la mujer socialistaKaren BenezraNo ratings yet
- Medidas de ResumenDocument28 pagesMedidas de ResumenJesus BaptistaNo ratings yet
- Inforne de Pasantías. Yudaivi BarazarteDocument34 pagesInforne de Pasantías. Yudaivi BarazarteYudaivi BarazarteNo ratings yet
- Exposición de CulombimetríaDocument23 pagesExposición de CulombimetríaFrank Pacheco100% (1)
- Cartilla médica con laboratorios y prestadores de PBADocument9 pagesCartilla médica con laboratorios y prestadores de PBACarla DelmonteNo ratings yet
- Dios es nuestro refugio y protectorDocument16 pagesDios es nuestro refugio y protectorNestor Enrique Ordoñez ArenasNo ratings yet
- 2 Biohuertos WEBDocument60 pages2 Biohuertos WEBIR CasianoNo ratings yet
- Medidas de manejo EDS PorvenirDocument12 pagesMedidas de manejo EDS PorvenirEco LicenciasNo ratings yet
- Plan combustible obras escalinatas HuancavelicaDocument6 pagesPlan combustible obras escalinatas HuancavelicaSaul Hitalo Quispe HuamaniNo ratings yet
- Planificación CRM IndigoDocument11 pagesPlanificación CRM IndigoatzirithNo ratings yet
- Informe Psicologico OrganizacionalDocument36 pagesInforme Psicologico Organizacionalantonella azucena salazarNo ratings yet
- Triptico Proteción AuditivaDocument2 pagesTriptico Proteción AuditivaAlejandra GomezNo ratings yet
- La Actualidad de La Acuicultura en El Perú y El MundoDocument17 pagesLa Actualidad de La Acuicultura en El Perú y El MundoBelmer Blanco EdquenNo ratings yet
- Materiales Resortes: Guía de referenciaDocument36 pagesMateriales Resortes: Guía de referenciaLuis Arnulfo PintoNo ratings yet
- Diario Emocional RosaDocument17 pagesDiario Emocional RosaMaria Fernanda0% (1)
- Laboratorio N°6 Sedimentación: I. ObjetivosDocument5 pagesLaboratorio N°6 Sedimentación: I. Objetivosghordi palomino villasanteNo ratings yet
- Removedor de Adhesivos AutomotricesDocument15 pagesRemovedor de Adhesivos AutomotricesIsrael CarrscoNo ratings yet
- Razonamiento Verbal 4to GradoDocument49 pagesRazonamiento Verbal 4to GradoZulema ApazaNo ratings yet
- Tipos de Analisis VolumetricosDocument5 pagesTipos de Analisis VolumetricosAngel Paul0% (1)
- Actitudes para Pensar, Sentir y Actuar de Una Forma Sistémica PDFDocument4 pagesActitudes para Pensar, Sentir y Actuar de Una Forma Sistémica PDFNereaNeNo ratings yet
- Empozoñamiento EscorpionicoDocument15 pagesEmpozoñamiento EscorpionicoMaria LauraNo ratings yet
- ComunitariaDocument22 pagesComunitariaNathaliPerezNo ratings yet
- Encuesta BioseguridadDocument10 pagesEncuesta BioseguridadDayanna NaranjoNo ratings yet
- Análisis Audiencia de Proceso Inmediato FinalDocument3 pagesAnálisis Audiencia de Proceso Inmediato FinalRuth Evelin Rocca AyquiNo ratings yet