Professional Documents
Culture Documents
Propiedades Termodinámicas de Etano
Uploaded by
RayB.QuispeColosCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Propiedades Termodinámicas de Etano
Uploaded by
RayB.QuispeColosCopyright:
Available Formats
Propiedades termodinmicas de etano
Por C. H. I. Berkeley, J. L. YALEITINn, O. y C. HIIRD (no socios)
Shell Development Company, San Fracisco, California
El creciente inters en lo profundo de refrigeracin de baja temperatura
fraccionamiento y las operaciones conexas hace deseable un conocimiento
preciso de las propiedades termodinmicas de hidrocarburos ligeros. En este
trabajo se aade etano a la lista de hidrocarburos ligeros para los que
termodinmico fiable propiedades estn disponibles
Dos estudios previos de las propiedades termodinmicas de etano tienen ha
publicado. (10) (14) La primera de estos es en alemn, los valores son
reportado en unidades mtricas, tabulaciones no estn incluidos, y la
temperatura se extiende slo a 250 F.. El segundo se considera que es poco
fiable en vista el hecho de que las entropas y las entalpas son incompatibles
con las derivados de mediciones de la capacidad de calor. Desde la publicacin
de estos papeles, cules son, cree que es ms reliabie han aparecido datos
volumtricos. (12) En vista de estos hechos, se decidi volver a evaluar las
propiedades termodinmicas de etano.
Fuentes de los Datos
constantes
El peso molecular de etano se tom como 30.068, el punto de hielo como
491.69 C, la constante de los gases como 10.7315 (lb./sq.i.) (Cu.f t.) / (Ib.
mol) ( R).. El nivel de referencia se conjunto. de manera que la entalpa y
entropa de etano slida son ambos cero .at 0 R.
Los valores de estado crtico eran elegido como Tc: 90.1 F., Vc = 0,0755
cq.ft./Ib., y Pc = 716 lb./sq.in.abs. Se eligi la temperatura crtica como la
experimental ms fiable valor; (2) (6) el volumen crtico se determin a partir
de la rectilnea de dimetro, sin tener en cuenta todas las determinaciones
experimentales; y la crtica la presin fue elegida como 716 lb./sq.in.
abdominales. (14) en lugar de 708: 3 ib./sri.in. (2) o 712 lb./sq.in (6)
nicamente en el inters de .consistencia con la ecuacin de estado que se
describe a continuacin.
presiones de vapor
Las presiones de vapor reportadas en la literatura (5) (6) (8) (11) (14) se
representaron como log P vs T, y una curva continua que pasa a travs de la
puntos. Esta curva podra representarse en todo el rango de 0,5 por ciento por
la siguiente ecuacin:
Los valores de presin de vapor utilizados en este el trabajo se calcula a partir
de esta ecuacin.
Densidades de lquido saturado eran tomadas de un grfico de los valores
tabulados de Plank y Kambeitz. (10) Esta tabla se compone de suavizados
datos de otros investigadores. (8) (9) volmenes de vapor saturado se
calcularon por medio de la Clapeyron la ecuacin de los calores latentes,
densidades de lquido, y
, calculadas por el ecuacin de presin de vapor.
Sobrecalentados volmenes de gas se calcularon por medio de la ecuacin de
Benedict, Webb, y Rubin. (3) datos volumtricos han aparecido desde las
constantes empricas fueron evaluados inicialmente, por lo que es aconsejable
volver a determinarlos. Las constantes utilizadas en esta compilacin se
calcularon para reproducir el comportamiento volumtrico del gas entre 100
F. y 460 F., y hasta 1.500 lb./sq.in.abs. solamente. No se ajustaron para
ajustarse presiones de vapor o calores latentes debajo la regin experimental,
ya que esta no se poda hacer sin disminuir la exactitud de los clculos
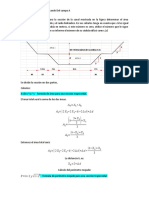
realizados en la regin gaseoso. La ecuacin usada es:
Donde:
d es la densidad en lb.mole / cu.ft., P est en lb./sq.in.abs. y T es en R.
Formas para la H-Ho y S-Tambin lo son para se encuentran en el documento
original. (3)
factores de compresibilidad calculan por el uso de la ecuacin se representaron
frente a la temperatura y la presin, la extrapolacin de ligeramente a 500 F.
A continuacin 100 , determinado experimentalmente composicin factores
de compresibilidad (1) (2) (14) tambin se representaron.
La comparacin mostr que la ecuacin podra ser utilizado para la
extrapolacin a la baja regin de temperatura para todas las presiones hasta
400 lb./sq.in.abs. Para presiones desde 400 lb./sq.in.abs. a la saturacin
suavizado de curvas se elaboraron a travs de los puntos experimentales. los
volmenes se calcularon a partir de vapor estas cartas de compresibilidad
suavizadas.
Capacidades de calor
capacidades calorficas son lquidos saturados disponible a partir del 15 K a la
crtica punto. (16) (17) capacidades de calor gaseosos se han medido a partir
de la punto de ebullicin a 100 C (4) Cero capacidades calorficas de presin
gaseosa calculados por mtodos estadsticos estn en buen acuerdo con los
derivados de la medicin experimental.
entalpas
entalpas de lquido saturado eran calculado por integracin grfica de los
datos de capacidad calorfica de Witt y Kemp (17) y por la conversin de la los
datos de entalpa de Wiebe, Hubbard y Brevoort (16) para B.t.u./lb. Cero
entalpas de presin de la el vapor se calcula mediante integracin de las
capacidades de calor evaluado a partir de la frecuencias fundamentales. (7)
(15)
Las frecuencias en cm-1 utilizados fueron: 827. (2) 993, 1170, (2) 1373, 1380,
1460, (2) 1465, (2) 2925, (2) 2960, (2) y 2980, (2) con un potencial de barrera
de 2750 cal./mole.
La correccin de la presin a entalpa se calcul utilizando la ecuacin de
estado. Cuando la ecuacin no lo hizo reproducir los volmenes, los calores se
calcularon mediante la integracin grfica:
You might also like
- Casos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSFrom EverandCasos de estudio de termodinámica: Solución mediante el uso de ASPENHYSYSRating: 4.5 out of 5 stars4.5/5 (7)
- Problemas de Geometría o Problemas Con La GeometríaDocument2 pagesProblemas de Geometría o Problemas Con La GeometríaHeidy Vásquez0% (1)
- Variables de Proceso2Document3 pagesVariables de Proceso2Manuel Dos SantosNo ratings yet
- Diagramas de Paridad UREA - Equipo 5Document11 pagesDiagramas de Paridad UREA - Equipo 5paola diazNo ratings yet
- Calor de Combustion de Acido BenzoicoDocument12 pagesCalor de Combustion de Acido BenzoicoDaniel Raydan67% (3)
- Taller 0-Unidades y Procesos de ConversionDocument5 pagesTaller 0-Unidades y Procesos de ConversionLuisDíasMarinNo ratings yet
- Problemas de Termodinámica IIDocument2 pagesProblemas de Termodinámica IIEdgar Enrique Muños CastroNo ratings yet
- Taller 2-Segundo Semestre de 2014Document3 pagesTaller 2-Segundo Semestre de 2014lolaNo ratings yet
- Como Calcular La Presión AtmosféricaDocument6 pagesComo Calcular La Presión AtmosféricaJorgeAlexanderBenaventeTiconaNo ratings yet
- Laboratorio Integral 4Document13 pagesLaboratorio Integral 4Analy NolascoNo ratings yet
- Preguntas de CrioscopíaDocument2 pagesPreguntas de CrioscopíaGina Gabriel VeraNo ratings yet
- Equilibrio de Fases en Sistemas de Un Componente 2012-1Document2 pagesEquilibrio de Fases en Sistemas de Un Componente 2012-1Van ArkNo ratings yet
- Instituto Politécnico Nacional Escuela Nacional de Ciencias BiológicasDocument8 pagesInstituto Politécnico Nacional Escuela Nacional de Ciencias BiológicasBertario Ríos GarcíaNo ratings yet
- R 11Document13 pagesR 11Damian PlascenciaNo ratings yet
- Informe 1Document4 pagesInforme 1Vanessa PelaezNo ratings yet
- Módulo 1-2C2015Document4 pagesMódulo 1-2C2015FranZsRomeroNo ratings yet
- (ASC) Examenes Parciales Labo Fiqui AI PDFDocument28 pages(ASC) Examenes Parciales Labo Fiqui AI PDFYanira CParedes100% (1)
- CALARIMETRIADocument8 pagesCALARIMETRIAJhoel Marcelo Vega CalaniNo ratings yet
- Laboratorio de Instrumentacion Por MaxiDocument10 pagesLaboratorio de Instrumentacion Por MaxiMaximo NuñezNo ratings yet
- Ley de HenryDocument7 pagesLey de HenryJuan Luis Ramírez AgudeloNo ratings yet
- Ley de BoyleDocument7 pagesLey de BoyleleumascossioNo ratings yet
- Parcial4 Publicar PDFDocument3 pagesParcial4 Publicar PDFJesus AguilarNo ratings yet
- Ley de AmontonsDocument4 pagesLey de AmontonsNury Palacios HolguinNo ratings yet
- Asignación #1 - Ene-Mar 2019Document3 pagesAsignación #1 - Ene-Mar 2019Joel SegoviaNo ratings yet
- Ley de AmontonsDocument3 pagesLey de Amontonsbrayan cardenas100% (1)
- Ejercicios Termo Bloque1Document4 pagesEjercicios Termo Bloque1Ulises Anleu Sevani0% (1)
- Guía 9 - MaxwelDocument2 pagesGuía 9 - MaxwelMatii VegaNo ratings yet
- Calidad Del VaporDocument5 pagesCalidad Del VaporGabriel MartinezNo ratings yet
- Equilibrio de Fases 2013-2Document2 pagesEquilibrio de Fases 2013-2matrixdolorisNo ratings yet
- Informe. Calor de CombustiónDocument6 pagesInforme. Calor de CombustiónJavier E. Verni BarruetaNo ratings yet
- TermometriaDocument24 pagesTermometriajulioNo ratings yet
- Taller 02 TermodinamicaDocument3 pagesTaller 02 Termodinamicasergio0% (2)
- Cuestionario #4Document20 pagesCuestionario #4raul rojas maldonadoNo ratings yet
- Propiedades Termodinamicas HelioDocument7 pagesPropiedades Termodinamicas Helioferchosb12No ratings yet
- Laboratorio Poder CaloríficoDocument12 pagesLaboratorio Poder CaloríficoJorge EsquerreNo ratings yet
- Boletin 1 PDFDocument3 pagesBoletin 1 PDFKaedarNo ratings yet
- Labo 1 FiquiDocument5 pagesLabo 1 FiquiFranco Airo Rey CordovaNo ratings yet
- Practica de Modelamiento y Simulacion de Procesos Ingenieria Quimica 8 Ciclo Viii CicloDocument3 pagesPractica de Modelamiento y Simulacion de Procesos Ingenieria Quimica 8 Ciclo Viii CicloPedro AlcantaraNo ratings yet
- Modelo de InformeDocument5 pagesModelo de InformeAle GorlaNo ratings yet
- 3 Capacidad Calorifica de Los GasesDocument30 pages3 Capacidad Calorifica de Los GasesyesiquisNo ratings yet
- Ejercicios-Unidades Utilizadas para Los Balances Energéticos.Document3 pagesEjercicios-Unidades Utilizadas para Los Balances Energéticos.compañia electricaNo ratings yet
- Laboratorio Ley de Amontons PDFDocument3 pagesLaboratorio Ley de Amontons PDFlosorioggm1965No ratings yet
- Unisim DesgnDocument13 pagesUnisim DesgnLourdes ArdónNo ratings yet
- Seminarios FisicoquimicaDocument41 pagesSeminarios FisicoquimicaAgustin GonzálezNo ratings yet
- Resumen Laboratorio TermodinamicaDocument13 pagesResumen Laboratorio TermodinamicaBrenda Angelica Alarcón TorresNo ratings yet
- Presion de VaporDocument7 pagesPresion de VaporManuel Alexander Huamán YánacNo ratings yet
- Trabajo Final de Termodinamica - GrupalDocument10 pagesTrabajo Final de Termodinamica - GrupalFelipe TrujilloNo ratings yet
- Gases Idea LesDocument2 pagesGases Idea Leselias8260508No ratings yet
- Heat Transfer IntercambiadoresDocument42 pagesHeat Transfer IntercambiadoresJUNIOR CCAIHUARI HOYOSNo ratings yet
- Tarea UDocument3 pagesTarea USamuel JesusNo ratings yet
- Determinacion Del Calor Específico de LiquidosDocument10 pagesDeterminacion Del Calor Específico de LiquidosAnamariaRoblesrivasNo ratings yet
- Guia de Lab - Ley de CharlesDocument7 pagesGuia de Lab - Ley de CharlesMaria JoseNo ratings yet
- Los Métodos de Diseño para Intercambiadores de Doble TuboDocument34 pagesLos Métodos de Diseño para Intercambiadores de Doble TuboEfrain Perez50% (2)
- Dimensionamiento de Un Intercambiador de Calor de Tubo y C Oraz A para Fluidos No Newtonianos Por Los Metodos de Kern y TinkerDocument11 pagesDimensionamiento de Un Intercambiador de Calor de Tubo y C Oraz A para Fluidos No Newtonianos Por Los Metodos de Kern y TinkerRomer Arrazola AponteNo ratings yet
- Práctica #4Document10 pagesPráctica #4latargus616No ratings yet
- Determinación Del Coeficiente de Dilatación Adiabática Del Aire en Condiciones Atmosféricas para La Ciudad de MedellínDocument7 pagesDeterminación Del Coeficiente de Dilatación Adiabática Del Aire en Condiciones Atmosféricas para La Ciudad de MedellínJuanda Amadeus100% (1)
- Termometria y Dilatación en SólidosDocument5 pagesTermometria y Dilatación en SólidosEric Bar LamasNo ratings yet
- Ley de BoyleDocument4 pagesLey de BoyleManuel GomezNo ratings yet
- Ingeniería química. Soluciones a los problemas del tomo IFrom EverandIngeniería química. Soluciones a los problemas del tomo INo ratings yet
- Criterios de Calidad de AlimentosDocument78 pagesCriterios de Calidad de AlimentosDaniel Alexander Ramirez Fernandez100% (2)
- Informe Técnico Almacen SSRDocument3 pagesInforme Técnico Almacen SSRRayB.QuispeColosNo ratings yet
- TornoDocument1 pageTornoRayB.QuispeColosNo ratings yet
- Cuestionario de Triaje Por Covid-19 Ficha de Sintomatologia TliDocument2 pagesCuestionario de Triaje Por Covid-19 Ficha de Sintomatologia TliRayB.QuispeColosNo ratings yet
- BASCDocument2 pagesBASCCRISTIAN CUBIDESNo ratings yet
- Criterios de Calidad de AlimentosDocument78 pagesCriterios de Calidad de AlimentosDaniel Alexander Ramirez Fernandez100% (2)
- CAPACITACION AlimDocument46 pagesCAPACITACION AlimRayB.QuispeColosNo ratings yet
- Charla MaquinasDocument1 pageCharla MaquinasRayB.QuispeColosNo ratings yet
- Trabajo Admi - V 2Document3 pagesTrabajo Admi - V 2RayB.QuispeColosNo ratings yet
- Matrices Entrada Plastiquisimos S.A.CDocument8 pagesMatrices Entrada Plastiquisimos S.A.CRayB.QuispeColosNo ratings yet
- Charla MaquinasDocument1 pageCharla MaquinasRayB.QuispeColosNo ratings yet
- Matrices Entrada Plastiquisimos S.A.CDocument8 pagesMatrices Entrada Plastiquisimos S.A.CRayB.QuispeColosNo ratings yet
- 18 Al 24 de JunioDocument7 pages18 Al 24 de JunioRayB.QuispeColosNo ratings yet
- Pasos para Implementar El PTSDocument30 pagesPasos para Implementar El PTSjdNo ratings yet
- Unido 2Document4 pagesUnido 2RayB.QuispeColosNo ratings yet
- ResumenDocument7 pagesResumenRayB.QuispeColosNo ratings yet
- Monitoreo OcupacionalDocument20 pagesMonitoreo Ocupacionaldiego llamoca pilpisNo ratings yet
- BRIGADAEVACUACIONDocument40 pagesBRIGADAEVACUACIONJulian Andrés Ferro ScarpettaNo ratings yet
- Avance de PlaniDocument2 pagesAvance de PlaniRayB.QuispeColosNo ratings yet
- Norma A.130 Requisitos de SeguridadDocument67 pagesNorma A.130 Requisitos de Seguridadclodobeo0% (1)
- Matriz Mio Analisis FodaDocument13 pagesMatriz Mio Analisis FodaRayB.QuispeColosNo ratings yet
- AdmDocument5 pagesAdmRayB.QuispeColosNo ratings yet
- Matriz Mio Analisis FodaDocument6 pagesMatriz Mio Analisis FodaJhon Kenner Rojas MorenoNo ratings yet
- PLANIDocument6 pagesPLANIRayB.QuispeColosNo ratings yet
- 44 VencenamelDocument2 pages44 VencenamelRayB.QuispeColosNo ratings yet
- DS 021 2009 VMA Descarga Agua Residu No DomesticDocument3 pagesDS 021 2009 VMA Descarga Agua Residu No DomesticTATITO0306091012No ratings yet
- PLANIDocument6 pagesPLANIRayB.QuispeColosNo ratings yet
- Matriz Mio Analisis FodaDocument6 pagesMatriz Mio Analisis FodaJhon Kenner Rojas MorenoNo ratings yet
- 493 1030 1 PBDocument12 pages493 1030 1 PBRayB.QuispeColosNo ratings yet
- Ponencia IPERC Base Ing. Frank Sinarahua Ab 2014 La Positiva Vida PDFDocument57 pagesPonencia IPERC Base Ing. Frank Sinarahua Ab 2014 La Positiva Vida PDFBam Bam D. Montalvan DiazNo ratings yet
- Coordenadas Normales y Tangenciales PDFDocument32 pagesCoordenadas Normales y Tangenciales PDFMaite ZuritaNo ratings yet
- Guia de Aprendizaje Nº18 Perimetro y Area de La CircunferenciaDocument4 pagesGuia de Aprendizaje Nº18 Perimetro y Area de La CircunferenciaAlfredo Jose Aaron CamargoNo ratings yet
- Angulos en El Plano y El EspacioDocument17 pagesAngulos en El Plano y El EspacioMichael FrankNo ratings yet
- C-3 CinematicaDocument46 pagesC-3 Cinematicaankatu05No ratings yet
- GUÍA GRÁFICAS FUNCIONES TRIGINOMÉTRICAS 2. (Tan y Cot)Document2 pagesGUÍA GRÁFICAS FUNCIONES TRIGINOMÉTRICAS 2. (Tan y Cot)Damián DazaNo ratings yet
- 2 - 4 Parametros Mecanicos y Textura de AlimentosDocument47 pages2 - 4 Parametros Mecanicos y Textura de AlimentosYuliza Lucio RoqueNo ratings yet
- 8 Densidad de RocasDocument6 pages8 Densidad de RocasAlex CalderonNo ratings yet
- Práctica 6 - ALUDocument11 pagesPráctica 6 - ALUMitzi Nyahn OrozcoNo ratings yet
- 2 - Taller Gráficos + FuncionesDocument12 pages2 - Taller Gráficos + FuncionesZuleika CamarenaNo ratings yet
- Proyecto Mecanismo Cortina Metalica CompletitoDocument76 pagesProyecto Mecanismo Cortina Metalica CompletitoCarlos Roberto GavarreteNo ratings yet
- Tabulacion CruzadaDocument11 pagesTabulacion CruzadaAlex Seña MurilloNo ratings yet
- Prueba DiagnosticaDocument3 pagesPrueba DiagnosticaEdu GoNo ratings yet
- Mec. de Mat. 1Document23 pagesMec. de Mat. 1Carlos cruz lealNo ratings yet
- Unidad #1 - Fisica - Magnitudes - UnidadesDocument6 pagesUnidad #1 - Fisica - Magnitudes - UnidadesMarian ElizabethNo ratings yet
- Práctica de Reforzamiento 6to GradoDocument4 pagesPráctica de Reforzamiento 6to GradoClaribel SanchezNo ratings yet
- Problemas de CircunferenciaDocument4 pagesProblemas de CircunferenciaJosé JoséNo ratings yet
- Guia Concrecion Curricular MatemáticaDocument25 pagesGuia Concrecion Curricular MatemáticaAriel Quispe100% (1)
- Analisis VectorialDocument11 pagesAnalisis VectorialMaicol Gutierrez MelendezNo ratings yet
- English Activity NumbersDocument3 pagesEnglish Activity NumbersromeroberriomariajoseNo ratings yet
- Solucion Taller Hidraulica de CanalesDocument5 pagesSolucion Taller Hidraulica de CanalesHernando Del campoNo ratings yet
- Practica 2 ResueltaDocument6 pagesPractica 2 ResueltaDavid Colmenarejo Camacho100% (3)
- Prueba Tercer Parcial - 1ro - Mate - 18 19Document3 pagesPrueba Tercer Parcial - 1ro - Mate - 18 19Ricardo ChimbaNo ratings yet
- Fisica IDocument5 pagesFisica IMauro Jesús Zambrana CastroNo ratings yet
- RSC TSHHKCSXTF TERCERODESECUNDARIALUNES05DEOCTUBREMATEMATICASDocument37 pagesRSC TSHHKCSXTF TERCERODESECUNDARIALUNES05DEOCTUBREMATEMATICASNorma BautistaNo ratings yet
- El Amortiguador Calculos.Document6 pagesEl Amortiguador Calculos.BrondonNo ratings yet
- PenduloDocument4 pagesPenduloBrayan RinconNo ratings yet
- Ciencia TeslaDocument34 pagesCiencia TeslaAlvaro Garrido GarciaNo ratings yet
- FACTORIZACIONDocument7 pagesFACTORIZACIONEli MacuriNo ratings yet
- Actividad4 EstadisticayprobabilidadDocument10 pagesActividad4 EstadisticayprobabilidadE-IONEXT MCNo ratings yet