Professional Documents
Culture Documents
Fico Tarea 1
Uploaded by
CristhianMoisesCuetoCalderon0 ratings0% found this document useful (0 votes)
34 views2 pagesFISICOQUIMICA -TECSUP
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentFISICOQUIMICA -TECSUP
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
34 views2 pagesFico Tarea 1
Uploaded by
CristhianMoisesCuetoCalderonFISICOQUIMICA -TECSUP
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 2
INTEGRATES.
Contreras Huamanahui, Jhon Carlos
Cueto Caldern, Cristhian Moiss
Luis Eslava, Jhana Noelia
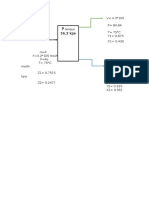
Problema nr:5
El tolueno (C7H8) es un hidrocarburo lquido muy importante en la
industria orgnica, utilizndose como disolvente, y tambin en la
fabricacin de tintes, colorantes, medicamentos y explosivos como el
TNT. Si cuando se quema un gramo de tolueno (C7H8) se desprenden 42,
5 kilojulios.
a) Cul ser el valor de su entalpa de combustin?
b) Calcula la entalpa estndar de formacin del tolueno, utilizando la
ley de Hess.
Entalpa estndar de formacin del CO2 (g): -393, 8KJ/mol
Entalpa estndar de formacin del H2O (liq): 285,8 KJ/mol.
Rapta: Hf0= +10.2 kJ/mol
a) Las entalpas de formacin del tolueno, dixido de carbono y agua
son las siguientes:
C + 4H2 C7H8
C + O2 CO2
H2 + 1/2O2 H20
H=+50.03 KJ/mol
H= -393.8 KJ/mol
H= -285.8 KJ/mol
Segn la Ley de Hess, la entalpa es una funcin de estado, slo
depende de los estados inicial y final, luego se pueden combinar las
reacciones (1), (2), y (3) para obtener la reaccin principal, haciendo
luego lo mismo con los valores de entalpas.
Si se invierte el sentido de la reaccin (1) y se le suman la (2)
multiplicada por 7 y la (3) por 4 lo mismo que se hace con las entalpas.
(C7H8 C + 4H2
7(C + O2 CO2
4 (H2 + 1/2O2 H20
H= -50.03 KJ/mol)
H= -393.8 KJ/mol)
H= -285.8 KJ/mol)
C7H8 + O2 CO2 +H2O H= -3949.84KJ/mol)
Reaccin exotrmica -3950.58
b) Calcula la entalpa estndar de formacin del tolueno, utilizando la
ley de Hess
C + 4H2 C7H8
H = 50.03 KJ/mol
C + O2 CO2
H = -393.8 KJ/mol
H2 + O2 H2O
H = -285.8 KJ/mol
C7H8 C+ 4H2
H = -50.03 KJ/mol
C + O2 CO2
H = -393.8 KJ/mol
H2 + O2 H2O
H = -285.8 KJ/mol
C7H8 C + 4H2
C + O2 CO2
4H2 + 2 O2 4H2O
C7H8+3 O2 CO2 + 4 H2O
H = -729.63Kj/mol
You might also like
- Cromatografia DiscusionesDocument2 pagesCromatografia DiscusionesCristhianMoisesCuetoCalderonNo ratings yet
- Desplazamiento HipsocromicoDocument1 pageDesplazamiento HipsocromicoCristhianMoisesCuetoCalderonNo ratings yet
- Calculos Paracetamol y IbuprofenoDocument2 pagesCalculos Paracetamol y IbuprofenoCristhianMoisesCuetoCalderonNo ratings yet
- Choc or Reccione SDocument3 pagesChoc or Reccione SCristhianMoisesCuetoCalderonNo ratings yet
- ClaseDocument20 pagesClaseCristhianMoisesCuetoCalderonNo ratings yet
- Calificacion de PasantiasDocument1 pageCalificacion de PasantiasCristhianMoisesCuetoCalderonNo ratings yet
- HV - Act. Promo Porta 2x1 - AbrilDocument5 pagesHV - Act. Promo Porta 2x1 - AbrilCristhianMoisesCuetoCalderonNo ratings yet
- Calculos Paracetamol y IbuprofenoDocument2 pagesCalculos Paracetamol y IbuprofenoCristhianMoisesCuetoCalderonNo ratings yet
- Análisis químico instrumental mediante espectroscopía de absorción atómicaDocument22 pagesAnálisis químico instrumental mediante espectroscopía de absorción atómicaCristhianMoisesCuetoCalderonNo ratings yet
- Análisis químico instrumental mediante espectroscopía de absorción atómicaDocument22 pagesAnálisis químico instrumental mediante espectroscopía de absorción atómicaCristhianMoisesCuetoCalderonNo ratings yet
- ClaseDocument20 pagesClaseCristhianMoisesCuetoCalderonNo ratings yet
- ClaseDocument1 pageClaseCristhianMoisesCuetoCalderonNo ratings yet
- Cuestionario y Conclusiones Lab 08Document5 pagesCuestionario y Conclusiones Lab 08CristhianMoisesCuetoCalderonNo ratings yet
- Copelacion 02-Fundamento TeoricoDocument5 pagesCopelacion 02-Fundamento TeoricoCristhianMoisesCuetoCalderonNo ratings yet
- Diagrama de Flujo de Benceno y ToluenoDocument1 pageDiagrama de Flujo de Benceno y ToluenoCristhianMoisesCuetoCalderonNo ratings yet
- Ana 1Document1 pageAna 1CristhianMoisesCuetoCalderonNo ratings yet
- CLASE 06 - Aplicación VolumétricaDocument38 pagesCLASE 06 - Aplicación VolumétricaCristhianMoisesCuetoCalderonNo ratings yet
- Análisis Simultáneo de Mezclas Binarias 2Document9 pagesAnálisis Simultáneo de Mezclas Binarias 2CristhianMoisesCuetoCalderonNo ratings yet
- Ana 1Document1 pageAna 1CristhianMoisesCuetoCalderonNo ratings yet
- Problemas CostosDocument3 pagesProblemas CostosCristhianMoisesCuetoCalderonNo ratings yet
- Ejerciciostermoquimica 2016Document4 pagesEjerciciostermoquimica 2016CristhianMoisesCuetoCalderonNo ratings yet
- Ejerciciostermoquimica 2016Document4 pagesEjerciciostermoquimica 2016CristhianMoisesCuetoCalderonNo ratings yet
- 61203Document63 pages61203goblin_red2No ratings yet
- Ejerciciostermoquimica 2016Document4 pagesEjerciciostermoquimica 2016CristhianMoisesCuetoCalderonNo ratings yet
- TRABAJOINVESTIGACIÓNDocument10 pagesTRABAJOINVESTIGACIÓNCristhianMoisesCuetoCalderonNo ratings yet
- Evaluación Lixiviación 40Document45 pagesEvaluación Lixiviación 40CristhianMoisesCuetoCalderonNo ratings yet
- INDICE Del ProyectoDocument1 pageINDICE Del ProyectoCristhianMoisesCuetoCalderonNo ratings yet
- 1-Informe de Metalurgia GeneralDocument12 pages1-Informe de Metalurgia GeneralAlicia WatsonNo ratings yet
- Convocatoria de Empleo Tecnicos Productos Paraiso Del Peru SacDocument1 pageConvocatoria de Empleo Tecnicos Productos Paraiso Del Peru SacCristhianMoisesCuetoCalderonNo ratings yet