Professional Documents
Culture Documents
SACAROSA
Uploaded by
Dania BaculimaOriginal Description:
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
SACAROSA
Uploaded by
Dania BaculimaCopyright:
Available Formats
Universidad De Cuenca
Facultad de Ciencias Químicas
Bioquímica y Farmacia
2. MOLÉCULA SACAROSA
Karina Ávila & Dania Baculima
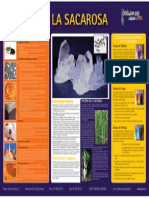
DESCRIPCIÓN BIOQUÍMICA: La sacarosa es un disacárido que habitualmente se la llama azúcar o
azúcar de mesa. Según Yurkanis (2012) menciona que la molécula de sacarosa se encuentra formado por una
glucosa, la cual aparece en forma de piranosa y una fructosa a modo de furanosa, unidas por un enlace
glucosídico entre el C-1 de la glucosa (en la posición α) y el C-2 de la fructosa (en la posición β). Es muy
soluble en agua debido a su polaridad y a la presencia de 8 grupos hidroxilos en su superficie.
Cuando se hidroliza la sacarosa por la acción de la enzima invertasa o se calientan sus soluciones a 110 – 145
ºC, sobretodo en presencia de ácidos se obtiene cantidades iguales de D-glucosa y D-fructosa. A más de 160
ºC se pueden producir reacciones de caramelización. Las abejas tienen enzimas que catalizan esta hidrólisis, lo
que les permite convertir sacarosa en miel. (Carey & Giuliano, 2014).
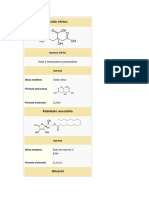
FORMULA CONDENSADA: C12H22O11 NOMBRES:
Fórmula condensada: C12H22O11
Nombre común: Sacarosa
IUPAC: (2R,3R,4S,5S,6R)-2-[(2S,3S,4S,5R)-3,4-
dihidroxi-2,5-bis(hidroximetil)oxolan-2-il]oxi-6-
(hidroximetil)oxano-3,4,5-triol
Nombre Sistemático: alfa-D-glucopiranosil(1->2)-
beta-D-fructofuranósido.
Estructura de la sacarosa. (Solíz, G. 2013)
ESTRUCTURA MOLECULAR ESPACIAL TIPO DE ENLACE
El enlace que une los dos monosacáridos es de tipo
O-glucosídico, este consiste en que uno de los
grupos hidroxilo (-OH) de cada molécula de
monosacárido, ha sido sustituido por un átomo de
oxígeno que ocupa los dos enlaces y se ha formado
una molécula de agua con los átomos de hidrógeno
y oxígeno sobrantes. (Carey, F. & Giuliano, R. 2014)
(Vladivostok, M. 2013).
SÍNTESIS QUÍMICA
La síntesis de la sacarosa se obtiene mediante la condensación de dos monosacáridos, la glucosa y fructosa,
liberando una molécula de agua.
Hart, Craine, Hart, & Hadad, 2007
FUNCIONES BIOQUÍMICAS: Es una de las moléculas energéticas por excelencia es decir, produce la
energía necesaria que el cuerpo necesita para que funcionen los diferentes órganos; Es el edulcorante más
utilizado para endulzar alimentos. El cerebro, por ejemplo, es responsable del 20% del consumo energético y
utiliza la glucosa como único substrato. Sin embargo, cuando el consumo es excesivo, produce una carga
glucémica elevada y está relacionada con enfermedades como la caries dental, la obesidad, sobrepeso y
diabetes mellitus. (Guerra, J. 2014)
BIBLIOGRAFÍA
Carey, F., & Giuliano, R. (2014). Química Orgánica. México: McGRAW-HILL/INTERAMERICANA.
Guerra, J. (2014). Bioquimica. Obtenido de http://libroelectronico.uaa.mx/index.html
Hart, H., Craine, L., Hart, D., & Hadad, C. (2007). Química Orgánica. Madrid: McGRAW-HIL
INTERAMERICANA DE ESPAÑA, S.A.U.
Klein, D. (2014). Química Orgánica. Madrid: Médica Panamericana.
Soliz, G. (s.f.). Saber más. Obtenido de https://www.sabermas.umich.mx/archivo/articulos/267-numero-
31/479-la-sacarosa-el-dulce-de-las-plantas.html
Vladivostok, M. (2013). Estructura espacial de la sacarosa. Obtenido de https://commons.ikimedia.
org/wiki/File:Dextran_ball-and-stick.png
Yurkanis, P. (2012). Quimica Orgánica. México: Pearson Education .
You might also like
- La SacarosaDocument1 pageLa SacarosaManuel Lozada GaytanNo ratings yet
- DISACARIDOS y PolisacaridosDocument20 pagesDISACARIDOS y PolisacaridosFiorella AlexandraNo ratings yet
- Medios de CultivoDocument8 pagesMedios de CultivoAndrea Cervantes QuiñonesNo ratings yet
- Exposicion Diapositivas Carbohidratos (Autoguardado)Document23 pagesExposicion Diapositivas Carbohidratos (Autoguardado)Elizabeth Clorinda Huaman EleraNo ratings yet
- Origen y Evolución de Las PlantasDocument9 pagesOrigen y Evolución de Las PlantasNicolle MuñozNo ratings yet
- Laboratorio Del AlmidonDocument10 pagesLaboratorio Del AlmidonAyleen CaqueoNo ratings yet
- Caracteristicas Generales Del Dominio ArchaeaDocument3 pagesCaracteristicas Generales Del Dominio ArchaeaJocy100% (1)
- FRUCTOSANASDocument5 pagesFRUCTOSANASAlejoRSolano50% (2)
- Glosario 2 M.o'sDocument4 pagesGlosario 2 M.o'sRafael GaribayNo ratings yet
- Alteracion y Adulteracion en Los AlimentosDocument13 pagesAlteracion y Adulteracion en Los AlimentosAracely Huaman DiazNo ratings yet
- Trabajo FernandaDocument7 pagesTrabajo FernandaSilvia MartinezNo ratings yet
- Informe Fermentacion - Tecnologia EnzimasDocument25 pagesInforme Fermentacion - Tecnologia EnzimasAndy Neciosup TapiaNo ratings yet
- Diapositivas BriofitasDocument15 pagesDiapositivas BriofitasELBERT ORDUZ67% (3)
- Estomas - Ficha de LaboratorioDocument16 pagesEstomas - Ficha de LaboratorioIsabella ArquinigoNo ratings yet
- La GlucogenesisDocument4 pagesLa GlucogenesisJonathan Paul Otoya BarturenNo ratings yet
- Marco Teórico PulmonesDocument2 pagesMarco Teórico PulmonesALeNo ratings yet
- Ciclopentano y CicloundecanoDocument3 pagesCiclopentano y Cicloundecanopedro gomez100% (1)
- Enlace GlucosidicosDocument5 pagesEnlace GlucosidicosGinger DiazNo ratings yet
- Funciones Del Agua en Los Seres VivosDocument18 pagesFunciones Del Agua en Los Seres VivosZoraida Daza AlcantaraNo ratings yet
- 2 Descomposición AlimentosDocument45 pages2 Descomposición AlimentosShirley MendozaNo ratings yet
- Carnes Rojas y BlancasDocument5 pagesCarnes Rojas y BlancasCarlos Noe Odar ArroyoNo ratings yet
- Informe de PolisacaridosDocument8 pagesInforme de Polisacaridosdany_289No ratings yet
- La Cristalización Es Un Proceso Típico de Laboratorio en El Que Un Sólido Cristalino en Solución Se Separa de Una Mezcla a Través de Cambios en Su Solubilidad La Disminución en Este Parámetro Conlleva a La ProducciónDocument3 pagesLa Cristalización Es Un Proceso Típico de Laboratorio en El Que Un Sólido Cristalino en Solución Se Separa de Una Mezcla a Través de Cambios en Su Solubilidad La Disminución en Este Parámetro Conlleva a La ProducciónAyrton Jimenez InfantesNo ratings yet
- Clasificación y Conclusiones ProtistaDocument4 pagesClasificación y Conclusiones ProtistaJowel V GuevaraNo ratings yet
- Informe S11 Lípidos Quimica SeminarioDocument11 pagesInforme S11 Lípidos Quimica SeminarioAlexander E. Bruckmann AvilaNo ratings yet
- Trabajo - El Acido CitricoDocument18 pagesTrabajo - El Acido CitricoEdgar C Medina100% (1)
- Introducción A Los CordadosDocument3 pagesIntroducción A Los CordadosMabelita SCNo ratings yet
- Laboratorio de Química SaponificaciónDocument6 pagesLaboratorio de Química SaponificaciónLeonardo GarciaNo ratings yet
- Bomba Sodio PotasioDocument2 pagesBomba Sodio PotasioGharts MedinaNo ratings yet
- Fermentación y RespiraciónDocument15 pagesFermentación y RespiraciónMariaNo ratings yet
- Disacaridos y Aldosas CetosasDocument3 pagesDisacaridos y Aldosas Cetosascheshireww0% (1)
- Glosario BioquímicaDocument4 pagesGlosario BioquímicaJuan BigotesNo ratings yet
- Importancia y Uso de La SacarosaDocument4 pagesImportancia y Uso de La SacarosaJoseph ZamoraNo ratings yet
- Clado ExcavataDocument4 pagesClado ExcavataMariajose MariajoseNo ratings yet
- Los Tejidos VegetalesDocument4 pagesLos Tejidos Vegetalescomparteciencia100% (2)
- Resumen Heterotrofos AerobiosDocument7 pagesResumen Heterotrofos AerobiosMarianela Del Río O.No ratings yet
- Extraccion de Proteinas de La LecheDocument6 pagesExtraccion de Proteinas de La LecheDaniel Guerra MartinezNo ratings yet
- Célula VegetalDocument6 pagesCélula VegetalCamila Traslaviña100% (1)
- Los TricomasDocument7 pagesLos TricomasdanielavjNo ratings yet
- Trabajo de Bioquimica Del YogurtDocument22 pagesTrabajo de Bioquimica Del Yogurtvalerio0% (1)
- Modelos Atómicos y Tabla PeriódicaDocument5 pagesModelos Atómicos y Tabla Periódicajhon pachecoNo ratings yet
- Informe 6 HISTOLOGIA VEGETAL 3Document9 pagesInforme 6 HISTOLOGIA VEGETAL 3Idyel T. CrisNo ratings yet
- Características de Clase CubozoaDocument4 pagesCaracterísticas de Clase CubozoaJuanita RodriguezNo ratings yet
- Respiracion y FotorrespiraciónDocument8 pagesRespiracion y FotorrespiraciónPipe MoraNo ratings yet
- Briofitas Musgos y Hepaticas 2 Parcial 2 Exposicion Grupal-Botanica SistematicaDocument10 pagesBriofitas Musgos y Hepaticas 2 Parcial 2 Exposicion Grupal-Botanica SistematicaMario Fierro0% (1)
- Ácidos Carboxílicos y Sus DerivadosDocument44 pagesÁcidos Carboxílicos y Sus DerivadosDayana Cera100% (1)
- Sistema Cardiorespiratorio en CaninosDocument5 pagesSistema Cardiorespiratorio en CaninosRossanaNo ratings yet
- Monografia de ExtraccionDocument5 pagesMonografia de ExtraccionRodrigo Glez0% (1)
- Linea Del Tiempo de La BioquímicaDocument5 pagesLinea Del Tiempo de La Bioquímicaazucena100% (1)
- Práctica Aceite de CocoDocument8 pagesPráctica Aceite de CocoYaret del Carmen Medina PalaciosNo ratings yet
- Zoologia InformeDocument3 pagesZoologia InformeMarcela AlexandraNo ratings yet
- Ácido CítricoDocument7 pagesÁcido CítricoJose andresNo ratings yet
- Principales Microorganismos Que Intervienen en La Fermentación AlcohólicaDocument4 pagesPrincipales Microorganismos Que Intervienen en La Fermentación AlcohólicaJoselynParedesNo ratings yet
- Laboratorio de AlgasDocument53 pagesLaboratorio de AlgasWendyVanessaPulgarinOvalleNo ratings yet
- El Alcohol y Sus UsosDocument3 pagesEl Alcohol y Sus UsosLîz ValerîeNo ratings yet
- Proyecto de BacteriologiaDocument29 pagesProyecto de BacteriologiaMARIA RENEE TICONA GANDARILLASNo ratings yet
- Capsula Foro AumentadoDocument2 pagesCapsula Foro AumentadochalesNo ratings yet
- Ensayo de BiologiaDocument2 pagesEnsayo de BiologiaAnthony Paste100% (1)
- Bioquimica UVM - Practica 1 Reconocimiento de Carbohidratos.Document11 pagesBioquimica UVM - Practica 1 Reconocimiento de Carbohidratos.EdgarNo ratings yet
- Trabajo Autónomo Hidratos de CarbonoDocument8 pagesTrabajo Autónomo Hidratos de Carbonokamari2218No ratings yet
- E6. Farmacología Ii AntiviricosDocument19 pagesE6. Farmacología Ii AntiviricosDania Baculima100% (1)
- 3 - ContinuidadDocument2 pages3 - ContinuidadDania BaculimaNo ratings yet
- Acido FolicoDocument5 pagesAcido FolicoDania BaculimaNo ratings yet
- Molécula HemoglobinaDocument2 pagesMolécula HemoglobinaDania BaculimaNo ratings yet
- 304 QuímicaDocument8 pages304 QuímicaDania BaculimaNo ratings yet
- MONOCITOPOYESISDocument7 pagesMONOCITOPOYESISDania BaculimaNo ratings yet
- Preguntas de FisicaDocument181 pagesPreguntas de FisicaDania BaculimaNo ratings yet
- Manual Técnico de Cultivo de GranadillaDocument33 pagesManual Técnico de Cultivo de GranadillaDania BaculimaNo ratings yet
- Capitulo 01 - Desigualdades, Ecuaciones y Graficas - PDF Precalculo ZillDocument46 pagesCapitulo 01 - Desigualdades, Ecuaciones y Graficas - PDF Precalculo ZillDania Baculima0% (1)
- Respuestas - PDF Precalculo Zill PDFDocument22 pagesRespuestas - PDF Precalculo Zill PDFDania BaculimaNo ratings yet
- Informe Hueso OccipitalDocument4 pagesInforme Hueso OccipitalDania BaculimaNo ratings yet
- Hueso Esfenoides Informe.Document7 pagesHueso Esfenoides Informe.Dania Baculima100% (1)
- Triangulos Del Cuello ExpoDocument6 pagesTriangulos Del Cuello ExpoDania Baculima0% (1)
- Quiz 2 Semana 7 Primer IntentoDocument7 pagesQuiz 2 Semana 7 Primer IntentoAlexandra MontoyaNo ratings yet
- Hospitalización Psiquiatrica en NNADocument10 pagesHospitalización Psiquiatrica en NNAgatoconejoNo ratings yet
- 2 Equipos de Proteccion Ind y ColetivosDocument17 pages2 Equipos de Proteccion Ind y ColetivosKim Brayan O ANo ratings yet
- Mind MapDocument1 pageMind MapBianka CruzNo ratings yet
- Caso Clínico Cirrosis Hepática NataliaDocument24 pagesCaso Clínico Cirrosis Hepática NataliaAnonymous FU8KJVVN0% (1)
- Anexo 1 2 3 Cie 10 CupsDocument994 pagesAnexo 1 2 3 Cie 10 CupsEmilse Margarita GuzmanNo ratings yet
- Guia para RAPDocument71 pagesGuia para RAPDaniel Bautista100% (1)
- Avances Cientificos para La CegueraDocument3 pagesAvances Cientificos para La CegueraDiego SanchezNo ratings yet
- Aplicación de Oxidación Electroquimica y OzonizaciónDocument107 pagesAplicación de Oxidación Electroquimica y Ozonizaciónsamykay.rodriguezNo ratings yet
- DIAGRAMA Proceso de La Preparación de Un BiofertilizanteDocument2 pagesDIAGRAMA Proceso de La Preparación de Un BiofertilizanteLaura Camila GonzalezNo ratings yet
- DislipidemiaDocument11 pagesDislipidemiaMarco Antonio Jimenez SosaNo ratings yet
- Importancia y Beneficios Del Reiki en Los NiñosDocument20 pagesImportancia y Beneficios Del Reiki en Los NiñosKarmen PitaluaNo ratings yet
- BiotecnologíaDocument22 pagesBiotecnologíaRosednell Rosario Perdomo PerezNo ratings yet
- 08 Fo-Log-07 Kardex Ver.01 (Agosto 2013)Document541 pages08 Fo-Log-07 Kardex Ver.01 (Agosto 2013)Gianfranconico Milan GamboaNo ratings yet
- 2.3BC Folleto de Microsistema Auricular PDFDocument29 pages2.3BC Folleto de Microsistema Auricular PDFGeorgette Minerva Bocaney100% (1)
- Velocidad de Sedimentación Globular Como Método de Diagnóstico NaturistaDocument6 pagesVelocidad de Sedimentación Globular Como Método de Diagnóstico NaturistaabiNo ratings yet
- Tesis Primeros AuxiliosDocument36 pagesTesis Primeros Auxiliosfiore2550% (20)
- Recursos Hídricos PerúDocument30 pagesRecursos Hídricos PerúROMMYNo ratings yet
- Seminario 2020Document32 pagesSeminario 2020Gaspar RaguexNo ratings yet
- Dislipidemias TERMINADODocument29 pagesDislipidemias TERMINADOPaola Magdalena Ortega EspinoNo ratings yet
- Sve Ruido Sst-HseqDocument18 pagesSve Ruido Sst-HseqCRISTIAN CAMILO OSORIO ORDOÑEZNo ratings yet
- Estomas IntestinalesDocument9 pagesEstomas IntestinalesXiomara CardonaNo ratings yet
- Fertilización en MaizDocument42 pagesFertilización en Maizeduardovirguez2008No ratings yet
- Vías de Administración de MedicamentosDocument12 pagesVías de Administración de MedicamentosBriseida Yareth Ibarra ZapataNo ratings yet
- Metodo ClinicoDocument2 pagesMetodo ClinicoDaniela TelloNo ratings yet
- Copia de PROGRAMA MALA ALIMENTACIÓN - Psicología SocialDocument6 pagesCopia de PROGRAMA MALA ALIMENTACIÓN - Psicología Socialkevin VegaxNo ratings yet
- Aceite Palma FDS QD 2018Document6 pagesAceite Palma FDS QD 2018Analista SigNo ratings yet
- Autoestima y ParejaDocument8 pagesAutoestima y ParejaConsuelo Márquez Lemp100% (1)