Professional Documents
Culture Documents
Tema 2. Exercicis I Qüestions Estructura Atòmica I S. Periòdic PDF
Uploaded by
Luisa Rubio VillarrealOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Tema 2. Exercicis I Qüestions Estructura Atòmica I S. Periòdic PDF
Uploaded by
Luisa Rubio VillarrealCopyright:
Available Formats
TEMA 2.
EXERCICIS I QÜESTIONS
D’ESTRUCTURA ATÒMICA I S. PERIÒDIC
1. a) Dóna una definició d’orbital atòmic.
b) Quin significat té dir que una magnitud està quantitzada? Posa un exemple
c) Què és l’electronegativitat? Indiqueu qualitativament com varia aquesta propietat en el
Sistema Periòdic i com influeix en el tipus d’enllaç que formen els elements químics en
combinar-se? (R: a) zona de l’espai on la probabilitat de trobar l’electró és màxima; b) Que no
pot prendre qualsevol valor. Per exemple en el model atòmic de Bohr el radi de l’òrbita, c) la
mesura de l’atracció d’un àtom sobre els electrons compartits. Augmenta cap a la dreta
(excepte els gasos nobles) en un període i cap a dalt en una família).
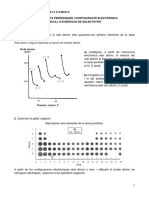
2. a) Com es pot representar gràficament un orbital atòmic? Dibuixa dos orbitals atòmics distints
de l’hidrogen
b) Escriu els números quàntics que correspondrien a un electró allotjat en els orbitals atòmics
dibuixats en el apartat anterior.
c) Escriu la configuració electrònica del ió sulfat S2- i de l’àtom de zinc.
Dades: Números atòmics: S=16; Zn=30 (R: a) estat fonamental: un orbital s esfèric del 1er
nivell i en estat excitat qualsevol altre; b) estat fonamental: (1,0,0,+1/2); c) 1s 22s22p63s23p6 i
1s22s22p63s23p64s23d10).
3. a) En el model atòmic de Bohr es parla de “òrbita” de l’electró i en el model atòmic de la
mecànica quàntica es parla de “orbital”. ¿ Quina diferència hi ha entre ambdós conceptes?
b) Definiu l’energia d’ionització. Com és la segona energia d’ionització respecte a la primera
(major, igual o menor)?: Justificar la resposta.
c) Els següents àtoms i ions tenen tots 10 electrons: N 3-, O2-, F-, Ne, Na+, Mg 2+. Ordena’ls
segons el radi creixent. (R: a) “òrbita” es referia al camí que seguia l’electró al voltant del nucli
i “orbital” a la zona de màxima probabilitat de trobar-lo; b) és l’energia que s’ha de comunicar
a un àtom en estat gasós i configuració fonamental per arrancar-li l’electró més extern. La
segona energia d’ionització és major degut a què el segon electró s’hauria d’arrancar a una
espècie que ja té un dèficit d’electrons i per tant està més fortament unit a l’àtom; c)
Mg2+<Na+<Ne<F-<O2-<N3-)
4. a) El comportament d’un electró pertanyent a un àtom d’hidrogen queda descrit pels
següents nombres quàntics:
n=3 l=2 m=1 s=1/2
En quin nivell energètic i en quin tipus d’orbital es troba aquest electró.
b) La primera fila del Sistema Periòdic té dos elements químics, la segona i la tercera tenen
vuit elements i la quarta i la cinquena fila tenen divuit elements. Dóna una explicació a
aquests fets. (R: a) En el 3er nivell i en un orbital p; b) les files o períodes corresponen al nivell
energètic i el nombre d’elements de cada fila és el nombre d’electrons que hi caben en cada
nivell).
5. A) Indicar quina o quines de les frases següents són certes.
A1) Segons Bohr la força que manté a l’electró en l’òrbita es deu solament a
l’atracció gravitatòria entre la partícula i el nucli.
A2) Per arrancar l’electró de l’àtom d’hidrogen, es consumeix la mateixa energia si
aquest es troba en un orbital 1s que si se troba en un orbital 2p.
A3) Els elements químics s’ordenen en el sistema periòdic segons els pesos atòmics
creixents.
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /1
B) Expliqueu per què es vertadera o falsa cada frase de l’apartat anterior. Escriviu
correctament les que són falses. (R: A1) falsa, segons ell era deguda a la força d’atracció
electrostàtica; A2) falsa, es consumeix menor energia en arrancar el situat en l’orbital 2p, ja
que es troba en estat excitat i la seua estabilitat és menor i hi ha menys energia d’atracció al
nucli; A3) falsa, s’ordenen segons els seu número atòmic).
6. Un àtom X té la configuració electrònica següent: 1s 2 2s 2 2p6 3s2 3p6 5s1. Quines de les
següents fórmules són correctes. Raonar la resposta.
A1) X es troba en estat fonamental.
A2) X pertany al grup dels metalls alcalins.
A3) X pertany al 5é període del sistema periòdic.
A4) Si l’electró passara des de l’orbital 5s al 6s, s’emetria energia lluminosa que donaria ll oc a
una línia en l’espectre d’emissió. (R: A1) Fals, l’estat és excitat; A2) Vertader, en estat
fonamental tindria una configuració [Ar]4s1; A3) Fals, pertanyeria al 4t període; A4) Fals, en el
salt que es descriu s’hauria de comunicar energia).
7. A) Indiqueu quina o quines de les frases següents són vertaderes.
A1) Las ratlles de l’espectre d’emissió de l’hidrogen són degudes a trànsits de l’electró entre
nivells d’energia.
A2) El ió òxid, O 2-, té un radi major que l’àtom d’oxigen.
A3) Segons ens desplacem d’esquerra a dreta en una fila del sistema periòdic disminueix
l’energia d’ionització.
B) Expliqueu per què és vertadera o falsa cada frase del apartat anterior. Escriviu
correctament aquelles que siguen falses. (R: Solució: A1) Vertadera, és el fonament d’un
espectre d’emissió; A2) Vertadera; el ió negatiu pateix una “expansió” de volum respecte a
l’àtom deguda a la repulsió entre els electrons de la última capa; A3) Fals, augmenta.)
8. A) Dels elements amb àtoms que guanyen electrons amb facilitat, es diu que són “agents
oxidants”. Raoneu quin dels següents elements és millor “agent oxidant”: Na=11, F=9, Ba=56,
Ne=10, O=9.
B) Quines millores aporta el model de Bohr respecte al model de Rutherford? Citeu-ne al
menys dues. (R: A) F>O>Ba>Na>Ne; B) El model de Bohr és capaç d’explicar la estabilitat de
l’àtom a partir de la introducció del concepte d’òrbites quantitzades).
9. A partir d’aquestes configuracions electròniques:
I) 1s22s22p6 II) 1s22s2 III) 1s 22s22p63s23p4
Indiqueu: A quins àtoms corresponen. A quins ions monopositius corresponen. A quins ions
mononegatius corresponen. (R: I) àtom: Ne; ió positiu: Na +; ió negatiu: F-; II) Be, B +, Li; III) S,
Cl+, P-)
10. A) La configuració electrònica de valència d’un element és 4s23d104p6. A quin període i família
del sistema periòdic pertany? Quin estat d’oxidació negatiu ha de tenir?
B) Quina o quines de les combinacions següents de números quàntics són vàlides, per un
electró d’un àtom de carboni en estat fonamental? Raoneu la resposta i indicar per què les
altres combinacions no són vàlides.
n l m s
B1 1 0 1 1/2
B2 3 1 -1 1/2
B3 2 2 0 -1/2
B4 2 0 -1 -1/2
(R: 4t període i família 18 (gas noble). És estable i no forma ions; B) B1: no vàlida m≠1, B2: no
vàlida, no hi ha nivell d’energia 3 per al carboni en estat fonamental; B3: no vàlida, l≠2; B4: no
vàlida, m≠1).
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /2
11. Donats els elements següents: He, F, S, As i Sn. Indiqueu el que millor correspon a cadascuna
de les propietats següents:
A) El més metàl·lic.
B) El de major radi
C) El més electronegatiu.
Dades: Números atòmics: He=2, F=9, S=16, As=33, Sn=50. (R: A) Sn; B) Sn; c) F).
12. Classifiqueu en ordre creixent de radis, els ions següents, (justifiqueu-lo)
O2-, Na+, F-, Mg 2+
Números atòmics: O=8, Na=11, F=9, Mg=12. (R: O2->F->Na+>Mg2+; les configuracions
electròniques són iguals però el número de protons en cada nucli és distint. En aquestes
condicions, quan major és el nº de protons, més atracció hi ha sobre els electrons i menor serà
el radio iònic).
13. Donats 3 elements químics de nombres atòmics 19,35 i 36. Indiqueu:
A) La configuració electrònica i el grup del sistema periòdic a què pertany cada element.
B) Dels tres elements quin té major energia d’ionització, quin major afinitat electrònica i quin
major radi atòmic. Raona r les respostes. (R: A) 1s22s22p63s23p64s1alcalins;
1s22s22p63s23p64s23d10 4p5halogens; 1s22s22p63s23p64s23d104p6gas noble. B) major energia
d’ionització: C, té més càrrega nuclear i més electrons que estan en el mateix nivell energètic
de B, per tant serà més difícil arrancar-li un electró. Major EA: B, és l’element més
electronegatiu, per tant alliberarà més energia en captar un electró per a formar un ió
negatiu. Major radi atòmic: A, pertanyen tots al mateix període però en A hi ha menys
càrregues i per tant la força d’atracció entre electrons i protons serà menor).
14. Respecte al número quàntic “n” que apareix en el model atòmic de Bohr, indiqueu de manera
raonada quines són correctes i quines incorrectes.
A) L’energia de l’electró en les òrbites està quantitzada i depèn de n.
B) El radi de les òrbites no depèn de n
C) Les ratlles de l’espectre d’ emissió de l’hidrogen són degudes a trànsits de l’electró d’una
òrbita a un altra de n major.
D) Quan l’ electró passa a tenir n = l’àtom s’ha ionitzat. (R: A) Vertadera, és un dels
postulats de Bohr; B) Fals, precisament, el radi de les òrbites ve donat per n; C) Fals, són
degudes a trànsits d’una òrbita major a una menor; D) Vertadera, equival a dir que l’electró
“s’ha perdut”).
15. Escriure la sèrie completa dels quatre nombres quàntics per a un dels electrons de valència de
l’àtom de sofre en l’estat fonamental. (Número atòmic del sofre 16). (R: Per exemple (3,1,-
1,+1/2))
16. Donades les següents configuracions electròniques de dos àtoms neutres:
X: 1s 22s 22p63s23p6 Y: 1s22s 22p63s23p54s1
Justifiqueu la validesa o falsedat de les següents afirmacions:
A) La configuració de Y correspon a un àtom de K.
B) Per a passar de X a Y es necessita aportar energia.
C) El radi de X es igual al radi de Y. (R: A) Falsa, el potassi té 19e -; B) Vertadera, Y és un estat
excitat de X; C) Falsa, Y és major ja que té un electró en un nivell superior).
17. Assenyala justificadament quines de les següents proposicions són correctes i quines no:
A) El número atòmic dels ions K+ és igual al del gas noble Ar.
B) Els ions K+ i els àtoms del gas noble Ar són isòtops.
C) El radi dels ions K+ és igual al dels àtoms de Ar. Dades: Números atòmics: Ar = 18; K = 19
(R: A) Falsa, el número atòmic depèn del número de protons del nucli de l’element, no de la
configuració electrònica. B) Falsa, els isòtops han de pertànyer al mateix element. C) Falsa, el
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /3
radi del ió K+ és major que el de l’àtom Ar, ja que encara que la configuració electrònica siga la
mateixa, la càrrega nuclear és distinta).
18. A) La configuració electrònica del crom, en l’estat fonamental, és 1s 22s22p63s 23p54s 13d5.
Justifiqueu la “aparent” anomalia existent en dita configuració.
B) Quin és el nombre màxim d’electrons que pot hi haver en un mateix àtom amb n=3? Quin
principi determina aquest nombre? (R: A) D’aquesta manera s’aconsegueix una configuració
amb els orbitals d semiplens. B) Principi d’exclusió de Pauli, 2n 2= 2.32= 18 electrons).
19. A) Definiu els conceptes de afinitat electrònica i energia d’ionització i indiqueu si existeix
alguna relació entre ells.
B) Indiqueu el valor que pot prendre el número quàntic “m” per a:
B.1) un orbital 2s
B.2) un orbital 3d
B.3) un orbital 4p
(R: A) En augmentar el potencial d’ionització, augmenta també l’afinitat electrònica, amb
excepció dels gasos nobles. B) B1: m=0; B2: m=-2,-1,0,-1,2; B3= -1,0-1)
20. Donats els següents conjunts de números quàntics per a l’electró en el àtom d’hidrogen,
indiqueu les combinacions que no siguen possibles i indiqueu en cada cas el motiu:
A) 2,2,1,+1/2
B) 4,0,2,-1/2
C) 1,0,0,+1/2
D) 3,-1,0,-1/2 (R: A) No, l≠2; B) No, m≠2; C)Si; D) No; l≠ -1)
21. Per als elements plata i seleni, els respectius nombres atòmics dels quals són 47 i 34,
indiqueu:
A) La seua situació en la taula periòdica (grup i període)
B) Els nombres quàntics dels electrons desaparellats.
C) L’estat d’oxidació més probable en els seus ions monoatòmics.
(R: A) Ag: període 5é; família IB ó 11; Se: període 4t; família VIA ó 16. B) Ag (5,0,0,+1/2); Se
(4,1,0,+1/2). C) Ag+; Se2-).
22. Els elements A, B, C i D tenen els nombres atòmics: 11, 15, 16 i 25. Responeu raonadament a
les qüestions següents:
a) Indiqueu el ió més estable que pot formar cadascun dels elements anteriors.
b) Escriviu l’estequiometria que presentaran els compostos més estables que formen A amb
C, B amb D i B amb C. (R: a) A+, B3-, C2-, D2+; b) A2C, D3B2, B2C3).
23. a) Ordeneu raonablement els elements A, B i C de nombres atòmics 3, 11 i 19 respectivament,
per ordre creixent d’energia d’ionització.
b) Ordeneu raonablement els elements D, E i F de nombres atòmics 4, 6 i 9, respectivament,
per ordre creixent de radi atòmic.
24. Els elements A, B, C i D tenen nombres atòmics 12, 14, 17 i 37, respectivament.
a) Escriviu la configuració electrònica d’A2+, B, C - i D.
b) Indiqueu, justificant la resposta, si les següents proposicions referides als elements
anteriors A, B, C i D, són vertaderes o falses:
b1) L’element que té el radi atòmic més xicotet és el B.
b2) L’element D és el que té major energia d’ionització I1.
b3) L’element C és el que té major afinitat electrònica.
b4) Quan es combinen C i D es forma un compost molecular.
25. Responeu, justificant la resposta, a les següents qüestions:
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /4
a) Si la configuració electrònica de la capa de valència d’un element és 4s23d104p3 indiqueu a
quin període i a quina família pertany aquest element. Quin estat d’oxidació negativa pot
tindre?
b) Quina o quines de les següents combinacions són conjunts vàlids de nombres quàntics per
a un electró d’un àtom de carboni en el seu estat fonamental? Raoneu la resposta i indiqueu
per què no són vàlides la resta de combinacions.
n l ml ms
B1 1 0 1 -1/2
B2 2 0 0 -1/2
B3 2 2 -1 -1/2
B4 3 1 -1 1/2
26. Tenim dos elements A i B els nombres atòmics dels quals són: Z(A) = 28; Z(B) = 35. Contesteu
les qüestions següents:
a) Escriviu la configuració electrònica de l’estat fonamental dels dos elements.
b) Quin element espereu que tinga un valor més elevat de la seua primera energia
d’ionització? Raoneu la resposta
c) Quin element té els àtoms més xicotets? Raoneu la resposta.
d) En el cas que els elements A i B es pogueren combinar per a formar un compost estable i
neutre, quina és la fórmula que creieu més probable per a aquest compost?
27. Contesteu per a cada un dels següents elements de la taula periòdica: A(Z=30); B(Z=35) i
C(Z=1).
a) Les configuracions electròniques.
b) Els valències iòniques.
c) Per a les següents combinacions entre ells, determineu quines són possibles i quin tipus
d’enllaç es forma: (A amb B), (B amb B) i C amb B).
28. Els elements A, B , C i D tenen nombres atòmics 10, 15, 17 i 20.
a) Escriu la configuració electrònica de A, C- i D2+ i indica el grup a què pertany cadascun dels
elements.
b) Dels quatre elements (neutres) indica, raonant la resposta, quin té major energia
d’ionització i quin major radi atòmic.
29. a) Agrupeu les següents configuracions electròniques en parelles que poden representar
elements de propietats químiques similars:
1s 22s 2 1s 22s 22p3 1s 22s 22p63s2 1s 22s 22p63s1 1s 22s 22p63s23p3 1s 22s 1
b) Indiqueu, justificant la resposta, si les següents proposicions són vertaderes o falses.
i) els elements d’un mateix grup tenen el mateix nombre atòmic.
ii)els elements del mateix període tenen fórmules anàlogues per als corresponents
compostos.
iii) el nombre atòmic coincideix amb el nombre de protons del nucli, però no sempre
coincideix amb el nombre d’electrons d’un àtom neutre.
iv) el volum del ió òxid O2-, és superior al de l’àtom de neó.
30. a) Expliqueu quines són les tendències generals en les variacions de la mida atòmica i de la
primera energia d’ionització en un període i en un grup o família de la taula periòdica
b) Ordeneu els següents elements segons la mida creixent dels seus àtoms, i justifiqueu la
resposta: Si, Ne, F, Mg, S, K.
c) Ordeneu els següents elements segons el valor creixent de la seua primera energia
d’ionització, i justifiqueu les possibles anomalies, si escau: Al, Ne, P, Mg, S, K. DADES:
nombres atòmics.- F: 9, Ne: 10, Mg: 12, Al: 13, Si: 14, S: 16, K: 19.
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /5
31. La configuració electrònica d’un element A és: 1s 22s 22p63s23p63d104s 24p64d105s 25p5.
Expliqueu raonadament, quines de les afirmacions següents són correctes:
1. El Sb (Z=51) té una energia d’ionització menor que l’àtom A.
2. El Sn (Z=50) té un radi atòmic major que l’àtom A.
3. L’energia d’ionització del Cl (Z=17) és major que la de l’àtom A.
4. De la combinació de l’element A amb l’element de Z=35 s’obtenen compostos
fonamentalment iònics.
5. L’element A és més electronegatiu que l’element de Z=17.
32. Contesteu raonadament les qüestions següents:
a) considereu els elements químics següents: Ne, F, Na, Mg i O ordeneu els elements químics
per ordre creixent de la seua primera energia d’ionització.
b) Indiqueu el ió més probable que formarien els elements anteriorment citats.
c) Ordeneu les espècies iòniques de l’apartat anterior per ordre creixent dels seus
corresponents radis iònics. DADES: nombres atòmics (Z): O(Z=8); F(Z=9); Ne(Z=10), Na(Z=11);
Mg (Z=12)
33. A continuació es donen una sèrie de configuracions electròniques del fluor (Z=9). Classifica-
les, raonadament, en estat fonamental, excitat o prohibit.
(a) 1s 22s 22px12py22pz2 (b) 1s22s22px22py12pz2
(c) 1s 22s 22px22py22pz1 (d) 1s22s22px22py32pz0
(e) 1s22s 22px12py12pz13s2 (f) 1s 22s22p5
2 2 3 1 1
(g) 1s 2s 2p 4s 5s
(h) 1s 2s 2p (i) 1s 2s 2p
(j) 1s 2s 2p 3p
34. (A) Indica els errors que existeixen en les següents combinacions de nombres quàntics:
(1,1,0); (2,-1,0); (3,3,1); (1,2,0); (2,1,-1); (4,0,1).
(B) Explica de forma raonada els electrons i orbitals que pot haver en el nivell n=2.
(C) Quina fórmula quàntica pot tenir l’electró diferenciador o últim electró del potassi
(Z=19), del fluor (Z=9), del silici (Z=14) i del calci (Z=20)?.
35. Explica el significat dels següents termes: a) fotó. b) orbital. c) electró desaparellat. d) nombre
quàntic. e) configuració electrònica.
36. Les següents configuracions podem suposar que pertanyen al sofre (Z=16). Classifica -les com
corresponents a estats fonamentals, excitats o prohibits, indicant, si s’escau el o els principis
que violen.
(a) 1s 22s 22p63s23p4
(b) 1s 22s22px22py02pz23s 23px23py23pz2
(c) 1s 22s 22p63s23px23py23pz0
(d) 1s 22s22p63s23px13py23pz1
(e) 1s22s 22p63s 23px13py13pz2
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /6
(f) 1s 2s 2p 3s 3p
(g) 1s 2s 2p 3s 3p
(h) 1s 2s 2p 3s 3p
37. (A) Dóna la fórmula quàntica de l’últim electró de la configuració h, de la pregunta anterior.
(B) Quina de les següents combinacions de nombres quàntics no correspon a cap electró de
l’oxigen (Z=8), al seu estat fonamental?. Per què?.
(1,0,0, ½) (2,1,-1,- ½) (2,1,0,- ½) (2,-1,1, ½) (2,0,0,- ½)
38. (A) El model de Rutherford i el model de Bohr, descriuen un àtom format per un nucli, situat
al centre i que conté pràcticament tota la massa de l’àtom, i els electrons girant en òrbites al
seu voltant. Quines modificacions va introduir Bohr per resoldre els dos problemes greus del
model de Rutherford: a) el caràcter autodestructiu de l’àtom i b) la impossibilitat d’explicar
els espectres atòmics?.
(B) Quines són les diferències més importants entre les òrbites de Bohr i els orbitals de la
Mecànica quàntica?.
39. Dedueix el nombre màxim de línies en l’espectre d’emissió d’un àtom d’hidrogen, l’electró del
qual es troba en el nivell n=5. (R: 10)
40. Calcula la longitud d’ona del límit i de la primera línia de l’ultraviolat de l’espectre de
l’hidrogen, sèrie Lyman. (R:9·10-8m i 1,2·10-7m)
41. Una línia de la sèrie de Balmer té una longitud d’ona de 434 nm. Calculeu el valor de n i que
correspon a la transició electrònica que origina aquesta línia. (R: ni=5)
42. Digues de les següents configuracions electròniques: (a) Quines corresponen a estats
excitats?. (b) Quines corresponen a àtoms en estat fonamental?. (c) Quines són incorrectes o
impossibles?.
(1) 1s22s22p63s 1 (2) 1s22s22p53p1
(3) 1s22s2 (4) 1s23d3
2 2 7
(5) 1s 2s 3p (6) 1s22s22p62d2
43. Hi ha alguna raó que justifique el fet que la massa d’un isòtop qualsevol estiga sempre
representada per nombres enters i la massa d’un àtom aparega, quasi sempre, representada
per nombres fraccionaris?. Raona la resposta.
44. Calcula la massa atòmica del plom si d’ell es coneixen quatre isòtops de masses atòmiques:
204, 206, 207 i 208 i els seus percentatges són respectivament: 1,5; 28,3; 20,1 i 50,1.
45. Calcula la freqüència i la longitud d’ona de la primera línia de la sèrie Balmer. Dades:
R=1,09678·107 m-1. (R: 6,56·10-7 m; 4,57·1014 Hz)
46. Considerem dos raigs monocromàtics de llum, un taronja ( =6,2·10-5 cm) i altre violat
( =4,2·10-5 cm), quin raig té major energia? (R: el violat)
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /7
47. L’energia de ionització del sodi és 495,8 kJ/mol. Quina és la freqüència més baixa de la llum
capaç de ionitzar el sodi? (R: 1,24·1015 s-1)
48. Un àtom d’hidrogen en estat fonamental absorbeix un fotó de llum de =97,2 nm. A
continuació desprèn un fotó que té de longitud d’ona 486 nm. Quin és l’estat final de l’àtom
d’hidrogen? (R: n=2)
49. En la transició electrònica de l’àtom d’hidrogen del nivell quàntic principal n=5 al nivell
quàntic n=2 s’emet un fotó de = 434 nm. Calcula l’energia de l’electró en el segon nivell
quàntic principal. L’energia del cinquè nivell quàntic és E 5= -0.54 eV. La constant de Planck és
6.626·10-34 J·s. Solució: -3,40eV
50. En la transició electrònica de l’àtom d’hidrogen del nivell quàntic principal n=2 al nivell
quàntic n=1 s’emet un fotó de = 121.6 nm. Calcula:
a) La freqüència i l’energia del fotó d’aquesta radiació.
b) L’energia de l’electró en el segon nivell quàntic principal.
c) L’energia necessària per arrencar l’electró del segon nivell quàntic principal (energia per a
traslladar-lo fins a l’infinit) i la longitud d’ona capaç d’efectuar aquesta transició.
L’energia del nivell quàntic principal és E0= -13.6 eV. La constant de Planck és 6.626·10 -34 J·s.
1eV= 1.6·10-19 J. Solució: a) 2.47·1015 Hz; 1.63·10·10-18 J = 10.2 eV; b) -3.40 eV; c) +3,40 eV
51. Quan un electró de l’àtom d’hidrogen passa del segon nivell quàntic principal, n=2 al tercer,
n=3 s’absorbeix un fotó de 3,03·10-19 J. Calcula la freqüència i la longitud d’ona del fotó
absorbit. Calcula l’energia del 3r nivell quàntic principal. Dades: l’energia en el segon nivell val
-3,40 eV. (1 eV= 1,6·10-19 J). Solució: a) 4.57·1014 Hz; 656 nm; b) -2.41·10-19 J = -1.51 eV
52. La següent taula d’energies de ionització (kJ/mol) no està ordenada de manera correcta.
Corregeix-la explicant els canvis:
He Li Be B O F
519 1312 895 2369 1678 799
53. De totes les partícules següents: Al +3, Ne, K+, S2-, Ca2+.
a) Indica a quina serà més fàcil arrancar un electró.
b) Quina el guanyarà més fàcilment?.
54. La taula adjunta dóna les primeres i segones energies de ionització (eV) del Li, Na i K.
Li Na K
1a 5,4 5,1 4,3
2a 75,6 47,3 31,8
a) Per què la primera energia de ionització disminueix del liti fins el potassi?.
b) Per què la segona energia de ionització de cada element és major que la primera?.
c) Per què la variació de la segona energia de ionització és inversa a la primera?.
55. Dos elements Q i R, representen a un alcalí i a un alcalinoterri consecutius en el sistema
periòdic. Si sabem que la EI1 de Q és major que la de R i que la EI 2 de R és major que la de Q,
¿quin és l’alcalí i quin l’alcalinoterri?. Per què?.
56. Ordena de major a menor els radis, potencials de ionització i electronegativitats de: magnesi,
potassi i calci.
57. Ordena els següents elements pel seu comportament metàl·lic: a) S, Cl, Na, Si, Al; b) F, I, Pb
58. Quatre elements que anomenarem A, B, C i D tenen, respectivament, els nombres atòmics: 2,
11, 17 i 25. Indica:
a) El grup i el període a què pertanyen.
b) Quins són metalls.
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /8
c) L’element que té major afinitat electrònica.
59. El nombre d’electrons dels elements A, B, C, D i E és 2, 9, 11, 12 i 13, respectivament. Indica,
raonant la resposta, quin d’ells:
a) Correspon a un gas noble.
b) És un metall alcalí.
c) És el més electronegatiu.
60. Raona el tamany relatiu de les següents parelles de ions isoelectrònics: a) K+ i Cl- b) Mg +2 i O-2.
61. Per al potassi, la primera energia de ionització és 419 kJ/mol i la segona 3052 kJ/mol. Per al
calci aquestes energies són, respectivament, 590 i 1145 kJ/mol. Compara els valors i explica
les diferències.
62. Els àtoms neutres X, Y, Z tenen les següents configuracions: X=1s22s22p1; Y=1s 22s22p5;
Z=1s22s22p63s 2.
a) Escriu el grup i el període a què pertanyen i dedueix quin té l’energia de ionització major.
b) Ordena’ls, raonadament, de menor a major electronegativitat.
c) Quin té l’energia de ionització major?
PBAT Tema 2. Exercicis i qüestions d’estructur a atòmica i sistema periòdic /9
You might also like
- AtomoDocument3 pagesAtomofaniNo ratings yet
- Dossier Estiu Recuperacio 3r ESO 2018Document42 pagesDossier Estiu Recuperacio 3r ESO 2018albaNo ratings yet
- Enunciats Cangur 1 ESO PDFDocument5 pagesEnunciats Cangur 1 ESO PDFericsuma10No ratings yet
- Físicaq Quimica 3eso Curs1617Document145 pagesFísicaq Quimica 3eso Curs1617Xelo Martinez RomanNo ratings yet
- U3 - Divisibilitat 1r ESODocument18 pagesU3 - Divisibilitat 1r ESOAlfredoNo ratings yet
- Cangur2016 1ESO ABDocument8 pagesCangur2016 1ESO ABlev76No ratings yet
- 3r ESO MATEMÀTIQUES PDFDocument12 pages3r ESO MATEMÀTIQUES PDFJosep AlcañizNo ratings yet
- Frases Fetes-Jana Ll. 3rbDocument6 pagesFrases Fetes-Jana Ll. 3rbJana LlussàNo ratings yet
- Mat2 Problemes Sobre FraccionsDocument1 pageMat2 Problemes Sobre FraccionsYolanda Carrillo100% (2)
- Dossier Recuperació 1r Trimestre Biologia I Geologia 1r ESODocument3 pagesDossier Recuperació 1r Trimestre Biologia I Geologia 1r ESOSurfmindNo ratings yet
- Feina Estiu 1 Eso Biologia GeologiaDocument19 pagesFeina Estiu 1 Eso Biologia GeologiaMaria Garcia AlonsoNo ratings yet
- Examen 3r ESO Adaptat - 2n Trimestre - 230315Document2 pagesExamen 3r ESO Adaptat - 2n Trimestre - 230315GerardNo ratings yet
- Examen ELS ÀTOMS Física I Química 2017 (I)Document4 pagesExamen ELS ÀTOMS Física I Química 2017 (I)jsabria9114No ratings yet
- Dossier Recuperacio 3r EsoDocument25 pagesDossier Recuperacio 3r EsoSonia SoniaNo ratings yet
- Examen Química Àtoms 3r ESODocument2 pagesExamen Química Àtoms 3r ESOMartolineta100% (1)
- Exercicis Nombres EntersDocument24 pagesExercicis Nombres Entersadelagguillen0% (1)
- 9209 - Unitat 3 - Llengua Catalana I Literatura 1 ESO-Activitats PDFDocument89 pages9209 - Unitat 3 - Llengua Catalana I Literatura 1 ESO-Activitats PDFOSRAMANo ratings yet
- Examen ByG 3o ESO-T4Document2 pagesExamen ByG 3o ESO-T4Rubén Gisbert GregoriNo ratings yet
- Bloci Dossier-I Naturals Potencies Mult 3Document58 pagesBloci Dossier-I Naturals Potencies Mult 3Lucia MartinezNo ratings yet
- Treball Estiu 3r ESO MatemàtiquesDocument7 pagesTreball Estiu 3r ESO Matemàtiquesftorre91656No ratings yet
- T1 OrganitzacioDocument35 pagesT1 OrganitzacioVioleta Gómez RosilloNo ratings yet
- Quadern Estiu 1er ESO NatuDocument8 pagesQuadern Estiu 1er ESO Natusaruri2603No ratings yet
- Dossier Deures Estiu Biologia 3 ESODocument33 pagesDossier Deures Estiu Biologia 3 ESOOSRAMA0% (1)
- Guia. Física I Química 3 ESO. TeideDocument233 pagesGuia. Física I Química 3 ESO. TeideElisabetNo ratings yet
- Av Matematiques 1r ESODocument31 pagesAv Matematiques 1r ESOjoseramirezmat100% (1)
- Prova Catala 2016 PDFDocument12 pagesProva Catala 2016 PDFMiguel MoNo ratings yet
- Medi Social PDFDocument20 pagesMedi Social PDFCè LiaNo ratings yet
- Quadern D'estiu Ciencies Naturals 3R D'eso PDFDocument52 pagesQuadern D'estiu Ciencies Naturals 3R D'eso PDFlidiaNo ratings yet
- Activitats Tema 1 LA CEL LULADocument1 pageActivitats Tema 1 LA CEL LULAhdhdhdNo ratings yet
- 1r Tecnologia DossierDocument17 pages1r Tecnologia DossierJOAN CIDNo ratings yet
- Els Nombres Decimals 1r ESODocument3 pagesEls Nombres Decimals 1r ESOxuelaNo ratings yet
- Teoria Cinètica I Estats de La MatèriaDocument4 pagesTeoria Cinètica I Estats de La MatèriaToni Vives SuredaNo ratings yet
- Electricitat I MagnetismeDocument2 pagesElectricitat I MagnetismeFelipeBlascoNo ratings yet
- Solucionari Naturals Llibre 2ESO CDocument45 pagesSolucionari Naturals Llibre 2ESO CJordi PeñaNo ratings yet
- Proves de Competències Bàsiques 6è Mates-2014Document12 pagesProves de Competències Bàsiques 6è Mates-2014Ana DiazNo ratings yet
- Examen Divisibilitat 16Document2 pagesExamen Divisibilitat 16Juanjo MonferrerNo ratings yet
- Catala 2017Document12 pagesCatala 2017ManuelNo ratings yet
- 09 Guia Didactica Val Forces Fluids PDFDocument36 pages09 Guia Didactica Val Forces Fluids PDFLaura PoNo ratings yet
- RelleuDocument12 pagesRelleumagulloNo ratings yet
- Examen DivisibilitatDocument2 pagesExamen DivisibilitatNuri S. C.No ratings yet
- Matemàtiques 3r ESO A-B Dossier Recuperació EstiuDocument18 pagesMatemàtiques 3r ESO A-B Dossier Recuperació EstiudavidtecnoNo ratings yet
- Deures D - 'Estiu de Catala 2n D - 'EsoDocument23 pagesDeures D - 'Estiu de Catala 2n D - 'EsoMªAngeles Beas100% (1)
- Raonaments 5è (1-10) CORRECCIÓDocument14 pagesRaonaments 5è (1-10) CORRECCIÓJordi Ribé100% (1)
- Formulació Inorgànica 1 BatxilleratDocument5 pagesFormulació Inorgànica 1 BatxilleratAina MariaNo ratings yet
- LC Nivell C PDFDocument222 pagesLC Nivell C PDFL'Aula d'Estudis Marta DomènechNo ratings yet
- Examen T2. Les ForcesDocument6 pagesExamen T2. Les ForcesAnna PagesNo ratings yet
- Quadern D'estiu Ciencies Naturals 1r D'esoDocument26 pagesQuadern D'estiu Ciencies Naturals 1r D'esoNaara A. SanchezNo ratings yet
- Pendents 3rESODocument33 pagesPendents 3rESOEva AlmirallNo ratings yet
- Formulació D''òxids I Sals BinàriesDocument6 pagesFormulació D''òxids I Sals BinàriesRida Eddellah MohamedNo ratings yet
- Exercicis Matemàtiques 1r ESODocument138 pagesExercicis Matemàtiques 1r ESOpepa1241547No ratings yet
- Solucionari CFGS Llengua I Literatura CatalanDocument33 pagesSolucionari CFGS Llengua I Literatura CatalanAnuar BenNo ratings yet
- Exercicis de RepàsDocument4 pagesExercicis de Repàslucarebenaque2No ratings yet
- Exercicis Propietats Periã DiquesDocument3 pagesExercicis Propietats Periã DiquesPAU YI RAMOSNo ratings yet
- Exercicis Q1 U7 Models AtomicsDocument4 pagesExercicis Q1 U7 Models AtomicsPaula Raga RoperoNo ratings yet
- Exercicis Estructura Atòmica FinalsDocument2 pagesExercicis Estructura Atòmica FinalsBy ÁlexNo ratings yet
- fq4 Exer DossierDocument39 pagesfq4 Exer Dossiermireia coleNo ratings yet
- Model Examen (V)Document2 pagesModel Examen (V)LauraNo ratings yet
- Sol - 01 - Ud02 - Quim1 - Batxcien - Batx 3Document3 pagesSol - 01 - Ud02 - Quim1 - Batxcien - Batx 3Isabella Castaño GonzálezNo ratings yet
- 1-0 Model Atomic Actual Exercicis 2324Document8 pages1-0 Model Atomic Actual Exercicis 2324aromuncalNo ratings yet
- 1BATQ UD2-5 Prop Periodiques I Config Electronica Recull Exercicis PAU Fins2022 2324 ALUMNATDocument5 pages1BATQ UD2-5 Prop Periodiques I Config Electronica Recull Exercicis PAU Fins2022 2324 ALUMNATaromuncalNo ratings yet