Professional Documents
Culture Documents
Ejercicios de estequiometría y cálculos de reacciones químicas
Uploaded by
ALEX RODOLFO MAYTA VARGASOriginal Description:
Original Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Ejercicios de estequiometría y cálculos de reacciones químicas
Uploaded by
ALEX RODOLFO MAYTA VARGASCopyright:
Available Formats
Ejercicios de estequiometría
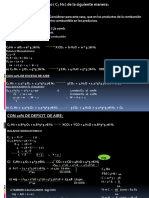
1. En la combustión del butano: C4H10 + O2 CO2 + H2O; ¿Cuántos moles de oxígeno son
necesarios para obtener 40g de H2O?
2C4H10 + 13O2 8CO2 + 10H2O
13 moles de O2 ------------------ 10 moles de H2O 𝑚𝑎𝑠𝑎 40𝑔
# moles = = = 2.2 moles de H2O
X moles de O2 ------------- 40 g de H2O 𝑚𝑎𝑠𝑎 𝑚𝑜𝑙𝑒𝑐𝑢𝑙𝑎𝑟 18𝑔
M.A. (H) = 1g
13 moles de O2 ------------------ 10 moles de H2O
M. A. (O) = 16g
X moles de O2 ------------- 2.2 moles de H2O
X = 2.86 moles de O2
2. El metano arde con oxígeno produciendo dióxido de carbono y agua. Si se queman 2
kg de metano. Calcule los gramos de dióxido de carbono producidos.
CH4 + 2O2 CO2 + 2H2O
16g + 64g 44g + 36g
16g de CH4 ----------- 44g de CO2
2000g de CH4 ------- Xg de CO2 M.A. (C) = 12g; M.A. (H) = 4g; M.A. (O) = 16g
X = 5500g de CO2
3. Teniendo la ecuación: NH3 + F2 N2F4 + HF; calcular el moles de F2 para reaccionar
con 4 moles de HF.
2NH3 + 5F2 N2F4 + 6HF
5 moles de F2 ----------- 6 moles de HF X = 3.3 moles de F2
X moles de F2 ----------- 4 moles de HF
4. Se tiene la siguiente fermentación: C6H12O6 (ac) C2H5OH (ac) + CO2 (g); si se consumen 9g
de glucosa, ¿qué volumen CO2 de a CN se pueden obtener?
C6H12O6 (ac) 2C2H5OH (ac) + 2CO2 (g)
180g de C6H12O6 --------- 2 x (22.4)L de CO2
M.A. (C) = 12g; M.A. (H) = 4g; M.A. (O) = 16g
9g de C6H12O6 ------------ xL de CO2
X = 2.24L de CO2 M 1(C6H12O6) = 180g
1[(6 x 12) + (1 x 22) + (6 x 16)]
(180)
A CN: 1 mol 22.4L
5. ¿Cuántos litros de oxígeno se requiere para la combustión de completa de 10 litros de
gas propano (C3H8)?
C3H8+ 5O2 3CO2 + 4H2O
1L de C3H8 ---------- 5L de O2 relación volumétrica
10L de C3H8 -------- XL de O2 relación entregada
X = 50L de O2
You might also like
- Ejercicios Resueltos de EstequiometriaDocument4 pagesEjercicios Resueltos de EstequiometriaSaavedra Vidal Brandon SaulNo ratings yet
- Calculos QuimicosDocument2 pagesCalculos QuimicosRAUL ROJAS RAMOSNo ratings yet
- Entalpía de Formación EstándarDocument6 pagesEntalpía de Formación EstándarRonald Altamirano GonzalesNo ratings yet
- Operaciones y Procesos Unitarios PDFDocument273 pagesOperaciones y Procesos Unitarios PDFMARIAAAAAAAAAAANo ratings yet
- 4a DEFORMACIÓN UNITARIA DEL VOLUMENDocument4 pages4a DEFORMACIÓN UNITARIA DEL VOLUMENDina CopaNo ratings yet
- Tp1 MT2Document11 pagesTp1 MT2Jose BenitezNo ratings yet
- Metodo de RuffiniDocument6 pagesMetodo de RuffiniChristian CampanaNo ratings yet
- Cocina eléctrica consumo mesDocument2 pagesCocina eléctrica consumo mesJessy EvaristoNo ratings yet
- Problemas de EstequiometríaDocument3 pagesProblemas de EstequiometríaquimicahuergoNo ratings yet
- Química Orgánica - Hidrocarburos alifáticos y aromáticosDocument2 pagesQuímica Orgánica - Hidrocarburos alifáticos y aromáticoshumberto salinasNo ratings yet
- Ejemplo - 2 - ForjaDocument4 pagesEjemplo - 2 - Forjadiego bgNo ratings yet
- Procesos de Obtención Del AcrilonitriloDocument9 pagesProcesos de Obtención Del AcrilonitriloKmila de la CruzNo ratings yet
- Primera Guia de Termodinámica (1) - 1Document4 pagesPrimera Guia de Termodinámica (1) - 1xxzvicNo ratings yet
- Nomenclatura y fórmulas de compuestos de coordinaciónDocument8 pagesNomenclatura y fórmulas de compuestos de coordinaciónSolanch Olanda100% (1)
- 18 ElectrólisisDocument17 pages18 ElectrólisisOmar Duvan Rodriguez100% (1)
- Solucionario Guía Estequiometría I. Leyes y Conceptos de La EstequiometríaDocument3 pagesSolucionario Guía Estequiometría I. Leyes y Conceptos de La EstequiometríadanielNo ratings yet
- Algebra - J. Aurelio Baldor Contenidos Resumen MatedraticosDocument2 pagesAlgebra - J. Aurelio Baldor Contenidos Resumen MatedraticosPatyEdy Prado ZommersNo ratings yet
- Datos Purga de CalderaDocument5 pagesDatos Purga de CalderaDulce Rubi García AlfonsoNo ratings yet
- REACCIONES QUIMICAS - U9 Clases 25,26 y 27Document44 pagesREACCIONES QUIMICAS - U9 Clases 25,26 y 27Steven OsorioNo ratings yet
- BereDocument12 pagesBereDiego AP100% (1)
- Ejercicios RefrigeracionDocument3 pagesEjercicios RefrigeracionGuillermo Silva San MartínNo ratings yet
- Fundamentos de TermodinmicaDocument39 pagesFundamentos de TermodinmicaLuis AgudeloNo ratings yet
- Discusión Unidad 3.0Document2 pagesDiscusión Unidad 3.0Monica OlivarNo ratings yet
- Tema-4 20 21Document27 pagesTema-4 20 21Pilar de la CruzNo ratings yet
- Guía 7-Ejercicios Le ChatelierDocument2 pagesGuía 7-Ejercicios Le ChatelierVicente100% (1)
- Ejerc. CangilonesDocument3 pagesEjerc. Cangilonesmelina100% (1)
- Ejercicios Calor y TrabajoDocument2 pagesEjercicios Calor y TrabajoYarleskyNo ratings yet
- CalcinaciónDocument8 pagesCalcinaciónValentina Montaño GrisalesNo ratings yet
- Proyecto Grua TorreDocument10 pagesProyecto Grua TorreDavid Rivera100% (1)
- Problemas Resueltos de Equilibrio QuimicoDocument7 pagesProblemas Resueltos de Equilibrio Quimicomario alexisNo ratings yet
- Cuestionario N°10Document14 pagesCuestionario N°10Roger inturiasNo ratings yet
- Cop y RefrigeradoresDocument7 pagesCop y RefrigeradoresAnaluz CabellosNo ratings yet
- ESTEQUIOMETRIADocument3 pagesESTEQUIOMETRIAVianca Yucra Meneses100% (1)
- Clase Práctica 10Document2 pagesClase Práctica 10correofake09No ratings yet
- Electrolisis Soluciones Selectividad PDFDocument11 pagesElectrolisis Soluciones Selectividad PDFTorSan LuizNo ratings yet
- Taller Refrigerante R22Document2 pagesTaller Refrigerante R22Nicolás Elias Rivera FloresNo ratings yet
- Transferencia de calor entre una placa y aletas rectangulares: resolución numérica mediante diferencias finitasDocument11 pagesTransferencia de calor entre una placa y aletas rectangulares: resolución numérica mediante diferencias finitasnfcdlNo ratings yet
- Mezclado Adiabático de Flujos de AireDocument8 pagesMezclado Adiabático de Flujos de AireBryanNo ratings yet
- Examenes Resueltos de Quimica Basica PDFDocument266 pagesExamenes Resueltos de Quimica Basica PDFGabriel Sánchez Marín100% (3)
- Practica 10Document7 pagesPractica 10arnoldo_mercadoNo ratings yet
- Definición de Ciclo TermodinámicoDocument3 pagesDefinición de Ciclo TermodinámicoAlí Naveros Junco100% (1)
- Trabajo Practico #1 - Ecuaciones de La Combustión Completa de CombustiblesDocument26 pagesTrabajo Practico #1 - Ecuaciones de La Combustión Completa de CombustiblesGabriel Di Benedetto100% (1)
- Monografia Historia Del MotorDocument19 pagesMonografia Historia Del MotorDANIEL100% (1)
- T7 Motor Termico EjerciciosDocument6 pagesT7 Motor Termico EjerciciostallerbierzoNo ratings yet
- Apuntes Sistema Biela-Manivela - ActualDocument29 pagesApuntes Sistema Biela-Manivela - Actualcarlos marquezNo ratings yet
- Motores Stirling vs DiéselDocument10 pagesMotores Stirling vs DiéselJuan PachecoNo ratings yet
- Ejercicios Resueltos de Gases IdealesDocument8 pagesEjercicios Resueltos de Gases IdealesgrayNo ratings yet
- Ejercicio de CompresoresDocument2 pagesEjercicio de CompresoresJuan Ariel Aspi ApazaNo ratings yet
- Tarea TermodinamicaDocument4 pagesTarea TermodinamicaMichelle CervantesNo ratings yet
- Apuntes Fis IIDocument529 pagesApuntes Fis IIMaycol FernandoNo ratings yet
- Examen Final Organica I 2020-ADocument5 pagesExamen Final Organica I 2020-AEnrique Velasquez FelipeNo ratings yet
- Oposiciones Secundaria - Máquinas térmicas: eficiencia bomba calorDocument12 pagesOposiciones Secundaria - Máquinas térmicas: eficiencia bomba calorAngel sanchez vallejoNo ratings yet
- Solucionario de Fisicoquimica Primera y Segunda LeyDocument12 pagesSolucionario de Fisicoquimica Primera y Segunda LeyKeity Romero Violeth100% (1)
- B2-Equilibrio QuimicoDocument16 pagesB2-Equilibrio QuimicoKOBRINJANo ratings yet
- Examen FINAL RaquelDocument5 pagesExamen FINAL RaquelRaquel FloresNo ratings yet
- Ministerio de Defensa Nacional proporciona ejercicios de estequiometríaDocument4 pagesMinisterio de Defensa Nacional proporciona ejercicios de estequiometríaAna María Orjuela Vera100% (1)
- Serie de Estequiometría. Química General IDocument5 pagesSerie de Estequiometría. Química General IEros AlterNo ratings yet
- ESTEQUIOMETRIADocument17 pagesESTEQUIOMETRIAEstrellagonsales GonsalesNo ratings yet
- Combustión de monóxido de carbonoDocument7 pagesCombustión de monóxido de carbonoRodrigoNo ratings yet
- Seguridad LaboratorioDocument41 pagesSeguridad LaboratorioALEX RODOLFO MAYTA VARGASNo ratings yet
- V Sesión - Desarrollo Histórico de La Ética IIDocument10 pagesV Sesión - Desarrollo Histórico de La Ética IIALEX RODOLFO MAYTA VARGASNo ratings yet
- IV Sesión - Desarrollo Histórico de La ÉticaDocument10 pagesIV Sesión - Desarrollo Histórico de La ÉticaALEX RODOLFO MAYTA VARGASNo ratings yet
- QuellavecoDocument2 pagesQuellavecoALEX RODOLFO MAYTA VARGASNo ratings yet
- Tercer Movimiento AffettuossoDocument1 pageTercer Movimiento AffettuossoALEX RODOLFO MAYTA VARGASNo ratings yet
- III Sesión - La Moral, Conceptos BásicosDocument13 pagesIII Sesión - La Moral, Conceptos BásicosALEX RODOLFO MAYTA VARGASNo ratings yet
- I Sesión - Ética y Moral Como Disciplina FilosóficaDocument17 pagesI Sesión - Ética y Moral Como Disciplina FilosóficaALEX RODOLFO MAYTA VARGASNo ratings yet
- Tarea 2. Lectura LocalizaciónDocument3 pagesTarea 2. Lectura LocalizaciónALEX RODOLFO MAYTA VARGASNo ratings yet
- I. Ambiental P. Entrada - OkDocument2 pagesI. Ambiental P. Entrada - OkALEX RODOLFO MAYTA VARGASNo ratings yet
- TareaDocument3 pagesTareaALEX RODOLFO MAYTA VARGASNo ratings yet
- Áncash y CajamarcaDocument3 pagesÁncash y CajamarcaALEX RODOLFO MAYTA VARGASNo ratings yet
- Análisis PaperDocument1 pageAnálisis PaperALEX RODOLFO MAYTA VARGASNo ratings yet
- Áreas SombreadasDocument3 pagesÁreas SombreadasALEX RODOLFO MAYTA VARGASNo ratings yet
- CaligramasDocument1 pageCaligramasALEX RODOLFO MAYTA VARGASNo ratings yet
- Análisis PoemaDocument1 pageAnálisis PoemaALEX RODOLFO MAYTA VARGASNo ratings yet
- Ensayo Aguas Del SilalaDocument36 pagesEnsayo Aguas Del SilalaFernandoRodriguez50% (6)
- ArequipaDocument1 pageArequipaALEX RODOLFO MAYTA VARGASNo ratings yet
- Imágenes de PresidentesDocument1 pageImágenes de PresidentesALEX RODOLFO MAYTA VARGASNo ratings yet
- Bienes PublicosDocument13 pagesBienes PublicosALEX RODOLFO MAYTA VARGASNo ratings yet
- ManzanaDocument1 pageManzanaALEX RODOLFO MAYTA VARGASNo ratings yet
- Materia OscuraDocument34 pagesMateria OscuraALEX RODOLFO MAYTA VARGASNo ratings yet
- Análisis semántico de términos y enunciadosDocument2 pagesAnálisis semántico de términos y enunciadosALEX RODOLFO MAYTA VARGASNo ratings yet
- MarcoDocument1 pageMarcoALEX RODOLFO MAYTA VARGASNo ratings yet
- Diagrama de FlujoDocument1 pageDiagrama de FlujoALEX RODOLFO MAYTA VARGASNo ratings yet
- Diagrama WordDocument1 pageDiagrama WordALEX RODOLFO MAYTA VARGASNo ratings yet
- LaboratorioDocument10 pagesLaboratorioALEX RODOLFO MAYTA VARGASNo ratings yet
- AlimentosDocument3 pagesAlimentosALEX RODOLFO MAYTA VARGASNo ratings yet
- Lab 8-1Document4 pagesLab 8-1ALEX RODOLFO MAYTA VARGASNo ratings yet
- Articulo de ChernobylDocument6 pagesArticulo de ChernobylALEX RODOLFO MAYTA VARGAS100% (1)
- Gasener, El Gasoducto VirtualDocument25 pagesGasener, El Gasoducto VirtualFederico A. MartinezNo ratings yet
- Anexos TermoDocument4 pagesAnexos TermoClaudio AguirreNo ratings yet
- Catalogo - Sweiss y EliteDocument7 pagesCatalogo - Sweiss y EliteGeovaniPachecoNo ratings yet
- Gas Natural en EcuadorDocument12 pagesGas Natural en EcuadorEstefano MaldonadoNo ratings yet
- Brouchure AlcanosDocument57 pagesBrouchure AlcanosREDEGAS INGENIERIANo ratings yet
- Ejercicios TermodinamicaDocument8 pagesEjercicios Termodinamicacarlos garciaNo ratings yet
- Fase 4 - Anthony BrownDocument8 pagesFase 4 - Anthony BrownKatherine TorresNo ratings yet
- Prueba de Química I Medio: Reacciones QuímicasDocument6 pagesPrueba de Química I Medio: Reacciones QuímicasFabian CardozaNo ratings yet
- Ejercicio 6.4Document3 pagesEjercicio 6.4Miguel Angel Moncca BernalNo ratings yet
- Presentacion 5 - Contaminación de Aguas Superficiales 2Document52 pagesPresentacion 5 - Contaminación de Aguas Superficiales 2Jancarlo Mendoza MartínezNo ratings yet
- Procesamiento y Cap. de ProduccionDocument5 pagesProcesamiento y Cap. de ProduccionBrayan SilveraNo ratings yet
- N 6 Laboratorio Camara HiltonDocument35 pagesN 6 Laboratorio Camara HiltonVictor AlejandroNo ratings yet
- Test Mecanica Aeronáutica PDFDocument34 pagesTest Mecanica Aeronáutica PDFTRUKIINo ratings yet
- Seminario 1Document4 pagesSeminario 1Fiorella Bellido GuerraNo ratings yet
- Visor de Liquido DanfossDocument8 pagesVisor de Liquido DanfossStephania OrtigozaNo ratings yet
- Estequiometría de GasesDocument25 pagesEstequiometría de GasesKANELLNo ratings yet
- Actividad Integradora 3-6Document2 pagesActividad Integradora 3-6clementevasquezmirenaNo ratings yet
- Examen de EstequiometriaDocument9 pagesExamen de EstequiometriaLeticia CastroNo ratings yet
- Antecedent EsDocument2 pagesAntecedent EsBrian Montaño FernandezNo ratings yet
- Proceso de turbina de gas BraytonDocument13 pagesProceso de turbina de gas Braytonronni bermudezNo ratings yet
- Ejercicios de SecundariaDocument2 pagesEjercicios de SecundariaSergio Delgado RamosNo ratings yet
- Lab-N°3-ANÁLISIS DE GASES DE COMBUSTIÓN-grupo-03Document19 pagesLab-N°3-ANÁLISIS DE GASES DE COMBUSTIÓN-grupo-03joaquin Rojas FranciscoNo ratings yet
- Q SSM Diri Sem09Document1 pageQ SSM Diri Sem09WILLIAM ALVA LÓPEZNo ratings yet
- ESTEQUIOMETRIADocument3 pagesESTEQUIOMETRIAEliecer JoseNo ratings yet
- Constantes Termodinámicas para Elementos y Compuestos - Tabla ExtendidaDocument10 pagesConstantes Termodinámicas para Elementos y Compuestos - Tabla ExtendidaEingel BarbozaNo ratings yet
- Micro Plantas para La Produccion GNLDocument20 pagesMicro Plantas para La Produccion GNLLizbeth Ramirez AlanyaNo ratings yet
- Compresor Reciprocante Serie WDocument4 pagesCompresor Reciprocante Serie WJose Antonio Andrade CruzNo ratings yet
- Estequiometria 2Document5 pagesEstequiometria 2Aandy MartínezNo ratings yet
- 4-Formacion de Hidruros e HidracidosDocument12 pages4-Formacion de Hidruros e HidracidosGabrielNo ratings yet
- Consumos y Precios Combustible 2021 A Junio 2022Document69 pagesConsumos y Precios Combustible 2021 A Junio 2022Claudio JuarezNo ratings yet