Professional Documents
Culture Documents
ds2 4eme Sadiki09
Uploaded by
Mohieddine KhailiOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
ds2 4eme Sadiki09
Uploaded by
Mohieddine KhailiCopyright:
Available Formats
pH des acides des bases
oscillation mécanique
Serie Sciences Physiques N°10
éme
Khaili Mohieddine | 20144-2015 | 4 année Tech-Sc-Math
Chimie ( 7 points )
Exercice 1 : (2,5 pts) :
Activité documentaire : Constante d’équilibre dans les phénomènes biologiques.
Objectifs : - comprendre le mécanisme chimique « simplifié » de régulation du pH sanguin
- comprendre le rôle de ce mécanisme dans l’adaptation cardio-respiratoire à l’effort
« Lors du métabolisme basal de l'homme, l'énergie nécessaire provient de la transformation en
milieu oxygéné du glucose en dioxyde de carbone et eau. Le dioxyde de carbone est transporté par le
sang jusqu'aux poumons où il est alors éliminé par ventilation. Lors d'un effort physique intense, les
besoins énergétiques des muscles augmentent : le métabolisme basal augmente ainsi que la
ventilation. Dans certains cas, lorsque la ventilation est insuffisante, l'énergie nécessaire au
fonctionnement du muscle devient insuffisante : la crampe apparaît. Il se forme, dans la cellule
musculaire, de l'acide lactique qui, lorsqu'il passe dans le sang, provoque une diminution locale de son
pH du fait de la création en abondance de dioxyde de carbone dissous dans le sang. Cette diminution
du pH sanguin déclenche des ordres hypothalamiques qui vont amplifier la ventilation .»
pH du sang
Le sang est une solution aqueuse dont le pH varie très peu. Il se maintient entre 7,35 et 7,45
et ne peut subir que de très faibles fluctuations. Dans le cas contraire, de fortes fluctuations nuiraient
gravement à la santé.
Certains couples acide /base jouent un rôle essentiel dans la régulation du pH du sang,
en particulier le couple :
dioxyde de carbone dissous CO2 , H2O(aq) / ion hydrogénocarbonate HCO3-(aq)
Ce couple participe à une réaction acido-basique avec le couple H3O+(aq) / H2O(l)
1) Le dioxyde de carbone dissous dans l’eau CO2 + H2O H2CO3 . (1)
H2CO3 + H2O HCO3 + H3O .
- +
(2)
La constante d’équilibre associée à l’équation (2) vaut K = 7,9.10 à 37°C (température du corps
-7
humain).
a) Donner l’expression de la constante K. Pourquoi a-t-on précisé la température ?
b) Exprimer le rapport R = [HCO3-(aq) ] éq / [H2CO3] éq en fonction de K et de la concentration en ions
hydronium H3O+ présents dans le sang .
c) En déduire pourquoi ce rapport doit rester constant dans le sang.
Régulation du pH du sang lors d’un effort physique
2)Lors d’un effort physique, la demande énergétique des muscles augmente. Cette demande
s’accompagne de la libération d’acide lactique CH3-CHOH-COOH dans le sang. Cet acide réagit avec les
ions hydrogénocarbonate HCO3- entraînant ainsi une diminution de leur concentration et une
augmentation de celle du dioxyde de carbone CO2 dissous.
a) Ecrire l’équation de la réaction entre l’acide lactique et les ions hydrogénocarbonate.
b) Justifier les variations de concentrations que cette réaction provoque.
3) Pour maintenir le rapport R et le pH sanguin constants, l’excès de dioxyde de carbone est éliminé
par la voie respiratoire et des ions hydrogénocarbonate sont produits au sein de l’organisme.
La respiration contribue au maintien de l’équilibre acido/basique en éliminant le dioxyde de carbone et
donc l’acide lactique en excès. Expliquer pourquoi le rythme respiratoire augmente au cours
d’un effort.
Exercice 2 : (4,5 pts) :
Collège Sadiki 1/ Devoir de synthèse n° : 2 2008/2009
Toutes les solutions sont prises à la température 25°C, température à laquelle pKe = 14.
On dispose de quatre solutions S1, S2, S3, et S4
Solution C(mol.L-1) pH
S1 (HCl) C1 2,90
S2 (CH3COOH ) C2= 0,10 2,90
S3 ( HCOOH ) C3= C2 2,40
S4 ( NH3 ) C4= 5.10-2 10,95
1- Montrer que l’acide éthanoïque CH3COOH est faible.
2- a- Sachant que l’acide chlorhydrique est fort, comparer sans calcul C 1 et C2. Justifier.
b- Calculer C1.
3- On considère la solution S2 d’acide éthanoïque
a- Dresser le tableau d’évolution de cette réaction au cours du temps puis calculer les
concentrations molaires des différentes espèces chimiques présentes dans la solution.
b- Calculer le taux d’avancement final 2f de la réaction. Montrer que CH3COOH est faiblement
ionisé.
c- Etablir alors la relation suivante : Ka =C2. 2f . Calculer le pKa du couple CH3COOH/CH3COO-
2
d- En utilisant la relation précédente, montrer que la dilution favorise l’ionisation d’un acide faible.
4- Calculer le taux d’avancement final .3f de l’acide méthanoïque. Dire, en le justifiant, si HCOOH
est plus fort ou plus faible que CH3COOH ?
5- Dans la suite, on suppose que la base NH3 est faiblement ionisée.
a- Donner l’expression de son pH en fonction de pKe, C4 et de pKa du couple NH4+/NH3.
b- A un volume V0=5 mL de la solution S4 on ajoute un volume d’eau Ve pour obtenir une solution
S’4 d’ammoniac de concentration molaire C’4=2,5.10-3mol.L-1.
Décrire le protocole expérimental permettant d’obtenir S’4.
Calculer le pH de S’4 ainsi que Ve.
R( )S(
Physique ( 13 points )
)
Exercice 1 : (6,5 pts) : O i x
Fig 1Fig.
Le pendule élastique horizontal de la 5
figure 1 est constitué par un solde (S) de masse m=0,2 Kg soudé à
l’une des extrémités d’un ressort (R ) à spires non jointives de masse négligeable et de constante de
raideur K, l’autre extrémité est attaché à un support fixe. A
x(cm)
l’équilibre, le centre d’inertie (G) du solide (S) coïncide avec
4
l’origine O d’un repère espace horizontal (O,\s\up9(o).
Partie A. 3
A partir du point O, on écarte le solide (S) vers un point
A d’abscisse xA et à la date t=0 s, on l’abandonne à lui- 2
même sans vitesse initiale. Au cours de son mouvement, le 1
solide (S) se déplace sans frottement et son centre t(s)
d’inertie (G) est repéré par l’élongation OG=x(t). Un
/
système d’acquisition de données, enregistre les variations
8
de l’élongation x au cours du temps (Voir figure 2).
1- En utilisant le graphe :
a- Préciser la nature de mouvement de (S).
Fig 2
b- Déterminer l’abscisse initiale xA du solide (S) et la
constante de raideur K du ressort.
c- Dans quel sens, débute le mouvement du solide (S).
Collège Sadiki 2/ Devoir de synthèse n° : 2 2008/2009
2- Ecrire la loi horaire x=f(t) de mouvement du solide. Déduire l’équation différentielle du
mouvement.
3- L’énergie cinétique du solide Ec = varie au cours du temps selon une fonction sinusoïdale de
période T
a- Etablir l’expression de EC en fonction du temps.
b- Donner la valeur de T.
4- L’énergie mécanique du système ={solide + ressort} est E =EC + Ep avec Ep= .
a- Montrer que cette énergie est constante.
b- Comment apparaît cette énergie aux instants t1=0s, t2= s et t3= s.
Partie B.
L’oscillateur est maintenant soumis à des forces de frottement visqueux équivalents à une
force unique \s\up9(o = - h.\s\up9(o avec h est une constante positive.
1- Etablir l’équation différentielle vérifiée par l’élongation x de (G).
2- Montrer que l’énergie totale du système ={solide + ressort} diminue au cours du temps.
3- A l’aide d’un dispositif approprié, on a enregistré le diagramme d’espace de mouvement du
solide, le résultat est donné par le graphe de la figure 3.
a- Quel est le nom du régime d’oscillations ?
b- Sachant que la variation de l’énergie totale du système {solide + ressort} est égal au travail de
la force de frottement. Calculer ce travail entre les instants t1=0s et t2= .
x(cm)
4
3
2
1
t(s)
/
8
Fig 3
Exercice 2 : (6,5 pts) )S(
R(
Un pendule élastique est constitué d’un
)
ressort à spires non jointives, de masse négligeable et de constante
de raideur K, et d’un solide (S) supposé ponctuel de masse m. Le O i x
solide (S) peut se déplacer sans frottement sur un plan horizontal. Sa Fig 1Fig.
5
position est repérée par son abscisse x dans le repère (O,\s\up9(o)
avec O la position d’équilibre de (S) (fig 1 ). On soumet (S) à une force excitatrice \s\up9(o= F.
\s\up9(o =Fmsin(t + F)\s\up9(o et à une force de frottement \s\up9(o= -h\s\up9(o avec \s\up9(o
la vitesse de (S) et h une constante positive.
1- Etablir l’équation différentielle régissant les variations de l’élongation x.
2- Pour une certaine valeur h1 de h et une valeur 1 de , on obtient les courbes de variations de
F et de x en fonction de temps (fig 2).
a- Montrer que la courbe C1 correspond à F(t).
b- Déterminer la valeur de 1, Fm, Xm, et F -x.
c- Quelle est la valeur de F ? Déduire celle de x.
d- Faire la construction de Fresnel correspondante. Déduire les expressions de X m et de
sin(F -x). Calculer h1.
Collège Sadiki 3/ Devoir de synthèse n° : 2 2008/2009
x(cm) F(N)
C1
0,2 N
C2 4 cm
t(s)
Fig 2
/24
3- Pour une certaine valeur r de , on constate r2(rad.s-1)2
que Xm prend sa valeur la plus élevée.
a- Dans quel état se trouve l’oscillateur ?
b- On donne la courbe de variation de r2 en 100
fonction de h2 (fig 3) ainsi que l’expression de
r = .
Déterminer K et m.
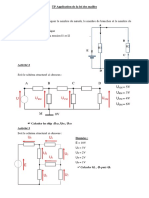
4- En précisant l’analogie utilisée donner:
a- Le schéma du montage du circuit électrique 40
analogue à l’oscillateur mécanique
précédent.
b- L’expression de la charge maximale Qm du h2(Kg.s-1)2
condensateur. 0
c- L’expression de la pulsation r 0 4 8
correspondant à la valeur la plus élevée de
Qm.
Collège Sadiki 4/ Devoir de synthèse n° : 2 2008/2009
You might also like
- Compo Physique TCDocument2 pagesCompo Physique TCLeila LaoualiNo ratings yet
- Togo BAC D 2020 Sciences PhysiquesDocument2 pagesTogo BAC D 2020 Sciences PhysiqueszedicusboonNo ratings yet
- 4e DC2 20010 2011finaleDocument4 pages4e DC2 20010 2011finalefethi1100% (1)
- Devoir 3 Modele 4 Physique Chimie 2 Bac SPC Semestre 2 1Document6 pagesDevoir 3 Modele 4 Physique Chimie 2 Bac SPC Semestre 2 1ال' وداديةNo ratings yet
- 4 Ème - SC - Exp Profs - Abid - Hrizi - Feki Et Cherchari. Collège Sadiki Devoir de Synthèse N - 2 Samedi Chimie (9 Points)Document5 pages4 Ème - SC - Exp Profs - Abid - Hrizi - Feki Et Cherchari. Collège Sadiki Devoir de Synthèse N - 2 Samedi Chimie (9 Points)torkitaher100% (1)
- Devoir de Controle 2 2024 Bac MathDocument4 pagesDevoir de Controle 2 2024 Bac MathHamdi MinyarNo ratings yet
- D3 TS2 2023 LSLL - WahabdiopDocument2 pagesD3 TS2 2023 LSLL - Wahabdiopxzzn7x2tc9No ratings yet
- Devoir III 2nde S LANL 14-15Document2 pagesDevoir III 2nde S LANL 14-15Doro CisséNo ratings yet
- Série D'exercices #14 - Sciences Physiques PH Des Solutions Aqueuses - Oscillations Mécaniques Forcées - Bac Sciences Exp (2014-2015) MR Adam Bouali PDFDocument4 pagesSérie D'exercices #14 - Sciences Physiques PH Des Solutions Aqueuses - Oscillations Mécaniques Forcées - Bac Sciences Exp (2014-2015) MR Adam Bouali PDFDadati SouNo ratings yet
- Série D'exercices N°1 - Sciences Physiques Cinétique Chmique, Dosage Acide-Base, Dipôle RL, Oscillations Mécaniques Forcées - Bac Sciences Exp (2010-2011) MR Abdmouleh NabilDocument5 pagesSérie D'exercices N°1 - Sciences Physiques Cinétique Chmique, Dosage Acide-Base, Dipôle RL, Oscillations Mécaniques Forcées - Bac Sciences Exp (2010-2011) MR Abdmouleh NabilhammouazizNo ratings yet
- Spectrographe de MasseDocument4 pagesSpectrographe de MasseHaykelGaouaNo ratings yet
- Devoir de Revision3 2023bac Math DefDocument5 pagesDevoir de Revision3 2023bac Math DefNour Nessah100% (1)
- 61295cc080954devoir 1 Physique Chimie Niveau Terminale D LyceeDocument3 pages61295cc080954devoir 1 Physique Chimie Niveau Terminale D LyceeJaphet BAOUNDOULANo ratings yet
- Devoir de Niveau N°6 de Sciences Physiques: EXERCICE 1 (5 Points)Document3 pagesDevoir de Niveau N°6 de Sciences Physiques: EXERCICE 1 (5 Points)Japhet BAOUNDOULANo ratings yet
- Devoir de Contrôle N°2 - Sciences PhysiquesDocument3 pagesDevoir de Contrôle N°2 - Sciences Physiqueskougfst ldhd100% (1)
- Devoir 4 20172018 TDocument3 pagesDevoir 4 20172018 TAmadou Makhtar SeckNo ratings yet
- Devoir Bac MathDocument5 pagesDevoir Bac MathLotfi KhemiliNo ratings yet
- Stock LesPdf Examens BAC Comores Sujet 2011 Comores Sujet C Physique-Chimie Bac 2011Document3 pagesStock LesPdf Examens BAC Comores Sujet 2011 Comores Sujet C Physique-Chimie Bac 2011Base Ninho NinhoNo ratings yet
- DS2 (06 03 09)Document7 pagesDS2 (06 03 09)Seif Souid100% (3)
- Devoir de Synthèse N°1 1er Semestre - Sciences Physiques - Bac Sciences Exp (2018-2019) MR Foued Bahlous PDFDocument7 pagesDevoir de Synthèse N°1 1er Semestre - Sciences Physiques - Bac Sciences Exp (2018-2019) MR Foued Bahlous PDFMohamed SaidiNo ratings yet
- Devoir de Synthèse N°2 - Sciences physiques Chimie pH et Dosage Physique Oscillations mécaniques - Bac Sciences exp (2012-2013) Mr EL Hafi MustaphaDocument4 pagesDevoir de Synthèse N°2 - Sciences physiques Chimie pH et Dosage Physique Oscillations mécaniques - Bac Sciences exp (2012-2013) Mr EL Hafi MustaphaFelhi mokhtarNo ratings yet
- Devoir de Synthèse N°2 Avec Correction 2012 2013 (Sidi Zikri)Document11 pagesDevoir de Synthèse N°2 Avec Correction 2012 2013 (Sidi Zikri)fayeNo ratings yet
- Devoir de Synthèse N°2 Lycée Pilote - Sciences Physiques - Bac Mathématiques (2010-2011) MR Sfaxi SalahDocument4 pagesDevoir de Synthèse N°2 Lycée Pilote - Sciences Physiques - Bac Mathématiques (2010-2011) MR Sfaxi SalahaladinNo ratings yet
- Bac Blanc D PMK 2021Document5 pagesBac Blanc D PMK 2021InnocentNo ratings yet
- Sujet S1S3 2021 RemplDocument4 pagesSujet S1S3 2021 Remplpapa samba sarrNo ratings yet
- 1 EXAMEN BLANC 2019 PC Tle DDocument2 pages1 EXAMEN BLANC 2019 PC Tle DabdoulhakimouabkarimousanouNo ratings yet
- WWW Devoir TN PDFDocument9 pagesWWW Devoir TN PDFBechir Ben MezhoudNo ratings yet
- Devoir 4Document4 pagesDevoir 4younesNo ratings yet
- Série D'exercices N°1 - Physique Série de Revision 2eme Trimestre - Bac Toutes Sections (2012-2013) Mme Titouhi ImenDocument6 pagesSérie D'exercices N°1 - Physique Série de Revision 2eme Trimestre - Bac Toutes Sections (2012-2013) Mme Titouhi ImenTawfiq Weld EL ArbiNo ratings yet
- Bac PC 2019 CDocument3 pagesBac PC 2019 Cmalick Semour100% (1)
- Chimie or Plase ProjDocument3 pagesChimie or Plase ProjSydahmed YoussefNo ratings yet
- 1cm5q85h9 308900Document4 pages1cm5q85h9 308900Armel Marc KouchoewanouNo ratings yet
- Bac 2015Document3 pagesBac 2015DaniokoNo ratings yet
- Cours - Physique DEVOIR CONTROLE N°2 - Bac Sciences Exp (2012-2013) MR TLILI TOUHAMIDocument3 pagesCours - Physique DEVOIR CONTROLE N°2 - Bac Sciences Exp (2012-2013) MR TLILI TOUHAMIMohamed HamdeneNo ratings yet
- Devoir Up PhysiqueDocument4 pagesDevoir Up PhysiquedianechibidouxNo ratings yet
- Compo1 20162017Document4 pagesCompo1 20162017GueyeNo ratings yet
- DS2 (05 03 10)Document9 pagesDS2 (05 03 10)Seif Souid100% (5)
- Sujet PC TDDocument2 pagesSujet PC TDagbegnezikomiNo ratings yet
- Dev 4 Ts 22019Document4 pagesDev 4 Ts 22019Amadou Makhtar SeckNo ratings yet
- Devoir de Contrôle N°3 - Sciences Physiques - Bac Sciences Exp (2013-2014) MR Bouhani & Shiri PDFDocument5 pagesDevoir de Contrôle N°3 - Sciences Physiques - Bac Sciences Exp (2013-2014) MR Bouhani & Shiri PDFLotfi BoucharebNo ratings yet
- DEVOIR DE CONTROLE 2 SCIENCES PHYSIQUES 4EME MATHDocument3 pagesDEVOIR DE CONTROLE 2 SCIENCES PHYSIQUES 4EME MATHMohamed ElouakilNo ratings yet
- Composition PC TS2 17 IaDocument3 pagesComposition PC TS2 17 Iat87d4jyrqkNo ratings yet
- C2 S1 1bac BIOF SM Prof - Elfatimy (WWW - Pc1.ma) PDFDocument2 pagesC2 S1 1bac BIOF SM Prof - Elfatimy (WWW - Pc1.ma) PDFahmedNo ratings yet
- DS3-4M - 2021 (Pilote Nabel)Document6 pagesDS3-4M - 2021 (Pilote Nabel)Jihed HorchaniNo ratings yet
- Devoir-1 - 2019Document1 pageDevoir-1 - 2019ygzybpsy6wNo ratings yet
- DC2 Q M Copie FINALEDocument4 pagesDC2 Q M Copie FINALEomar sellemi0% (2)
- Bac Blanc 2019 1Document4 pagesBac Blanc 2019 1Amadou Makhtar SeckNo ratings yet
- Chimie (7 Points) : EsterDocument2 pagesChimie (7 Points) : EsterboustakatbNo ratings yet
- Bac Blanc 2 ts2 1Document5 pagesBac Blanc 2 ts2 1Amadou Makhtar SeckNo ratings yet
- SP SUJET TS2-01-2022-iakaf-WahabDiopDocument4 pagesSP SUJET TS2-01-2022-iakaf-WahabDiopSerigne saliou GayeNo ratings yet
- Chimie (7 Points) : Durée 2hDocument2 pagesChimie (7 Points) : Durée 2hSalimoune TihouNo ratings yet
- Annales de Mathématiques, Baccalauréat C et E, Cameroun, 2008 - 2018: Sujets et CorrigésFrom EverandAnnales de Mathématiques, Baccalauréat C et E, Cameroun, 2008 - 2018: Sujets et CorrigésRating: 4.5 out of 5 stars4.5/5 (4)
- 1 Com Nat Recueil Exercices IeBC PDFDocument23 pages1 Com Nat Recueil Exercices IeBC PDFMohieddine KhailiNo ratings yet
- Noyauatomique PDFDocument19 pagesNoyauatomique PDFMohieddine KhailiNo ratings yet
- D - Croissance Radioactive BIOF PDFDocument8 pagesD - Croissance Radioactive BIOF PDFAicha DaouNo ratings yet
- TP Étudier La Propagation D'une Onde UltrasonoreDocument1 pageTP Étudier La Propagation D'une Onde UltrasonoreMohieddine KhailiNo ratings yet
- D - Croissance Radioactive BIOF PDFDocument8 pagesD - Croissance Radioactive BIOF PDFAicha DaouNo ratings yet
- MAG Oscillations Mecanique4M Pages 1 - 17 - Text Version - AnyFlipDocument17 pagesMAG Oscillations Mecanique4M Pages 1 - 17 - Text Version - AnyFlipMohieddine KhailiNo ratings yet
- TS - Chim 8 - CoursDocument6 pagesTS - Chim 8 - CoursMohieddine KhailiNo ratings yet
- Terminale D PDFDocument75 pagesTerminale D PDFMohieddine Khaili100% (6)
- Livret RadioactiviteDocument10 pagesLivret RadioactiviteMohieddine KhailiNo ratings yet
- TS - Chim 7 - CoursDocument8 pagesTS - Chim 7 - CoursMohieddine KhailiNo ratings yet
- TP5 Titrage PHmetrique CorrectionDocument4 pagesTP5 Titrage PHmetrique CorrectionMohieddine KhailiNo ratings yet
- TD Oscillations Mécaniques LibresDocument2 pagesTD Oscillations Mécaniques LibresMohieddine Khaili100% (3)
- Mouvement PDFDocument6 pagesMouvement PDFMohieddine KhailiNo ratings yet
- Ondes Et ElectromagnetismeDocument242 pagesOndes Et ElectromagnetismeAbdelhak Sassi100% (7)
- Chap1: Les Caractéristiques D'un Mouvement.: A La Fin Du Chapitre, Tu Dois ConnaitreDocument5 pagesChap1: Les Caractéristiques D'un Mouvement.: A La Fin Du Chapitre, Tu Dois ConnaitreMohieddine KhailiNo ratings yet
- Cours Mouvements Et Forces PDFDocument6 pagesCours Mouvements Et Forces PDFMohieddine KhailiNo ratings yet
- Activité 2 PDFDocument1 pageActivité 2 PDFMohieddine KhailiNo ratings yet
- Chapitre6 Mouvement Mecanique PDFDocument15 pagesChapitre6 Mouvement Mecanique PDFMohieddine KhailiNo ratings yet
- Cinematique Du Point CorrectionDocument8 pagesCinematique Du Point CorrectionMohieddine Khaili100% (1)
- 1 Sec ch-2,3,4,5,6Document7 pages1 Sec ch-2,3,4,5,6Mohieddine KhailiNo ratings yet
- Ordre de Réaction - WikipédiaDocument1 pageOrdre de Réaction - WikipédiaMohieddine Khaili100% (1)
- 1 Sec ch-2,3,4,5,6Document3 pages1 Sec ch-2,3,4,5,6Mohieddine KhailiNo ratings yet
- 4 RL PDFDocument8 pages4 RL PDFAzizElheniNo ratings yet
- 1 Sec ch-2,3,4,5,6Document3 pages1 Sec ch-2,3,4,5,6Mohieddine KhailiNo ratings yet
- Exercices Sur Le Dipôle RLDocument8 pagesExercices Sur Le Dipôle RLMohieddine KhailiNo ratings yet
- Dosage Acide Base IndicDocument3 pagesDosage Acide Base IndicAs Ma50% (2)
- Cours de Chimie Des Solutions F PDFDocument76 pagesCours de Chimie Des Solutions F PDFaziz120786% (7)
- Activité 1Document1 pageActivité 1Mohieddine KhailiNo ratings yet
- c1 Cinetique ChimiqueDocument4 pagesc1 Cinetique ChimiqueMohieddine KhailiNo ratings yet
- Série D'exercices - Sciences Physiques - Oscillations Mécaniques Libres - Bac Sciences Exp (2018-2019) MR Guesmi JamelDocument6 pagesSérie D'exercices - Sciences Physiques - Oscillations Mécaniques Libres - Bac Sciences Exp (2018-2019) MR Guesmi Jamelmaram lassouedNo ratings yet
- CONVERGENCE 2nd Devoir Du 2nd Trimestre de 2ndeDocument2 pagesCONVERGENCE 2nd Devoir Du 2nd Trimestre de 2ndeSawadogoNo ratings yet
- DS 1 - CorrectionDocument4 pagesDS 1 - CorrectionTN HUNTERSNo ratings yet
- DL N°4Document6 pagesDL N°4Chai mae AgnawNo ratings yet
- La TensionDocument7 pagesLa TensionPierre GazeillesNo ratings yet
- Concours Advance Sujet Corrige 2017 PhysiqueDocument8 pagesConcours Advance Sujet Corrige 2017 PhysiqueAbderrazzakHamamaNo ratings yet
- Surveillance Des Machines Par Analyse Des VibrationsDocument337 pagesSurveillance Des Machines Par Analyse Des VibrationsIdren9792% (12)
- Alchimie Et Chimie PDFDocument40 pagesAlchimie Et Chimie PDFfuzzy_slugNo ratings yet
- Etude Experimentale Du Sechage Convectif de La MenDocument6 pagesEtude Experimentale Du Sechage Convectif de La Menkhaoula-adelNo ratings yet
- Lecon 1 Travail Et Puissance - OdtDocument5 pagesLecon 1 Travail Et Puissance - OdtAuray VilaynardNo ratings yet
- TD2 Mécanique Quantique 2020Document1 pageTD2 Mécanique Quantique 2020sakhir sarrNo ratings yet
- Les Bases de La Mecanique SynergetiqueDocument8 pagesLes Bases de La Mecanique SynergetiqueLionel ElyansunNo ratings yet
- 13.8. Exo Bac Muons Et VolcanDocument5 pages13.8. Exo Bac Muons Et VolcanMontacir YoussefNo ratings yet
- P 3 TD Meca Extrait BtsDocument8 pagesP 3 TD Meca Extrait BtsFatima ZoheaNo ratings yet
- Cinématique ExercicesDocument9 pagesCinématique ExercicesSébastien NiyonzimaNo ratings yet
- Cours CH1 - Cinétique Des Systèmes MatérielsDocument15 pagesCours CH1 - Cinétique Des Systèmes MatérielsAdamNo ratings yet
- PycnomètreDocument3 pagesPycnomètreToto ToualiNo ratings yet
- L3MEC Tdmeca 2015-16-New PDFDocument20 pagesL3MEC Tdmeca 2015-16-New PDFBruno GomesNo ratings yet
- TDMeca 7Document4 pagesTDMeca 7Ihsan MokhlisseNo ratings yet
- Chap 9 Dynamique D'un Solide en Rotation Autour D'un Axe PDFDocument9 pagesChap 9 Dynamique D'un Solide en Rotation Autour D'un Axe PDFkoung nkombaNo ratings yet
- Examen Régional Oriental 2018Document2 pagesExamen Régional Oriental 2018rawadNo ratings yet
- Lecon 2 Énergie Mécanique Et Énergie CinétiqueDocument2 pagesLecon 2 Énergie Mécanique Et Énergie CinétiqueSomephone DupontNo ratings yet
- Chapitre 2 Cours Sur L'electromagnetismeDocument4 pagesChapitre 2 Cours Sur L'electromagnetismewillfriedNo ratings yet
- Énergie Potentielle ExercicesDocument3 pagesÉnergie Potentielle ExercicesBHIH ChaimaeNo ratings yet
- Mouv Rect CoursDocument7 pagesMouv Rect Coursamine bouguernNo ratings yet
- Ch15 Force Mouvement SportDocument5 pagesCh15 Force Mouvement Sporthakima032No ratings yet
- Apsim CNC Sii MP Psi 2020Document13 pagesApsim CNC Sii MP Psi 2020Lamiaa CherkaNo ratings yet
- Mecanique Des Fluides Pour Ingenieurs PDFDocument211 pagesMecanique Des Fluides Pour Ingenieurs PDFNgongang100% (2)
- Touret A Meuler Corrige PDFDocument2 pagesTouret A Meuler Corrige PDFMohamed Soibaha ChaambaneNo ratings yet
- Physique - S4 - Tle CDocument5 pagesPhysique - S4 - Tle Calbertmanyinga100% (1)