Professional Documents
Culture Documents
Clase Práctica No 4
Uploaded by
Victor GarciaCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Clase Práctica No 4
Uploaded by
Victor GarciaCopyright:
Available Formats
Clase práctica No.
1. Demuestre que la expresión de Clausius-Clapeyron: lnP = -Hvap./RT + C es, para dos condiciones
distintas de P (P1 y P2) a temperaturas respectivas T1 y T2, equivalente a la expresión:
ln P1/P2 = (Hvap./R)((T1 – T2)/(T1*T2))
2. La presión de vapor del benceno, C6H6, es de 40.1 mmHg a 7.6°C. ¿Cuál es su presión de vapor a
60.6°C? El calor molar de vaporización del benceno es de 31.0 kJ/mol. R. 331 mmHg
3. Una muestra de agua de 1.2 g se inyecta en un matraz al vacío con capacidad de 5 L a 65°C. ¿Qué
porcentaje de agua se evapora cuando el sistema alcanza el equilibrio? Suponga un comportamiento
ideal del vapor de agua y no considere el volumen del agua líquida. La presión de vapor de agua a
65°C es de 187.5 mmHg. R. 66.8%
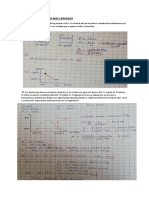
4. A continuación se muestran varias mediciones de presión de vapor para el mercurio a distintas
temperaturas. Determine mediante una gráfica el calor molar de vaporización del mercurio.
t (°C) 200 250 300 320 340
P (mmHg) 17.3 74.4 246.8 376.3 557.9
R. 59 kJ/mol (de la Tabla 11.6)
5. La presión de vapor del etanol es de 100 mmHg a 34.9°C. ¿Cuál es su presión de vapor a 63.5°C?
(El calor molar de vaporización del etanol es de 39.3 kJ/mol). R. 369 mmHg
6. Los calores molares de fusión y sublimación del yodo molecular son 15.27 kJ/mol y 62.30 kJ/mol,
respectivamente. Calcule el calor molar de vaporización del yodo líquido. R. 47.03 kJ/mol
7. Calcule el calor que se libera cuando 68 g de vapor a 124 ºC se convierten en agua a 45 ºC.
Hcond. = - 40.79 KJ/mol; svapor = 1.99 J/g.ºC; sagua liq. = 4.184 J/g.ºC R. 173 kJ
8. ¿Cuánto calor (en kJ) se necesitaría para convertir 866 g de hielo a -10°C en vapor a 126°C? (Los
calores específicos del hielo y del vapor son 2.03 J/g.°C y 1.99 J/g.°C, respectivamente. Los calores
molares de fusión y vaporización son 6.01 kJ/mol y 40.79 kJ/mol).
R. 2.67*103 kJ
9. El café secado por liofilización se prepara extrayendo por lixiviación (extracción sólido-líquido) los
componentes solubles, luego se congela el extracto y posteriormente se elimina directamente el hielo
mediante el uso de presiones de vacío. Describa los cambios de fase que suceden en este proceso.
10. En el gráfico que se muestra, marque las regiones A, B y C y prediga
que sucedería si: a) a partir de A, la temperatura se eleva a presión ● B
P ● A
constante, b) a partir de C, la temperatura se reduce a presión constante
y c) a partir de B, la presión se reduce a temperatura constante.
● C
You might also like
- Guia Problemas Cambio Estado SP-GR PDFDocument10 pagesGuia Problemas Cambio Estado SP-GR PDFManuel Bravo AntorNo ratings yet
- Practica 02 FQ 2018Document3 pagesPractica 02 FQ 2018juancalp81100% (1)
- Problemas Sobre CalorímetrosDocument1 pageProblemas Sobre CalorímetrosAndres Valencia50% (2)
- Ejercicios Castellan Fisicoquimica 2 ResueltosDocument2 pagesEjercicios Castellan Fisicoquimica 2 Resueltosbraulio moises gutierrez mozombite0% (2)
- Equilibrio QuimicoDocument6 pagesEquilibrio QuimicoLeonardo SashaNo ratings yet
- Tarea 23Document5 pagesTarea 23ODALYSNo ratings yet
- T2 Fisicoquimica Seccion 2Document10 pagesT2 Fisicoquimica Seccion 2EsliDavidMolerosIngunzaNo ratings yet
- Ejercicios Diametro Molecular.Document6 pagesEjercicios Diametro Molecular.Nilton CesarNo ratings yet
- Evaluacion2 2018Document4 pagesEvaluacion2 2018Fidel Sanchez GallegosNo ratings yet
- Problemas Resueltos Tema IIDocument15 pagesProblemas Resueltos Tema IIPaulina AlcocerNo ratings yet
- Examen de Fisicoquimica I FiqDocument1 pageExamen de Fisicoquimica I FiqALVAREZ QUITO ALBERTO BRYAMNo ratings yet
- Endarodríguez PDFDocument14 pagesEndarodríguez PDFBrenda Rodriguez100% (1)
- Pendulo Mas (Preguntas Resaltadas)Document4 pagesPendulo Mas (Preguntas Resaltadas)JhomiraRoñaNo ratings yet
- PD Quimica Sem 7Document6 pagesPD Quimica Sem 7Lesa BreliNo ratings yet
- Informe Nº6 Labo de Q.organica 1 (Aldehidos y Cetonas)Document24 pagesInforme Nº6 Labo de Q.organica 1 (Aldehidos y Cetonas)AldoCabreraFernandezNo ratings yet
- Tarea de Balance de Materia y Energía Kenny CoxDocument13 pagesTarea de Balance de Materia y Energía Kenny CoxKenny CoxNo ratings yet
- Tarea 9 - Definiciones Ácido - Base PDFDocument2 pagesTarea 9 - Definiciones Ácido - Base PDFCuau SuarezNo ratings yet
- RESOLVERDocument2 pagesRESOLVERAna María Muñoz JaramilloNo ratings yet
- YODOMETRIADocument17 pagesYODOMETRIASalazar Terrazas Nicole VivianaNo ratings yet
- Determinacion Del Calor Específico de LiquidosDocument10 pagesDeterminacion Del Calor Específico de LiquidosAnamariaRoblesrivasNo ratings yet
- Grupo 2Document5 pagesGrupo 2Jhonatan choqueNo ratings yet
- Trabajo Grupal 5Document1 pageTrabajo Grupal 5Richard Qvispe CNo ratings yet
- Aporte Los Tres Ejercicios DesarrolladosDocument9 pagesAporte Los Tres Ejercicios Desarrolladosmaria duarteNo ratings yet
- Ejercicios de TecnoDocument12 pagesEjercicios de TecnoESTEBAN JAIR RODAS CASTILLONo ratings yet
- Termo 5Document43 pagesTermo 5Esvit AlzamoraNo ratings yet
- Presion Manometrica Marco TeoricoDocument4 pagesPresion Manometrica Marco TeoricoAlexia Gomez MartelNo ratings yet
- Introducción A La Transferencia de CalorDocument13 pagesIntroducción A La Transferencia de Calorluis salinas rojasNo ratings yet
- Huaman Montoya Elmer YandirDocument9 pagesHuaman Montoya Elmer YandirErnesto Laura PeñaNo ratings yet
- Ejercicios Unidad IiiDocument3 pagesEjercicios Unidad IiiRoosvel Soto DiazNo ratings yet
- Problemas de Producto de SolubilidadDocument3 pagesProblemas de Producto de SolubilidadAlonsoNo ratings yet
- TALLER 3 BalanceDocument5 pagesTALLER 3 BalanceJhonatan SalazarNo ratings yet
- Ejercicios de Análisis GravimétricoDocument1 pageEjercicios de Análisis GravimétricoRosmery GonzalesNo ratings yet
- Balances de Masa y Ecuaciones DiferencialesDocument9 pagesBalances de Masa y Ecuaciones DiferencialesCastillolera CitivilNo ratings yet
- Ejercicios BalanceDocument2 pagesEjercicios BalanceCarlos Garduza GarcíaNo ratings yet
- Laboratorio Analítica Práctica 9Document10 pagesLaboratorio Analítica Práctica 9Ethel DekkerNo ratings yet
- TallerDocument1 pageTallerEnrique Jose Briceño Torres0% (1)
- Separata - Problemas de Termoquímica PDFDocument35 pagesSeparata - Problemas de Termoquímica PDFEduardo Daniel Ortiz TorresNo ratings yet
- Fluidos Ideales Parcial 4 Edith Yulieth Moreno MuñozDocument11 pagesFluidos Ideales Parcial 4 Edith Yulieth Moreno MuñozJulieth MorenoNo ratings yet
- Práctica de Laboratorio N°5 Determinación de Capacidad Calorífica y Calor Específico de Un SólidoDocument7 pagesPráctica de Laboratorio N°5 Determinación de Capacidad Calorífica y Calor Específico de Un Sólidomadara limaNo ratings yet
- Practica de FenomenosDocument4 pagesPractica de Fenomenoshermogenez martinez alcaNo ratings yet
- Taller # 1 - QA - UdeA - 02-2019Document7 pagesTaller # 1 - QA - UdeA - 02-2019CATALINA BUITRAGO OROZCONo ratings yet
- Informe 4 Labo Instrumental FinalDocument15 pagesInforme 4 Labo Instrumental FinalIsmael M'sanchezNo ratings yet
- Entalpía de Vaporización InformeDocument6 pagesEntalpía de Vaporización InformeCarlos E Acosta DiazNo ratings yet
- Ejercicio 1 y 9Document3 pagesEjercicio 1 y 9andrea jimenezNo ratings yet
- Lab 3Document8 pagesLab 3Anonymous DxNy3jlTnNo ratings yet
- Taller 1 TermoDocument4 pagesTaller 1 TermoDaniel RoseroNo ratings yet
- Ejercicios Viscosidad de LíquidosDocument2 pagesEjercicios Viscosidad de LíquidosIncodecsa PerusacNo ratings yet
- 053 BCD 2018 II Gas Ideal RealDocument61 pages053 BCD 2018 II Gas Ideal RealJasmin Yanina Solis SantiagoNo ratings yet
- TareaFQ3 GasesIdealesDocument2 pagesTareaFQ3 GasesIdealesDavid Molina0% (1)
- Clase3 - Balance - 1P PDFDocument1 pageClase3 - Balance - 1P PDFRodrigo SurculentoNo ratings yet
- HIDRATOSDocument1 pageHIDRATOSanonimomaNo ratings yet
- Ejercicio Oficial de FQDocument4 pagesEjercicio Oficial de FQLuis CorderoNo ratings yet
- Problemas PropuestosDocument3 pagesProblemas PropuestosPablo LuchoNo ratings yet
- Guia IP 2018-2Document6 pagesGuia IP 2018-2naymarNo ratings yet
- Clausius Clapeyron Problemas Con Respuesta para Entregar PDFDocument5 pagesClausius Clapeyron Problemas Con Respuesta para Entregar PDFChristian GerardoNo ratings yet
- Liquidos EjerciciosDocument3 pagesLiquidos EjerciciosLuis Vaca0% (4)
- Liquidos QG1-2012Document2 pagesLiquidos QG1-2012Luis Vaca100% (1)
- FDocument12 pagesFRCTR XD0% (1)
- Equilibrio de Fases 2013-2Document2 pagesEquilibrio de Fases 2013-2matrixdolorisNo ratings yet
- Equilibrio de Fases en Sistemas de Un ComponenteDocument2 pagesEquilibrio de Fases en Sistemas de Un ComponenteCu ExNo ratings yet
- Clase DX - Tubo y Coraza - Parte 3Document70 pagesClase DX - Tubo y Coraza - Parte 3Victor GarciaNo ratings yet
- TQ Proyecto de Curso - 4T1Q - I Sem 2021Document11 pagesTQ Proyecto de Curso - 4T1Q - I Sem 2021Victor GarciaNo ratings yet
- Clase 2.5.1 Muestreo de Aceptacion AtributosDocument28 pagesClase 2.5.1 Muestreo de Aceptacion AtributosVictor GarciaNo ratings yet
- Clase Practica Balance de Materia Con Reacción Química.Document5 pagesClase Practica Balance de Materia Con Reacción Química.Victor Garcia0% (1)
- Apéndice B - Van Ness - 5ta EdDocument3 pagesApéndice B - Van Ness - 5ta EdVictor GarciaNo ratings yet
- Clase DX - Tubo y Coraza - Parte 2 - I Sem 2021Document35 pagesClase DX - Tubo y Coraza - Parte 2 - I Sem 2021Victor GarciaNo ratings yet
- Derivados Bromados Del Hexano VAGBDocument4 pagesDerivados Bromados Del Hexano VAGBVictor GarciaNo ratings yet
- Examen Final 1Document4 pagesExamen Final 1Victor GarciaNo ratings yet
- Clase Practica de Balance de Energía en Calentadores (Enfriadores) y EvaporadoresDocument5 pagesClase Practica de Balance de Energía en Calentadores (Enfriadores) y EvaporadoresVictor GarciaNo ratings yet
- Clase Práctica de Balance de Energía Con Reacción Química.Document7 pagesClase Práctica de Balance de Energía Con Reacción Química.Victor GarciaNo ratings yet
- Clase Practica de PsicometriaDocument4 pagesClase Practica de PsicometriaVictor GarciaNo ratings yet
- Clase Práctica de Balance de Energía en Mezcladores, Evaporadores y Torres de RectificaciónDocument7 pagesClase Práctica de Balance de Energía en Mezcladores, Evaporadores y Torres de RectificaciónVictor GarciaNo ratings yet
- Clase Practica de Extraccion SolidoliquidoDocument4 pagesClase Practica de Extraccion SolidoliquidoVictor Garcia100% (1)
- Guia Aprendizaje - 1.3 Reologia - 2020pDocument2 pagesGuia Aprendizaje - 1.3 Reologia - 2020pVictor GarciaNo ratings yet
- Metales de TransiciónDocument19 pagesMetales de TransiciónVictor GarciaNo ratings yet
- Clase Practica de Recirculacion y DerivacionDocument4 pagesClase Practica de Recirculacion y DerivacionVictor GarciaNo ratings yet
- Tarea de Balance de EnergíaDocument4 pagesTarea de Balance de EnergíaVictor Garcia100% (1)
- Und2 cp1 BalanceDocument1 pageUnd2 cp1 BalanceVictor GarciaNo ratings yet
- Guia de Clases PracticasDocument20 pagesGuia de Clases PracticasVictor GarciaNo ratings yet
- Metodos de Runge Kutta y HeunDocument3 pagesMetodos de Runge Kutta y HeunVictor GarciaNo ratings yet
- NTON 03 070 06 de Etiquetado de Bebidas FermentadasDocument7 pagesNTON 03 070 06 de Etiquetado de Bebidas FermentadasVictor GarciaNo ratings yet
- Teoria de Maquinas - Tema 2 - Cinematica de MecanismosDocument50 pagesTeoria de Maquinas - Tema 2 - Cinematica de MecanismosjencopaNo ratings yet
- Best Pneumatics 2. Datos Técnicos - SMCDocument8 pagesBest Pneumatics 2. Datos Técnicos - SMCEsteban Brusil ArellanoNo ratings yet
- Primera Ley de La Termodinamica PDFDocument7 pagesPrimera Ley de La Termodinamica PDFCarlos Pupuche RodriguezNo ratings yet
- DerretimientoDocument3 pagesDerretimientoPaul Gordon PerezNo ratings yet
- Tensión SuperficialDocument13 pagesTensión Superficialmichael ardiles giraldoNo ratings yet
- Determinacion de La Formula de Un HidratoDocument7 pagesDeterminacion de La Formula de Un HidratoSeilin De LeónNo ratings yet
- La DensidadDocument6 pagesLa DensidadDazy Gonzales RNo ratings yet
- Ilovepdf MergedDocument115 pagesIlovepdf MergedBruno Aaron Ramirez GarciaNo ratings yet
- Quimica I - Repaso General I Fase - .Lunes 18 de EneroDocument14 pagesQuimica I - Repaso General I Fase - .Lunes 18 de EneroAlexander GustavoNo ratings yet
- End-Pr-Ivt-01 Procedimiento VT Asme b31.3 - 2010Document7 pagesEnd-Pr-Ivt-01 Procedimiento VT Asme b31.3 - 2010Charles CisnerosNo ratings yet
- Clase HIDROGEOLOGÍA SET18Document66 pagesClase HIDROGEOLOGÍA SET18Dajhanna Grados AlvaradoNo ratings yet
- Hoja de Calculo Robert L Mott Diseno de Elementos de MaquinasDocument38 pagesHoja de Calculo Robert L Mott Diseno de Elementos de MaquinasEL CONDE DE LAVACACONDENo ratings yet
- Promecol AluminioDocument3 pagesPromecol AluminiojuantrakeNo ratings yet
- 06 PH AmortiguadoresDocument10 pages06 PH AmortiguadoresNestor Catacora ChuraNo ratings yet
- Fisica IIIDocument2 pagesFisica IIItareasaramisNo ratings yet
- TRABAJO EN CLASE 2 - Disponibilidad IntrínsecaDocument14 pagesTRABAJO EN CLASE 2 - Disponibilidad IntrínsecaJean Carlos MontesdeocaNo ratings yet
- Determinación de La Banda Prohibida en Un SemiconductorDocument17 pagesDeterminación de La Banda Prohibida en Un SemiconductorIsrael GarcíaNo ratings yet
- Línea Eco Frío/Calor 5000 Watts: Ficha TécnicaDocument2 pagesLínea Eco Frío/Calor 5000 Watts: Ficha TécnicaCaty 2019No ratings yet
- Proceso de Manufactura de Los Microchips Desde El SilicioDocument15 pagesProceso de Manufactura de Los Microchips Desde El SilicioJpapoNo ratings yet
- Facultad de Ciencias y Tecnologia: Laboratorio de Operaciones Unitarias IIDocument18 pagesFacultad de Ciencias y Tecnologia: Laboratorio de Operaciones Unitarias IILuz Erika Quispe MuñozNo ratings yet
- 6ta Practica Labb h2Document10 pages6ta Practica Labb h2Jose OrtNo ratings yet
- Ejercicios Resistencia - Capitulo 5Document7 pagesEjercicios Resistencia - Capitulo 5Lizeth De La HozNo ratings yet
- Ficha de Datos de Seguridad Sanfresh® C20 O15Document15 pagesFicha de Datos de Seguridad Sanfresh® C20 O15FcoJ PedrosaNo ratings yet
- Informe Laboratorio Operaciones UnitariasDocument56 pagesInforme Laboratorio Operaciones UnitariasVALERIA MUNOZ SEGURANo ratings yet
- Inv E-126 Límite Plástico e Índice de Plasticidad de Los SuelosDocument10 pagesInv E-126 Límite Plástico e Índice de Plasticidad de Los SuelosCristian DiazNo ratings yet
- 01 Reactivos Faltantes de La Guía Oficial IPN - IyCFM - 2019 PDFDocument4 pages01 Reactivos Faltantes de La Guía Oficial IPN - IyCFM - 2019 PDFRoberto CervantesNo ratings yet
- Movimiento Circular Uniforme IDocument3 pagesMovimiento Circular Uniforme Imesias ailla guamanNo ratings yet
- Lamas MI 2022 Problemas Resueltos Transmision de CalorDocument106 pagesLamas MI 2022 Problemas Resueltos Transmision de CalorJhonatan Zavaleta QuirozNo ratings yet
- Ejercicios - de Quimica-Rxs - Qcas.Document3 pagesEjercicios - de Quimica-Rxs - Qcas.FRANK GERMAN JIMENEZ CORONADONo ratings yet