Professional Documents
Culture Documents
Investigacion LCB
Uploaded by
Diana Gutiérrez0 ratings0% found this document useful (0 votes)
27 views4 pagesvaloraciones
Original Title
Investigacion Lcb
Copyright
© © All Rights Reserved
Available Formats
DOCX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this Documentvaloraciones
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
27 views4 pagesInvestigacion LCB
Uploaded by
Diana Gutiérrezvaloraciones
Copyright:
© All Rights Reserved
Available Formats
Download as DOCX, PDF, TXT or read online from Scribd
You are on page 1of 4
1.
- Análisis químico cuantitativo (Skoog)
a) Finalidad u objetivo del análisis cuantitativo
La química analítica comprende la separación, identificación y
determinación de las cantidades relativas de los componentes que forman
una muestra de materia.
Proporciona la cantidad en términos numérico de uno o más analitos.
b) Métodos de análisis químico cuantitativo
- Masa o Volumen
- Medición de alguna cantidad que es proporcional a la cantidad de analito
en dicha muestra
- Método gravimétrico
- Método electro analítico
- Métodos espectroscópicos
- Espectrometría de masas
2.- Métodos volumétricos o análisis volumétrico o métodos estequiométricos
(Harris)
a) Fundamento
El método volumétrico es el volumen de una solución que contiene suficiente
reactivo para reaccionar completamente con el analito
b) Material de Laboratorio que se usa
Matras volumétrico o aforado, pipetas y jeringas, micropipetas
c) Clasificación
Acido – base: Aquellos donde el analito reacciona con un agente
oxidante o reductor de concentración conocida.
Volumétricas acido – base: se valora una disolución de una
acido o sal de base débil y un acido fuerte mediante una base
(Alcalimetría) o bien una base y una sal de base fuerte y un
ácido débil mediante un ácido (acidimetría).
Volumétricas REDOX: El reactivo valorante provoca la
oxidación o reducción de la sustancia a analizar.
Volumétricas de precipitación: El reactivo valorante provoca la
precipitación de un compuesto de composición bien definida.
Volumétricas de complejacion: El reactivo forma un complejo
con la sustancia a analizar si aquel es una complexona el
método se denomina complexometria.
Volumétrica directa: La reacción se verifica entre la sustancia a
determinar y el reactivo valorante
Volumétrica indirecta: Se verifica entre una sustancia producida
o que a reaccionado cuantitativamente con la que se quiere
determinar y el reactivo.
3.- Que es una titulación o valoración
Determinación en un análisis acido – base que se va agregando sistemática y
cuidadosamente una solución que contiene el titulante a otra que contiene la
muestra. La meta es añadir una cantidad suficiente y exactamente suficiente de
titulante para que este reaccione con el constituyente deseado de la muestra para
así revelar el cambio de color.
4.- Titulaciones acido-base (4 tipos) (Harris)
Acido fuerte con base fuerte:
Acido débil con base fuerte:
Base débil con ácido fuerte:
Sistemas diproticos:
Se calcula la región antes del punto de equivalencia, la región del punto de
equivalencia y después del punto de equivalencia y la curva de valoración.
5.- Bureta: descripción, limpieza, llenado, manejo y capacidad. (Harris)
Descripción: Es un tubo de vidrio fabricado con precisión que tiene una gran
duración que permite medir el volumen del liquido a z de una llave (Válvula) en su
extremo inferior, los números descritos en la bureta aumentan de arriba abajo con
la marca de cero mililitros cerca del extremo superior.
Limpieza, llenado, Manejo:
- Lavar la bureta con disolución nueva
- Eliminar cualquier burbuja de aire antes de usarla
- Verter el líquido lentamente
- Verter fracciones de gota cerca del punto final
- Leer la parte baja del menisco cóncavo
- Estimar las lecturas hasta un décimo de la división
- Evitar el error de paralaje
- Tener en cuenta el grosor de las rayas al hacer la lectura
Capacidad: Las buretas de clase A (mas exactas) garantizan que cumplen las
tolerancias: si la lectura en una bureta de 50 ml es de 27.26 ml el volumen real
puede ser cualquiera entre 27.21 y 27.11 ml y seguir estando dentro de la tolerancia
mas menos 0.05 ml certificada por el fabricante
Vol. De la bureta (ml) Graduacion mínima (ml) Tolerancia (ml)
5 0.01 ± 0.01
10 0.05 o 0.02 ± 0.02
25 0.1 ± 0.03
50 0.1 ± 0.05
100 0.2 ± 0.10
6.- Estandarización de una disolución (Ramette)
La estandarización de disolución es el proceso mediante el cual se determina con
exactitud la concentración de una solución. Algunas veces se puede preparar una
disolución estándar disolviendo una muestra pesada con exactitud en un volumen
de soluto medido con exactitud en química analítica, es una disolución que contiene
una concentración conocida de un elemento o sustancia especifica llamada Patrón
primario que por su especial estabilidad se emplea para valorar la concentración de
otras soluciones como las disoluciones valorantes.
7.- Patrón primario: definición, características y ejemplos de patrones
primarios de naturaleza acido y básica (Quimica Analitica I - UAM)
Un patrón primario, tambein llamado estándar primario es una sustancia utilizada
en química como referencia al momento de hacer una valoracion o estandarizacion.
Usualmente son solidos que cumplen con las sig características:
i) Tiene composición conocida es decir, se ha de conocer la estructura
y elementos que lo componen lo cual servirá para hacer los caculos
estequeometricos.
ii) Deben tener elvada pureza, para una correcta estandarixaicon se
debe utilizar un patron que tenga la mínima cantidad de impurezas
iii) Debe ser estable a temperatura ambiente, no sepuede utilizar
sustancias que cambien sus composición o estructura por efectos de
las temperaturas que difieran ligeramente con al temperatura del
ambiente
iv) Debe ser posible su secado en estufa, además de los cambios de
temperatura ambiente también debe soportar temperaturas mayores
para que sea posible su secado
v) No debe abseber gases, ya que este hecho ganaría posibles errores
por interferentes asi como también de generación del patron
vi) Debe reaccionar rápido y estequiométricamente con el titulante, de
este manera se puede visulizar con mayor exactitud el punto final de
las titulaciones por volumetría y entonces se puedan realizar los
cálculos respectivos.
vii) Debe tener un peso equivalentes grande, ya que este hecho reduce
considerablemente el error de la pesada del patron.
Ejemplos para bases:
A) Ftalato acido de potasio ( KHC8H4O4/ KHP) ejemplo de la ecuación: NaOH
+ KHC8H4O4 <> KNaC8H404 + H20
B) Acido benzoico (C6H5COOH)
C) Acido Sulfanilico (NH2C6H5SO3H)
D) Acido Sulfamico (NH2SO3H)
E) Acido Oxalico (C2O4H2)
Ejemplos para Acidos
A) TRIS ( HCl + H2NC(CH2OH)3 <> Cl + H3NC(CH2OH)3
B) Carbonato de Sodio Na2CO3
C) Borax Na2B4O7 – 10 H2O
8.- Selección de indicadores acido – base para cada tipo de valoración
9.- Curva de valoración: definición y tipos de cuervas de valoración acido –
base
10.- Proceso de secado de una sustancia solida
11.- Desecador: descripción, manejo y funcionamiento
12.- Ka= Constante de disociación acida: definición y tablas
13.- Kb= Constante de disociación básica y tablas
14.- Hidrolisis de sales
15.- Calculo de pH de ácidos y bases débiles
You might also like
- De Prod Com 7 LmeDocument15 pagesDe Prod Com 7 LmeAreelii VaaldeezNo ratings yet
- (QUIMICA GENERAL) .Alvarez Gildo Fredi Noel. (Practica de Laboratorio) .Valoracion de Disoluciones Acido-BaseDocument7 pages(QUIMICA GENERAL) .Alvarez Gildo Fredi Noel. (Practica de Laboratorio) .Valoracion de Disoluciones Acido-BaseFredi N Álvarez Gildo.No ratings yet
- Volumetria 2013 IiDocument107 pagesVolumetria 2013 IiLeonelaRondonNo ratings yet
- Informe de EstandarizaciónDocument30 pagesInforme de EstandarizaciónGino AragonNo ratings yet
- OBJETIVOSDocument5 pagesOBJETIVOSJulio Cesar Fernadez EstelaNo ratings yet
- Tarea 2. Valoración Ácido BaseDocument5 pagesTarea 2. Valoración Ácido BaseJeremy GonzálezNo ratings yet
- Analisis VolumetricoDocument15 pagesAnalisis VolumetricoJhoseline CxNo ratings yet
- Manual de Metodos Cuantitativos 2022Document30 pagesManual de Metodos Cuantitativos 2022Flor Alejandra Piña RodriguezNo ratings yet
- VOLUMETRÍADocument27 pagesVOLUMETRÍAArnieRiveraTiconaNo ratings yet
- Informe Laboratorio 3Document17 pagesInforme Laboratorio 3Macyory GutierrezNo ratings yet
- PRYECTO 2. EQUILIBRIO ÁCIDO BASE PROBLEMA 2 Determinar Experimentalmente La Concentración de Disoluciones de Reactivos Analíticos (Fuertes y Débiles) A Partir de Una Disolución Valorante EstandarizadaDocument11 pagesPRYECTO 2. EQUILIBRIO ÁCIDO BASE PROBLEMA 2 Determinar Experimentalmente La Concentración de Disoluciones de Reactivos Analíticos (Fuertes y Débiles) A Partir de Una Disolución Valorante EstandarizadaMauricio SGNo ratings yet
- Determinación de ácido acético mediante valoración volumétricaDocument28 pagesDeterminación de ácido acético mediante valoración volumétricaLuis Huarache De Bistec ACNo ratings yet
- CAP VIII Metodo Gravimet y Vulumet QADocument7 pagesCAP VIII Metodo Gravimet y Vulumet QADaniela Leveau AlvaNo ratings yet
- Practica 7. Valoracion Acido BaseDocument4 pagesPractica 7. Valoracion Acido BaseValentina RaposoNo ratings yet
- Volumetria de NeutralizaciónDocument10 pagesVolumetria de NeutralizaciónPaul Silva GalvezNo ratings yet
- NeutralizaciónDocument12 pagesNeutralizaciónMiguel CarmonaNo ratings yet
- Determinación concentración ácido sulfúricoDocument10 pagesDeterminación concentración ácido sulfúricoThe GoldenNo ratings yet
- Resultados y Calculos DiscusionDocument6 pagesResultados y Calculos DiscusionPatty LuNo ratings yet
- Volumetria de NeutralizaciónDocument10 pagesVolumetria de NeutralizaciónAlex Huancahuari EvananNo ratings yet
- Manual de Metodos CuantitativosDocument122 pagesManual de Metodos CuantitativosEve de LandazuriNo ratings yet
- Volumetria Acido BaseDocument21 pagesVolumetria Acido BaseAntonio Alfaro VictorioNo ratings yet
- Informe 4Document17 pagesInforme 4Báez Alvaro87% (30)
- Informe 8 de Quimica UNSCHDocument13 pagesInforme 8 de Quimica UNSCHAldana HuamanNo ratings yet
- PRÁCTICADocument7 pagesPRÁCTICAIvonne RiveraNo ratings yet
- Informe Preparacion y Valoracion Se Soluciones de Acidemetria AlcalimetriaDocument11 pagesInforme Preparacion y Valoracion Se Soluciones de Acidemetria AlcalimetriaZIRB AL0% (1)
- Laboratorio Número 10 Ale RuizDocument12 pagesLaboratorio Número 10 Ale RuizJoel Pablo MamaniNo ratings yet
- Informe Técnico N°5 - GRUPO 5Document19 pagesInforme Técnico N°5 - GRUPO 5MUÑOZ LUNA GIANCARLONo ratings yet
- Metodos Clasicos de AnalisisDocument23 pagesMetodos Clasicos de AnalisisMagda KarinaNo ratings yet
- Volume TriaDocument6 pagesVolume TriaLudmila CaripilNo ratings yet
- Análisis Volumétrico: Fundamentos y Tipos de ValoracionesDocument10 pagesAnálisis Volumétrico: Fundamentos y Tipos de ValoracionesLuis RamirezNo ratings yet
- Práctica Número 1 - Estandarización HCL y NaOHDocument7 pagesPráctica Número 1 - Estandarización HCL y NaOHDrakoLG YTNo ratings yet
- Practica N 7 Volumetria de NeutralizacioDocument9 pagesPractica N 7 Volumetria de NeutralizacioKarnol Ruiz BarbozaNo ratings yet
- Prelab 10Document4 pagesPrelab 10Edith NavaNo ratings yet
- LQ-218 Practica # 6 Preparacion de SolucionesDocument18 pagesLQ-218 Practica # 6 Preparacion de SolucionesYamileth HernandezNo ratings yet
- Practica Nº1 Volumetria Acido BaseDocument7 pagesPractica Nº1 Volumetria Acido BaseQUÍMICA0% (3)
- Definición de Análisis VolumétricoDocument2 pagesDefinición de Análisis VolumétricoDaniel HospinaNo ratings yet
- Taller Solucionado EstandarizacionDocument23 pagesTaller Solucionado EstandarizacionEsteban lozano100% (1)
- Acidos BasesDocument34 pagesAcidos BasesTHANYANo ratings yet
- Volumetrías 40Document18 pagesVolumetrías 40Jhonatan Rimache ArotomaNo ratings yet
- Laboratorio #1Document6 pagesLaboratorio #1MIMBELA, GEISELNo ratings yet
- Manual de Metodos Cuantitativos 2017Document44 pagesManual de Metodos Cuantitativos 2017ErikRodriguezNo ratings yet
- Analitica ESTANDARIAZIONDocument12 pagesAnalitica ESTANDARIAZIONJhan marco Flores ChávezNo ratings yet
- RUBeN MARCELO SaENZ RODRIGUEZ - Elaborar Un Resumen de La 9na-SemanaDocument4 pagesRUBeN MARCELO SaENZ RODRIGUEZ - Elaborar Un Resumen de La 9na-SemanaRubenMarceloSaenzRodriguezNo ratings yet
- Práctica Profesionalizante I "Introduccion Al Analisis Volumetrico"Document9 pagesPráctica Profesionalizante I "Introduccion Al Analisis Volumetrico"Ruben Eduardo LunaNo ratings yet
- Analisis Volumétrico 1Document16 pagesAnalisis Volumétrico 1XDXD XDXDNo ratings yet
- Informe de Analisis Quimico 7Document24 pagesInforme de Analisis Quimico 7Lucero Gomez CabreraNo ratings yet
- Informe de Laboratorio N°3 y 4Document8 pagesInforme de Laboratorio N°3 y 4Santiago UcciNo ratings yet
- Práctica 4 - Valoración NaOH y HCLDocument5 pagesPráctica 4 - Valoración NaOH y HCLSteven TejadaNo ratings yet
- Guía Práctica #6 SolucionesDocument15 pagesGuía Práctica #6 SolucionesJohan Anthony Terry CamposNo ratings yet
- Titulaciones Acido en Medio AcuosoDocument7 pagesTitulaciones Acido en Medio AcuosoGeovi Condori CortezNo ratings yet
- Informe 8 FINALDocument14 pagesInforme 8 FINALLuis Beraun AlaniaNo ratings yet
- Informe Titulacion BASE DÉBIL-ACIDO FUERTEDocument23 pagesInforme Titulacion BASE DÉBIL-ACIDO FUERTEirene154100% (4)
- Informe #2 - Q. Analítica Lab - Grupo 4Document30 pagesInforme #2 - Q. Analítica Lab - Grupo 4STEFHANY PAOLA MENDOZA HERNANDEZNo ratings yet
- Manual de MAEI 23Document49 pagesManual de MAEI 23Yahir SuárezNo ratings yet
- CUESTIONARIO AnaliticaDocument3 pagesCUESTIONARIO AnaliticaAlejandra Herrera BarreraNo ratings yet
- Qai (T) 02 2023-I UnwDocument37 pagesQai (T) 02 2023-I UnwNancy Hilario CotrinaNo ratings yet
- VolumetríaDocument39 pagesVolumetríaERICK100% (1)
- P4 NormalizacionDocument9 pagesP4 NormalizacionToni Vives BalaguerNo ratings yet
- Técnicas analíticas básicas: En el control de la calidad del agua según normatividadFrom EverandTécnicas analíticas básicas: En el control de la calidad del agua según normatividadNo ratings yet
- Sofia 201 Fqo3JuB Pirazol 1°intento Eq3 PDocument22 pagesSofia 201 Fqo3JuB Pirazol 1°intento Eq3 PDiana GutiérrezNo ratings yet
- Ejercicio CuantificaciónDocument1 pageEjercicio CuantificaciónDiana GutiérrezNo ratings yet
- Sistema Inmune MucosasDocument7 pagesSistema Inmune MucosasDazamNo ratings yet
- Introduccion HongosDocument1 pageIntroduccion HongosDiana GutiérrezNo ratings yet
- Bioetica PrincipialistaDocument10 pagesBioetica PrincipialistaClaudio PidotoNo ratings yet
- Previo SedantesDocument2 pagesPrevio SedantesDiana GutiérrezNo ratings yet
- Anticonceptivos FarmacologiaDocument8 pagesAnticonceptivos FarmacologiaDiana GutiérrezNo ratings yet
- Caso Baby DoeDocument2 pagesCaso Baby DoeyanamajuliNo ratings yet
- Equipo 4 Distribucion ExposiciónDocument40 pagesEquipo 4 Distribucion ExposiciónDiana GutiérrezNo ratings yet
- Reporte Practica 4 BQNDocument10 pagesReporte Practica 4 BQNDiana GutiérrezNo ratings yet
- Habitos SaludablesDocument1 pageHabitos SaludablesDiana GutiérrezNo ratings yet
- CuestionarioPrevio7 DianaGutierrezPatiñoDocument3 pagesCuestionarioPrevio7 DianaGutierrezPatiñoDiana GutiérrezNo ratings yet
- Previo SedantesDocument2 pagesPrevio SedantesDiana GutiérrezNo ratings yet
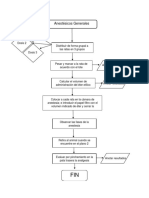
- Diagrama AnesticosDocument1 pageDiagrama AnesticosDiana GutiérrezNo ratings yet
- InformeDocument8 pagesInformeDiana GutiérrezNo ratings yet
- FluidizaciónDocument9 pagesFluidizaciónDiana GutiérrezNo ratings yet
- Redox 1276Document16 pagesRedox 1276Camus TrejoNo ratings yet
- Destilación Operaciones Unitarias FarmaceúticasDocument10 pagesDestilación Operaciones Unitarias FarmaceúticasDiana GutiérrezNo ratings yet
- Diseño LCBIIDocument8 pagesDiseño LCBIIDiana GutiérrezNo ratings yet
- Diseño IIDocument7 pagesDiseño IIDiana GutiérrezNo ratings yet
- MetodologiaDocument2 pagesMetodologiaDiana GutiérrezNo ratings yet
- Ejercicios1 5036 PDFDocument3 pagesEjercicios1 5036 PDFDiana GutiérrezNo ratings yet
- Gui On Practic As 0809Document19 pagesGui On Practic As 0809Eder ValverdeNo ratings yet
- Practica 4Document6 pagesPractica 4Diana GutiérrezNo ratings yet
- MicrobiologiaDocument6 pagesMicrobiologiaDiana GutiérrezNo ratings yet
- Conceptos FarmaDocument2 pagesConceptos FarmaDiana GutiérrezNo ratings yet
- Diseño IIDocument7 pagesDiseño IIDiana GutiérrezNo ratings yet
- Trabajo final Farmacología General equipos fármacosDocument11 pagesTrabajo final Farmacología General equipos fármacosDiana GutiérrezNo ratings yet
- MicrobiologiaDocument7 pagesMicrobiologiaDiana GutiérrezNo ratings yet
- Metformina d2Document7 pagesMetformina d2Luis Guillermo Sanchez LezamaNo ratings yet
- Guia de Armado de AlcantarillasDocument8 pagesGuia de Armado de AlcantarillasLeidy Laura Ojeda MartinezNo ratings yet
- 682 PDFDocument5 pages682 PDFkelly chacon murciaNo ratings yet
- Fenitoina Efectod AdversosDocument7 pagesFenitoina Efectod Adversosmario antonio moya torresNo ratings yet
- Métodos de Toma de Muestras de Contaminantes QuímicosDocument2 pagesMétodos de Toma de Muestras de Contaminantes QuímicosKarol BNo ratings yet
- ResistenciaDocument33 pagesResistenciaDiegoNo ratings yet
- Imanes MolecularesDocument3 pagesImanes MolecularesMAGDALÑENO ANGON PELAGIONo ratings yet
- Control de Malos Olores en PTASDocument12 pagesControl de Malos Olores en PTASChristian Hauser HeckerNo ratings yet
- Manual Del Propietario Honda CB600F-1Document161 pagesManual Del Propietario Honda CB600F-1Jordi Blanco0% (1)
- PDF Desarrollo Del Proceso Acessssssssssssss 21sssssss DLDocument3 pagesPDF Desarrollo Del Proceso Acessssssssssssss 21sssssss DLJoseph RamirezNo ratings yet
- Regulacion de La Expresion Genetica en BacteriaDocument27 pagesRegulacion de La Expresion Genetica en BacteriaMaggie Tapia ZúñigaNo ratings yet
- Terminacion Cervical y Tipos de CoronasDocument24 pagesTerminacion Cervical y Tipos de CoronasJuan Martin Fierro Aquinto86% (7)
- TotalImplant-catalogo Mar 2020Document36 pagesTotalImplant-catalogo Mar 2020OMAR EMILIO SANDOVAL SANTIAGONo ratings yet
- MargaritaDocument124 pagesMargaritaGustavo OrtegaNo ratings yet
- Quimica Inorganica 8 InformeDocument28 pagesQuimica Inorganica 8 InformeJuan camilo Aguirre LópezNo ratings yet
- Ejercicios Del Tema 4 (Estructura de La Materia)Document2 pagesEjercicios Del Tema 4 (Estructura de La Materia)Patrivsky Rodríguez0% (1)
- Materiales para ExterioresDocument7 pagesMateriales para ExteriorespaoNo ratings yet
- Ing. Osby García S Osby - Garcia@udep - Edu.peDocument85 pagesIng. Osby García S Osby - Garcia@udep - Edu.peedgar lopezNo ratings yet
- Los Bloques NutricionalesDocument6 pagesLos Bloques NutricionalesKenn SantanaNo ratings yet
- AgregadoDocument12 pagesAgregadopercyrojasrodriguezNo ratings yet
- Amorceur Lampe IM 1000 WDocument4 pagesAmorceur Lampe IM 1000 Wtariq boukhlikNo ratings yet
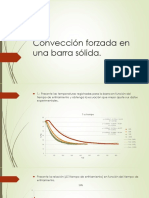
- Convección forzada en barra sólida: coeficiente de transferencia de energíaDocument12 pagesConvección forzada en barra sólida: coeficiente de transferencia de energíaKarliita LomNo ratings yet
- Pañales ecológicos: Guía completa sobre pañales de telaDocument17 pagesPañales ecológicos: Guía completa sobre pañales de telaPaula BrunengoNo ratings yet
- Informe de AlgasDocument17 pagesInforme de AlgasLeidy Cely CastilloNo ratings yet
- Licuado Antiinflamatorio y Reparador Del IntestinoDocument2 pagesLicuado Antiinflamatorio y Reparador Del IntestinoMiguel Onofre LavinNo ratings yet
- Laboratorio de Microbiología e Higiene de los AlimentosDocument3 pagesLaboratorio de Microbiología e Higiene de los AlimentosmateoNo ratings yet
- Cómo preparar Hematoxilina de HarrisDocument12 pagesCómo preparar Hematoxilina de HarrisEnrique Patricio Leon IbarraNo ratings yet
- Receta Cerveza Lager 20Document7 pagesReceta Cerveza Lager 20Patrick Rodriguez AyalaNo ratings yet
- Evaluación 1er Quimestre Tren de RodajeDocument2 pagesEvaluación 1er Quimestre Tren de RodajeOmar PerezNo ratings yet