Professional Documents
Culture Documents
Injuria Celular, Apoptosis y Necrosis (Parte 1) .PPSX
Uploaded by
BarbaraSilva0 ratings0% found this document useful (0 votes)
42 views78 pagesOriginal Title
1.- Injuria celular, apoptosis y necrosis (Parte 1).ppsx
Copyright
© © All Rights Reserved
Available Formats
PPSX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PPSX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
42 views78 pagesInjuria Celular, Apoptosis y Necrosis (Parte 1) .PPSX
Uploaded by
BarbaraSilvaCopyright:
© All Rights Reserved
Available Formats
Download as PPSX, PDF, TXT or read online from Scribd
You are on page 1of 78
Injuria celular,
apoptosis y necrosis
Jaime López Puga
Patología 2013
Apoptosis o muerte celular programada.
Apoptosis – Hepatitis viral.
Apoptosis – Apoptosis en liquen ruber plano, piel: infiltración de linfocitos en la
dermis superficial (papilar) con numerosas masas acidófilas en la zona de unión
dermo-epidérmica que corresponden a células apoptóticas llamadas cuerpos de
Civatte (H/E – 200x).
Apoptosis: masas acidófilas, globulares y homogéneas (cuerpos de Civatte) en la
zona de la membrana basal de la piel (H/E – 500x).
Apoptosis – Cuerpo de Civatte (ME): masa constituida por filamentos intermedios,
restos de organelos y rodeada por fragmentos de lámina densa de membrana
basal (citrato de plomo y acetato de uranilo – 10.000x).
Apoptosis: decidua que muestra células de citoplasma acidófilo. Núcleo hiper-
basófilo y fragmentado o cariorrexis (H/E – 500x).
Apoptosis: decidua sub-coriónica con numerosas células apoptóticas que
muestran citoplasma acidófilo y núcleos fragmentados o cariorrexis (H/E – 500x).
Necrosis (en negro) – Hepatitis aguda.
Necrosis masiva de hígado (ingurgitación sanguínea de sinusoides y
proliferación de conductillos – atrofia roja sub-aguda).
Necrosis estructurada: necrosis hepática masiva.
Necrosis coagulativa (carcinoma ductal mamario).
Necrosis coagulativa (carcinoma ductal mamario).
Necrosis: tejido miocárdico normal.
Necrosis: tejido miocárdico con necrosis coagulativa.
Tejido infartado mostrando necrosis coagulativa con pérdida de núcleos y
aglutinación de citoplasmas pero con preservación de los contornos básicos de la
arquitectura glomerular y tubular.
Un foco de necrosis de licuefacción causado por infección micótica. El foco es
llenado con leucocitos y restos celulares, creando un absceso que oblitera la
arquitectura normal.
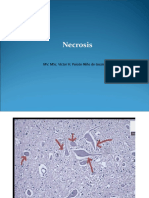
Necrosis – Epitelio tubular renal: al centro hay un túbulo con necrosis de su
epitelio, con cromatolisis e hiper-acidofilia del citoplasma; compárese con el
epitelio de túbulos vecinos (H/E – 500x).
Necrosis – Necrosis miocárdica: necrosis de algunos cardiomiocitos, habiendo
picnosis nuclear e hiper-acidofilia del citoplasma con pérdida de la estructura
sarcoplasmática. En la vecindad hay infiltración de células polinucleares (H/E –
500x).
Necrosis – Necrosis en el mesencéfalo: al centro hay una neurona con necrosis,
evidenciándose cariorrexis, cromatolisis y homogenización del pericarion con
tenue coloración gris-verdosa (tinción cresil violeta – 500x).
Imagen de ME del miocardio con estructura conservada y leves alteraciones
mitocondriales en forma de zonas de la matriz (8.000x).
Imagen con ME de mitocondrias con lesiones reversibles: tumefacción y
aclaramiento de la matriz (15.000x).
Imagen con ME de lesiones mitocondriales irreversibles: floculaciones de la matriz
(20.000x).
Necrosis – Necrosis de reperfusión en miocardio: fibras miocárdicas con bandas
transversales acidófilas densas separadas por zonas de sarcoplasma rarefacto (H/E
– 200x).
Necrosis – Necrosis de reperfusión en miocardio: necrosis de reperfusión en una
fibra con mineralización de mitocondrias; compárese con la fibra vecina de
estructura relativamente bien conservada; corte semifino (tinción azul de Toluidina
– 1.250x).
Necrosis de coagulación – Infarto anémico del bazo: cuña amarillenta,
ligeramente tumefacta y periférica.
Necrosis de coagulación – Infarto del miocardio: superficie de corte del ventrículo
izquierdo con zonas amarillentas en el tercio interno del espesor.
Necrosis estructurada – Necrosis centrolobulillar hepática: hepatocitos con
picnosis y citoplasma acidófilo (H/E – 200x).
Necrosis de caseificación – Pulmón con ganglio linfático peribronquial con
necrosis de caseificación: superficie de corte amarillo pálido.
Necrosis no estructurada – Necrosis de caseificación: necrosis de caseificación
delimitada por células epiteloideas (ganglio linfático – H/E – 260x).
Necrosis cérea – Necrosis en músculo esquelético: necrosis cérea al centro, fibras
con picnosis nuclear y acentuada acidofilia del sarcoplasma, parcialmente
fragmentado (H/E – 200x).
Degeneración cérea en el miocardio: al centro, fibras con sarcoplasma
homogeneizado y acentuadamente acidófilo con núcleo bien condensado.
Necrosis de colicuación – Cerebro: necrosis de colicuación en el territorio de la
arteria cerebral media; cavitación incipiente.
Necrosis de colicuación – Cerebro: necrosis de colicuación antigua en territorio
superficial de la arteria cerebral media; encefalomalacia cavitada.
Necrosis de colicuación en remoción – Cerebro: foco de pérdida tisular completo
de macrófagos microgliales (H/E – 200x).
Corpúsculos gránulo-adiposos: microglia transformada en macrófago con
abundante citoplasma espumoso y con algunas vacuolas (H/E – 500x).
Corpúsculos gránulo-adiposos: macrófagos microgliales con abundante citoplasma
finamente granular con múltiples gotas de grasa (tinción Sudán IV – 500x).
Necrosis de colicuación – Páncreas: foco necrótico rodeado de infiltrado celular
inflamatorio; pancreatitis necrotizante del shock (H/E – 80x).
Necrosis – Adiponecrosis peripancreática: al centro un foco de adiponecrosis
peripancreática; el tejido adiposo necrosado con zonas basófilas finamente
granulares, jabones de calcio (H/E – 80x).
Necrosis – Foco de miolisis del miocardio: en la zona comprometida se reconoce
solo la trama fibrilar y células del intersticio (H/E – 200x).
Necrosis – Foco de miolisis del miocardio: desaparición de fibras miocárdicas con
conservación de la trama fibrilar (tinción retículo de Gomori – 500x).
Imagen con ME de una miolisis del miocardio; del cardiomiocito afectado se
reconoce solo la membrana basal y restos del sarcoplasma (4.000x).
Necrosis – Infarto del miocardio: en la superficie de corte del ventrículo izquierdo
se observan zonas de necrosis de coagulación en el tercio interno.
Necrosis – Infarto del miocardio: zona de necrosis de fibras miocárdicas con leve
infiltración celular inflamatoria; junto a la zona comprometida hay tejido miocárdico
conservado.
Necrosis en hígado: necrosis celular asilada de hepatocitos (H/E – 500x).
Necrosis – Necrosis mediolobulillar hepática en fiebre amarilla: al centro la vena
central está rodeada de hepatocitos no necrosados; más periféricamente hay una
zona con hepatocitos necróticos (H/E – 200x).
Necrosis – Necrosis perilobulillar hepática: necrosis perilobulillar con foquitos
hemorrágicos (eclampsia); al centro el espacio portal.
Necrosis hepática: necrosis focal hepática (H/E – 200x).
Necrosis – Necrosis hepática masiva: el tejido hepático ha desaparecido en su
mayor parte; quedan restos de la trama fibrilar, en parte con infiltración celular
inflamatoria. Se reconocen conductillos y pseudo-conductillos (sin lumen)
regenerativos (H/E – 80x).
Infarto anémico del riñón con compromiso de la corteza y médula; halo hemorrágico.
Necrosis – Necrosis papilar del riñón.
Necrosis – Necrosis cortical renal en recién nacido: las bandas de necrosis
perpendiculares a la superficie externa corresponden a necrosis en las columnas
de Bertin.
Gangrena isquémica húmeda: gangrena isquémica húmeda de los dedos del pie.
Gangrena isquémica húmeda: soldado de las trincheras.
Gangrena isquémica húmeda – Dermis e hipodermis: los gérmenes se encuentran
en la profundidad de la piel (H/E – 80x).
Gangrena isquémica seca: gangrena isquémica seca de mano y antebrazo.
Gangrena isquémica seca – Piel: los gérmenes (sustancia basófila finamente
granular) se mantienen en la superficie (H/E – 80x).
Gangrena isquémica: gangrena isquémica seca en la EEII derecha de un paciente diabético.
Gangrena infecciosa: gangrena infecciosa a nivel apendicular.
Gangrena infecciosa: gangrena infecciosa en una neumonía.
Gangrena infecciosa – Pulmón: el tejido gangrenado aparece algo basófilo, pálido
y en parte hemorrágico con múltiples colonias bacterianas como masas granulares
basófilas (H/E – 80x).
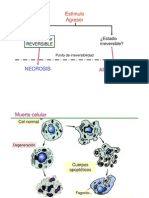
Representación esquemática de una célula normal y los cambios
en lesiones reversibles e irreversibles. Las lesiones reversibles se
caracterizan por la inflamación (hinchazón) generalizada de las
células y sus organelos, blebbing de la membrana plasmática
(se generan unas estructuras a modo de evaginaciones esféricas
surgidas a partir de la membrana y le confieren a la célula un
aspecto “boiling” al inicio de la apoptosis), separación de los
ribosomas del retículo endoplásmico y aglutinación de la
cromatina nuclear.
Blebbing de la membrana plasmática.
La transición hacia una lesión irreversible se caracteriza por el
aumento de la inflamación, inflamación y ruptura de los
lisosomas, presencia de grandes densidades amorfas en
mitocondrias inflamadas, ruptura de membranas celulares y
profundos cambios nucleares. El último incluye condensación
nuclear o picnosis seguido por fragmentación o cariorrexis y,
finalmente, disolución del núcleo o cariolisis.
Estructuras laminadas (figuras de mielina) derivadas de las
membranas de organelos y de membrana plasmática dañada
aparecen primero durante la etapa reversible y se vuelven más
pronunciadas en células dañadas irreversiblemente.
El rol de las especies reactivas de oxígeno en la lesión tisular. El
oxígeno es convertido a superóxido por enzimas oxidativas en el
retículo endoplásmico, mitocondrias, membrana plasmática,
peroxisomas y citosol.
El oxígeno es convertido en peróxido de hidrógeno por
dismutación y desde allí a radical hidroxilo; el peróxido de
hidrógeno es derivado u obtenido directamente de las oxidasas
ubicadas en los peroxisomas. No se muestra otro radical
potencialmente injurioso.
El daño resultante de los radicales a lípidos (peroxidación),
proteínas y DNA produce varias formas de lesión celular. Nótese
que el superóxido cataliza la reducción del hierro.
Las principales enzimas anti-oxidantes son la superóxido
dismutasa (SOD), catalasa y la glutatión peroxidasa (participa en
la vía REDOX de los glutationes, la cual se encuentra en estrecha
relación con la vía de las pentosas fosfato, también conocida
como vía de las hexosas monofosfato, donde se regulan a nivel
celular las concentraciones de NADPH).
Injuria celular,
apoptosis y necrosis
Jaime López Puga
Patología 2013
You might also like
- Diccionario Tecnico de AviacionDocument136 pagesDiccionario Tecnico de AviacionTUBI12345678980% (5)
- PALS Handbook - En.esDocument66 pagesPALS Handbook - En.esBarbaraSilva100% (1)
- Electricidad BasicaDocument32 pagesElectricidad BasicaKenny LoyolaNo ratings yet
- Asma Inducido y Caso Clinico Practica N°03 - 2021-IiDocument16 pagesAsma Inducido y Caso Clinico Practica N°03 - 2021-IiJULIO CESAR VILCAHUAMAN CUEVANo ratings yet
- Estabilidad Del PozoDocument16 pagesEstabilidad Del PozoLauriTerrazasMartines100% (2)
- Transformadores de CorrienteDocument27 pagesTransformadores de CorrienteMarcos100% (1)
- Patología Del SISTEMA NERVIOSODocument14 pagesPatología Del SISTEMA NERVIOSOYOCELINNo ratings yet
- PitahayaDocument74 pagesPitahayaMaxValdiviaRodriguezNo ratings yet
- Patologias Del Sistema Nervioso CentralDocument63 pagesPatologias Del Sistema Nervioso CentralErick Toledo SanchezNo ratings yet
- Sistema Nervioso Central Resumen PatologiaDocument8 pagesSistema Nervioso Central Resumen PatologiaDanny España100% (1)
- Atlas de Pato PUCDocument432 pagesAtlas de Pato PUCuzume278No ratings yet
- 2da Practica Pato Gene AcumulacionesDocument41 pages2da Practica Pato Gene AcumulacionesCamille KirschbaumNo ratings yet
- Banco LaminillasDocument17 pagesBanco LaminillasMoises Agustin Preciado AlvarezNo ratings yet
- Necrosis 2019Document34 pagesNecrosis 2019Diana Vallejos RodriguezNo ratings yet
- Seminario de Patología GeneralDocument5 pagesSeminario de Patología GeneralCristina GonzálezNo ratings yet
- Presentación Tema 30.. 2020Document127 pagesPresentación Tema 30.. 2020sevillistaNo ratings yet
- Alteraciones VascularesDocument40 pagesAlteraciones VascularesJosayda daileht Aguilar floresNo ratings yet
- Tema Vi CirculatorioDocument58 pagesTema Vi CirculatorioHeyerlin SiviraNo ratings yet
- Renal enDocument155 pagesRenal enperaltalorcaNo ratings yet
- Necrosis 07 08 WebDocument38 pagesNecrosis 07 08 WebAlvaro EspinozaNo ratings yet
- Asignatura Ciclo: Patología General: V Semestre Academico: 2022-IiDocument36 pagesAsignatura Ciclo: Patología General: V Semestre Academico: 2022-IiAngela PalominoNo ratings yet
- SNcentral y PerifericoDocument167 pagesSNcentral y PerifericoNaru MendozaNo ratings yet
- Laminas de PatologíaDocument21 pagesLaminas de PatologíaKassandra Reynoso ArreolaNo ratings yet
- 420-2014-03-20-10 Necrosis OseaDocument25 pages420-2014-03-20-10 Necrosis OseaDiana Diaz FloresNo ratings yet
- Practica Patología 12.2Document26 pagesPractica Patología 12.2Rodrigo MirandaNo ratings yet
- Patologia Cardiovascular: MG Víctor Martin González PalominoDocument131 pagesPatologia Cardiovascular: MG Víctor Martin González PalominoSung Soon ChangNo ratings yet
- Afecciones Más Frecuente de La Columna VertebralDocument11 pagesAfecciones Más Frecuente de La Columna Vertebralleandro planasNo ratings yet
- Guia de Practica Patologia 2021-IiDocument65 pagesGuia de Practica Patologia 2021-IiGuianela Polo0% (1)
- PG - 2022 - 1 - Práct-NecrosisDocument27 pagesPG - 2022 - 1 - Práct-NecrosisItzae Abdiel Levano GutierrezNo ratings yet
- Práctica Semana 15 FSPDocument132 pagesPráctica Semana 15 FSPMarianela Mori GonzalesNo ratings yet
- Expo PatologiaDocument6 pagesExpo PatologiaRicardo Velasco TapiaNo ratings yet
- Clase V (Tema 2) Patologia General UncausDocument79 pagesClase V (Tema 2) Patologia General UncausgabrielaNo ratings yet
- Guia de Practica Patologia 2022-IDocument78 pagesGuia de Practica Patologia 2022-IGisela VidaurreNo ratings yet
- Anatomía PatológicaDocument5 pagesAnatomía PatológicaFilomentor VargasNo ratings yet
- Repaso para El Parcial de FisiopatologiaDocument61 pagesRepaso para El Parcial de Fisiopatologiamarlyn jaimesNo ratings yet
- PATOLOGIA-Clase N°15-Patologia Del Sistema NerviosoDocument97 pagesPATOLOGIA-Clase N°15-Patologia Del Sistema NerviosoGiannella SilvestreNo ratings yet
- ExámenesDocument15 pagesExámenesMecagoen DiezNo ratings yet
- 1ra. PRÁCTICA B-NECROSIS-PATOLOGIA GENERAL 2022-2Document27 pages1ra. PRÁCTICA B-NECROSIS-PATOLOGIA GENERAL 2022-2Nayelyn HuamanNo ratings yet
- Fisiopatología Del Infarto CerebralDocument13 pagesFisiopatología Del Infarto CerebralYelNo ratings yet
- Tejidos AnimalesDocument131 pagesTejidos AnimalesCieloNo ratings yet
- NEURO DR FajardoDocument33 pagesNEURO DR FajardoLaura Juliana Quintero WiderkehrNo ratings yet
- Patologia General - Conferencia 12 Trastornos Cirsulatorios. Parte IIIDocument56 pagesPatologia General - Conferencia 12 Trastornos Cirsulatorios. Parte IIIROCIO GIRA AGUIRRENo ratings yet
- PATOLOGIA-Clase N°9-I-Patologia de Los Organos HematopoyeticosDocument67 pagesPATOLOGIA-Clase N°9-I-Patologia de Los Organos HematopoyeticosFIORELLA ALEXANDRA CARRASCO VARGASNo ratings yet
- Patología 2017 Imagenes Primera UnidadDocument13 pagesPatología 2017 Imagenes Primera UnidadBeanella Barrios100% (1)
- Teoria 1 Patologia CardiovascularDocument128 pagesTeoria 1 Patologia Cardiovascularnicol yazminNo ratings yet
- PatosistemicaDocument7 pagesPatosistemicaRonald Fabian YucraNo ratings yet
- 1 Era PRACTICA PATO GENE-ADAPTACIONES 2023-1Document54 pages1 Era PRACTICA PATO GENE-ADAPTACIONES 2023-1anaNo ratings yet
- Capitulo 28 - SNCDocument20 pagesCapitulo 28 - SNCAlejandra AristizábalNo ratings yet
- ACV IsquemicoDocument7 pagesACV IsquemicoMarianaGómezNo ratings yet
- Micro y MacroDocument2 pagesMicro y MacroAnthuan MitreyaNo ratings yet
- Anatomía Patológica Del Sistema Nervioso CentralDocument7 pagesAnatomía Patológica Del Sistema Nervioso CentralSofía De MarcoNo ratings yet
- Tema 11Document4 pagesTema 11atabepacNo ratings yet
- Patologia OVINOS Con BibliografiaDocument21 pagesPatologia OVINOS Con BibliografiaEVELYN JOHANNA RAMOS SANCHEZNo ratings yet
- Reacción de Las Neuronas A La Lesión, Edema Cerebral, Hipertensión Intracraneana, Malformaciones y Lesión Cerebral PerinatalDocument8 pagesReacción de Las Neuronas A La Lesión, Edema Cerebral, Hipertensión Intracraneana, Malformaciones y Lesión Cerebral PerinatalCesar Alberto Alzate SantaNo ratings yet
- Acv AndreDocument5 pagesAcv AndreFilomentor VargasNo ratings yet
- Practica 3 Inflamacion Aguda y CronicaDocument17 pagesPractica 3 Inflamacion Aguda y Cronicaarianna trujilloNo ratings yet
- Patologìa Sistema NerviosoDocument121 pagesPatologìa Sistema NerviosoVictormanuel Haro MoriNo ratings yet
- Final de Patologia Ordenada Por TemasDocument28 pagesFinal de Patologia Ordenada Por TemasAllan FurtadoNo ratings yet
- Histo Corazóny VasosDocument109 pagesHisto Corazóny VasosDiegoAlejandroCardonaNo ratings yet
- Examen 2023 ApgDocument4 pagesExamen 2023 ApgJorge Bou benagesNo ratings yet
- Aptes APSDocument17 pagesAptes APSAinoa Bersani RuizNo ratings yet
- Patologia FINALDocument71 pagesPatologia FINALAllan FurtadoNo ratings yet
- Trastornos HemodinámicosDocument10 pagesTrastornos HemodinámicosBruna AlviteNo ratings yet
- ScieloDocument5 pagesScieloBarbaraSilvaNo ratings yet
- Masaje Uterino BimanualDocument1 pageMasaje Uterino BimanualBarbaraSilvaNo ratings yet
- Enartrosis ArticulacionDocument1 pageEnartrosis ArticulacionBarbaraSilvaNo ratings yet
- Poa - GMQDocument5 pagesPoa - GMQJomovi VinNo ratings yet
- Esi JM - Fundamentación FinalDocument4 pagesEsi JM - Fundamentación FinalYamila Farías SarquísNo ratings yet
- Plan de Cuidado y Seguridad CSP y PasDocument5 pagesPlan de Cuidado y Seguridad CSP y Paskedekede2010No ratings yet
- Laboratorio de Fisica II N.°1Document9 pagesLaboratorio de Fisica II N.°1Diego TorresNo ratings yet
- Carta de Cristo 6Document38 pagesCarta de Cristo 6bersaca7No ratings yet
- Agentes Fisicos IDocument38 pagesAgentes Fisicos IMassiel Torres AriasNo ratings yet
- Tesis de La MusicaDocument59 pagesTesis de La Musicadarla ariasNo ratings yet
- Monografia Sobre Las DrogadiccionDocument5 pagesMonografia Sobre Las Drogadiccionjhon aymar chura mamaniNo ratings yet
- InfografiaDocument4 pagesInfografiajuwi75No ratings yet
- Resolucion Ministerial - N 822 2018 MINSADocument21 pagesResolucion Ministerial - N 822 2018 MINSAJessyAngelicaRosasBarretoNo ratings yet
- 5 Valvulas de Equilibrado HidraulicoDocument20 pages5 Valvulas de Equilibrado HidraulicoRene Arenas EnecalNo ratings yet
- Análisis Del Caso Mi Adicción Mi MaldiciónDocument2 pagesAnálisis Del Caso Mi Adicción Mi MaldiciónfranciscoNo ratings yet
- Memoria de Cálculo-Ventilacion de Estacionamientos R5Document2 pagesMemoria de Cálculo-Ventilacion de Estacionamientos R5Myrian Graciela Pompa RiverosNo ratings yet
- Cantos Misa Pascua - Tiempo Ordinario 2024.Document2 pagesCantos Misa Pascua - Tiempo Ordinario 2024.Daniela BracamonteNo ratings yet
- PercepcionDocument12 pagesPercepcionJuanita ArzaNo ratings yet
- Diseño de TrabajoDocument12 pagesDiseño de TrabajoNicolás TovarNo ratings yet
- Caso Clinico Gota en MujerDocument3 pagesCaso Clinico Gota en MujercaballonskiNo ratings yet
- UT 2 - Analisis Energetico Equipos y SistemasDocument49 pagesUT 2 - Analisis Energetico Equipos y SistemasEnrique TorrezNo ratings yet
- Tarea 5. Atmosfera y Respiracion.Document2 pagesTarea 5. Atmosfera y Respiracion.kermitNo ratings yet
- Cinética EnzimáticaDocument6 pagesCinética EnzimáticaAlicia Valencia VázquezNo ratings yet
- Conflictos Sociales en PeruDocument55 pagesConflictos Sociales en PeruHector Jimmy Sanchez DozaNo ratings yet
- CHECK List de Grua.Document1 pageCHECK List de Grua.Kevin Castro MejiaNo ratings yet
- NEMÁTODOSDocument36 pagesNEMÁTODOSEdde PalenciaNo ratings yet
- La Opción CreyenteDocument2 pagesLa Opción CreyenteMatias NavarreteNo ratings yet