Professional Documents
Culture Documents
Eficacia Antinociceptiva Del Parecoxib Vs Morfina en Modelo PIFIR
Uploaded by
Denisse MatosOriginal Title
Copyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Eficacia Antinociceptiva Del Parecoxib Vs Morfina en Modelo PIFIR
Uploaded by
Denisse MatosCopyright:
Available Formats
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA
Eficacia antinociceptiva de Parecoxib frente a Morfina en el modelo PIFIR
Flores Agostini, Fernando N.1, La Torre Dvila, Andrea R.2, Lobato Jer, Carlos J.3, Manrique Loayza, Javier A.4, Matos Pipa, Denisse Y.5 6 QF. Robles Esquerre, Mnica J.
1,2,3,4,5 6
Alumnos del curso de Farmacologa 2011-I de la Facultad de Medicina de la Universidad Ricardo Palma Docente del curso de Farmacologa de la FAMURP
RESUMEN Este es un estudio preclnico experimental, con el objetivo de comparar la eficacia antinociceptiva de Parecoxib vs Morfina, va intraperitoneal (anlogo de la administracin por va IV), usando el modelo PIFIR (Alteracin Funcional por Induccin de Dolor en Ratones), los experimentos se realizaron en ratones. En este experimento se utiliz el Hot Plate Test, con el que se midi el tiempo transcurrido necesario para que el ratn se lama las patas, despus de haber sido colocado en una plancha caliente, pudiendo comparar, as, la eficacia de la Morfina y el Parecoxib. Estos se expresaron como ndice de Funcionalidad (IF%); que al ser de 0 el tiempo de inicio de dolor en la plancha caliente se estableci, posteriormente a su administracin, la relacin de sus eficacias, completando 9 ratones para el estudio. A partir de los resultados, se observ una eficacia comparada con control negativo de 98% para Morfina y de 96 % para Parecoxib. Concluyndose que existi eficacia antinociceptiva entre ambos frmacos. Palabras claves: Parecoxib, Morfina, antinociceptivo, modelo PIFIR
ABSTRACT This is an experimental preclinical study aimed at comparing the antinociceptive efficacy of Parecoxib vs. morphine, administered both intraperitoneally (analogous to intravenous administration), using the PIFIR model (Pain-Induced Functional Impairment in the Rat), the experiments were conducted in mice. In this experiment we used the Hot Plate Test with that we measured the time required for the mouse to lick their legs, after being placed on a hot griddle, so we can compare the effectiveness of morphine and parecoxib. These were expressed as the Functionality Index (FI%) that when 0 the start time of pain in the hot plate was established after its administration, the relation of their efficiencies, completing 9 mice for the study. From the results, there was a negative control efficacy compared with 98% for morphine and 96% for parecoxib. We concluded that there was antinociceptive effectiveness between the two drugs. Key words: Parecoxib, Morphine, antinociceptive, PIFIR model
1
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA INTRODUCCIN El presente trabajo busca comparar la eficacia de frmacos para el tratamiento del dolor, como se mencionar ms adelante, existen los frmacos de tipo opioides y los no opioides. La bsqueda de medicamentos que no causen el dao que producen los efectos adversos de los opioides ha llevado al estudio de nuevos frmacos que no posean tales reacciones, como el Parecoxib cuyas propiedades antinociceptivas se describirn ha detalle comparndolo con la morfina en este trabajo. El dolor, ms que un proceso patolgico, es un mecanismo de proteccin del organismo que se manifiesta siempre que un tejido es daado y que hace que la persona se aparte del estmulo doloroso. El dolor se clasifica en dos tipos: dolor rpido y dolor lento. El dolor rpido no se siente en los tejidos profundos, mientras que el dolor lento puede sentirse a nivel de la piel u rganos internos. Los receptores para dolor son siempre terminaciones nerviosas libres y pueden ser excitadas por tres tipos de estmulos: mecnico, qumico y trmico. La caracterstica principal de estos receptores es que no tienen la capacidad de adaptacin sino que se van sensibilizando cada vez ms. Para los estmulos trmicos existen tres tipos de receptores. Un grupo de receptores para fro, un grupo de receptores para calor y un grupo de receptores para dolor producido por temperaturas extremas (muy fro o muy caliente). Cuando las temperaturas son muy bajas, se activan las fibras del dolor por fro, y se inactivan cuando el estmulo alcanza los 10-15C y en este momento se estimulan los receptores para fro. Pero cuando la temperatura alcanza los 40C se inactivan estos receptores y a su vez, ya estn estimulados los receptores de calor. Las fibras C son fibras nerviosas de conduccin lenta, no mielinizados que responden a estmulos trmicos, mecnicos y qumicos, y son llamadas nociceptores-C polimodales. Este tipo de dolor es conducido a travs de la va paleoespinotalmico. Las fibras perifricas de esta va comienzan por la percepcin del estmulo doloroso (en este caso calorfico), por parte de los termorreceptores denominados corpsculos de Ruffini, stos llevan la sensacin de calor y terminan en las lminas II y III de las astas dorsales. Despus, la mayora de las seales atraviesa una o ms neuronas adicionales del interior de las astas dorsales antes de penetrar en la lmina V. Aqu, la ltima neurona de la serie emite axones largos que en su mayora se unen a las fibras de la va rpida atravesando primero hasta el lado contrario de la medula ascendente hasta el encfalo. Una dcima a un cuarto parte de las fibras llegan hasta el tlamo, las dems terminan en una de las tres reas siguientes: los ncleos reticulares del bulbo, el puente y el mesencfalo, el tectum del mesencfalo y la sustancia gris que rodea el acueducto de Silvio. Este tracto contribuye al procesamiento afectivo de la nocicepcin. La norepinefrina es el neurotransmisor de las fibras C, al igual que el glutamato, su degradacin es lenta, razn para pensar que a esto se debe su efecto prolongado. Sin embargo, aunque el dolor sea un mecanismo de defensa, presenta una molestia para el paciente, especialmente si es un tipo de dolor crnico, y para ello se utilizan diversos frmacos que su eleccin va depender de cun intenso sea 1 el dolor. Podemos agrupar a los frmacos utilizados para el tratamiento del dolor en dos grupos: los frmacos opioides y los no opioides. Los frmacos opioides son comnmente utilizados en el tratamiento del dolor. Existen opioides dbiles como el tramadol, la codena y la hidrocodona, y tambin existen opioides fuertes como la metadona, fentanilo y la morfina que es el frmaco representativo y de eleccin en este grupo. La morfina se administra por va parenteral IV, intratecal, pero tambin puede ser administrada por va subcutnea y oral, aunque
2
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA en este caso la biodisponibilidad es solo del 25%. La morfina se distribuye rpidamente en los tejidos pero debido a su naturaleza hidroflica, la velocidad con la que atraviesa la barrera hematoenceflica es menor a la de otras sustancias liposolubles como la codena y metadona. El 33% de la morfina administrada se une a protenas plasmticas y su concentracin es mnima pasada 24 horas de la administracin. El metabolismo de la morfina se da principalmente por glucoronoconjugacin a nivel heptico, formando dos metabolitos: morfina-6glucornido y morfina-3-glucornido. La morfina6-glucornido es ms potente que la morfina en s, y la morfina-3-glucornido tiene muy poca afinidad por los receptores opioides por lo que se le atribuye los efectos excitadores de la morfina. La semivida de la morfina es de 2 horas, y la semivida de la morfina-6-glucornido es un poco ms larga. Se elimina muy poca morfina sin cambios por filtracin glomerular, y la mayora lo hace como morfina-3-glucornido y en menor cantidad como morfina-6-glucornido.2 La morfina est indicada para el alivio del dolor prolongado limitado en el tiempo, como en una enfermedad terminal, dolor canceroso, tambin para el alivio inmediato del dolor sbito intenso, y para el alivio del dolor moderado a intenso en situaciones post-operatorias.3 La morfina ejerce sus efectos analgsicos principales a nivel de los receptores opioides , y a esta interaccin tambin se deben las reacciones adversas como la depresin respiratoria (centro respiratorio bulboprotuberancial), retencin de orina por inhibicin de la diuresis, nauseas, vmitos, y la dependencia fsica intensa que se produce en los pacientes que reciben crnicamente un tratamiento con morfina.3 Debido a estos efectos adversos muy marcados e importantes es que las investigaciones sobre el tratamiento del dolor se centraron tambin en otras sustancias que pudiesen tener una accin analgsica igual de efectiva que la morfina y con menos reacciones adversas. Dentro de los frmacos no opioides se encuentran los inhibidores de la ciclooxigenasa (COX), enzima encargada de catalizar la sntesis de prostaglandinas (PG), son frmacos muy utilizados en la actualidad, debido a su fcil adquisicin y a sus diferentes presentaciones, que permiten una administracin ambulatoria. Existen dos isoformas de la COX, la COX-1 es una enzima constitutiva presente en todas las clulas del organismo, y tiene como funcin principal la citoproteccin, la COX-2 es una enzima inducible presente en procesos inflamatorios. Los primeros frmacos en aparecer en el mercado fueron inhibidores no selectivos de la COX, estos bloquean la sntesis de PG por las dos vas, y es ah donde aparecen los efectos adversos: Al inhibir la COX-1, las funciones fisiolgicas de las PG tambin se inhiban, entonces el tratamiento con estos frmacos traa como resultado la principal reaccin adversa: la lcera gstrica, por inhibicin de la secrecin del moco gstrico e incremento de la secrecin del cido gstrico (cido clorhdrico, HCl). Actualmente se siguen utilizando estos frmacos pero la vigilancia mdica es muy importante. En los ltimos aos, la introduccin en el mercado de un frmaco inhibidor selectivo de la COX-2, ha llamado mucho la atencin del personal de salud. El nombre genrico es Parecoxib y se comercializa como Dinastat. Es importante mencionar que su uso adems produjo inters en el sentido de ser el Parecoxib sdico, el primer frmaco de su grupo (inhibidores selectivos de la enzima COX-2) administrable por va parenteral, por vas intravenosa e intramuscular (de aqu en adelante, IV e IM, respectivamente), ya que anteriormente solo se dispona de presentaciones para administracin por va oral. Los estudios realizados hasta el momento demuestran que el Parecoxib presenta menos reacciones adversas ya que no inhibe las funciones fisiolgicas de las PGs, sino solo las que median los procesos inflamatorios, y presenta, en algunos casos, una mayor eficacia que otros inhibidores no selectivos de la COX.
3
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA El Parecoxib una vez administrado se transforma a Valdecoxib rpidamente por desoximetilacin, y este Valdecoxib es la forma activa del frmaco con una vida media de 7-8 horas. Tiene una extensa unin a protenas plasmticas (97-99%) y un metabolismo heptico por las enzimas del sistema microsomal CYP3A, CYP2C9. Se 2 elimina por va renal. El Parecoxib est indicado para alivio del dolor consecutivo a la extraccin de piezas dentarias y brindan alivio de la inflamacin en la osteoartritis y la artritis reumatoide (eficacia dosis dependiente). Sin embargo, su uso ms comn, aunque no generalizado, es en el perioperatorio, cuando los pacientes no pueden ingerir frmacos.2 En las investigaciones revisadas por la FDA, se encontr, dentro de los efectos adversos, que el Valdecoxib incrementaba el riesgo de infarto de miocardio y accidente cerebrovascular por lo que debe evitarse en personas predispuestas, tambin se seala algunas reacciones cutneas o de hipersensibilidad. El Parecoxib inhibe el metabolismo del metoprolol, permitiendo que se acumule, y tiene interacciones similares con inhibidores selectivos de la recaptacin de serotonina, antidepresivos tricclicos, agentes neurolpticos y frmacos antiarrtmicos.2 Se han realizado diversos estudios en los que se compara la eficacia del Parecoxib frente a otros frmacos, sobretodo inhibidores no selectivos de la COX, como el Ketorolaco, demostrando que el Parecoxib tiene una potencia y eficacia muy similar y con menos reacciones adversas. Adems, es mejor tolerado en pacientes adultos mayores. Asimismo, otros estudios similares a este, comparan la eficacia del Parecoxib frente a otro tipo de frmacos, como los opioides (como la Morfina) y se demostr que el Parecoxib tiene una eficacia parecida a la morfina en dosis bajas, considerando, naturalmente, que la morfina a dosis farmacolgicas es moderadamente ms potente que el Parecoxib. El objetivo de esta investigacin es comparar la eficacia antinociceptiva del Parecoxib con la Morfina utilizando el modelo PIFIR.
MATERIALES Y METODOLOGIA
Los experimentos de analgesia se realizaron empleando ratones, con un peso de 20-40 gramos, los cuales se mantuvieron a una temperatura constante de 22C, humedad y ambiente fsico de trabajo acordes con el correcto funcionamiento tanto de las equipos de laboratorio como de la viabilidad de realizar de manera correcta el proyecto por parte de los ejecutantes. Para su realizacin, utilizamos el modelo de alteracin funcional inducida por dolor (PIFIR por sus siglas en ingls) que se caracteriza por la induccin de dolor de tipo mecnico-calorfico producido por el Hot Plate, un equipo elctrico constituido y regulado por un ultra termostato que determina la temperatura a emplear, el mismo que es manejado exteriormente por un panel frontal que indica el calor de la placa o plato de metal en su superficie. El panel frontal est constituido de una serie de botones, como el botn marcador Heat (que indica calor) el cual regula la produccin trmica y por consiguiente la temperatura de la placa, este botn toma la funcin de un swicht para los dos botones adyacentes que gradan el incremento o decremento de la temperatura la que a su vez se encuentra entre el rango de 0 100 C. El plato metlico en la superficie est hecho en su mayor parte de acero inoxidable, material conductor de calor. Por otro lado, el modelo del equipo Hot Plate utilizado nos proporcionaba un cronmetro digital, el cual funcionaba con un dispositivo manual externo unido por un cable de conexin elctrica, este dispositivo fue manipulado minuciosamente para 39 efectos de la toma de tiempo en el trabajo . En primer trmino, se procedi a encender el equipo elctrico (Hot Plate), a una temperatura
4
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA de 55 C ya establecida por el grupo como estndar para el proyecto, esto se estableci por concordancia con referencia a diversas fuentes bibliogrficas de trabajos anteriores similares. En segundo lugar, se procedi a colocar los ratones en una jaula previamente dividindolos en 03 grupos de 03, marcndolos con plumones; uno en la cabeza (color negro) otro en el lomo (color azul) y otro en la cola (color rojo) para cada ratn de los grupos igualitariamente. Esto se hizo con la finalidad de poder clasificarlos en los 3 tratamientos distintos a evaluar con Suero Fisiolgico (control negativo), con Morfina (control positivo) y con Parecoxib (grupo control). Luego, se procedi a cargar las 09 jeringas con sus respectivos frmacos a dosis conocidas y volumen calculado en el laboratorio. Seguidamente, con los ratones ya marcados, se procedi a colocar a cada uno en el Hot Plate previamente estandarizado a una temperatura de 55 C. Se les tom as el tiempo basal de resistencia al dolor con el dispositivo manual y el cronmetro digital del aparato pulsndolo dos veces; la primera en el comienzo del contacto del animal con el plato y la segunda cuando el ratn se lame las patas, en donde observamos la resistencia natural nociceptiva de cada animal pre administracin de frmacos. Una vez tomado el tiempo, se retiraron a los ratones rpidamente y se procedi a colocarlos secuencialmente en otra jaula, como ya mencionamos segn iban lamindose las patas, signo fundamental en nuestro estudio para determinar el dolor causado por la superficie del plato. Se procedi a esperar 30 minutos segn cronmetro manual para volver a proceder en la toma de tiempo pero esta vez post administracin de frmacos. Luego de la toma basal, procedimos con la administracin de los frmacos por va intraperitoneal, ya que es la va de eleccin para trabajar en animales de experimentacin pequeos, adems se consigue una adecuada rapidez farmacocintica y del mecanismo de accin del frmaco, sus acciones y efectos farmacolgicos deseados. Las drogas empleadas fueron: Suero Fisiolgico en solucin de 0.1 mL/10 g. inyectada a los ratones marcados en la cabeza para cada grupo, Morfina a una dosis de 10 mg/Kg inyectada a los ratones marcados en el lomo para cada grupo y Parecoxib a una dosis de 31.6 mg/Kg para los ratones marcados en la cola por grupo. La administracin curs exitosamente y sin ningn inconveniente. Posteriormente, habindose concluido los 30 minutos, se realiz la primera toma del tiempo post tratamiento, obtenindose los datos respectivos y apuntndolos cuidadosamente, as se procedi repetitivamente por 8 veces lo que nos dio un tiempo total de 4 h. stos datos se expresaron tambin como porcentaje de ndice de funcionalidad (IF%); al ser este IF% = 0 al reflejarse dolor en los ratones con suero fisiolgico al lamerse las patas. Utilizando la frmula diremos que; IF% = [(Fx-C-)/C-] X 100% ; Donde: Fx: Frmaco analgsico en cuestin (morfina, M; Parecoxib, P) C: Control negativo (Suero Fisiolgico; S) ANALGESIA = (DP DB)/3
; Donde:
DP: dato parcial (dato obtenido en cada medicin con el hot plate, para un ratn individual) DB: dato basal de ese mismo ratn
5
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA RESULTADOS
FARMACOS
IF%
SUERO FISIOLOGICO
MORFINA
98%
PARECOXIB
96%
CUADRO II. Comparacin de IF%, obtenidos segn la frmula anteriormente descrita. La administracin de Suero fisiolgico, por representar el control negativo, no presenta IF%, pero es til en el clculo del IF% de los dems frmacos (ver frmula)
FIGURA II. Curva temporal, representando la relacin entre el tiempo transcurrido (intervalos de 30 minutos a partir de un tiempo inicial T0) y la analgesia; usando: ANALGESIA = (DP D B)/3; donde: DP: dato parcial (dato obtenido en cada medicin con el hot plate, para un ratn individual). DB: dato basal de ese mismo ratn; es decir, consiste en el promedio (para los tres ratones usados con cada frmaco, en una medicin determinada, de ah su divisin entre 3 de la diferencia entre los datos) de las tres diferencias (de los tres ratones) entre el dato obtenido en esa medicin y el dato basal inicial. La diferencia realizada, representa el grado de ANALGESIA comparada entre la administracin del Frmaco y su basal
De un total de nueve ratones que recibieron los tratamientos correspondientes, se obtuvieron los siguientes datos (Tabla 1): En los tres ratones a los que se administr suero fisiolgico (Control Negativo), el promedio de tiempo de resistencia al dolor, menos sus respectivos tiempos basales, fue de 3.03 segundos. En los tres ratones, a los que se administr morfina, el promedio de tiempo de resistencia al dolor, menos sus respectivos tiempos basales, fue de 6 segundos. En los tres ratones, a los que se administr Parecoxib, el promedio de tiempo de resistencia al dolor, menos sus respectivos tiempos basales, fue de 5.94 segundos. Siendo el suero fisiolgico el control negativo, se hall el ndice de Funcionalidad (IF%) del
FIGURA I. Representacin comparada del IF% entre Parecoxib y Morfina.
6
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA Parecoxib y de la Morfina, dividiendo la diferencia entre sus promedios de resistencia al dolor (de morfina y Parecoxib) y los promedios del control negativo, con los mismos promedios, multiplicndolos por cien. Resultando que la Morfina presenta un IF% de 98% y el Parecoxib un IF% de 96%. DISCUSIN Los ratones del grupo de suero fisiolgico mostraron un aumento de resistencia al dolor producido por el calor, evidenciado en la diferencia entre sus basales y el promedio de resistencia en los periodos que fueron sometidos al calor (55 C); aumento en promedio unos 3.03 segundos, esto se justifica, porque existe un sistema de analgesia en el encfalo y la mdula espinal, que consta de tres componentes:1) la regin gris periacueductal y las areas periventriculares del mesencfalo y la parte superior de la protuberancia que rodean al acueducto de Silvio y a las porciones del tercer y del cuarto ventrculo. Desde estas zonas, las neuronas envan seales hacia 2) el ncleo magno del rafe, un ncleo delgado de la lnea media situado en las partes inferior de la protuberancia y superior del bulbo raqudeo, y el ncleo reticular paragigantocelular, que ocupa una posicin lateral de este ltimo. A partir de estas estructuras, se transmiten seales descendentes de segundo orden por las columnas dorso laterales de la mdula espinal hacia 3) un complejo inhibidor del dolor localizado en las astas dorsales de la mdula espinal. A este nivel, las seales analgsicas tienen la capacidad de bloquear el dolor antes de su transmisin al encfalo. La estimulacin elctrica de la regin gris periacueductal o del ncleo magno del rafe es capaz de suprimir muchas seales dolorosas potentes que penetran a travs de las races medulares dorsales. As mismo la activacin de los ncleos periventriculares del hipotlamo, que quedan adyacentes al tercer ventrculo, y en menor medida, el fascculo prosenceflico medial, tambin del hipotlamo. Diversas sustancias transmisoras participan en el sistema analgsico, especialmente la encefalina y la serotonina. Muchas fibras nerviosas derivadas de los ncleos periventriculares y de la regin gris periacueductal segregan encefalina en sus terminaciones. Las terminaciones de numerosas fibras en el ncleo magno del rafe tambin liberan encefalina al ser estimulados. Las fibras nacidas en esta zona envan seales hacia las astas dorsales de la mdula para segregar serotonina en sus terminaciones. La serotonina hace que las neuronas medulares locales liberen tambin encefalina. Se cree que la encefalina propicia una inhibicin presinptica y postsinptica de las fibras para el dolor del tipo C y A al hacer sinapsis en las astas dorsales. Por lo tanto, el sistema de analgesias es capaz de bloquear las seales de dolor en su punto de entrada inicial a la mdula espinal. Existe tambin un sistema de opioides cerebrales: endorfinas y encefalinas, se han descubierto varias sustancias opioides en diferentes puntos del sistema nervioso y todas ellas son producto de la degradacin de tres grandes molculas proteicas: proopiomelanocortina, proencefalina y prodinorfina. Entre las ms importantes figuran la endorfina, la metencefalina, la leu- encefalina y la dinorfina. Las dos encefalinas estn presentes en el tronco del encfalo y la mdula espinal, dentro de las porciones de analgesia descritas antes y la endorfina lo est en el hipotlamo y en la hipfisis. La dinorfina est en las mismas zonas que la encefalina, pero en una cantidad mucho menor. Es importante mencionar que por encima de los 30 C, comienzan a estimularse los receptores para el calor; pero, tambin, se extinguen, ms o menos, sobre los 49 C. Los resultados en los ratones a los que se les administr morfina corroboraron los datos tericos, conocidos con anterioridad, ya que aument de manera evidente la resistencia al dolor producido por el hot plate en comparacin a su basal, aumento en promedio de 6 segundos. Esto se debi a fenmenos farmacocinticos y farmacodinmicos del frmaco. Con respecto a los primeros, la morfina se administra por va oral, subcutnea, endovenosa e intramuscular,
7
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA en nuestro caso se le administr a los ratones por va intraperitoneal (anloga de la va IV). ANLISIS DE LA CURVA TEMPORAL Se encontr que, a partir de la administracin, la analgesia se fue incrementando, alcanzando su pico mximo a las 2.5 horas, que, aparentemente, no correspondera al terico para administracin por va IV (0.1 a 0.3 horas), esto probablemente se deba al tipo de morfina; ya que, como se mencion anteriormente, existen tres tipos de este frmaco, de liberacin rpida, lenta y ultra lenta, que aunque se administran por va oral, son factibles de administrarse por va parenteral (IM e IV), modificando la dosis; se presume que la morfina empleada corresponde a la de infusin retardada (lenta), usada en el establecimiento de donde se obtuvo el frmaco; por lo que se deduce que, el tiempo de actividad mxima antinociceptiva quedar retrasado; asumiendo que para administracin por va oral de este tipo de morfina lleva al Cmax a 3-3.5 horas, entonces para la va utilizada en este experimento sera menor, por la biodisponibilidad mucho mayor; por lo que es explicable el tiempo obtenido para el Cmax. Asimismo, es posible observar, en la misma grfica, un ascenso en la curva al finalizar la grfica, ste puede deberse a lo siguiente: la morfina, como se indic anteriormente, se metaboliza, principalmente, en dos productos, M6-G y M-3-G, donde el segundo se encuentra en mucha mayor concentracin que el primero, la M6-G tiene mayor actividad analgsica que la morfina original, por lo que se eleva la curva; sin embargo, como la M-3-G es antagonista de los efectos analgsicos de la morfina, adems de mediar sus principales efectos adversos, eso podra explicar que el ascenso no sea tan marcado, siendo, inclusive, inferior al de Parecoxib sdico. Adems, este efecto podra deberse a que la exposicin de los ratones a temperaturas elevadas haya causado un dao tisular que produzca la destruccin de fibras nerviosas las cuales insensibilizaran a los ratones ante el dolor. El grupo de los ratones a los cuales se les administr Parecoxib, mostraron una eficaz resistencia al dolor producido por el calor , con un aumento y declive de esta en lapsos de 30 minutos, pero en promedio el Parecoxib aument la resistencia en aproximadamente el doble que el basal (el incremento fue de 5,94 segundos en promedio), todo esto se debi, tambin, a criterios farmacocinticos y farmacodinmicos, el Parecoxib (inhibidor especfico de la COX-2) es un pro frmaco, que se convierte con rapidez (15 minutos) y casi en su totalidad (> 95%), en el producto activo Valdecoxib, en alrededor de 15 a 52 minutos (lo que explica el primer declive en la curva temporal del Parecoxib en el lapso de 1 a 1.5h) por hidrlisis enzimtica en el hgado. Como se menciona anteriormente se pareca una distribucin en zigzag. Probablemente este se deba al continuo metabolismo de Parecoxib a Valdecoxib, lo que explica el descenso de la curva (metabolismo) y su posterior ascenso (accin farmacolgica del Valdecoxib). La actividad mxima del Parecoxib se dio a las 3 horas (dentro del rango esperado) y la duracin de efecto, de 6 a 12 horas, por lo que no se tiene datos para su confirmacin debido a que el estudio termino a las 4h de la administracin de los frmacos, pero esto permite deducir que la grfica continua con la misma dinmica. En las condiciones experimentales empleadas para desarrollar el estudio, Parecoxib present efectos analgsicos tan grandes como los generados por el compuesto opioide prototipo morfina, ya que presento un IF% de 96% comparado con un 98% de la morfina. Lo que corrobora la utilidad analgsica que puede tener Parecoxib. Nuestro hallazgo, con respecto a la magnitud de antinocicepcin demuestra equiefectividad entre la morfina y el Parecoxib en comparacin con nuestro artculo base, Eficacia antinociceptiva de Parecoxib vs morfina en el modelo PIFIR, realizado en 108 ratas, fue la misma, teniendo en cuenta que nuestra poblacin fue mucho menor.
8
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA Nuestro artculo base se fundamenta en que dentro de los frmacos utilizados para el control del dolor crnico ltimamente se han utilizado los llamados inhibidores selectivos COX-2, principalmente celecoxib y rofecoxib; recientemente se cuenta con el nico de stos en presentacin inyectable, Parecoxib sdico, por lo que se requera comparar los efectos analgsicos, la eficacia y la potencia antinociceptiva de ste con el opioide prototipo morfina, ya que este ltimo grupo de medicamentos se asocia a mltiples efectos colaterales. El objetivo de este estudio, por lo tanto fue el de comparar los efectos analgsicos, la eficacia y potencia de Parecoxib vs morfina en el modelo PIFIR. CONCLUSION En este estudio preclnico, utilizando el modelo PIFIR, el Parecoxib mostr utilidad analgsica (eficacia) tan buena como la mostrada por el opioide morfina. 11. REFERENCIAS BIBLIOGRFICAS 1. Guyton & Hall. Tratado de Fisiologa Mdica 11 Edicin. Editorial Elsevier S.A. Espaa. 2009 Goodman & Gilman. Las Bases Farmacolgicas de la Teraputica 11 Edicin. Editorial McGraw-Hill Interamericana S.A. Mxico. 2007. Plan Nacional para la Enseanza y Formacin en Tcnicas y Tratamiento del Dolor. Farmacologa de los Analgsicos No Opioides (AINEs). Unidad 3-Captulo 1 P. Acn, C. Bono, R. Martnez, A. Faci, E. Facorro, I. Manzanares, M J. Velamazn, M. Sanz, E. Pasto1 Estabilidad de Parecoxib en dilucin con otros frmacos y administracin en perfusin continua IV para el control del dolor postoperatorio. Rev. Soc. Esp. Dolor 3: 185-193; 2007P.GarcaHarel,J.L, Casielles,M.P.Heredia ,A.Gutierrez-Guilln, R.Rodriguez-Mejas y M. De las Mulas, Parecoxib frente a 12. Ketorolaco en control del dolor agudo postoperatorio moderado., 2005, Espaa. Rang, H.P., Dale, M.M. Farmacologa, 6ta Edicin, Editorial Elsevier (2008) pginas, 596-607. UK Medicines Information Pharmacists Group. New Medicines on the market, Evaluated information for the NHS, United Kingdom (2002). Drugdex Evaluations. Micromedex Healthcare Series. Parecoxib. Ibuprofen. Naproxen en http://www.thomsonhc.com Accesado Febrero 2007. British National Formulary. British Medical Association and the Royal Pharmaceutical Society of Great Britain. Accesado en Febrero de 2007. Ministerio de Salud del Per. DIGEMID. Base de Datos de Registro Sanitario del Per. PERUDIS en http://www.digemid.minsa.gob.pe/aplicacion es/Perudis/listado-b.asp. Accesado en Febrero 2007. Barden J., et al. Oral Valdecoxib and injected Parecoxib for acute postoperative pain: a quantitative systematic review. BMC Anesthesiology 2003; 3:1-8. Kranke P., et al. Patients Global Evaluation of Analgesia and Safety of Injected Parecoxib for Postoperative Pain: A Quantitative Systematic Review. Anesthesia Analgesia 2004; 99:797-806. Tang J., et al. Effect of Parecoxib, A Novel Intravenous Cyclooxygenase Type-2 Inhibitor, on the Postoperative Opioid Requirement and Quality of Pain Control. Anesthesiology 2002; 96:1305 1309. Nussmeier N., et al. Safety and Efficacy of the Cyclooxygenase-2 Inhibitors Parecoxib and Valdecoxib after Noncardiac Surgery. Anesthesiology 2006; 104:518-526. Hubbard R. y et al. Parecoxib sodium has opioid-sparing effects in patients undergoing total knee arthroplasty under spinal anaesthesia. British Journal of Anaesthesia 2003; 90 (2): 166-172.
6.
7.
8.
9.
10.
2.
13.
3.
4.
14.
15.
9
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA 16. Philip Malan T., et al. The Cyclooxygenase2-Specific Inhibitor Parecoxib Sodium Is as Effective as 12 mg of Morphine Administered Intramuscularly for Treating Pain After Gynecologic Laparatomy Surgery. Anaesthesia Analgesia 2005; 100:454-460. 17. Bikhazi G., et al. A clinical trial demonstrates the analgesic activity of intravenous Parecoxib sodium compared with ketorolac or morphine after gynaecologic surgery with laparotomy. American Journal of Obstetrics and Gynecology 2004; 191:1183-1191. 18. European Medicines Agency (EMEA). Emea Public Statement On Valdecoxib (Bextra/Valdyn) and Parecoxib Sodium (Dynastat/Rayzon) Cardiovascular Risks In Coronary Artery Bypass Graft (CABG), Surgery And Serious Adverse Skin Reactions. London, 15 December 2004. 19. Amabile C., Spencer A. Parecoxib for Parenteral Analgesia in Postsurgical Patients. The Annals of Pharmacotherapy 2004; 38:882-886. 20. Drugdex Evaluations. Micromedex Healthcare Series. Parecoxib. Ibuprofen. Naproxen en http://www.thomsonhc.com Accesado Febrero 2007. 21. British National Formulary. British Medical Association and the Royal Pharmaceutical Society of Great Britain. Accesado en Febrero de 2007. 22. European Medicines Agency (EMEA). Emea Public Statement On Valdecoxib (Bextra/Valdyn) and Parecoxib Sodium (Dynastat/Rayzon) Cardiovascular Risks In Coronary Artery Bypass Graft (CABG), Surgery And Serious Adverse Skin Reactions. London, 15 December 2004. 23. Mason L, Edwards JE, Moore RA, McQuay HJ. Dosis nica oral de Naproxeno y Naproxeno sdico para el dolor postoperatorio agudo. En: La Biblioteca Cochrane Plus, 2006 Nmero 4. Oxford: Update Software Ltd. Disponible en: http://www.update-software.com. Fecha de la modificacin: 25 de agosto de 2004. 24. Drugdex Evaluations. Micromedex Healthcare Series. Parecoxib. Ibuprofen. Naproxen en http://www.thomsonhc.com Accesado Febrero 2007. 25. Kranke P., et al. Patients Global Evaluation of Analgesia and Safety of Injected Parecoxib for Postoperative Pain: A Quantitative Systematic Review. Anesthesia Analgesia 2004; 99:797-806. 26. Bainbridge D., et al. NSAID-analgesia, pain control and morbidity in cardiothoracic surgery. Canadian Journal of Anesthesia 2006; 53 (1): 4659. 27. Hubbard R. y et al. Parecoxib sodium has opioid-sparing effects in patients undergoing total knee arthroplasty under spinal anaesthesia. British Journal of Anaesthesia 2003; 90 (2): 166-172. 28. Chen L., et al. Systematic review of the analgesic efficacy and tolerability of COX-2 inhibitors in postoperative pain control. Journal of Clinical Pharmacy and Therapeutics 2004; 29:215-229. 29. Amabile C., Spencer A. Parecoxib for Parenteral Analgesia in Postsurgical Patients. The Annals of Pharmacotherapy 2004; 38:882-886. 30. Drugdex Evaluations. Micromedex Healthcare Series. Parecoxib. Ibuprofen. Naproxen en http://www.thomsonhc.com Accesado Febrero 2007. European Medicines Agency (EMEA). 31. European Medicines Agency (EMEA). Emea Public Statement On Valdecoxib (Bextra/Valdyn) and Parecoxib Sodium (Dynastat/Rayzon) Cardiovascular Risks In Coronary Artery Bypass Graft (CABG), Surgery And Serious Adverse Skin Reactions. London, 15 December 2004. 32. European Medicines Agency (EMEA). Emea Public Statement On Valdecoxib (Bextra/Valdyn) and Parecoxib Sodium (Dynastat/Rayzon) Cardiovascular Risks In Coronary Artery Bypass Graft (CABG), Surgery And Serious Adverse Skin Reactions. London, 15 December 2004.
10
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA 33. World Health Organization. Drug Information 2002; 16(3):228. 34. World Health Organization. Drug Information 2002; 16(3):228. 35. Ministerio de Salud del Per. DIGEMID DAUM. Alertas. Accesado Febrero del 2007 en http://www.digemid.minsa.gob.pe/alertas/ind ex.htm 36. European Medicines Agency (EMEA). Emea Public Statement On Valdecoxib (Bextra/Valdyn) and Parecoxib Sodium (Dynastat/Rayzon) Cardiovascular Risks In Coronary Artery Bypass Graft (CABG), Surgery And Serious Adverse Skin Reactions. London, 15 December 2004. 37. Bainbridge D., et al. NSAID-analgesia, pain control and morbidity in cardiothoracic surgery. Canadian Journal of Anesthesia 2006; 53 (1): 4659. 38. Food and Drug Administration. Alert for Healthcare Professionals Valdecoxib. En http://www.fda.gov/cder/drug/InfoSheets/HC P/ValdecoxibHCP.pdf. 39. MANUAL DE USO HOTPLATE & STIRRES, Stuart marca registrad, Reino Unido.
11
LIMA, PER 2011
UNIVERSIDAD RICARDO PALMA
FACULTAD DE MEDICINA HUMANA TABLA 1
TIEMPO DE RESISTENCIA AL DOLOR EN EL HOT PLATE TEST (segundos) PESO (g) FARMACOS Vol. (ml.) TTOS Basal 21 26 29 35 33.5 26 24 27.5 27 PARECOXIB MORFINA SUERO FISIOLOGICO 0.21 0.26 0.29 0.35 0.335 0.26 0.24 0.275 0.27 1 2 3 4 5 6 7 8 PROMEDIO PROMEDIO-Basal PROMEDIO (PROMEDIO-Basal) 23"48 7"94 12"94 10"68 10"97 11"07 12"98 10"54 6"67 IF% OBS -
16"44 17"42 27"71 24"75 19"13 22"87 27"82 21"04 27"10 5"42 6"91 7"91 6"33 8"66 7"54 8"32 8"54 9"28 13"41 14"65 18"74 14"21 8"89 7"74 14"50 11"86 12"93 5"34 6"37 7"06 12"38 8"80 13"27 10"65 11"32 15"58 4"80 10"71 9"66 13"28 9"90 9"73 16"10 9"01 9"36 4"58 4"13 13"20 6"70 16"68 17"42 12"38 9"15 8"89 5"44 10"33 14"40 11"03 19"60 5"04 14"45 14"65 14"36 3"51 8"55 8"16 6"83 7"90 13"92 16"37 9"41 13"21 3"41 8"12 4"89 5"43 4"86 7"36 9"10 5"40 8"18
7.04 2.52 -0.47 5.34 6.17 6.49 7.54 7.03 3.26
3.03
98%
5.94
96%
CUADRO I. Datos obtenidos durante el proceso experimental, segn tiempos, es importante aclarar, en este cuadro, que los nmeros arbigos presentes en la parte superior de la tabla, corresponden al tiempo, comenzando con el tiempo de 30 minutos despus de la administracin (indicado con el nmero 1), y con intervalos de media hora entre tomas de datos (por ejemplo, nmero 2: toma de muestra 60 minutos despus de la primera), hasta alcanzar las 4 horas.
12
LIMA, PER 2011
You might also like
- EmocionesDocument1 pageEmocionesElizabeth HernándezNo ratings yet
- Esa U1 EaDocument4 pagesEsa U1 EaAdnil OrtegaNo ratings yet
- .Ar-Aplicaciones Móviles Un Recurso para EnfermeríaDocument4 pages.Ar-Aplicaciones Móviles Un Recurso para Enfermeríaflavia MaturanoNo ratings yet
- Informe de Practica 2017.................Document53 pagesInforme de Practica 2017.................Elena PeñalozaNo ratings yet
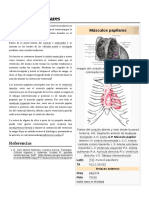
- Músculos PapilaresDocument2 pagesMúsculos PapilaresJENNY NAIDÚ GAMA AGUDELONo ratings yet
- Ensayo de Epidemiologia y Salud Publica en VenezuelaDocument5 pagesEnsayo de Epidemiologia y Salud Publica en VenezuelaAndresMarquezNo ratings yet
- .-Cuestionario de Turismo de Salud.Document2 pages.-Cuestionario de Turismo de Salud.RAUL FRANCIS PEREZ TATAMUESNo ratings yet
- Mapas ConceptualesDocument2 pagesMapas ConceptualesAnonymous iOjp1iRy100% (3)
- NocicepciónDocument3 pagesNocicepcióngabriela alejandra alvarez albanNo ratings yet
- CUESTIONARIOSDocument12 pagesCUESTIONARIOSjuanmog100% (2)
- Infecciones Causadas Por El Género MalasseziaDocument23 pagesInfecciones Causadas Por El Género MalasseziaHaisekiNo ratings yet
- Catálogo CreateviaDocument9 pagesCatálogo CreateviaPequeño Trio de Risas, Amor PuroNo ratings yet
- Respuestas Examen Ope Sacyl 2016Document13 pagesRespuestas Examen Ope Sacyl 2016Raquel EstebanNo ratings yet
- Guia Clinica de Trauma AbdominalDocument11 pagesGuia Clinica de Trauma AbdominalMariela Calle100% (1)
- Entrevista Diagnóstica para El Síndrome de AspergerDocument3 pagesEntrevista Diagnóstica para El Síndrome de AspergerantoncitoNo ratings yet
- Intervención en Crisis A Cargo de La PolicíaDocument39 pagesIntervención en Crisis A Cargo de La Policíajuramera100% (1)
- Pruebas de CompatibilidadDocument26 pagesPruebas de CompatibilidadFernanda VilchesNo ratings yet
- ÉBOLA ResumenDocument3 pagesÉBOLA ResumenMauricio Farias Hernandez0% (1)
- SAR - Parto EutócicoDocument22 pagesSAR - Parto EutócicoSamuel AcostaNo ratings yet
- Psicoterapia IntegrativaDocument5 pagesPsicoterapia IntegrativaRaisa Edith Rodriguez Solis100% (1)
- Anestesia InhalatoriaDocument104 pagesAnestesia InhalatoriaulisesNo ratings yet
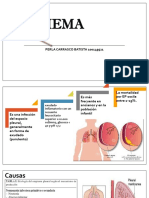
- Empiema Mi Expo Grupo1Document21 pagesEmpiema Mi Expo Grupo1Perla Carrasco BatistaNo ratings yet
- Cotizacion de Precio UnicoDocument6 pagesCotizacion de Precio UnicoDavid ValdiviaNo ratings yet
- Guia de La Dosis de Ejercicio Cardiosaludable en La Practica ClinicaDocument38 pagesGuia de La Dosis de Ejercicio Cardiosaludable en La Practica Clinicacerebrin80No ratings yet
- Baños de Vapor VaginalesDocument4 pagesBaños de Vapor VaginalesVerónica ChmielNo ratings yet
- Metodos de Diagnostico ParasitologicoDocument6 pagesMetodos de Diagnostico ParasitologicoEmireth RomeroNo ratings yet
- Walter RisoDocument7 pagesWalter RisoYeimis Carolina Reyes RamirezNo ratings yet
- MASOTERAPIADocument5 pagesMASOTERAPIARosa Lilibeth Quispe cansaya100% (1)
- HematuriaDocument5 pagesHematuriaarthkiuNo ratings yet
- Fármacos InotrópicosDocument9 pagesFármacos InotrópicosYango la RosaNo ratings yet