Professional Documents
Culture Documents
Destilacion Binaria Discontinua
Uploaded by
Edgar Jamanca AntonioCopyright
Available Formats
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
Available Formats
Destilacion Binaria Discontinua
Uploaded by
Edgar Jamanca AntonioCopyright:
Available Formats
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
AO DE LA UNIN NACIONAL FRENTE A LAS CRISIS EXTERNA
ESCUELA ACADMICO PROFESIONAL DE INGENIERA QUMICA
ASIGNATURA TEMA DOCENTE CICLO ALUMNO : Laboratorio de Operaciones Unitarias : Destilacin Discontinua. : Ing. Jimnez Escobedo Manuel : VII :JAMANCA ANTONIO, Edgar Martin
HUACHO PER
Laboratorio de Operaciones Unitarias
Pgina 1
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
ndice
ndice ..................................................................................................................................................... 2 Resumen ................................................................................................................................................ 4 DESTILACIN DISCONTINUA ................................................................................................................... 4 Introduccin ....................................................................................................................................... 4 Antecedentes...................................................................................................................................... 4 Fundamento Terico ........................................................................................................................... 6 Destilacin ...................................................................................................................................... 6 Fundamentos de destilacin. Tipos. Principales aplicaciones ............................................................ 6 Relacin de equilibrio termodinmico Liquido Vapor ..................................................................... 8 Coeficiente local y global en la transferencia de masa ..................................................................... 9 Mezcla Azeotrpica. Criterios de separacin .................................................................................. 10 Criterios y relaciones bsicas para una Destilacin Batch ............................................................... 11 Seccin Experimental ........................................................................................................................ 13 Equipo y Materiales Empleados ..................................................................................................... 13 Metodologa Experimental ............................................................................................................ 13 Tabulacin de Datos Experimentales Recolectados ........................................................................ 14 Resultados ........................................................................................................................................ 15 Tabla de Propiedades Fsicas ......................................................................................................... 15 Equilibrio Lquido Vapor ................................................................................................................ 16 Temperaturas de Burbuja y Roco .................................................................................................. 17 Nmero de Etapas de Equilibrio..................................................................................................... 17 Reflujo Mnimo ............................................................................................................................. 17 Reflujo Mximo............................................................................................................................. 18 Balance de Materiales a partir de los datos de composicin inicial, final y composicin del destilado ..................................................................................................................................................... 18 Anlisis y Discusin de Resultados ..................................................................................................... 20 Conclusiones ..................................................................................................................................... 20 Recomendaciones ............................................................................................................................. 21 Referencias Bibliogrficas ................................................................................................................. 21 Apndice .............................................................................................................................................. 22 Ejemplo de Clculos .......................................................................................................................... 22 Tabla de Propiedades de la Mezcla a partir de la Temperatura Promedio ....................................... 22 Hallando la composicin de etanol en el vapor a partir de la ecuacin - ................................... 22
Laboratorio de Operaciones Unitarias
Pgina 2
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Temperatura de Roco y Burbuja ................................................................................................... 24 Deduccin de Ecuaciones .................................................................................................................. 24 Mtodo - : ............................................................................................................................... 24 Temperatura de Roco y Burbuja ................................................................................................... 26 Reflujo Externo e Interno ............................................................................................................... 26 Balance de Materiales................................................................................................................... 26 Tablas adicionales, grficos y figuras varias ...................................................................................... 27 Tablas ........................................................................................................................................... 27 Grficos ........................................................................................................................................ 28 Cuestionario ..................................................................................................................................... 30
Laboratorio de Operaciones Unitarias
Pgina 3
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Resumen
La destilacion binaria discontinua es una operacin de las mas empleadas en la industria alimentaria, farmaceutica y perfumeria, para la separacion de los componentes que forman mezclas liquidas miscibles. La destilacion es una operacin unitaria de transferencia de masa, en si la destilacion es la operacin cuyo fin es la separacion de dos o mas liquidos miscibles mediante la ebullicion. Los vapores obtenidos se recuperan como producto deseable y se condensan. Los vapores condensados son mas ricos en el liquido o liquidos mas volatiles, mientras que los liquidos remanentes, son mas ricos en sustancias menos volatiles. Esta operacin recibe tambien el nombre de alambicacion, refinacion, agotamiento, fraccionamiento o rectificacion.
DESTILACIN DISCONTINUA Introduccin
La destilacin sirve para separar mezclas lquidas formadas por lquidos solubles entre s. A la destilacin en mltiples etapas en contracorriente se le da el nombre de rectificacin. Para el banco de ensayos se recomienda emplear una mezcla de etanol y agua como mezcla lquida. Se llena en el caldern (fondo de la columna). El vapor generado asciende por la columna. Est enriquecido con el componente de menor punto de ebullicin (etanol). Abandona la columna por la parte superior, se condensa en un condensador parcial y se recoge en un depsito de separacin de fases. Una parte de este condensado se recoge como producto en un depsito y la otra parte se devuelve como reflujo a la columna. All experimenta, en su descenso, un ntimo intercambio de calor y materia con el vapor ascendente. Este intercambio da como resultado un mayor enriquecimiento de la fase vapor en etanol y de la fase lquida en agua. La fase lquida cae hacia el fondo de la columna (caldern) y se acumula all. Se dispone de una columna de platos perforados y de una columna de relleno. La columna de relleno contiene anillos Raschig. La relacin de reflujo se puede ajustar con vlvulas. Los valores de medicin relevantes se registran con sensores y se indican digitalmente en el armario de distribucin. El dispositivo de calefaccin al fondo de la columna (caldern) se ajuste con un regulador PID.
Antecedentes
Las operaciones de destilacin azeotrpica presentan un comportamiento complejo y al mismo tiempo interesante, difcil de calcular o simular. Su estudio debe hacerse a la vista de las regiones de destilacin y de las fronteras que las separan, que surgen como consecuencia de la estructura de los mapas de curvas de residuo y de lneas de destilacin. stos se utilizan como una representacin grfica del equilibrio lquido-vapor en sistemas ternarios.
Laboratorio de Operaciones Unitarias
Pgina 4
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
La relacin entre los diagramas de equilibrio de las mezclas ternarias y los procesos de destilacin se estableci a principios del siglo XX. En los trabajos de Scheinemakers (1901) y Ostwald (1896-1902) sobre las curvas de residuo, lneas de destilacin y fronteras de destilacin, se destaca la importancia de la topologa de las superficies de lquido saturado en los diagramas temperatura-composicin y su influencia sobre la forma que adoptan las curvas que describen la composicin del residuo de una destilacin simple. En estos trabajos se establece la creencia, que se ha mantenido durante muchos aos, de que estas fronteras coinciden con la proyeccin de las crestas y los valles de la superficie de lquido saturado (lquido a su temperatura de burbuja) sobre el tringulo de composicin de la base de los diagramas temperatura-composicin. A raz de estos trabajos, durante mucho tiempo se pens que las curvas de residuo (y por tanto las fronteras de destilacin), no podan atravesar las crestas y los valles de la superficie de lquido saturado. Sin embargo, en 1945 se plantea la primera contradiccin con este esquema, postulada por Ewell y Welch a partir de datos experimentales. Los conceptos de regin de destilacin (y por tanto de fronteras de destilacin) tal y como se utilizan en la actualidad, aparecen ya recogidos en el libro "Destilacin y Rectificacin" de E. Kirschbaum, editado en 1948 y traducido al castellano en 1954. En 1963, Swietoslawski presenta un resumen de las investigaciones realizadas hasta el momento acerca de la relacin entre la destilacin azeotrpica y la forma de las superficies de lquido saturado, y establece claramente que los valles y crestas de dicha superficie no coinciden exactamente con las fronteras de destilacin. En esta poca, diversos cientficos analizan la trayectoria de los perfiles de composicin en columnas de rectificacin multicomponente, en las proximidades de los azetropos y de los compuestos puros. Siguiendo esta lnea, en 1977, Matsuyana y Nishimura desarrollan y aplican anlisis de este tipo a la separacin de mezclas homogneas multicomponentes, pero son fundamentalmente Doherty y colaboradores quienes, en sus trabajos pioneros en el rea de la destilacin azeotrpica han propuesto, desde 1978, una serie de nuevos conceptos, diseando algoritmos y analizando el comportamiento del proceso bajo distintas condiciones de operacin. En estos trabajos se ha establecido de forma clara y rotunda la necesidad de utilizar diagramas ternarios para el diseo de operaciones de destilacin azeotrpica y se han redefinido los conceptos de fronteras de destilacin y curvas de residuo. Posteriormente (1984), Van Dongen y Doherty recogen los argumentos correctos de los artculos precedentes para llegar a la conclusin definitiva de que los valles y las crestas no han de coincidir necesariamente con las fronteras de destilacin simple. Otros investigadores tambin han presentado resultados que han contribuido a un mejor conocimiento de las operaciones de destilacin azeotrpica. Despus de que durante algunos aos se haya centrado el objetivo de las investigaciones en esclarecer las cuestiones pendientes acerca de las caractersticas de los mapas de curvas de residuo, la naturaleza exacta de las fronteras de destilacin y su relacin con los procesos de destilacin, en la actualidad, la mayor parte de los trabajos que aparecen publicados relacionados con estos temas se centran en el estudio de la existencia de mltiples estados estacionarios y en el diseo de sntesis de columnas. No obstante, y a pesar de los avances de los ltimos aos en las tcnicas y mtodos de resolucin, todava quedan por resolver algunas Laboratorio de Operaciones Unitarias Pgina 5
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
cuestiones relativas a la consistencia y fiabilidad de los mtodos y algoritmos existentes, la fiabilidad de la prediccin del equilibrio entre fases, la existencia de multiplicidad y la determinacin de qu es exactamente una verdadera frontera de destilacin.
Fundamento Terico Destilacin
Proceso que consiste en calentar un lquido hasta que sus componentes ms voltiles pasan a la fase de vapor y, a continuacin, enfriar el vapor para recuperar dichos componentes en forma lquida por medio de la condensacin. El objetivo principal de la destilacin es separar una mezcla de varios componentes aprovechando sus distintas volatilidades, o bien separar los materiales voltiles de los no voltiles. En la evaporacin y en el secado, normalmente el objetivo es obtener el componente menos voltil; el componente ms voltil, casi siempre agua, se desecha. Sin embargo, la finalidad principal de la destilacin es obtener el componente ms voltil en forma pura. Por ejemplo, la eliminacin del agua de la glicerina evaporando el agua, se llama evaporacin, pero la eliminacin del agua del alcohol evaporando el alcohol se llama destilacin, aunque se usan mecanismos similares en ambos casos. Si los puntos de ebullicin de los componentes de una mezcla slo difieren ligeramente, no se puede conseguir la separacin total en una destilacin individual. Un ejemplo importante es la separacin de agua, que hierve a 100 C, y alcohol, que hierve a 78,5 C. Si se hierve una mezcla de estos dos lquidos, el vapor que sale es ms rico en alcohol y ms pobre en agua que el lquido del que procede, pero no es alcohol puro. Con el fin de concentrar una disolucin que contenga un 10% de alcohol (como la que puede obtenerse por fermentacin) para obtener una disolucin que contenga un 50% de alcohol (frecuente en el whisky), el destilado ha de destilarse una o dos veces ms, y si se desea alcohol industrial (95%) son necesarias varias destilaciones.
Fundamentos de destilacin. Tipos. Principales aplicaciones
Teora de la destilacin En la mezcla simple de dos lquidos solubles entre s, la volatilidad de cada uno es perturbada por la presencia del otro. En este caso, el punto de ebullicin de una mezcla al 50%, por ejemplo, estara a mitad de camino entre los puntos de ebullicin de las sustancias puras, y el grado de separacin producido por una destilacin individual dependera solamente de la presin de vapor, o volatilidad de los componentes separados a esa temperatura. Esta sencilla relacin fue anunciada por vez primera por el qumico francs Franois Marie Raoult (1830-1901) y se llama ley de Raoult. Esta ley slo se aplica a mezclas de lquidos muy similares en su estructura qumica, como el benceno y el tolueno. En la mayora de los casos se producen amplias desviaciones de esta ley. Si un componente slo es ligeramente soluble en el otro, su volatilidad aumenta anormalmente. En el ejemplo anterior, la volatilidad del alcohol en disolucin acuosa diluida es varias veces mayor que la predicha por la ley de Raoult. En disoluciones de alcohol muy concentradas, la desviacin es an mayor: la destilacin de alcohol de 99% produce un vapor de menos de 99% de alcohol. Por esta razn el Laboratorio de Operaciones Unitarias Pgina 6
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
alcohol no puede ser concentrado por destilacin ms de un 97%, aunque se realice un nmero infinito de destilaciones. Este proceso, conocido como rectificacin o destilacin fraccionada, se utiliza mucho en la industria, no slo para mezclas simples de dos componentes (como alcohol y agua en los productos de fermentacin, u oxgeno y nitrgeno en el aire lquido), sino tambin para mezclas ms complejas como las que se encuentran en el alquitrn de hulla y en el petrleo. La columna fraccionadora que se usa con ms frecuencia es la llamada torre de burbujeo, en la que las placas estn dispuestas horizontalmente, separadas unos centmetros, y los vapores ascendentes suben por unas cpsulas de burbujeo a cada placa, donde burbujean a travs del lquido. Las placas estn escalonadas de forma que el lquido fluye de izquierda a derecha en una placa, luego cae a la placa de abajo y all fluye de derecha a izquierda. La interaccin entre el lquido y el vapor puede ser incompleta debido a que puede producirse espuma y arrastre de forma que parte del lquido sea transportado por el vapor a la placa superior. En este caso, pueden ser necesarias cinco placas para hacer el trabajo de cuatro placas tericas, que realizan cuatro destilaciones. Un equivalente barato de la torre de burbujeo es la llamada columna apilada, en la que el lquido fluye hacia abajo sobre una pila de anillos de barro o trocitos de tuberas de vidrio. Destilacin por vapor Si dos lquidos insolubles se calientan, ninguno de los dos es afectado por la presencia del otro (mientras se les remueva para que el lquido ms ligero no forme una capa impenetrable sobre el ms pesado) y se evaporan en un grado determinado solamente por su propia volatilidad. Por lo tanto, dicha mezcla siempre hierve a una temperatura menor que la de cada componente por separado. El porcentaje de cada componente en el vapor slo depende de su presin de vapor a esa temperatura. Este principio puede aplicarse a sustancias que podran verse perjudicadas por el exceso de calor si fueran destiladas en la forma habitual. Destilacin al vaco Otro mtodo para destilar sustancias a temperaturas por debajo de su punto normal de ebullicin es evacuar parcialmente el alambique. Por ejemplo, la anilina puede ser destilada a 100 C extrayendo el 93% del aire del alambique. Este mtodo es tan efectivo como la destilacin por vapor, pero ms caro. Cuanto mayor es el grado de vaco, menor es la temperatura de destilacin. Si la destilacin se efecta en un vaco prcticamente perfecto, el proceso se llama destilacin molecular. Este proceso se usa normalmente en la industria para purificar vitaminas y otros productos inestables. Se coloca la sustancia en una placa dentro de un espacio evacuado y se calienta. El condensador es una placa fra, colocada tan cerca de la primera como sea posible. La mayora del material pasa por el espacio entre las dos placas, y por lo tanto se pierde muy poco. Destilacin molecular centrfuga Si una columna larga que contiene una mezcla de gases se cierra hermticamente y se coloca en posicin vertical, se produce una separacin parcial de los gases como resultado de la gravedad. En una centrifugadora de alta velocidad, o en un instrumento llamado vrtice, las fuerzas que Laboratorio de Operaciones Unitarias Pgina 7
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
separan los componentes ms ligeros de los ms pesados son miles de veces mayores que las de la gravedad, haciendo la separacin ms eficaz. Por ejemplo, la separacin del hexafluoruro de uranio gaseoso, UF6, en molculas que contienen dos istopos diferentes del uranio, uranio 235 y uranio 238, puede ser llevada a cabo por medio de la destilacin molecular centrfuga. Sublimacin Si se destila una sustancia slida, pasndola directamente a la fase de vapor y otra vez a la fase slida sin que se forme un lquido en ningn momento, el proceso se llama sublimacin. La sublimacin no difiere de la destilacin en ningn aspecto importante, excepto en el cuidado especial que se requiere para impedir que el slido obstruya el aparato. La rectificacin de dichos materiales es imposible. El yodo se purifica por sublimacin. Destilacin destructiva Cuando se calienta una sustancia a una temperatura elevada, descomponindose en varios productos valiosos, y esos productos se separan por fraccionamiento en la misma operacin, el proceso se llama destilacin destructiva. Las aplicaciones ms importantes de este proceso son la destilacin destructiva del carbn para el coque, el alquitrn, el gas y el amonaco, y la destilacin destructiva de la madera para el carbn de lea, el cido etanoico, la propanona y el metanol. Este ltimo proceso ha sido ampliamente desplazado por procedimientos sintticos para fabricar distintos subproductos. El craqueo del petrleo es similar a la destilacin destructiva.
Relacin de equilibrio termodinmico Liquido Vapor
Los procesos de transferencia de energa y masa en una columna real de destilacin son demasiado complicados para poder modelarlos con facilidad en forma directa. Esta dificultad se supera mediante el modelo de etapa de equilibrio. Por definicin, la corriente de vapor y la del lquido que salen de una etapa de equilibrio estn en equilibrio completo entre si y se pueden utilizar relaciones termodinmicas para relacionar las concentraciones de las dos corrientes en equilibrio. Se disea una columna hipottica que se compone de etapas de equilibrio (en lugar de verdaderos platos de contacto) para realizar las separaciones especificas para la columna real. A continuacin, el nmero de etapas hipotticas de equilibrio se debe convertir en un nmero dado de platos reales, por medio de eficiencias de plato que describe el punto hasta el cual el rendimiento de una bandeja real de contacto corresponde al rendimiento de una etapa de equilibrio. El empleo de concepto de etapa de equilibrio separa el diseo de columna de destilacin en tres partes principales: Los datos y los mtodos termodinmicos que se requieren para predecir las composiciones de equilibrio de fases se tienen que determinar cuidadosamente. Se debe calcular el nmero de etapas de equilibrio que se requieren para logar una separacin especfica o la separacin que se obtendr con un nmero dado de etapas de equilibrio El nmero de etapas de equilibrio se debe convertir en un nmero de equivalente de platos reales de contacto, o determinar la altura de empaquetamiento y el dimetro.
Laboratorio de Operaciones Unitarias
Pgina 8
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Para una mezcla binaria, la temperatura y presin determinan las composiciones del lquido y de vapor en el equilibrio. Por consiguiente los datos experimentales se presentan con frecuencia en forma de tablas de la fraccin mol de vapor y la fraccin mol del lquido x, para un constituyente, en un intervalo de temperatura T, para una presin fija P en un intervalo de presin, para una temperatura fija.
Coeficiente local y global en la transferencia de masa
La transferencia de materia entre fases es importante en la mayor parte de los procesos en los que estn incluidos gases y lquidos. Cuando un lquido se evapora y se convierte en gas, solo es necesario calcular la transferencia de masa en la fase gaseosa, es decir, la transferencia de masa en la fase de lquido puro no est incluida. Por el contario cuando un gas puro se absorbe en un liquido, solo es necesario considerar la transferencia de masa en la fases liquida. En ocasiones la transferencia de masa en una de las dos fases puede despreciarse, incluso cuando los componentes puros no estn involucrados. Este sera el caso en que la resistencia a la transferencia de masa es bastante ms elevada en una fase que en la otra. Cuando se transfiere material de una fase a otra, a travs de la interfase que las separa, la resistencia a la transferencia de masa de una fase a la otra causa un gradiente de concentraciones como en la figura.
Las concentraciones del material se difunden en las dos fases inmediatamente adyacentes a la interfase son por lo general desiguales, incluso si se expresan en las misma unidades, pero tambin se supone por lo general que estn relacionadas entre s por las leyes del equilibrio termodinmico, por consiguiente se supone que se alcanza el equilibrio termodinmico en al interfase gas liquido casi inmediatamente que entra en contacto el gas y el liquido.
Laboratorio de Operaciones Unitarias
Pgina 9
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Para los sistemas en que las concentraciones en las fases liquidas y gaseosa son diluidas, la velocidad de transferencia se puede expresar por medio de ecuaciones en las que la velocidad de transferencia de masa es proporcional a la diferencia entre la concentracin masiva y a la concentracin en la interfase gas-lquido. Por consiguiente:
Donde:
en el lquido de la interfase Por definicin, los coeficientes de transferencia de masa y son iguales a las razones de los flujos molales de masa respecto a las fuerzas impulsadoras de las concentraciones respectivamente. Una expresin opcional para la velocidad de transferencia en los sistemas diluidos esta dado por: ..ecuacin (2) Donde: =m velocidad de transferencia de masa
Los coeficientes de transferencia de masa, definidos por las ecuaciones se relacionan como sigue:
= Donde: = presin total del sistema utilizada durante las determinaciones experimentales de los valores de . =densidad molar promedio de la fase liquida. El coeficiente es relativamente independiente de la presin total del sistema y en consecuencia es ms conveniente utilizarlo en comparacin con que es inversamente proporcional ala presin total del sistema.
Mezcla Azeotrpica. Criterios de separacin
Un azetropo es una mezcla liquida que tiene un mximo o un mnimo en los puntos de ebullicin, con relacin a los puntos de ebullicin de las composiciones de las mezclas a su
Laboratorio de Operaciones Unitarias
Pgina 10
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
alrededor.los puntos de ebullicin de los componentes puros presentes en la mezcla deben ser lo sufrientemente cercanos para permitir la formacin de un azetropo. Una mezcla cuyos componentes tienen puntos de ebullicin cercanos puede formar un azetropo cuando ocurren pequeas desviaciones de unas soluciones liquidas ideales. Una mezcla con puntos de ebullicin distantes de sus componentes puede no formar un azetropo, aun cuando constituya una mezcla liquida, con caractersticas considerablemente no ideales. Los azetropo se presentas raras veces en alas mezclas constituidas por componentes cuyo puntos de ebullicin difieren en ms de 30 (54 ).
Un azetropo es homogneo solo si est presente una fase liquida. El punto de ebullicin mximo de un azetropo homogneo puede presentarse, si las desviaciones de la ley de Raoult, dadas por la ecuacin:
=
Son negativas ( <1.0). Para que un azetropo presente un punto de ebullicin mnimo es necesario que las desviaciones de la ley Raoult sean positivas ( >1.0). Si las desviaciones positivas son lo suficientemente grandes <<1.0) Puede ocurrir la separacin de las fases y se formara un azetropo heterogneo, con un punto de ebullicin mnimo y con una fase vapor en equilibrio con las fases liquidas. Los tres tipos de azetropo son importantes. La comprensin de la ocurrencia de azetropo es importante por dos motivos. En primer lugar los azetropo no se pueden separa por destilacin simple, en un intervalo particular de presin. Sin embargo en segundo trmino, los azetropo se pueden utilizar para separar mezclas que por general, no se separan por destilacin simple, o bien, para incrementar el rendimiento de recuperacin de algunos componentes presentes en ciertas mezclas.
Criterios y relaciones bsicas para una Destilacin Batch
La destilacin por lotes, que es el proceso de separacin de una cantidad especfica (la carga) de una mezcla liquida en productos, se utiliza ampliamente en el laboratorio, y en las unidades pequeas de productos, donde la misma cantidad puede tener que servir para muchas mezclas. Cuando existen N componentes en el material de alimentacin, ser suficiente una columna por lotes, donde se requerirn N-1 columnas de destilacin. Muchas instalaciones grandes tienen un alambique por lotes. El material que se tiene que separar puede tener un contenido elevado de slidos, o bien, alquitranes o resinas que ensucien o atasquen una unidad continua. El uso de una unidad por lotes puede mantener separados los slidos y permitir el retiro conveniente al terminarse el proceso. Destilacin por lotes simples: La forma ms simple de alambique consiste en un recipiente calentando (olla o caldera), un condensador y uno a mas tanques acumuladores. No se proporcionan platos o empaque. La alimentacin se introduce al recipiente y se llevan los lquidos hasta ebullicin. Ningn flujo es regresado. La relacin de vaporizacin es a veces, controlada para evitar los choques de la carga y evitar que se sobrecargue en el condensador, pero los dems controles son mnimos. Laboratorio de Operaciones Unitarias Pgina 11
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Destilacin por lotes con rectificacin: Para obtener productos con un rango estrecho de composiciones, se usa un alambique rectificador. Los componentes de esta unidad son la olla, una columna de rectificacin, un condensador, un medio para dividir la porcin de vapor condensado (destilado) como reflujo y uno ms acumuladores. La temperatura del destilado se controla para hacer regresar el reflujo cerca de la temperatura de la columna, con el fin de permitir la indicacin verdadera de la cantidad de reflujo y mejorar el funcionamiento de la columna. A continuacin se emplea un intercambiador de calor hasta subenfriamiento para el resto del destilado que es enviado a un acumulador o recipiente. La columna puede funcionar tambin a presin o al vacio, en cuyo caso se debern incluir los dispositivos adecuados para obtener presiones deseadas. Se debe verificar el diseo de cada mezcla, cuando se vayan a procesar varias de ellas. Tambin se deben verificar en ms de un punto de la mezcla, puesto que la composicin cambia en la columna conforme avanza la destilacin. El diseo de la olla se basa en el tamao del lote y la relacin necesaria de vaporizacin. En funcionamiento, se introduce al rehervidor una carga del lquido y se lleva primeramente el sistema al estado estacionario con un reflujo total. A continuacin se retira en forma sucesiva una porcin del producto superior, de conformidad con la norma de reflujo establecido. Se pueden modificar las condiciones operacionales. Toda la columna funciona como seccin de enriquecimiento. A medida que transcurre el tiempo, la composicin del material que se destila se va haciendo cada vez menos rica en el componente ms voltil y se detiene la destilacin de un corte cuando el destilado combinado alcanza la composicin promedio que se desea. El proceso de la destilacin por lotes se puede controlar de varios modos distintos: El reflujo constante, composicin en el domo variable: el reflujo se ajusta en un valor predeterminado, donde se mantiene la operacin. Puesto que la composicin liquida de la olla cambia, la composicin instantnea del destilado tambin cambia. Reflujo variable, composicin constante en el domo: si se desea mantener la composicin constante en el domo tratndose de una mezcla binaria, la cantidad de reflujo que vuelve a la columna debe ir aumentado constantemente, durante toda la operacin, conforme trascurre el tiempo, el rehervidor se vaca en forma del componente, ms ligero. Finalmente se llega a un punto en que la relacin de reflujo alcanza un valor muy alto. Entonces se cambian los cumuladores, se reduce el reflujo y se toma un corte intermedio, como antes. esta tcnica tambin puede hacerse extensiva a mezclas multicomponentes. Otros mtodos de control. Con frecuencia se usan procedimientos de ciclaje para establecer el patrn de funcionamiento de la columna. La unidad funciona a reflujo hasta que se estable el equilibrio. Entonces se toma el destilado como producto total durante un espacio breve, y despus de ello, se hace regresar a la columna al reflujo total. Este ciclo se repite durante la destilacin. Otra posibilidad es optimizar la relacin de reflujo para lograr la separacin deseada en un tiempo mnimo. Las operaciones complejas pueden involucrar la extraccin de corriente laterales, la provisin para los intercondensadores, la adicin de alimentaciones a los platos y la adicin de una carga peridica a la olla.
Laboratorio de Operaciones Unitarias
Pgina 12
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Seccin Experimental Equipo y Materiales Empleados
El equipo a emplear consta de: 1. 2. 3. 4. 5. 6. 7. 8. 9. Una columna de destilacin Batch, equipada con instrumentos y accesorios. Fuente de agua fra. Recipiente calibrado, o una probeta, para medir caudal. Cronometro. Un (01) termmetros. Dos (02) Multitester. Muestra a destilar nueve (09) litros de Chicha de jora previamente fermentada. Un alcoholmetro. Recipientes de plstico, varios.
Metodologa Experimental
Siguiendo con los siguientes pasos: 1. Estudie la ubicacin de las vlvulas, y familiarizase con la operacin del equipo. 2. Carga la mezcla a destilar, en el baln (boiler, capacidad mxima 12 litros). 3. Encender la resistencia elctrica, y desde ese momento tomar el tiempo en que la mezcla llega a ebullicin, ver termmetro en el niple. Esta informacin es necesaria para determinar las perdidas calorficas en el hervidor, se conoce valor terico (potencia elctrica). 4. Registrar el tiempo en que el vapor demora en atravesar la columna empacada. 5. Esperar que el sistema alcance el equilibrio; esto ocurre cuando las temperaturas del fondo y en el tope son iguales, mantenindose constante. Para lograr esto, se debe operar a reflujototal (debe cerrar la vlvula del destilado y abrir la vlvula de reflujo). 6. Despus de alcanzar el equilibrio, se abre la vlvula para iniciar la operacin de destilado, anotando las temperaturas inciales del tope y del fondo. Inicialmente la temperatura del tope se mantendr constante, mientras la que del fondo se ir incrementando debido a que la concentracin alcohlica ir disminuyendo; se debe registrar los volmenes de destilado y temperatura respectiva (as mismo debe medirse la concentracin alcohlica). Con las vlvulas se puede ir regulando los flujos de destilado y de reflujo. 7. Determinar el flujo mximo que alcanza el sistema; para tal efecto debe cerrar totalmente la vlvula de reflujo y recolectar un cierto volumen de destilado en una unidad de tiempo requerido. 8. La operacin de destilacin, en el laboratorio, debe terminar cuando la temperatura del tope se incrementa y comienza a superar la temperatura de ebullicin del componente ms voltil; (p. ej.: la temperatura de ebullicin del etanol es 78 C, se puede detener la operacin cuando el sistema alcanza 80 C). 9. El equipo opera como un sistema abierto, por tanto debe determinar la presin. 10. Terminado el trabajo, tem 8, desconectar la resistencia elctrica y esperar un tiempo prudencial de enfriamiento para efectuar una limpieza del equipo.
Laboratorio de Operaciones Unitarias
Pgina 13
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Tabulacin de Datos Experimentales Recolectados Sobre la columna de destilacin
a) Tipo de material dimensiones: Material de la columna: Acero Longitud: 100cm Dimetro exterior: 21 cm Long columna rectificada = 148 cm b) Capacidad y accesorios Capacidad mxima 12 litros c) Caractersticas y potencia elctrica del hervidor Factor de potencia: 1500 W
Caractersticas de la mezcla binaria
a) Volmenes iniciales utilizados en cada componente Alcohol: 8.1 litros Agua: 0.9 litros b) Temperatura de ebullicin de cada componente Etanol: 78.2 Agua: 100 c) Composicin inicial, usando alcoholmetro Etanol: 10 GL
Mediciones del caudal y composicin de destilado
TABLA N1 - DATOS DE CAUDAL Y COMPOSICIN DE DESTILACIN MEZCLA ETANOL - AGUA Caudal (v/t) Caudal Caudal T Destilado Composicin (ml/s) (m3/s) (C) (GL) Volumen (ml) Tiempo (s) 260 353 42 92 0.7365 7.365 x 10-7 214 287 45 90 0.7456 7.456 x 10-7 75 98 46 85 0.7653 7.653 x 10-7
DATO 1 2 3
Tiempo que demora la mezcla en llegar a ebullicin
28 minutos con 5 segundos.
Tiempo en llegar el vapor a la parte superior de la columna
TABLA N2 - TIEMPO QUE DEMORA EL VAPOR EN ATRAVESAR LA COLUMNA H (cm) Tiempo 0 2805 10 3447 20 3526 30 3546 40 3610 50 3631 60 3651 70 3718 80 3736 90 3751 100 3805 Laboratorio de Operaciones Unitarias Pgina 14
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Flujo mximo
Dato 1 2 3 TABLA N3 - CAUDAL DE FLUJO MXIMO Volumen (ml) Tiempo (s) Caudal (ml/s) 70 75 0.9333 80 89 0.8989 90 107 0.8411 Caudal (m3/s) -7 9.333 x 10 8.989 x 10-7 8.411x 10-7
Caudal Mximo = 8.911 x 10-7 m3/s
Temperatura de refrigerante
Temperatura de Entrada: 24.5 C Temperatura de Salida: 50C Gasto de Agua: 10 GPH
Resultados Tabla de Propiedades Fsicas
TABLA N4 - PROPIEDADES FSICAS DE LA MEZCLA ETANOL AGUA
Etanol X(1) 0.0 0.1 0.2 0.3 0.4 0.5 0.6 0.7 0.8 0.9 1.0
Agua X(2) 1.0 0.9 0.8 0.7 0.6 0.5 0.4 0.3 0.2 0.1 0.0
T (K) 373.15 370.97 368.79 366.61 364.43 362.25 360.07 357.89 355.71 353.53 351.35
(Kg/m3) 958.380 941.442 924.504 907.566 890.628 873.690 856.752 839.814 822.876 805.938 789.000
Cp (KJ/KgK) 4.2190 4.0847 3.9504 3.8161 3.6818 3.5475 3.4132 3.2789 3.1446 3.0103 2.8760
x 103 (Kg/m .s) 0.2838 0.3554 0.4270 0.4987 0.5703 0.6419 0.7135 0.7851 0.8568 0.9284 1.0000
k (BTU/hr.ft.F) 0.3944 0.3732 0.3519 0.3307 0.3094 0.2882 0.2670 0.2457 0.2245 0.2032 0.1820
Laboratorio de Operaciones Unitarias
Pgina 15
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Equilibrio Lquido Vapor
TABLA N5 - VALORES DEL EQUILIBRIO LQUIDO - VAPOR
x1 0.0000 0.0190 0.0721 0.0966 0.1238 0.1661 0.2337 0.2608 0.3273 0.3965 0.5079 0.5198 0.5732 0.6763 0.7472 0.8943 0.9650 1.0000
x2 1.0000 0.9810 0.9279 0.9034 0.8762 0.8339 0.7663 0.7392 0.6727 0.6035 0.4921 0.4802 0.4268 0.3237 0.2528 0.1057 0.0350 0.0000
T (C) 100.00 95.50 89.00 86.70 85.30 84.10 82.70 82.30 81.50 80.70 79.80 79.70 79.30 78.74 78.41 78.35 78.25 78.20
T (K) 373.15 368.65 362.15 359.85 358.45 357.25 355.85 355.45 354.65 353.85 352.95 352.85 352.45 351.89 351.56 351.50 351.40 351.35
227.5087 194.2376 153.3701 140.7450 133.4929 127.5272 120.8499 118.9966 115.3612 111.8191 107.9433 107.5196 105.8390 103.5231 102.1784 101.9354 101.5316 101.3302
101.3332 86.1248 67.5461 61.8333 58.5583 55.8680 52.8609 52.0272 50.3927 48.8016 47.0622 46.8722 46.1186 45.0808 44.4784 44.3696 44.1888 44.0986
0.1974 0.2001 0.2042 0.2057 0.2067 0.2075 0.2084 0.2087 0.2093 0.2098 0.2104 0.2105 0.2108 0.2112 0.2114 0.2115 0.2115 0.2116
0.8105 0.8075 0.8032 0.8016 0.8006 0.7998 0.7988 0.7985 0.7979 0.7974 0.7967 0.7966 0.7964 0.7960 0.7957 0.7957 0.7956 0.7956
6.1215 5.2184 3.7037 3.2672 2.8937 2.4639 2.0068 1.8738 1.6243 1.4430 1.2512 1.2357 1.1754 1.0917 1.0531 1.0085 1.0009 1.0000
1.0000 1.0059 1.0119 1.0108 1.0073 0.9980 0.9764 0.9659 0.9372 0.9039 0.8458 0.8394 0.8102 0.7526 0.7127 0.6297 0.5905 0.5714
1.0669 1.0485 1.0277 1.0215 1.0178 1.0145 1.0107 1.0096 1.0074 1.0054 1.0032 1.0030 1.0022 1.0011 1.0005 1.0000 1.0001 1.0000
1.0000 0.9913 0.9824 0.9794 0.9780 0.9774 0.9766 0.9765 0.9764 0.9763 0.9768 0.9768 0.9771 0.9785 0.9798 0.9845 0.9872 0.0000
y1 0.0000 0.1812 0.3933 0.4292 0.4637 0.5077 0.5534 0.5685 0.6009 0.6280 0.6748 0.6796 0.7022 0.7535 0.7931 0.9002 0.9500 1.0000
y2 1.0000 0.8188 0.6067 0.5708 0.5363 0.4923 0.4466 0.4315 0.3991 0.3720 0.3252 0.3204 0.2978 0.2465 0.2069 0.0294 0.0500 0.9898
Laboratorio de Operaciones Unitarias
Pgina 16
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Temperaturas de Burbuja y Roco
TABLA N 6 - TEMPERATURA DE PUNTO DE BURBUJA Y ROCO PARA CADA COMPOSICIN
x1 0.0000 0.0190 0.0721 0.0966 0.1238 0.1661 0.2337 0.2608 0.3273 0.3965 0.5079 0.5198 0.5732 0.6763 0.7472 0.8943 0.9650 1.0000
x2 1.0000 0.9810 0.9279 0.9034 0.8762 0.8339 0.7663 0.7392 0.6727 0.6035 0.4921 0.4802 0.4268 0.3237 0.2528 0.1057 0.0350 0.0000
y1 0.0000 0.1812 0.3933 0.4292 0.4637 0.5077 0.5534 0.5685 0.6009 0.6280 0.6748 0.6796 0.7022 0.7535 0.7931 0.9002 0.9500 1.0000
y2 1.0000 0.8188 0.6067 0.5708 0.5363 0.4923 0.4466 0.4315 0.3991 0.3720 0.3252 0.3204 0.2978 0.2465 0.2069 0.0998 0.0500 0.0000 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 78.1987 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977 99.9977
T burbuja (C) 100.00 99.58 98.43 97.89 97.30 96.38 94.90 94.31 92.86 91.35 88.93 88.67 87.50 85.26 83.71 80.50 78.96 78.20
T burbuja (K) 373.15 372.73 371.58 371.04 370.45 369.53 368.05 367.46 366.01 364.50 362.08 361.82 360.65 358.41 356.86 353.65 352.11 351.35
T roco (C) 100.00 96.05 91.42 90.64 89.89 88.93 87.93 87.61 86.90 86.31 85.29 85.18 84.69 83.57 82.71 80.37 79.29 78.20
T roco (K) 373.15 369.20 364.57 363.79 363.04 362.08 361.08 360.76 360.05 359.46 358.44 358.33 357.84 356.72 355.86 353.52 352.44 351.35
Nmero de Etapas de Equilibrio
El nmero de etapas en equilibrio segn el mtodo grfico de McCabe Thiele en el grfico N 4 es de 5 etapas.
Reflujo Mnimo
El reflujo mnimo podemos hallarlo de la siguiente manera:
Adems:
Sabemos:
Laboratorio de Operaciones Unitarias
Pgina 17
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Reemplazando:
Reflujo Mximo
El reflujo mximo podemos hallarlo de la siguiente manera:
Adems:
Sabemos:
Reemplazando:
Balance de Materiales apartir de los datos de composicin inicial, final y composicin del destilado
Datos por consignar:
Composicin Inicial
Volumen de la solucin= 9 litros.
Laboratorio de Operaciones Unitarias
Pgina 18
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Moles de etanol:
Moles de agua:
Composicin Destilado
Moles totales: F= 465.65 moles.
Moles de etanol:
Moles Agua:
Moles totales: D= 11.59 moles.
Composicin Final
Mole de Etanol:
Moles de Agua:
Moles total:B= 454.06 moles
Laboratorio de Operaciones Unitarias
Pgina 19
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Composiciones en Volumen
Volumen Inicial: 9 Litros. Volumen Etanol: 10 GL= 9x 0.1 = 0.9 litros= 900 ml. Volumen Agua: 8.1 L=8100 ml Composicin: 10 GL.
Volumen Final=8.451 L
Anlisis y Discusin de Resultados
Los resultados de las propiedades de las mezclas, muchas veces no se cumple, ya que los datos deducidos son con aproximaciones estadsticas simples; pero se debe resaltar la importancia ya que sirve al menos como una referencia del comportamiento de las propiedades segn concentracin de sus componentes. El equilibrio liquido vapor realizado con la ecuacin Gamma Phi, tiene un margen bajo de error, adems que tiene la tendencia con los datos cientficos, coincidiendo hasta en el punto en el cual se comporta como una mezcla azeotrpica. El balance de materiales realizado a partir de los datos de entrada, salida y destilado pueden no ser muy confiables ya que un balance de materiales basado en el equilibrio liquido vapor presente tendra un valor ms real ya que estudia y deduce a partir de de las cosas que suceden experimentalmente.
Conclusiones
Se concluyo que con la destilacin discontinua puede ser muy eficiente si se controlan todos los parmetros de temperatura, refrigeracin, etc. Se comprob la existencia de estados de equilibrio lquido vapor en la cual ocurra la destilacin mantenindose constante la temperatura. Adems a partir de los clculos se vio la diferencia que tiene entre la relacin de reflujo mximo y mnimo, donde el reflujo mximo te da un destilado de alta concentracin de Laboratorio de Operaciones Unitarias Pgina 20
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
etanol y la parte baja o sobra tiene una baja concentracin de etanol; en contraste con el reflujo mnimo donde se logra el destilado pero la parte baja aun contiene etanol y por tanto llega a ser muchas veces ineficiente.
Recomendaciones
Se recomienda para la parte experimental, tener muy presente la temperatura en la parte superior de la columna de destilacin, ya que si se sobrepasa demasiado la destilacin sera con poco contenido del componente menos soluto y por ende una baja eficiencia de destilacin. Regular correctamente el flujo de agua ya que muchas veces no se toma atencin a los datos, que sirven para clculos superiores. En la parte terica, usar ecuaciones que no se basen en componentes ya sea gases o soluciones ideales, ya que los resultados con los experimentales o cientficos sern demasiado diferentes, muchas veces llevando a errores de interpretaciones de grficas, etc. Tener presente los mtodos iterativos para los clculos, ya que al usar ecuacin de componentes no ideales se vuelven complejas para el clculo analtico.
Referencias Bibliogrficas
J.M.Smith,H.C.Van Ness,M.M. Abbott.-INTRODUCCIN A LA TERMODINMICA EN INGENIERA QUMICA Stima Edicin McGraw Hill. Warren L.McCabe JulianC.Smith PeterHarriott.-OPERACIONES UNITARIAS EN INGENIERA QUMICA cuarta edicin Robert H. Perry, Don W. Green, James O. Maloney MANUAL DEL INGENIERO QUMICO Sexta Edicin Tomo IV
Laboratorio de Operaciones Unitarias
Pgina 21
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Apndice Ejemplo de Clculos Tabla de Propiedades de la Mezcla a partir de la Temperatura Promedio
A partir de la tabla 10, en las tablas de datos adicionales tenemos las propiedades de las especies puras, lo que se pide hallar es las propiedades a partir de las composiciones promedio y adems de la temperatura promedio: Para una composicin de etanol (x1) de 0.1 y agua (x2) de 0.9, obtenemos su temperatura promedio:
De igual manera la densidad:
Y as las dems propiedades y para las diferentes composiciones de la mezcla que se manifiestan en la tabla 1.
Hallando la composicin de etanol en el vapor a partir de la ecuacin -
A partir de la tabla N 7, 8 y 9 de los datos adicionales tenemos las constantes de la ecuacin de Antoine, constantes de la ecuacin de Wilson y datos del factor acntrico de especies puras y considerando la presin del sistema que es 101.325 KPa. Procedemos a hallar la temperatura de saturacin de cada componente de la mezcla de composicin x1=0.0721, X2=0.9279, y una temperatura del sistema 89 C, segn la tabla N 5: Hallando presin de saturacin de ambas especies:
Luego las valores de de cada especie por la ecuacin de Wilson, donde los valores de las constantes estn en la tabla 8:
Laboratorio de Operaciones Unitarias
Pgina 22
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Seguido y conocido todos los datos procedemos a hallar los
Anlogamente:
Por ltimo se procede a hallar los :
Siendo la temperatura reducida 0.6838 y 0.5767 para el etanol y el agua respectivamente, de las ecuaciones anteriores tenemos:
A partir de la tabla de factores acntricos:
Y de esta manera se halla:
Adems:
Reemplazando los datos hallados
Anlogamente se propone . Entonces se propone un mtodo iterativo donde los valores iniciales de ambos es 1 y hallamos los valores de y1 e y2, a partir de esta ecuacin, hasta que arroja los valores de la composicin del vapor y : Laboratorio de Operaciones Unitarias Pgina 23
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Y as se hallan los dems datos y los resultados se publican en la tabla N 5.
Temperatura de Roco y Burbuja
A partir dela tabla N 7, de los datos adicionales tenemos las constantes de la ecuacin de Antoine, donde a partir de la presin del sistema que es 101.325 KPahallamos la temperatura de saturacin de cada componente de la mezcla de composicin x1=0.0721, X2=0.9279, Y1=0.3933, Y2=0.6067, segn la tabla N 6:
Seguido hallamos la temperatura de burbuja y roco:
Las dems composicin estas estn en la tabla N 6 donde los dems datos se completan de manera anloga.
Deduccin de Ecuaciones Mtodo - :
Resuelvo: a) b) : Ecuacin de Antonie: : Ecuacin de Wilson:
Laboratorio de Operaciones Unitarias
Pgina 24
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Para:
Segn la ecuacin:
Para hallar
Donde:
Al combinar las ecuaciones (1.7), (1.8) y (1.9):
Para un sistema binario:
Para phi :
Laboratorio de Operaciones Unitarias
Pgina 25
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Correlacin Lee/Kesler:
Temperatura de Roco y Burbuja
A partir de la modificacin de la ecuacin de Antoine tenemos:
Reflujo Externo e Interno
En el punto de destilacin: Rmin: en el punto de destilacin se cumple xD=yD, la condicin inicial de la olla (xp,yp) a partir de estos datos podemos obtener:
Adems:
Balance de Materiales
Balance Total: Balance de Etanol:
Laboratorio de Operaciones Unitarias
Pgina 26
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Tambin se puede deducir la composicin promedio del destilado:
Tablas adicionales, grficos y figuras varias Tablas
TABLA N 7 - CONSTANTES DE LA ECUACIN DE ANTOINE
Etanol Agua
A 16.8958 16.3872
B 3795.17 3885.70
C 230.918 230.170
Tmin (C) 3 0
Tmax (C) 96 200
T (C) 78.2 100
TABLA N 8 - CONSTANTES DE LA ECUACIN DE WILSON
a12 -2.7362
a21 0.0898
b12 415.6457
b21 -111.9061
TABLA N 9 - FACTOR ACNTRICO DE LAS ESPECIES PURAS
FACTOR ACNTRICO w1 (etanol) 0.345 w2 (Agua) 0.645
TABLA N 10TABLA DE PROPIEDADES DE LAS ESPECIES PURAS
T (K) Agua Etanol 373.15 351.35
(Kg/m3) 958.38 789
Cp (KJ/KgK) 4.219 2.876
x 103 (Kg/m .s) 0.2838 1
k (BTU/hr.ft.F) 0.3944 0.182
Laboratorio de Operaciones Unitarias
Pgina 27
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Grficos T vs x, y
GRFICO N 01 T VS X,Y
Temperatura de Burbuja, Roco vs x, y
GRFICO N 02 T VS X,Y
Laboratorio de Operaciones Unitarias
Pgina 28
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Relacin de Equilibrio Lquido Vapor, con etapas de equilibrio
GRFICO N 03 Y VS X CURVA DE EQUILIBRIO LQUIDO - VAPOR
GRFICO N 04 Y VS X CURVA DE EQUILIBRIO LQUIDO VAPOR CON ETAPAS DE EQUILIBRIO
Laboratorio de Operaciones Unitarias
Pgina 29
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Relacin de Equilibrio Lquido Vapor, reflujo mximo
GRFICO N 05 Y VS X CURVA DE EQUILIBRIO LQUIDO VAPOR CON REFLUJO MXIMO
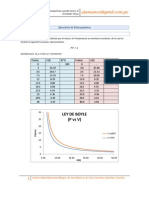
Cuestionario
1. Por qu difieren los valores de presin de vapor, y de la presin parcial? Simplemente porque no se encuentran en equilibrio la presin de vapor del liquido y la presin parcial del gas; para que estn en equilibrio este debe llegar a su punto de saturacin, y no necesariamente es as siempre. En conclusin se debera dejar un tiempo largo para que el liquido se encuentre en equilibrio con el gas (el gas adquirir molculas del liquido, y la vaporizacin seguir hasta que alcancen el equilibrio), en ese caso la presin de vapor del liquido se encontrara en equilibrio con la presin parcial y serian iguales. 2. Es predominante el efecto de asumir el criterio de idealidad de Raoult? Qu precisin se tendr cuando se usan otros modelos para determinar los clculos? Se usa primordialmente para un componente cuya fraccin molar se aproxima a la unidad o para disoluciones de componentes de naturaleza qumica muy similar, como los hidrocarburos de cadena recta.
Laboratorio de Operaciones Unitarias
Pgina 30
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
Ley de Henry. Se usa primordialmente para un componente cuya fraccin molar se acerca a cero, como cuando un gas diluido se disuelve en un lquido: a.- En muchos casos, la presin parcial en la fase gaseosa de un soluto diluido en un una mezcla en equilibrio se puede calcular usando la ley de Henry. b.- Tambin en muchos casos es posible calcular la presin parcial en la fase gaseosa de un disolvente o de compuestos de naturaleza qumica similar en equilibrio por medio de la ley de Raoult. c.- Las composiciones vapor-lquido se pueden determinar con la ayuda de un coeficiente de equilibrio (que en s puede ser una funcin de la temperatura, la presin y la composicin). Ley de Raoult para el componente ms voltil. 3. Explique qu fase, de una sustancia o mezcla, se presentara en el punto crtico. Se presentara una fase vapor, pero sin que se pueda notar el momento en que el lquido se vaporice, ya que no se formara una interfaz entre las fases, no se podr ver la superficie del lquido. Este punto crtico es en el estado donde las propiedades de la fase gas y el lquida son iguales, y se logra a temperaturas y presiones altas. 4. Cmo se explica los conceptos de Destilacin extractiva y Destilacin reactiva? Destilacin Reactiva: Es una tecnologa que integra la reaccin y la separacin en un mismo equipo. Esta integracin tiene diversas ventajas potenciales, como son: Reduccin en los costos, mejoras en la conversin de los reactivos y en la selectividad de los productos, as como ahorros en el uso de energa y reactivos entre otros.se aplica esta tecnologa al proceso para la produccindel acetato de metilo. El anlisis en destilacin reactiva es considerablemente ms compleja que en destilacin convencional y debido a las diferencias entre los diversos tipos de reaccin (exotrmicas, irreversibles, etc.) la generalizacin de reglas de diseo es difcil y cada sistema reactivo debe ser analizado de forma muy particular. Las principales lneas de investigacin de esta tecnologa son en el diseo, modelado, simulacin, control y anlisis de fenmenos no lineales como multiplicidad de estados y dinmica no lineal. Destilacin Extractiva: La destilacin extractiva es una tcnica utilizada para separar mezclas binarias azeotrpicas, en la que se adiciona un agente de separacin o solvente, cuya caracterstica principal es que no presenta la formacin de azetropos con ninguno de los componentes de la mezcla a separar. El solvente altera de manera conveniente las volatilidades relativas de los componentes de la mezcla, por tal razn debe tener baja volatilidad para asegurar su permanencia en la fase lquida, adems, para garantizar el contacto con la mezcla a lo largo de toda la columna debe tener un punto de ebullicin superior al de los componentes a separar y se debe adicionar en una de las etapas cercanas al condensador, por encima de la etapa de mezcla azeotrpica.
Laboratorio de Operaciones Unitarias
Pgina 31
Facultad de Ingeniera Qumica, Metalurgia y Ambiental
5. Cmo se explica la variacin del comportamiento de vapores condensables y no condensables? Mencione ejemplos ilustrativos. Gas Condensable: Gas que existe por debajo de su temperatura crtica porque puede condensarse. Si se comprime continuamente un gas puro a temperatura constante, siempre que la temperatura sea menor que la temperatura crtica, tarde o temprano se alcanzar una presin en la que el gas comenzar a condensarse y convertirse en lquido (o slido). Una compresin adicional no aumenta la presin pero si incrementa la fraccin del gas que se condensa. La reversin del procedimiento descrito har que el lquido pase otra vez al estado gaseoso (es decir, se vaporice). De aqu en adelante, reservaremos la palabra vapor para describir un gas por debajo de su punto crtico en un proceso en el que el cambio de fase tiene inters primordial, Gas no condensable: Gas que est por encima del punto crtico o un gas en un proceso en el que no se puede condensar.
Laboratorio de Operaciones Unitarias
Pgina 32
You might also like
- Propiedades de Los Materiales DentalesDocument43 pagesPropiedades de Los Materiales DentalesAle Herrera100% (3)
- Retorno de Condensado FUCKING TESIS MALADocument74 pagesRetorno de Condensado FUCKING TESIS MALAIsbel Cedillo100% (1)
- Determinación del pH y acidez del zumo de limónDocument13 pagesDeterminación del pH y acidez del zumo de limónKevin Yacila100% (2)
- INFORME Producción-de-Ácido-AcrílicoDocument153 pagesINFORME Producción-de-Ácido-AcrílicoAngie Ojeda Egoavil0% (1)
- Bioreactor Anaerobio de Lecho de LodosDocument50 pagesBioreactor Anaerobio de Lecho de LodosELIZABETHNo ratings yet
- Taller en Parejas Carlos García y Antonio ContrerasDocument9 pagesTaller en Parejas Carlos García y Antonio ContrerasCarlos García GarcíaNo ratings yet
- Proyecto de Planta de Produccion de FormaldehidoDocument120 pagesProyecto de Planta de Produccion de FormaldehidoJhonny RodriguezNo ratings yet
- FLOTACIONDocument64 pagesFLOTACIONjorgecatalinahuanca50% (2)
- Secador de BandejasDocument35 pagesSecador de BandejasEdgar Jamanca Antonio50% (2)
- Informe Final de SimuDocument56 pagesInforme Final de Simuirving_mendoza_58No ratings yet
- Tecnicas de Gestion Energetica en Sistemas de VaporDocument66 pagesTecnicas de Gestion Energetica en Sistemas de VaporDNI17909752No ratings yet
- Trabajo 5Document30 pagesTrabajo 5Castañeda UrupequeNo ratings yet
- HumidificacionDocument23 pagesHumidificacionEdgar Jamanca Antonio100% (6)
- Informe FinalDocument50 pagesInforme FinalABNERNo ratings yet
- Grupo N3. RtacDocument51 pagesGrupo N3. RtacAndrea MujicaNo ratings yet
- Informe Parcial #1Document103 pagesInforme Parcial #1irving_mendoza_58No ratings yet
- Informe Aislantes TermicosDocument30 pagesInforme Aislantes TermicosMariant Carolina SalasNo ratings yet
- Wiac - Info PDF Lab n6 Intercambiadores de Calor PDF PRDocument46 pagesWiac - Info PDF Lab n6 Intercambiadores de Calor PDF PRYEFERSON RAMIREZ OSCCONo ratings yet
- Terrazas y Cosecha de AguaDocument31 pagesTerrazas y Cosecha de AguaJose GamboaNo ratings yet
- 2do Labo de Fluidos 18-2Document26 pages2do Labo de Fluidos 18-2Junior AlvarezNo ratings yet
- Másteres de La Uam 2017 - 2018: Hidrogenación de Benceno: Análisis de Alternativas e Incorporación de Líquidos IónicosDocument50 pagesMásteres de La Uam 2017 - 2018: Hidrogenación de Benceno: Análisis de Alternativas e Incorporación de Líquidos IónicosValentina MenesesNo ratings yet
- Destilación batch con rectificación para la separación de etanol y aguaDocument19 pagesDestilación batch con rectificación para la separación de etanol y aguaChris QCNo ratings yet
- Acetona 3º AvanceDocument22 pagesAcetona 3º AvanceArturo LandeoNo ratings yet
- Grupo A-Pérdidas Por FricciónDocument45 pagesGrupo A-Pérdidas Por FricciónCriz Espinoza ChavezNo ratings yet
- La Cuenca y Los Procesos HidrologicosDocument62 pagesLa Cuenca y Los Procesos HidrologicosAlejandra SalasNo ratings yet
- La Cuenca y Los Procesos HidrologicosDocument62 pagesLa Cuenca y Los Procesos HidrologicosFredy G.A.No ratings yet
- Labo N2 ProcesosDocument22 pagesLabo N2 ProcesosNielsNo ratings yet
- Diseño de Una Planta para La Producción de Etileno A Partir Del Acoplamiento Oxidativo Del Metano Proveniente Del Gas Natural PDFDocument94 pagesDiseño de Una Planta para La Producción de Etileno A Partir Del Acoplamiento Oxidativo Del Metano Proveniente Del Gas Natural PDFAriel Flores OrtuñoNo ratings yet
- Validacion de Dqo en Agua Residual Documento GuiaDocument79 pagesValidacion de Dqo en Agua Residual Documento GuiaKarmen PerezNo ratings yet
- Diseño de Un Sistema de Floculacion de Paletas Giratorias para Un Aplanta de Potabilizacion de AguaDocument170 pagesDiseño de Un Sistema de Floculacion de Paletas Giratorias para Un Aplanta de Potabilizacion de AguadjmegarelaNo ratings yet
- Informe 4 LOUDocument12 pagesInforme 4 LOUOmar Torres100% (1)
- Informe Resalto HidraulicoDocument33 pagesInforme Resalto HidraulicoYocastaHerbasTejerinaNo ratings yet
- Investigación TAC GAPV Marzo 10Document34 pagesInvestigación TAC GAPV Marzo 10l18200934No ratings yet
- Catalá - Diseño de Un Reactor de Hidroformilación, Con Recuperación de Catalizador, para La Produ...Document62 pagesCatalá - Diseño de Un Reactor de Hidroformilación, Con Recuperación de Catalizador, para La Produ...yhon manuelNo ratings yet
- Informe N°5 DestilacionDocument19 pagesInforme N°5 DestilacionReynaldo HuachacaNo ratings yet
- Lab D BalanceDocument41 pagesLab D BalanceHans AnthonyNo ratings yet
- Proyecto EbulliciónDocument8 pagesProyecto EbulliciónNati MolinaNo ratings yet
- Diseño de Una Planta de Vapor para Una Finca en ConstruccionDocument22 pagesDiseño de Una Planta de Vapor para Una Finca en ConstruccionIgorLayaNo ratings yet
- ArbelaezValentina 2022 ManualCanalesEscalonadosDocument40 pagesArbelaezValentina 2022 ManualCanalesEscalonadosMiguel Angel Cueva InzaNo ratings yet
- Equilibrio Líquido-Vapor en Sistemas Binarios de Interés IndustrialDocument43 pagesEquilibrio Líquido-Vapor en Sistemas Binarios de Interés IndustrialCristóbal Haro GalarzaNo ratings yet
- Habela Sanz Federico TFMDocument54 pagesHabela Sanz Federico TFMFelipe Leyva HaroNo ratings yet
- Informe D-1.6 DestiladoDocument25 pagesInforme D-1.6 DestiladoPiero HerreraNo ratings yet
- Informe Evaporacion LOU IDocument18 pagesInforme Evaporacion LOU Iquiksilver21No ratings yet
- CATALOGO E Arevalo 2022Document189 pagesCATALOGO E Arevalo 2022Evelyn ValenciaNo ratings yet
- Planta de Producción Del Dimetil Éter A Partir de Metanol 1Document27 pagesPlanta de Producción Del Dimetil Éter A Partir de Metanol 1Sergio Carhuas CordovaNo ratings yet
- Instrumentos de control en planta de producción de dimetil éter a partir de metanolDocument27 pagesInstrumentos de control en planta de producción de dimetil éter a partir de metanolsaraNo ratings yet
- Parte+B+ +Estudio+de+Calidad+Del+AguaDocument42 pagesParte+B+ +Estudio+de+Calidad+Del+AguaPaul Reategui RamosNo ratings yet
- Investigaciòn DestilaciònDocument33 pagesInvestigaciòn DestilaciònJORGE IGNACIO CHAVEZ RODRIGUEZNo ratings yet
- Intercambiador Clase R - AmdlDocument15 pagesIntercambiador Clase R - AmdlJOSE RAFAEL CAÑAS ROJASNo ratings yet
- GonzalezJSleinmE - Informe 3 - Curva de DescargaDocument58 pagesGonzalezJSleinmE - Informe 3 - Curva de DescargaingridamorNo ratings yet
- Fenomeno Aletas 2Document27 pagesFenomeno Aletas 2Harol Joseth Robles MendozaNo ratings yet
- Caldero MonograficoDocument29 pagesCaldero MonograficoRubi Angela Cabezudo MontoyaNo ratings yet
- Informe Parcial #2Document251 pagesInforme Parcial #2irving_mendoza_58No ratings yet
- Hortensia SDocument101 pagesHortensia SbuffysangoNo ratings yet
- Cuenco de Disipacion Pag. 34Document125 pagesCuenco de Disipacion Pag. 34Erick Fernando Zumárraga PotosíNo ratings yet
- 9-6A-Ensayo, Extracción Líquido-Líquido.Document12 pages9-6A-Ensayo, Extracción Líquido-Líquido.Paola QuinteroNo ratings yet
- Análisis Conceptual Constructivo y Experimental de Un Electrolizador Con Diferentes ElectrodosDocument65 pagesAnálisis Conceptual Constructivo y Experimental de Un Electrolizador Con Diferentes ElectrodosHarlan SimonettiNo ratings yet
- Alcalinidad - Acidez - Dureza - Calcio VF PDFDocument21 pagesAlcalinidad - Acidez - Dureza - Calcio VF PDFCesar RamirezNo ratings yet
- Monografía 2-Transferencia de Gases y Purificación de Las Fuentes SuperficialesDocument9 pagesMonografía 2-Transferencia de Gases y Purificación de Las Fuentes SuperficialesJALINEE ROSARIO BLAS GARCIANo ratings yet
- Tareea Termodinamia Quimica DosDocument40 pagesTareea Termodinamia Quimica DosElyReyesNo ratings yet
- Tratamiento Biológico Aerobio de Agua Residuales Municipales en La Quebrada La Sardina en El Sector Del Puente Torcido Florencia-CaquetáDocument19 pagesTratamiento Biológico Aerobio de Agua Residuales Municipales en La Quebrada La Sardina en El Sector Del Puente Torcido Florencia-CaquetáRiver AquilesNo ratings yet
- Equipo 8. Anilina - EntregaDocument37 pagesEquipo 8. Anilina - EntregaSaul ErnestoNo ratings yet
- Transferencia de calor en evaporadorDocument43 pagesTransferencia de calor en evaporadorYessenia Camacho MejiaNo ratings yet
- 1 Evapotranspiracion PDFDocument39 pages1 Evapotranspiracion PDFYOEL BANGNo ratings yet
- Trabajo de HysysDocument16 pagesTrabajo de HysysEdgar Jamanca Antonio100% (1)
- Curso de LlenadoDocument6 pagesCurso de LlenadoEdgar Jamanca AntonioNo ratings yet
- Modelos de Primer OrdenDocument34 pagesModelos de Primer OrdenEdgar Jamanca AntonioNo ratings yet
- Curva XY HysysDocument8 pagesCurva XY HysysEdgar Jamanca AntonioNo ratings yet
- Modelado y Simulacion de Un TanqueDocument10 pagesModelado y Simulacion de Un TanqueEdgar Jamanca AntonioNo ratings yet
- Simulacion Del SyngasDocument41 pagesSimulacion Del SyngasEdgar Jamanca Antonio100% (1)
- Evaporador Triple Efecto - NetbeansDocument15 pagesEvaporador Triple Efecto - NetbeansEdgar Jamanca AntonioNo ratings yet
- Calculo de Numero de Platos - DestilacionDocument5 pagesCalculo de Numero de Platos - DestilacionEdgar Jamanca AntonioNo ratings yet
- Diseño de AtmosferasDocument10 pagesDiseño de AtmosferasEdgar Jamanca AntonioNo ratings yet
- Regresion Lineal y MultipleDocument15 pagesRegresion Lineal y MultipleEdgar Jamanca AntonioNo ratings yet
- Ejercicios de FisicoquímicaDocument5 pagesEjercicios de FisicoquímicaEdgar Jamanca AntonioNo ratings yet
- Cuba de ReynoldsDocument29 pagesCuba de ReynoldsEdgar Jamanca Antonio80% (5)
- Tiempo de EscurrimientoDocument35 pagesTiempo de EscurrimientoEdgar Jamanca AntonioNo ratings yet
- PINCH & HENDocument9 pagesPINCH & HENEdgar Jamanca AntonioNo ratings yet
- Optimización de Una Columna de DestilaciónDocument15 pagesOptimización de Una Columna de DestilaciónEdgar Jamanca AntonioNo ratings yet
- Factores de FriccionDocument19 pagesFactores de FriccionEdgar Jamanca Antonio0% (1)
- Tutorial Estructura de DatosDocument8 pagesTutorial Estructura de DatosEdgar Jamanca AntonioNo ratings yet
- Informe Final de Analisis y SintesisDocument55 pagesInforme Final de Analisis y SintesisEdgar Jamanca AntonioNo ratings yet
- Trabajo Final de IonDocument71 pagesTrabajo Final de IonEdgar Jamanca AntonioNo ratings yet
- Sistema Turbo Gene Rad or de EnergiaDocument14 pagesSistema Turbo Gene Rad or de EnergiaEdgar Jamanca AntonioNo ratings yet
- N IDA: D Nacional deDocument14 pagesN IDA: D Nacional deMarvin Rafael Huayaney ZaragozaNo ratings yet
- Practica 3 Q.o.2Document19 pagesPractica 3 Q.o.2Alex RomaNo ratings yet
- Resolucion de Quiz 2Document7 pagesResolucion de Quiz 2Carlos PerniaNo ratings yet
- Norma Covenin 928 Año 2019Document67 pagesNorma Covenin 928 Año 2019yency pirelaNo ratings yet
- SESION-2-Transferencia de Calor Unidimensional en Régimen EstacionarioDocument31 pagesSESION-2-Transferencia de Calor Unidimensional en Régimen EstacionarioTANIA YESENIA OREJON MONTALVONo ratings yet
- Factores Que Afectan La Durabilidad Del ConcretoDocument14 pagesFactores Que Afectan La Durabilidad Del ConcretoArturo lopez abucharNo ratings yet
- Recipiente con orificioDocument1 pageRecipiente con orificioCarolina AarhuataNo ratings yet
- Historia de La CristalografiaDocument4 pagesHistoria de La CristalografiaAlejandro Gianfranco Pucllas LimacheNo ratings yet
- Tcal Lab05Document14 pagesTcal Lab05Sebastian MorenoNo ratings yet
- 6907 Numeros Cuanticos y Configuracion Electronica-1589770430Document11 pages6907 Numeros Cuanticos y Configuracion Electronica-1589770430G̶r̶a̶f̶o̶v̶ J̶.̶ Z̶a̶c̶a̶r̶i̶e̶s̶No ratings yet
- Termometro de Gas PDFDocument2 pagesTermometro de Gas PDFEmma GomezNo ratings yet
- DiscusiónnnDocument2 pagesDiscusiónnnJaqueline CruzNo ratings yet
- Contenido de QuímicaDocument1 pageContenido de QuímicaKathleen CastroNo ratings yet
- Tarea de CienciasDocument2 pagesTarea de CienciasE.s. MellaNo ratings yet
- Teoria Del FuegoDocument39 pagesTeoria Del FuegoJhon Andres MoralesNo ratings yet
- Physics Vibrations and Waves - 231120 - 112915Document72 pagesPhysics Vibrations and Waves - 231120 - 112915Isabella mcvNo ratings yet
- g1 - g8. Preguntas Byf-Tf IDocument16 pagesg1 - g8. Preguntas Byf-Tf IElizabethNo ratings yet
- Química Semana 5 PDocument6 pagesQuímica Semana 5 PPaola BuenoNo ratings yet
- Enlace Ionico Vs CovalenteDocument10 pagesEnlace Ionico Vs CovalenteIvonne BustamanteNo ratings yet
- CARATULADocument14 pagesCARATULAbetsiNo ratings yet
- Mapa conceptual del acondicionamiento de gasDocument2 pagesMapa conceptual del acondicionamiento de gasJafet OceguedaNo ratings yet
- SILABO Quimica General 2019-IDocument14 pagesSILABO Quimica General 2019-IBryan C AlvanNo ratings yet
- Entre GaDocument13 pagesEntre GaLuhelo HLNo ratings yet
- Práctica No. 6. Informe Preparación de Disoluciones y DilucionesDocument18 pagesPráctica No. 6. Informe Preparación de Disoluciones y Dilucionesjulian alfonsoNo ratings yet
- PDF Ejercicios Balance de Materia Ingenieria - CompressDocument52 pagesPDF Ejercicios Balance de Materia Ingenieria - CompressJuan M.L.No ratings yet
- Formulacion InorganicaDocument25 pagesFormulacion InorganicaGemma PerezNo ratings yet