Professional Documents
Culture Documents
Aminoácidos: fórmula general, nomenclatura, clasificación y propiedades
Uploaded by
Maye Cayllahua Peña0 ratings0% found this document useful (0 votes)
48 views23 pagesOriginal Title
aminoácidos JMOL
Copyright
© © All Rights Reserved
Available Formats
PPTX, PDF, TXT or read online from Scribd
Share this document
Did you find this document useful?
Is this content inappropriate?
Report this DocumentCopyright:
© All Rights Reserved
Available Formats
Download as PPTX, PDF, TXT or read online from Scribd
0 ratings0% found this document useful (0 votes)
48 views23 pagesAminoácidos: fórmula general, nomenclatura, clasificación y propiedades
Uploaded by
Maye Cayllahua PeñaCopyright:
© All Rights Reserved
Available Formats
Download as PPTX, PDF, TXT or read online from Scribd
You are on page 1of 23
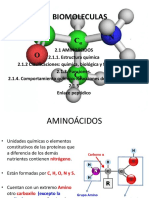
Frmula general
NH2: Grupo Amino
COOH: Grupo
Carboxilo
H: Hidrogeno
R: Cadena Lateral
(Cualquier compuesto,
marcando la diferencia
entre cada
aminocido)
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Nomenclatura
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Los aminocidos tienen dos sistemas de nomenclatura:
1. El clsico sistema de tres letras, que
permite la representacin de la estructura
primaria de una protena mediante el enlace
de cada triplete de letras mediante guiones,
disponiendo a la izquierda el aminocido N-
terminal y a la derecha el aminocido C-
terminal. Por ejemplo:
Ala-Glu-Gly-Phe- ... -Tyr-Asp-Gly
Representa la estructura primaria de una protena cuyo
aminocido N-terminal es alaninRepresenta la estructura
primaria de una protena cuyo aminocido N-terminal es
alanina (Ala) y cuyo aminocido C-terminal es glicina
(Gly).a (Ala) y cuyo aminocido C-terminal es glicina
(Gly).
2. El actual sistema de una sola letra,
impuesto en gentica molecular e
imprescindible para el uso de bases de
datos, que permite la representacin de la
estructura primaria de una protena mediante
la disposicin consecutiva de letras sin
espacios ni signos intermedios, disponiendo
a la izquierda el aminocido N-terminal y a
la derecha el aminocido C-terminal. Por
ejemplo:
LSIMAG ... AYSSITH
Representa la estructura primaria de una protena cuyo
aminocido N-terminal es leucina (L) y cuyo aminocido
C-terminal es histidina (H).
Codificacin
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Estereoisomeria
Un esteroisomero
es una sustancia
cuyas molculas
tienen el mismo
numero y tipos de
tomo y se
diferencian
nicamente en el
arreglo espacial.
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Esteroisomeria
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Carbono presenta 4 sustituyentes
diferentes.
Esteroisomeria
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
ENANTIOMEROS
Esteroisomeria
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
La Glicina es el nico
aminocido que no
presenta quiralidad, ya que
dos de los grupos unidos
al carbono son iguales (H).
Clasificacin de los aminocidos
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Existen muchas
formas de clasificar
los aminocidos; las
dos que se
presentan a
continuacin son las
ms comunes.
Segn las propiedades de su cadena
Segn su obtencin
Los aminocidos se clasifican habitualmente segn
las propiedades de su cadena lateral
A los aminocidos que deben ser captados como parte de
los alimentos se los llama esenciales; la carencia de estos
aminocidos en la dieta limita el desarrollo del organismo,
ya que no es posible reponer las clulas de los tejidos que
mueren o crear tejidos nuevos, en el caso del crecimiento.
Para el ser humano
Segn las propiedades de su cadena:
Grupos R apolares alifticos:
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Segn las propiedades de su cadena:
Grupos R CICLICOS
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Segn las propiedades de su cadena:
Grupos R AROMATICOS
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Segn las propiedades de su cadena:
Grupos R POLARES SIN CARGA
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Segn las propiedades de su cadena:
Grupos R CARGADOS POSITIVAMENTE
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Segn las propiedades de su cadena:
Grupos R CARGADOS NEGATIVAMENTE
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Variacin de la formula general de un aminocido.
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Un Zwitterion puede actuar como acido (donador de protones) o base
(aceptor de protones), los compuestos con esta propiedad se conocen como
anfolitos.
PH Acido PH Neutro PH Bsico
Punto Isoelctrico, curva de valoracin y pK
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
El pH caracterstico en el que la carga elctrica neta
es cero y se designa como pI.
pK: Es el pH en el cual las concentraciones del donador
de protones (cidos) y el aceptor de protones (bases)
son iguales.
Punto Isoelctrico, curva de valoracin y pK
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Grupos Ionizables
La cadena R de algunos
aminocidos contiene
grupos ionizables
Carboxlico
(COO-): Acido
glutaminico y
aspartico
Amino (NH3+):
Lisina, arginina e
histidina
Sulfidrilo (SH):
Cistena
Fenol (OH):
Tirosina
Punto Isoelctrico, curva de valoracin y pK
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Segn su obtencin
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
A los aminocidos que deben ser captados como parte de los alimentos se los llama
esenciales; la carencia de estos aminocidos en la dieta limita el desarrollo del
organismo, ya que no es posible reponer las clulas de los tejidos que mueren o crear
tejidos nuevos, en el caso del crecimiento.
Segn su obtencin: ESENCIALES
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Valina (Val, V)
Leucina (Leu, L)
Treonina (Thr, T)
Lisina (Lys, K)
Triptfano (Trp, W)
Histidina (His, H) *
Fenilalanina (Phe, F)
Isoleucina (Ile, I)
Arginina (Arg, R) *
Metionina (Met, M)
Segn su obtencin: NO ESENCIALES
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
Alanina (Ala, A)
Prolina (Pro, P)
Glicina (Gly, G)
Serina (Ser, S)
Cistena (Cys, C) **
Asparagina (Asn, N)
Glutamina (Gln, Q)
Tirosina (Tyr, Y) **
cido asprtico (Asp, D)
cido glutmico (Glu, E)
Aminocidos que pueden sintetizarse en
el propio organismo
Propiedades
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
cido-bsicas.
Se refiere al comportamiento de cualquier aminocido cuando se ioniza. Cualquier aminocido puede
comportarse como cido y como base, por lo que se denominan sustancias anfteras.
Cuando una molcula presenta carga neta cero est en su punto isoelctrico. Si un aminocido tiene un
punto isoelctrico de 6,1 su carga neta ser cero cuando el pH sea 6,1.
Los aminocidos y las protenas se comportan como sustancias tampn.
Propiedades
AMINOACIDOS
Q.F. Julio Miguel Oscanoa Lagunas Bioqumica
pticas.
Todos los aminocidos excepto la glicina tienen 4 sustityentes distintos sobre su carbono alfa
(carbono asimtrico o quiral), lo que les confiere actividad ptica; esto es, sus disoluciones desvan
el plano de polarizacin cuando un rayo de luz polarizada las atraviesa. Si el desvo del plano de
polarizacin es hacia la derecha (en sentido horario), el compuesto se denomina dextrgiro,
mientras que si se desva a la izquierda (sentido antihorario) se denomina levgiro. Un aminocido
puede en principio existir en sus dos formas enantiomricas (una dextrgira y otra levgira), pero en
la naturaleza lo habitual es encontrar slo una de ellas.
Estructuralmente, las dos posibles formas enantiomricas de cada aminocido se denominan
configuracin D o L dependiendo de la orientacin relativa en el espacio de los 4 grupos distintos
unidos al carbono alfa. Todos los aminoacidos proteicos son L-aminocidos, pero ello no significa
que sean levgiros.
Se consideran L-aminocidos los que estructuralmente derivan de L-gliceraldehdo y D-aminocidos
los derivados del D-gliceraldehdo.
You might also like
- Agua, Aminoácidos - Clase 1Document36 pagesAgua, Aminoácidos - Clase 1JEISSON DAVID CABOS SANCHEZNo ratings yet
- AMINOACIDOS PPT_031314Document26 pagesAMINOACIDOS PPT_031314Ania MagaluNo ratings yet
- Aminoacidos ProteinasDocument66 pagesAminoacidos ProteinasFany Lu HuancachoqueNo ratings yet
- Aa 2023Document38 pagesAa 2023Frans oNo ratings yet
- Aminoácidos: los ladrillos de las proteínasDocument37 pagesAminoácidos: los ladrillos de las proteínasfrank ganz bravoNo ratings yet
- Tarea 2 - Jennifer Karina PedrazaDocument13 pagesTarea 2 - Jennifer Karina PedrazayuliNo ratings yet
- ProteínasDocument50 pagesProteínasIsabella Agnello De GraziaNo ratings yet
- Tema 1 - Química de Las Biomóleculas - Aminoácidos y ProteinasDocument62 pagesTema 1 - Química de Las Biomóleculas - Aminoácidos y ProteinasAleydis PonceNo ratings yet
- Aminoacidos Bio PrevioDocument10 pagesAminoacidos Bio PrevioLeonardo ValdiviaNo ratings yet
- ProteinasDocument70 pagesProteinasPaola Azucena SalasNo ratings yet
- Clase 6 AMINOACIDOSDocument28 pagesClase 6 AMINOACIDOSKalin Kast GonzNo ratings yet
- Concepto de proteínas: Las moléculas orgánicas más abundantesDocument79 pagesConcepto de proteínas: Las moléculas orgánicas más abundantesTrai TraiNo ratings yet
- Cap13 - Aminoácidos y ProteinasDocument46 pagesCap13 - Aminoácidos y ProteinasJhordin Dario León AlvaradoNo ratings yet
- Semana 2 Aminoacidos y Espectrofotometría PDFDocument69 pagesSemana 2 Aminoacidos y Espectrofotometría PDFYassimNo ratings yet
- Acidos NucleicosDocument52 pagesAcidos NucleicosRocio VillegasNo ratings yet
- Unidad 4 - PresentaciónDocument129 pagesUnidad 4 - PresentaciónhorseriderspiritNo ratings yet
- Aminoácidos y ProteínasDocument98 pagesAminoácidos y ProteínasAndrea Trujillo CardosoNo ratings yet
- 2019 6B Eq3T ProteinasDocument45 pages2019 6B Eq3T ProteinasEdith QmNo ratings yet
- Aminoácidos y ProteínasDocument116 pagesAminoácidos y ProteínasCarolina QuinteroNo ratings yet
- Practica Nº8Document19 pagesPractica Nº8Anonymous VIfM9dFYdNo ratings yet
- SEMANA 14 - AMINOÁCIDOS Y PROTEINASDocument44 pagesSEMANA 14 - AMINOÁCIDOS Y PROTEINASシドloveNo ratings yet
- Aminoácidos y péptidos: formación y funcionesDocument24 pagesAminoácidos y péptidos: formación y funcionesGuille AlvarengaNo ratings yet
- Sesión 09 10 AminoácidosDocument105 pagesSesión 09 10 Aminoácidosfvb_123No ratings yet
- Protein AsDocument131 pagesProtein Asanon_998357053No ratings yet
- Bioquimica ProteinasDocument31 pagesBioquimica ProteinasAmy AyalaNo ratings yet
- Guia LabBq1 - Propiedades de Los Aminoacidos PDFDocument4 pagesGuia LabBq1 - Propiedades de Los Aminoacidos PDFJuan Diego CamachoNo ratings yet
- Informe-6-Propiedades Físicas y Químicas de Los AminoácidosDocument3 pagesInforme-6-Propiedades Físicas y Químicas de Los AminoácidosAndres CardonaNo ratings yet
- Bioquimica de Las Proteinas y Aminoacido BioqDocument44 pagesBioquimica de Las Proteinas y Aminoacido Bioqjessica benitez duarteNo ratings yet
- 07 ProteinasDocument6 pages07 Proteinasromina rodriguezNo ratings yet
- Aminoácidos: definición y clasificaciónDocument20 pagesAminoácidos: definición y clasificaciónRubi Estefany Silvera valleNo ratings yet
- Ácidos Carboxílicos: Propiedades y ReaccionesDocument11 pagesÁcidos Carboxílicos: Propiedades y ReaccionesJanett AranaNo ratings yet
- Tema NDocument42 pagesTema NPe DeepNo ratings yet
- Aminoácidos y Titulación Del Ácido GlutámicoDocument12 pagesAminoácidos y Titulación Del Ácido GlutámicoAmilcar Solares100% (1)
- Anestesicos LocalesDocument80 pagesAnestesicos LocalesALESSANDRA REYESNo ratings yet
- Reactividad de AA y proteínasDocument11 pagesReactividad de AA y proteínasKEVIN SANTIAGO VARGAS LEALNo ratings yet
- Tema 2. BioquímicaDocument2 pagesTema 2. BioquímicaPaola Martin ZalukaevaNo ratings yet
- Bloque 1 - Parte 1!Document20 pagesBloque 1 - Parte 1!sandra garciNo ratings yet
- Aminoacidos y ProteinasDocument46 pagesAminoacidos y ProteinasNelson Choque MamaniNo ratings yet
- MacromoléculasDocument31 pagesMacromoléculasPaula SoriaNo ratings yet
- Aminoacidos WienerDocument54 pagesAminoacidos WienerDiego Padilla SantosNo ratings yet
- Aminoácidos y ProteinasDocument18 pagesAminoácidos y ProteinasSandy Salazar100% (1)
- Biología I Guía 2 Verano 2022Document12 pagesBiología I Guía 2 Verano 2022Alex gugolNo ratings yet
- DiapoDocument23 pagesDiapoYazmin Valverde RodriguezNo ratings yet
- Aminoacidos Proteínas PDFDocument24 pagesAminoacidos Proteínas PDFjacquelineNo ratings yet
- Biología S04.s1 Aminoacidos y ProteinasDocument46 pagesBiología S04.s1 Aminoacidos y ProteinasTeteNo ratings yet
- Aa y ProteinasDocument56 pagesAa y ProteinasOscar Daniel Ramirez MercadoNo ratings yet
- 024.propiedades Fisicas y Acido-Basicas de Los AminoacidosDocument4 pages024.propiedades Fisicas y Acido-Basicas de Los AminoacidosNones namesNo ratings yet
- Tema 1 Aminoácidos Estructura y Clasificación..Document20 pagesTema 1 Aminoácidos Estructura y Clasificación..isaNo ratings yet
- Aminoácidos - Péptidos ProteínasDocument62 pagesAminoácidos - Péptidos ProteínasMaria Claudia Soto PrudencioNo ratings yet
- Wuolah Free BIOQUÍMICADocument94 pagesWuolah Free BIOQUÍMICAJosé Luis RomeoNo ratings yet
- Conceptos Básicos de Aminoácidos Y ProteínasDocument117 pagesConceptos Básicos de Aminoácidos Y ProteínasErik Raul Miranda LazaroNo ratings yet
- Clase 1. Aminoacidos y ProteinasDocument28 pagesClase 1. Aminoacidos y ProteinasGeraldine PerezNo ratings yet
- Proteínas-Química-BiológicaDocument19 pagesProteínas-Química-BiológicaRobin MaryNo ratings yet
- Aminoácidos y Proteínas - Laboratorio Química Orgánica 2Document19 pagesAminoácidos y Proteínas - Laboratorio Química Orgánica 2AyudaFIQ-SMNo ratings yet
- Aminoácidos esenciales y sus funcionesDocument29 pagesAminoácidos esenciales y sus funcionesKarla G. Hiller CervantesNo ratings yet
- Diapositiva Amino MODDocument19 pagesDiapositiva Amino MODGabriel CarrilloNo ratings yet
- Proteinas - UnjbgDocument88 pagesProteinas - UnjbgVanessa Plata SotoNo ratings yet
- TeóRico QuímicaDocument66 pagesTeóRico QuímicaJuli GrandNo ratings yet
- AminoácidosDocument24 pagesAminoácidosRoger FigueroaNo ratings yet
- Parte TeoricaDocument40 pagesParte TeoricaMaye Cayllahua PeñaNo ratings yet
- Rúbrica de Emprendimiento e Innovación - Parcial - 2018-20Document3 pagesRúbrica de Emprendimiento e Innovación - Parcial - 2018-20Maye Cayllahua PeñaNo ratings yet
- Rúbrica de Emprendimiento e Innovación - Parcial - 2018-20Document2 pagesRúbrica de Emprendimiento e Innovación - Parcial - 2018-20Maye Cayllahua PeñaNo ratings yet
- Curriculum Vitae No Documentadocirugia PlasticaDocument78 pagesCurriculum Vitae No Documentadocirugia PlasticaMaye Cayllahua PeñaNo ratings yet
- Expooo Pato FinalDocument13 pagesExpooo Pato FinalMaye Cayllahua PeñaNo ratings yet
- Modelo de Perfil Snip III ModuloDocument13 pagesModelo de Perfil Snip III ModuloMaye Cayllahua PeñaNo ratings yet
- FIOSOFIA DE ARISTÓTELES, EPICURO Y PLATÓNDocument14 pagesFIOSOFIA DE ARISTÓTELES, EPICURO Y PLATÓNMaye Cayllahua PeñaNo ratings yet
- Rúbrica de Emprendimiento e Innovación - Parcial - 2018-20Document3 pagesRúbrica de Emprendimiento e Innovación - Parcial - 2018-20Maye Cayllahua PeñaNo ratings yet
- Consigna de Trabajo Parcial Emprendimiento e Innovación 2018-20Document2 pagesConsigna de Trabajo Parcial Emprendimiento e Innovación 2018-20Maye Cayllahua PeñaNo ratings yet
- Curriculum Vitae No Documentadocirugia PlasticaDocument2 pagesCurriculum Vitae No Documentadocirugia PlasticaMaye Cayllahua PeñaNo ratings yet
- Pat Oooo Oooooooooo Ssssss SssssssssDocument30 pagesPat Oooo Oooooooooo Ssssss SssssssssMaye Cayllahua PeñaNo ratings yet
- Protocolo Feminicidios 20042012 FINAL 2 PDFDocument96 pagesProtocolo Feminicidios 20042012 FINAL 2 PDFGriselda AsmuziNo ratings yet
- Rúbrica de Emprendimiento e Innovación - Parcial - 2018-20Document2 pagesRúbrica de Emprendimiento e Innovación - Parcial - 2018-20Maye Cayllahua PeñaNo ratings yet
- Exposicion HematologiaDocument46 pagesExposicion HematologiaMaye Cayllahua PeñaNo ratings yet
- Fitoesteroles VegetalesDocument8 pagesFitoesteroles VegetalesMaye Cayllahua PeñaNo ratings yet
- Malformaciones renales y del tracto urinario: guía de anatomía patológicaDocument31 pagesMalformaciones renales y del tracto urinario: guía de anatomía patológicaMaye Cayllahua PeñaNo ratings yet
- FIOSOFIA DE ARISTÓTELES, EPICURO Y PLATÓNDocument14 pagesFIOSOFIA DE ARISTÓTELES, EPICURO Y PLATÓNMaye Cayllahua PeñaNo ratings yet
- Expo PaolaDocument56 pagesExpo PaolaMaye Cayllahua PeñaNo ratings yet
- SuerosDocument9 pagesSuerosMaye Cayllahua PeñaNo ratings yet
- YaconnnnnDocument71 pagesYaconnnnnMaye Cayllahua PeñaNo ratings yet
- ReciclajeDocument15 pagesReciclajeMaye Cayllahua PeñaNo ratings yet
- Expooo Pato FinalDocument13 pagesExpooo Pato FinalMaye Cayllahua PeñaNo ratings yet
- Seguridad AlimentariaDocument6 pagesSeguridad AlimentariaMaye Cayllahua PeñaNo ratings yet
- Perfil de Proyecto ModeloDocument4 pagesPerfil de Proyecto ModeloMaye Cayllahua PeñaNo ratings yet
- Ventilación Mecánica en NeonatoDocument1 pageVentilación Mecánica en NeonatoMaye Cayllahua PeñaNo ratings yet
- Hipertension EmbarazadasDocument354 pagesHipertension EmbarazadasMaye Cayllahua PeñaNo ratings yet
- Presentación1 LUCYkk KDocument32 pagesPresentación1 LUCYkk KMaye Cayllahua PeñaNo ratings yet
- Hipospadias LUCYDocument33 pagesHipospadias LUCYMaye Cayllahua PeñaNo ratings yet
- Examen de RazonamientoDocument2 pagesExamen de RazonamientoMaye Cayllahua PeñaNo ratings yet
- 2.amebas de Vida LibreDocument4 pages2.amebas de Vida LibreJuan Diego CamposNo ratings yet
- Proteínas: estructura, clasificación y funcionesDocument24 pagesProteínas: estructura, clasificación y funcionesIves Julian Yoplac TafurNo ratings yet
- AminoácidoDocument7 pagesAminoácidoBetty LopezNo ratings yet
- Taller Número 3 de BioquímicaDocument4 pagesTaller Número 3 de BioquímicaLUIS ANGEL LLANOS ACUÑANo ratings yet
- Bioeconomía, Una Oportunidad para La Agroindustria. Parte 3Document50 pagesBioeconomía, Una Oportunidad para La Agroindustria. Parte 3CEDAITNo ratings yet
- Magistrales VademecumDocument30 pagesMagistrales VademecumELISANo ratings yet
- Aceite de cacahuate: propiedades, composición y usosDocument3 pagesAceite de cacahuate: propiedades, composición y usosJairoNo ratings yet
- AminoácidoDocument17 pagesAminoácidoandresleonliveNo ratings yet
- Aminoácidos BiologíaDocument55 pagesAminoácidos Biologíapaoka100% (1)
- Seminario 2 AminoacidosDocument3 pagesSeminario 2 AminoacidosNicolás BustosNo ratings yet
- Ficha Tecnica Cuy Forte Gazapos EngordeDocument2 pagesFicha Tecnica Cuy Forte Gazapos EngordeEricka Llaros SalasNo ratings yet
- Ácidos grasos: definición, tipos y principales representantesDocument16 pagesÁcidos grasos: definición, tipos y principales representantesAnita26010% (1)
- Aminoácidos y LongevidadDocument68 pagesAminoácidos y LongevidadAlejandro JaimeNo ratings yet
- 11) Metabolismo de Los Aminoácidos y Proteínas (Transaminación y Desaminación Oxidativa)Document22 pages11) Metabolismo de Los Aminoácidos y Proteínas (Transaminación y Desaminación Oxidativa)Marcos Morales ArceNo ratings yet
- Score QuimicoDocument30 pagesScore QuimicoAngely Chacón BNo ratings yet
- Presentacion - C.Esqueletos CarbonadosDocument10 pagesPresentacion - C.Esqueletos CarbonadosVale MtzNo ratings yet
- Punto Isoelectrico TallerDocument1 pagePunto Isoelectrico TallerYaney Yulei BrownNo ratings yet
- AnnotatedDocument5 pagesAnnotatedSebas LanuzaNo ratings yet
- AminoacidosDocument2 pagesAminoacidosMALEJA SANTANANo ratings yet
- Biosíntesis de Prolina y ArgininaDocument5 pagesBiosíntesis de Prolina y ArgininaRocio M.RosasNo ratings yet
- Anabolismo de AminoacidosBQIIDocument60 pagesAnabolismo de AminoacidosBQIILolaNo ratings yet
- AMINOACIDOSDocument4 pagesAMINOACIDOSAna RosalesNo ratings yet
- Aa EsencialesvalladolidDocument48 pagesAa EsencialesvalladolidandreigustvNo ratings yet
- Nombres y fórmulas de compuestos orgánicosDocument14 pagesNombres y fórmulas de compuestos orgánicosManu GomezNo ratings yet
- Apuntes BioquimicaDocument4 pagesApuntes BioquimicaFernando ZapanaNo ratings yet
- Ejercicios OnceDocument5 pagesEjercicios OnceMaria Jose Rodriguez RodriguezNo ratings yet
- PROTIDOSDocument19 pagesPROTIDOSOrtiz JavierNo ratings yet
- Potencialidades Semillas PDFDocument1 pagePotencialidades Semillas PDFDiana BonyuetNo ratings yet
- Tabla de Aminoácidos EstandarDocument2 pagesTabla de Aminoácidos EstandarLuis RodriguezNo ratings yet
- Amino Power - Ficha Tecnica. 20Document3 pagesAmino Power - Ficha Tecnica. 20jaeles albNo ratings yet
- Guia - Practica 5Document7 pagesGuia - Practica 5BEIMAR RAPHAEL PEREYRA FUENTESNo ratings yet